A DNS-metiláció, a folát és a neurokognitív fejlődés kölcsönhatása
EpiFASSTT tanulmány, Biomedical Sciences, Ulster University, Coleraine, Egyesült Királyság
EpiFASSTT tanulmány, Biomedical Sciences, Ulster University, Coleraine, Egyesült Királyság
EpiFASSTT tanulmány, pszichológia, Ulster Egyetem, Coleraine, Egyesült Királyság
EpiFASSTT tanulmány, Biomedical Sciences, Ulster University, Coleraine, Egyesült Királyság
EpiFASSTT tanulmány, pszichológia, Ulster Egyetem, Coleraine, Egyesült Királyság
EpiFASSTT tanulmány, Számítástudományi Kutatóintézetek, Ulster Egyetem, Londonderry, Egyesült Királyság
EpiFASSTT tanulmány, Biomedical Sciences, Ulster University, Coleraine, Egyesült Királyság
* A levelezés szerzője:
EpiFASSTT tanulmány, Biomedical Sciences, Ulster University, Coleraine, Egyesült Királyság
Absztrakt
A DNS-metiláció vonzó lehetséges módot kínál a környezeti inputok magzati életben történő terjesztésére és a felnőttek későbbi mentális egészségének befolyásolására, ami fokozott együttműködéshez vezet a molekuláris biológusok, táplálkozási és pszichiáterek között. Érdekes terület a folát potenciális szerepe, nemcsak az idegi csövek bezáródásában a korai terhességben, hanem a későbbi nagyobb neurodevelopmentális eseményekben is, amelyek következményei lehetnek a későbbi szociokognitív érésnek. Itt állítjuk be a legújabb felfedezések színterét azáltal, hogy áttekintjük a magzati élet idegi fejlődésének főbb eseményeit, különös tekintettel azokra a szövetekre és struktúrákra, ahol dinamikus metilációs változások ismertek. Ezt követően megadjuk a metiláció által megcélzott, a neurológiai és viselkedési fejlődés szempontjából fontos gének néhány fő osztályát. Végül kiemelünk néhány kognitív rendellenességet, ahol a metilációs változások fontos szerepet játszanak.
Az első benyújtott tervezet: 2016. január 6 .; Közzétételre elfogadva: 2016. március 17 .; Online közzététel: 2016. június 20
E: Ependymális réteg; EGL: Külső szemcsés réteg; I: Középső zóna; IGL: Belső szemcsés réteg; M: peremréteg; P: Purkinje sejtek; V: Kamrai oldal.
Elemek újrarajzolva a [19,20] engedélyével.
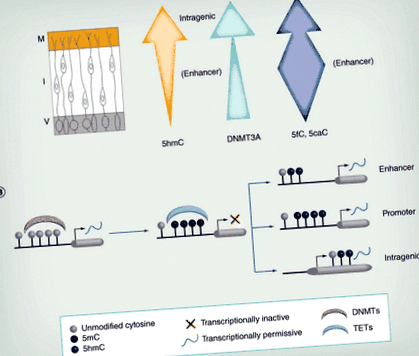
(A) Ahogy a neuronok a V-ből vándorolnak, az 5hmC szintje általában növekszik. Emellett lokalizációja megváltozik, az M intragén régióiban, de az I. fokozóiban gazdagodik. A DNMT3A expresszió (zöld nyíl) szintén növekszik az idegcsőben. Az 5fC/5caC szintek a migráció során változnak, jobban fokozódnak a fokozó régiókban, különösen a köztes zónán belül (kék nyíl). (B) A naiv DNS metilezése DNMT-k révén gyakran társul transzkripciós represszióval. Ezt a metilációt megfordíthatják a TET-ek, amelyek 5 mHC-t termelnek, általában transzkripciós aktivációval társulva. A hidroximetilezés az enhanszeren és a promóteren átmenetibbnek tűnik, és valószínűleg aktív demetilációt tükröz ezekben a régiókban, míg az intragén 5hmC stabilabb, és az optimális transzkripciós sebességhez folyamatosan szükség lehet rá.
5 mHC: 5-hidroxi-metil-citozin; DNMT: DNS-metil-transzferáz; I: Középső zóna; M: Marginal zone; TET: Tíz tizenegy translocase; V: Kamrai zóna.
3. ábra. 8 éves gyermek magnetoencefalográfiai vizsgálata és a megfelelő jelkimenet.
A 8 éves fiú magnetoencefalográfiás vizsgálata felhasználóbarát, nem invazív rendszert mutat, megfelelő agyi aktivitásméréssel a képernyőn.
A legújabb kutatások arra a váratlan betekintésre vezettek, hogy az agy sejtjei nagyobb plaszticitással rendelkeznek a DNS-metiláció tekintetében, mint azt korábban feltételezték. Az idegsejtek replikatív nyugalma és az a dogma, miszerint a metiláció csak passzívan veszíthető el hígítással a sejt megkettőzését követően, úgy gondolták, hogy a differenciálódás után kevés változás történhet. Bár ez ellentétesnek tűnt az agyban észlelt magas metil-transzferáz-szinttel, csak a központi idegrendszer idegsejtjeiben végzett 5-hidroxi-metilezés (5 hM) felfedezésével [1,2] lehetséges dinamikus változás és alkalmazkodás lehetséges mechanizmusa látható. Ezenkívül az idegsejtekben előforduló, elterjedt nem CG-metiláció (CpH-metiláció) közelmúltbeli azonosítása további érdeklődést váltott ki az agy epigenetikai szabályozása iránt [3]. A felnőttkori betegség lehetséges fejlődési eredetéről szóló befolyásos javaslattal párosulva [4,5] ez a kutatások robbanásához vezetett a neurodevelopment, az epigenetika és a pszichiátria közötti határfelületen.
Folát és DNS metiláció
A folát (szintetikus formájában folsavként emlegetik, mint az étrend-kiegészítőkben vagy a dúsított élelmiszerekben található), vízben oldódó B-vitamin, amely elengedhetetlen az életképes embrionális fejlődéshez, és az egész életen át fontos étrendi alkotóelem marad. Biológiailag a folátra van szükség az egy szénatomú anyagcseréhez, amely magában foglalja az egy szénatom egységeinek átadását és hasznosítását az alapvető utakban. Az emberi test nem képes szintetizálni a folátot de novo és így két kritikus út függ az elegendő táplálék bevitelétől, mint egy szén szénforrás: a DNS-szintézis [9] és a DNS-metilációs ciklus, áttekintve a Kirkbride-ben et al. [10]. Az előbbi valószínűleg különösen fontos a terhesség korai szakaszában, amikor a növekedés a leggyorsabb, mivel ez elengedhetetlen a sejtosztódáshoz és a szövetek növekedéséhez. Ez utóbbi fontosabb lehet az idegfejlődés későbbi szakaszaiban, amikor a DNS-metiláció genomszerte történő átalakulása tapasztalható, amint azt alább leírjuk. A DNS-metiláláshoz S-adenozil-metionin (SAM) szükséges, mint univerzális egy szén-donor, amelyet a folátból származó metilcsoportokból nyernek.
A DNS-metilációs minták az embrionális fejlődés során jönnek létre, és az embrió metilációs profilja dinamikusan megváltozik az egész törzs specifikációja és differenciálása során. A folát egy korlátozó tényező a metilációs ciklusban, és ennélfogva az optimálisnál alacsonyabb tápanyag-bevitel a méhben megváltoztathatja az esszenciális gének epigenetikai jeleit, például azokat, amelyek szerepet játszanak az idegi fejlődésben, és amelyekre a DNS-metiláció irányul. Ezek a módosítások fenntartható funkcionális változásokhoz vezethetnek az egész életen át, potenciálisan hajlamosítva a fejlődő egyént neurológiai rendellenességekre. A folát hozzáférhetőségének hatása azonban a méhben a neurális DNS metilációs mintáira és az agy működésére gyakorolt hatásokat jelenleg rosszul jellemzik. A tápanyagok embrionális expozíciója a méhben túlnyomórészt anyai kontroll alatt áll, így az anyai étrend megváltoztatása közvetlenül befolyásolhatja a fejlődő egyén epigenomját, későbbi életkövetkezményekkel jár.
A folsav-kiegészítés bizonyított szerepe az NTD-k megelőzésében
Rövid idővonal
A jelenlegi ismeretek hiányosságai
A folsav megakadályozza az NTD-ket
A folsav előnyei vagy sem a későbbi agyi fejlődésben
Bár az anyai folsav-kiegészítést elengedhetetlen védőintézkedésnek ítélték az NTD-k ellen, és a nőknek 400 mikrogramm/nap folsavat ajánlott perikoncepcionálisan és az első trimeszter végéig szedni, klinikai ajánlások arra, hogy a terhes nőknek folytatniuk kell-e ezt vagy sem. Az utolsó két trimeszter alatt a kiegészítés megoldatlan marad. A folyamatos kiegészítés bebizonyosodott, hogy hatékonyan növeli mind az anyai, mind a köldökvér folát állapotát [37]; ennek a növekedésnek az anyára és a csecsemőre gyakorolt hatásait azonban még teljes mértékben ki kell deríteni.
ASD: autizmus spektrum rendellenesség; NTD: Idegcsőhiba.
Agy képalkotás és magnetoencefalográfia.
Vezetői összefoglaló
A molekuláris biológia legújabb munkája kimutatta, hogy az agyban a DNS-metiláció dinamikusabb, mint azt korábban gondolták.
Egyidejűleg a társadalom- vagy egészségtudományi epidemiológiai munka keretében összegyűjtött nagy kohorszok epigénszintű elemzése összefüggést mutatott a DNS-metilációs változások és az egyes szociokognitív eredmények között.
A fejlődés során a DNS-metilációhoz szükséges kulcsfontosságú tápanyag a folát, amely az univerzális metil-donor S-adenozil-metionint szolgáltatja.
A terhes anya folát elégtelensége az első trimeszterben egyértelmű példa arra, hogy az anya környezeti ráfordítása megváltoztatja az utódok neurokognitív eredményeit.
A folát vagy más környezeti változó hatással lehet a metilációs mintázatokra a fejlesztés során, de ezt még fel kell tárni.
Ebben az áttekintésben kiemeljük a magzati agy fejlődésének kulcsfontosságú szakaszait, ahol dinamikus metilációs változások következnek be, amelyek potenciálisan megzavaródhatnak.
Az idegcső bezáródása az első trimeszter elején érzékeny a folát elégtelenségre, ami idegi csőhibákat eredményezhet, és ezt a hatást utánozhatják a DNS metiltranszferáz inhibitorai.
A terhesség korai közepétől a közepéig a differenciálódó neuronok hullámai sugárirányban kifelé mozognak az idegcsőben az őssejtrétegtől a belső, vezikuláris oldalon.
A második trimeszterben a kisagy kialakul, és a migráció megszűnésével a kéreg és a kisagy szövettani érése következik be.
A harmadik trimeszterben előfordul a mielináció és a szinaptogenezis megindulása, valamint az agykéreg érése és a magasabb kognitív képességek kivitelezésére szakosodott régiók megjelenése.
A sejtek idegcsőben történő kifelé vándorlása dinamikus változásokkal jár a metilációban, az érő idegsejtekben az 5hmC és a CpH metiláció növekedése következik be, mivel transzkripciós programok jönnek létre.
Valószínűleg fontos olyan specifikus gének számára is, mint pl BDNF és CNTNAP2 a metilezésnek megalapozott szerepe van a HOX, VAGY és PCDH az idegi fejlődésben részt vevő géncsaládok.
A DNS metilációs változásai számos neurokognitív rendellenességben érintettek az idegcső hibáin kívül, beleértve az Angelman-szindrómát, az autizmus spektrum rendellenességeit és a Rett-szindrómát.
Köszönetnyilvánítás
A szerzők hálásak A Caffrey-nak és L-A Henry-nek az értékes beszélgetésekért.
Pénzügyi és versengő érdekek nyilvánosságra hozatala
A szerzői laboratóriumokban végzett munkát az Észak-Írországi Népegészségügyi Ügynökség HSC Kutatási és Fejlesztési Osztályának engedélyező kutatási díja (STL/5043/14) támogatja (K Pentieva, CP Walsh és H McNulty), MRC projekt támogatás (MR/J007773/1 - CP Walsh) és az ESRC/BBSRC Epigenetics Initiative támogatása (az EpiFASSTT ES/N000323/1 tanulmánya CP Walsh, K Pentieva, T Cassidy, H McNulty, DL Lees-Murdock, M McLaughlin és G Prasad). A szerzőknek nincs más releváns kapcsolata vagy pénzügyi közreműködése olyan szervezetekkel vagy szervezetekkel, amelyek pénzügyi érdekeltséggel rendelkeznek vagy pénzügyi konfliktusban vannak a kéziratban tárgyalt témával vagy anyagokkal, a közzétetteken kívül.
A kézirat elkészítéséhez nem használtak írásbeli segítséget.
Nyílt hozzáférésű
Ez a munka az Attribution-NonCommercial-NoDeratives 4.0 Unported License alatt van licencelve. A licenc másolatának megtekintéséhez látogasson el a http://creativecommons.org/licenses/by-nc-nd/4.0/ oldalra.
A különös figyelmet érdemlő dolgozatokat a következők kiemelték: • érdeklődésre számot tartó; •• jelentős érdeklődés
- Az epigenetikai étrend hatása a rákos epigenom epigenomikájára
- Az étrend, az uráttranszporterek és a köszvény és a hiperurikémia kockázatának kölcsönhatása jelenlegi és
- Az adipocita hipertrófia és a hipoxia szerepe az elhízással társult zsír kialakulásában
- Világbank-csoport - Nemzetközi fejlődés, szegénység,; Fenntarthatóság
- Wyszukiwarka mieszkań - Unimax fejlesztés