Dostinex
Találja meg a legalacsonyabb árakat a
Mi a Dostinex és hogyan alkalmazzák?
A Dostinex (kabergolin) egy dopamin-receptor antagonista, amelyet olyan hormon-egyensúlyhiány kezelésére használnak, amelyben a vérben túl sok a prolaktin (más néven hyperprolactinemia).
Milyen mellékhatásai vannak a Dostinex-nek?
A Dostinex gyakori mellékhatásai a következők:
- hányinger,
- hányás,
- gyomorrontás vagy fájdalom,
- emésztési zavar,
- székrekedés,
- gáz,
- szédülés,
- forgó érzés,
- könnyedség,
- álmosság,
- idegesség,
- fáradtság,
- fejfájás,
- depressziós hangulat,
- forró villanások,
- zsibbadás vagy bizsergő érzés, vagy
- száraz száj.
Mondja el orvosának, ha a Dostinex ritka, de súlyos mellékhatásait tapasztalja, beleértve:
- légszomj,
- tartós köhögés,
- duzzadó bokák vagy lábak,
- szokatlan fáradtság,
- mentális/hangulati változások (például idegesség),
- szokatlan erős késztetések (például fokozott szerencsejáték, fokozott szexuális késztetés),
- látásváltozások,
- fájdalmas menzesz, vagy
- mellfájdalom.
LEÍRÁS
A DOSTINEX tabletta kabergolint, egy dopamin receptor agonistát tartalmaz. A kabergolin kémiai neve 1 - [(6-allilergolin-8p-il) -karbonil] -1- [3- (dimetilamino) propil] -3-etil-karbamid. Empirikus képlete C26H37N5O2, molekulatömege 451,62. A szerkezeti képlet a következő:
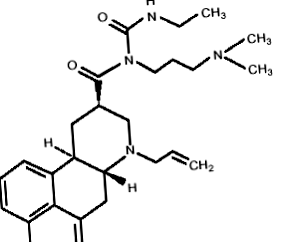 |
A kabergolin etil-alkoholban, kloroformban és N, N-dimetil-formamidban (DMF) oldható fehér por; kissé oldódik 0,1 N sósavban; nagyon kevéssé oldódik n-hexánban; és vízben nem oldódik.
Az orális alkalmazásra szánt DOSTINEX tabletta 0,5 mg kabergolint tartalmaz. Az inaktív összetevők leucinból, USP-ből és laktózból, NF-ből állnak.
JELZÉSEK
A DOSTINEX tabletta hiperprolaktinémiás rendellenességek kezelésére javallt, akár idiopátiás, akár az agyalapi mirigy adenoma miatt.
ADAGOLÁS ÉS ADMINISZTRÁCIÓ
A DOSTINEX tabletta ajánlott adagja a terápia megkezdéséhez hetente kétszer 0,25 mg. Az adag hetente kétszer 0,25 mg-mal növelhető heti 1 mg-os dózisig, a beteg szérum prolaktinszintjének megfelelően. A kezelés megkezdése előtt kardiovaszkuláris értékelést kell végezni, és mérlegelni kell az echokardiográfiát a szelepbetegség felmérése érdekében.
Az adag növelése nem történhet gyorsabban, mint 4 hetente, így az orvos fel tudja mérni a beteg válaszát az egyes adagolási szintekre. Ha a beteg nem reagál megfelelően, és magasabb dózisok esetén nem tapasztalható további előny, akkor a maximális választ elérő legalacsonyabb dózist kell alkalmazni, és más terápiás megközelítéseket kell figyelembe venni. A hosszú távú DOSTINEX-kezelésben részesülő betegeknek rendszeresen fel kell mérniük a szív állapotukat, és mérlegelni kell az echokardiográfiát.
A normál szérum prolaktinszint 6 hónapos fenntartása után a DOSTINEX abbahagyható, a szérum prolaktin szintjének időszakos monitorozásával annak eldöntése érdekében, hogy a DOSTINEX kezelést újra meg kell-e állítani. A hatékonyság tartóssága a DOSTINEX 24 hónapos kezelésén túl nem bizonyított.
HOGYAN KÍNÁLHATÓ
A DOSTINEX tabletta fehér, hasított, kapszula alakú tabletta, amely 0,5 mg kabergolint tartalmaz. Mindegyik tabletta az egyik oldalán bemetszéssel rendelkezik, és a törésvonal mindkét oldalán P és U betűk vannak. A tabletta másik oldalán 700-as szám van bevésve.
DOSTINEX az alábbiak szerint áll rendelkezésre:
8 tablettát tartalmazó palackok NDC 0013-7001-12
Tárolás
Tárolja szabályozott szobahőmérsékleten, 20-25 ° C (68-77 ° F) [lásd USP].
Lehet, hogy a termék címkéje frissült. A teljes felírási információkért látogasson el a www.pfizer.com weboldalra
Forgalmazza: Pharmacia & Upjohn Company Division of Pfizer Inc., NY, NY 10017. Felülvizsgálva: 2014. szept.
DIABEMUTATÁS
MELLÉKHATÁSOK
A DOSTINEX tabletták biztonságosságát több mint 900 hiperprolaktinémiás rendellenességben szenvedő betegnél értékelték. A legtöbb nemkívánatos esemény enyhe vagy közepesen súlyos volt.
Egy 4 hetes, kettős-vak, placebo-kontrollos vizsgálatban a kezelés placebót vagy kabergolint tartalmazott fix dózisokban, heti 0,25, 0,5, 0,75 vagy 1,0 mg adagban. Az első hét során a feleket megfelezték. Mivel csak duzzanat esetén figyeltek meg lehetséges dózisfüggő hatást, a négy kabergolin-kezelési csoportot egyesítették. A placebo-kontrollos vizsgálat során a leggyakoribb nemkívánatos események előfordulását az alábbi táblázat mutatja be.
A jelentett nemkívánatos események előfordulása a 4 hetes, kettős-vak, placebokontrollált vizsgálat során
| Nemkívánatos esemény* | Cabergoline (n = 168) 0,125–1 mg hetente kétszer | Placebo (n = 20) |
| Szám (százalék) | ||
| Emésztőrendszer | ||
| Hányinger | 45 (27) | 4 (20) |
| Székrekedés | 16. (10) | 0 |
| Hasi fájdalom | 9. cikk (5) bekezdés | 1. cikk (5) bekezdés |
| Dyspepsia | 4. cikk (2) bekezdés | 0 |
| Hányás | 4. cikk (2) bekezdés | 0 |
| Központi és perifériás idegrendszer | ||
| Fejfájás | 43 (26) | 5 (25) |
| Szédülés | 25. cikk (15) | 1. cikk (5) bekezdés |
| Paresztézia | 2. cikk (1) bekezdés | 0 |
| Szédülés | 2. cikk (1) bekezdés | 0 |
| A test mint egész | ||
| Aszténia | 15. cikk (9) bekezdés | 2 (10) |
| Fáradtság | 12. cikk (7) bekezdés | 0 |
| Forró villanások | 2. cikk (1) bekezdés | 1. cikk (5) bekezdés |
| Pszichiátriai aluszékonyság | 9. cikk (5) bekezdés | 1. cikk (5) bekezdés |
| Depresszió | 5. cikk (3) bekezdés | 1. cikk (5) bekezdés |
| Idegesség | 4. cikk (2) bekezdés | 0 |
| Vegetativ idegrendszer | ||
| Testtartás által bekövetkezett vérnyomáscsökkenés | 6. cikk (4) bekezdés | 0 |
| Reproduktív - női mellfájdalom | 2. cikk (1) bekezdés | 0 |
| Dysmenorrhoea | 2. cikk (1) bekezdés | 0 |
| Látomás | ||
| Rendellenes látás | 2. cikk (1) bekezdés | 0 |
| * A kabergolin esetében ≥ 1% | ||
A bromokriptinnel végzett összehasonlító vizsgálat 8 hetes, kettős-vak periódusában a DOSTINEX-et (hetente kétszer 0,5 mg-os dózisban) 221 betegből 4-ben (2%) 4 mellékhatás miatt abbahagyták, míg a bromokriptint (dózisban naponta kétszer 2,5 mg-os adagot) 231 betegből 14-ben abbahagyták (6%). A DOSTINEX-kezelés abbahagyásának leggyakoribb okai a fejfájás, hányinger és hányás voltak (3, 2, illetve 2 beteg); a bromokriptin-kezelés abbahagyásának leggyakoribb okai az émelygés, hányás, fejfájás és szédülés vagy vertigo voltak (10, 3, 3 és 3 beteg). A bromokriptinnel végzett összehasonlító vizsgálat kettős-vak szakaszában a leggyakoribb nemkívánatos események előfordulását a következő táblázat mutatja be.
Egyéb nemkívánatos események, amelyekről a
FIGYELMEZTETÉSEK
Terhesség
A dopamin-agonisták általában nem alkalmazhatók terhesség okozta magas vérnyomásban, például preeclampsia, eklampszia és posztpartum hipertónia esetén, kivéve, ha a lehetséges előny megítélése szerint meghaladja a lehetséges kockázatot.
Fibrotikus szövődmények
Szív valvulopathia
Minden betegnek szív- és érrendszeri értékelésen kell átesnie, beleértve az echokardiogramot is a szelepi betegség lehetséges jelenlétének felmérése érdekében. Szelepi betegség észlelése esetén a beteget nem szabad DOSTINEX-szel kezelni. (Lát ELLENJAVALLATOK) A DOSTINEX-et kapó betegeknél a forgalomba hozatalt követően kardiális valvulopathiáról számoltak be. Ezek az esetek általában a DOSTINEX nagy adagjának (> 2mg/nap) adagolása során fordultak elő a Parkinson-kór kezelésében. Szív-valvulopathia eseteiről beszámoltak azoknál a betegeknél is, akik alacsonyabb DOSTINEX-dózist kaptak hiperprolaktinémiás rendellenességek kezelésére.
Több országra kiterjedő, retrospektív kohortvizsgálatot végeztek az Egyesült Királyságban, Olaszországban és Hollandiában az általános gyakorlatok és az összekapcsolási rendszerek felhasználásával, hogy értékeljék a dopamin agonisták, köztük a kabergolint (n = 27 812) Parkinson-kór és a hiperprolaktinémia és a szív a szelepes regurgitáció (CVR), egyéb fibrózisok és egyéb kardiopulmonáris események legfeljebb 12 éves követés során. Ebben a tanulmányban a cabergolin Parkinson-kóros betegek körében történő alkalmazása a CVR megnövekedett kockázatával társult, összehasonlítva a nem ergot eredetű dopamin-agonistákkal (DA) és a levodopával [10 000 személyévre eső 68,1 (95) előfordulási arány (IR) % konfidencia intervallum (CI): 37,2–115,3) a kabergolin esetében 10,0 (95% CI: 5,2–19,4) nem ergot DA esetén és 11,3 (95% CI: 7,2 –17,0) levodopa esetén]. A dopamin agonistával kezelt hiperprolaktinémiában szenvedő személyekre korlátozódó vizsgálati elemzésben (n = 8 386), a nem használókkal összehasonlítva (n = 15 147), a kabergolinnak kitett személyeknél nem volt magasabb a CVR kockázata. A cabergolin kezeléssel járó CVR kockázatának megállapításai a Parkinson-kórban (fokozott kockázat) és a hiperprolaktinémiában szenvedőknél (nincs megnövekedett kockázat) összhangban állnak más közzétett vizsgálatok eredményeivel.
Az orvosoknak a legalacsonyabb hatékony DOSTINEX adagot kell alkalmazniuk a hiperprolaktinémiás rendellenességek kezelésére, és időszakosan újra kell értékelniük a DOSTINEX-kezelés folytatásának szükségességét. A kezelés megkezdése után klinikai és diagnosztikai monitorozást kell végezni (például mellkasröntgen, CT-vizsgálat és szív-echokardiogram) a szív-valvulopathia kockázatának felmérése érdekében. A rutinszerű echokardiográfiai monitorozás ajánlott gyakorisága 6–12 havonta, vagy klinikailag indokolt jelek és tünetek jelenlétével, például ödéma, új szívmormor, dyspnoe vagy pangásos szívelégtelenség.
A DOSTINEX-kezelést abba kell hagyni, ha az echokardiogram új szelepi regurgitációt, szelepkorlátozást vagy szelepfecskendő-megvastagodást mutat.
A DOSTINEX-et körültekintően kell alkalmazni azoknál a betegeknél, akik más, valvulopathiával összefüggő gyógyszerekkel vannak kitéve.
Extracardialis fibrotikus reakciók
A pleuralis, a pericardialis és a retroperitoneális fibrózis forgalomba hozatalt követő eseteiről számoltak be a DOSTINEX beadását követően. Néhány jelentés olyan betegekről szólt, akiket korábban más ergotin dopamin agonistákkal kezeltek. A DOSTINEX nem alkalmazható olyan betegeknél, akiknek kórtörténetében szív- vagy extracardialis fibrotikus rendellenességek szerepelnek.
A fibrotikus rendellenességek alattomos módon jelentkezhetnek, és a betegeket ellenőrizni kell a progresszív fibrózis megnyilvánulása szempontjából. Ezért a kezelés során figyelmet kell fordítani a következőkre:
- Pleuro-tüdőbetegség, például nehézlégzés, légszomj, tartós köhögés vagy mellkasi fájdalom.
- Veseelégtelenség vagy húgycső/hasi érelzáródás, amely az ágyék/szár és az alsó végtag ödémájának fájdalmával, valamint esetleges hasi tömegekkel vagy érzékenységgel járhat, amelyek retroperitoneális fibrózisra utalhatnak.
- Szívelégtelenség: A szelepes és a pericardialis fibrózis esetei gyakran szívelégtelenségként nyilvánulnak meg. Ezért a szelepfibrózist (és a konstriktív pericarditist) ki kell zárni, ha ilyen tünetek jelentkeznek.
A klinikai és diagnosztikai monitorozást, mint például az eritrocita szedimentáció sebességét, a mellkas-röntgen sugárzást, a szérum kreatinin mérést és más vizsgálatokat meg kell fontolni a kiinduláskor és szükség szerint, amíg a betegeket DOSTINEX-sel kezelik.
A pleurális effúzió vagy a tüdőfibrózis diagnózisát követően a DOSTINEX abbahagyása a jelek és tünetek javulását eredményezte.
- A ginzeng arany orális felhasználása, mellékhatások, kölcsönhatások, képek, figyelmeztetések; Adagolás - WebMD
- Glimepirid (Amaryl) - Mellékhatások, kölcsönhatások, felhasználások, adagolás, figyelmeztetések
- Gyömbér előnyei, mellékhatásai, adagolása, kölcsönhatásai
- A kőszénkátrány helyi felhasználása, mellékhatások, kölcsönhatások, képek, figyelmeztetések; Adagolás - WebMD
- Édeskömény felhasználás, mellékhatások, kölcsönhatások, adagolás és figyelmeztetés