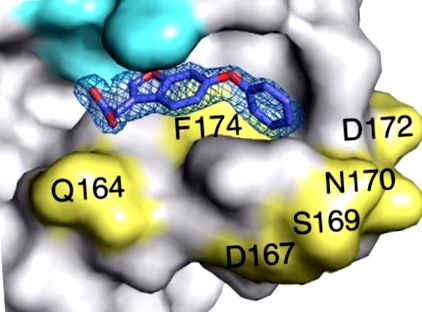
A benzofurán sláger töredékalapú kifejlesztése az Escherichia coli DsbA inhibitorok új osztályaként
A 6 - 12 kulcsfontosságú benzofuránok szintézise kidolgozásra. Reagensek és körülmények: (a) etil-4-klór-acetacetát, H2S04 vagy MsOH, 0 ° C, 2 óra, szobahőmérséklet és 24 óra; (b) 2 M NaOH, 80 ° C és 16 óra; (c) CH30H, SOCI2, visszafolyatás és 16 óra hosszat.
(A) Aril-amin képződés a C-6-on Buchwald – Hartwig kapcsolással és ezt követő észter-hidrolízissel. (B) Alkil-éter képződés a 6-os helyzetben Williamson-éter-szintézissel. (C) Aril-éter képződés C-6-on Ullmann-típusú kapcsolással. (D) Benzilképződés C-6-on Negishi-kapcsolással és ezt követő hidrolízissel. Reagensek és körülmények: (a) aril-amin, K2CO3, Pd2 (dba) 3, XPhos, t-BuOH, visszafolyatás közben, 16 óra; (b) 2 M NaOH, 80 ° C, 16 óra; (c) alkil-bromid, K2C03, CH3CN, visszafolyatás közben, 16 óra; (d) szubsztituált fenol, CuI, pikolinsav, K3PO4, CH3SOCH3, 90 ° C, 24 óra. (e) (1) Zn, LiCl, BnBr, THF, 0 ° C, 1,5 óra; (2) 11, Pd (OAc) 2, XPhos, THF, 50 ° C, 18 óra.
A 4.27-es tetrazol szintézise karboxi-izosztereként. Reagensek és körülmények: (a) (1) PCI5, CH2Cl2, reflux, 1 óra; (2) NH3, 5 m. (b) SOCl2, toluol, visszafolyatás közben, 1,5 óra. (c) NaN3, Et3N-HCl, toluol, visszafolyatás közben, 3 nap.
6-bróm- és 6-fenil-indol-származékok szintézise. Reagensek és körülmények: (a) NaH, (CH3) 2C03, THF, visszafolyatás közben, 16 óra. (b) (1) Br2, CC14, szobahőmérséklet, 24 óra; (2) Na2S03, H20, szobahőmérsékleten, 24 óra. (c) KOH, CH30H: H20 (9: 1), visszafolyatás közben, 2 óra. (d) Ph (BOH) 2, CsF, Pd (dppf) Cl2, CH3CN: H20 (4: 1), 90 ° C, 24 óra.
11 aminosav elődjeként bróm- és azido-intermedierekkel történő aminálása. Reagensek és körülmények: (a) NBS, AIBN, CC14, visszafolyatás, 16 óra; (b) NaN3, DMF, -40 ° C, 1 óra; (c) H2, PtO2, MeOH.
Absztrakt
A 6 - 12 kulcsfontosságú benzofuránok szintézise kidolgozásra. Reagensek és körülmények: (a) etil-4-klór-acetacetát, H2S04 vagy MsOH, 0 ° C, 2 óra, szobahőmérséklet és 24 óra; (b) 2 M NaOH, 80 ° C és 16 óra; (c) CH30H, SOCI2, visszafolyatás és 16 óra hosszat.
(A) Aril-amin képződés a C-6-on Buchwald – Hartwig kapcsolással és ezt követő észter-hidrolízissel. (B) Alkil-éter képződés a 6-os helyzetben Williamson-éter szintézissel. (C) Aril-éter képződés C-6-on Ullmann-típusú kapcsolással. (D) Benzilképződés C-6-on Negishi-kapcsolással és ezt követő hidrolízissel. Reagensek és körülmények: (a) aril-amin, K2CO3, Pd2 (dba) 3, XPhos, t-BuOH, visszafolyatás közben, 16 óra; (b) 2 M NaOH, 80 ° C, 16 óra; (c) alkil-bromid, K2C03, CH3CN, visszafolyatás közben, 16 óra; (d) szubsztituált fenol, CuI, pikolinsav, K3PO4, CH3SOCH3, 90 ° C, 24 óra. (e) (1) Zn, LiCl, BnBr, THF, 0 ° C, 1,5 óra; (2) 11, Pd (OAc) 2, XPhos, THF, 50 ° C, 18 óra.
A 4.27-es tetrazol szintézise karboxi-izosztereként. Reagensek és körülmények: (a) (1) PCI5, CH2Cl2, reflux, 1 óra; (2) NH3, 5 m. (b) SOCl2, toluol, visszafolyatás közben, 1,5 óra. (c) NaN3, Et3N-HCl, toluol, visszafolyatás közben, 3 nap.
6-bróm- és 6-fenil-indol-származékok szintézise. Reagensek és körülmények: (a) NaH, (CH3) 2C03, THF, visszafolyatás közben, 16 óra. (b) (1) Br2, CC14, szobahőmérséklet, 24 óra; (2) Na2S03, H20, szobahőmérsékleten, 24 óra. (c) KOH, CH30H: H20 (9: 1), visszafolyatás közben, 2 óra. (d) Ph (BOH) 2, CsF, Pd (dppf) Cl2, CH3CN: H20 (4: 1), 90 ° C, 24 óra.
A 11 aminosav-prekurzorként bróm- és azido-intermedierekkel történő aminálása. Reagensek és körülmények: (a) NBS, AIBN, CC14, visszafolyatás, 16 óra; (b) NaN3, DMF, -40 ° C, 1 óra; (c) H2, PtO2, MeOH.
- Molekulák teljes szöveges azonosítása és β-szitoszterin β-d-glükozid mennyiségi meghatározása
- Molekulák az avokádó mézélettani hatásainak teljes szövegű antibakteriális hatásmechanizmusai
- Az élő rendszerekben megfigyelt molekulák szabad teljes szövegű lehetséges biológiai hatásmechanizmusok
- Molekulák szabad teljes szövegbeli egyenlőtlenség a nyitott államok előfordulásának gyakoriságában függ
- Molekulák nélküli, teljes szövegű NMR lipidprofil az alpesi kecskékből származó tejben, kiegészített kendermaggal és