A borjak megelőző antibiotikus kezelése: dysbiosis megjelenése elhízott állapotú és mobil multirezisztenciát hordozó baktériumok terjedését okozza
Sport, Testedzés és Élettudományi Központ, Coventry Egyetem, Coventry, Egyesült Királyság
Ezek a szerzők egyformán járultak hozzá ehhez a munkához. Keressen további cikkeket a szerzőtől
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Ezek a szerzők egyformán járultak hozzá ehhez a munkához. Keressen további cikkeket a szerzőtől
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Sport, Testedzés és Élettudományi Központ, Coventry Egyetem, Coventry, Egyesült Királyság
Moreton Morrell College Farm, Warwickshire College, Warwickshire, CV35 9BL, Egyesült Királyság
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Természettudományi és Pszichológiai Iskola, Liverpool John Moores Egyetem, Liverpool, Egyesült Királyság
Levelezésre. E-mail [email protected]; Tel. + (44) 24776 58794. ** E-mail: [email protected]; Tel. +44 (0) 151 231 2542.
Sport, Testedzés és Élettudományi Központ, Coventry Egyetem, Coventry, Egyesült Királyság
Levelezésre. E-mail [email protected]; Tel. + (44) 24776 58794. ** E-mail: [email protected]; Tel. +44 (0) 151 231 2542.
Sport, Testedzés és Élettudományi Központ, Coventry Egyetem, Coventry, Egyesült Királyság
Ezek a szerzők egyformán járultak hozzá ehhez a munkához. Keressen további cikkeket a szerzőtől
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Ezek a szerzők egyformán járultak hozzá ehhez a munkához. Keressen további cikkeket a szerzőtől
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Sport, Testedzés és Élettudományi Központ, Coventry Egyetem, Coventry, Egyesült Királyság
Moreton Morrell College Farm, Warwickshire College, Warwickshire, CV35 9BL, Egyesült Királyság
Élettudományi Kar, Coventry Egyetem, Coventry, Egyesült Királyság
Természettudományi és Pszichológiai Iskola, Liverpool John Moores Egyetem, Liverpool, Egyesült Királyság
Levelezésre. E-mail [email protected]; Tel. + (44) 24776 58794. ** E-mail: [email protected]; Tel. +44 (0) 151 231 2542.
Sport, Testedzés és Élettudományi Központ, Coventry Egyetem, Coventry, Egyesült Királyság
Levelezésre. E-mail [email protected]; Tel. + (44) 24776 58794. ** E-mail: [email protected]; Tel. +44 (0) 151 231 2542.
Finanszírozási információk:
A DAD-ot az NERC támogatása támogatta az IM számára (NE/N019288/1), az MTFL-t pedig a Coventry Egyetem Egészségügyi Élettudományi Kar Sport-, Testmozgás- és Élettudományi Kutatóközpontja támogatta.
Összegzés
Bevezetés
A bél mikrobiota kritikus fontosságú az emberek és állatok homeosztázisában, és az antibiotikum-rezisztencia gének természetes tárházát képviseli (Salyers et al., 2004; Dethlefsen et al., 2007; Sommer et al., 2009; Allen et al., 2010). Az antibiotikumokat (AB) általában használják az állattenyésztésben a fertőzések megelőzésére és kezelésére, valamint a fejlődő országokban a növekedés támogatására, annak ellenére, hogy elősegítik a multirezisztens kórokozók, köztük a „legvégső antibiotikumoknak” rezisztens kórokozók, például a kolisztin ( Cabello, 2006; McEwen, 2006; Martínez, 2008; Hasman et al., 2015; Liu et al., 2016; Paterson és Harris, 2016). Azt is régóta gondolták, hogy az ilyen kezelések közvetlenül kiválasztják az előírt antibiotikummal szemben rezisztens baktériumokat, ami az alkalmazott antibiotikumra specifikus rezisztencia-meghatározók kialakulásához vezet (pl. Hayden et al., 2005; Sanchez Garcia et al., 2010; Endimiani et al., 2011). Úgy tűnik azonban, hogy az AB-kezelés a mikrobiota dysbiosis általánosabb egyensúlyhiányát okozza, amely további hatásokkal járhat, ideértve az olyan baktériumok arányának aránytalan növekedését, amelyek hordozhatják a multirezisztens géneket tartalmazó mobil elemeket (Barlow, 2009; Shin et al., 2015) és/vagy elhízással jár.
Itt ellenőrzött körülmények között tartott és tenyésztett borjakat megelőző antibiotikus terápiának tették ki florfenicol; Nuflor márkanév a rezisztómára és a bél mikrobiotájára gyakorolt hatások értékelésére. Ez az első jelentés a borjúbél mikrobiotájának molekuláris elemzéséről válaszként egy megelőző antibiotikum-terápiára, amely hajlamosítja az állatokat a dysbiosisra és a betegségekre, elősegítve az olyan baktériumok szaporodását, amelyek rendkívül mobil, klinikailag releváns rezisztenciákat hordoznak, amelyek emberre is átvihetők.
Eredmények
Az antibiotikum-kezelés kiegyensúlyozatlan mikrobiális közösséghez vezet az állati bélben
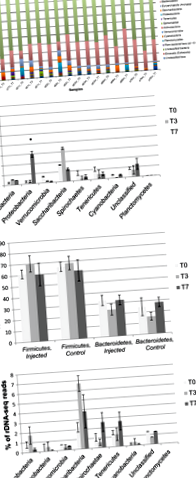
A 18 minta mély szekvenálása 5 578 146 szekvencia-leolvasást eredményezett a baktérium 16S rDNS V3 – V4 hipervariábilis régióiban; 2 888 547 gyógyszeres és 2 689 599 nem gyógyszeres borjú. Mindegyik mintában legfeljebb 10 különböző bakteriális phylát (1A. Ábra) azonosítottak, metanogénnel együtt Archaea (2. ábra). Az uralkodó phyla volt Firmicutes (64 ± 1,7%) és Bacteroidetes (26 ± 2,6%; 1A. És 1. ábra), amelyekről kimutatták, hogy az emberi és állati bélben vannak a leggyakoribbak (Eckburg et al., 2005; Sun és Chang, 2014). Alacsonyabb prevalenciánál voltak Saccharibacteriumok, Tenericutes, Spirochaetes, Actinobaktériumok, Proteobaktériumok, Verrucomicrobia és Cianobaktériumok. Kivéve Proteobaktériumok, a phyla általános előfordulása nem változott szignifikánsan az antibiotikum-kezelésre adott válaszként (1B. és 1. ábra).
Megjelenése E. coli hordozható mobil mcr ‐ 2, fenntartása oqxB gének és a klinikai antibiotikumokkal szembeni rezisztencia a florfenicol hatására
A pOLA52 plazmid jelenlétét a kezelt mintákban T7-nél megerősítettük a metagenomikus DNS beágyazott PCR-jének Sanger-szekvenálásával, amely egy véletlenszerűen kiválasztott 215 bp-os szekvenciát célzott meg a plazmidban. Ezek az eredmények határozottan arra utalnak, hogy az egészséges állatok megelőző antibiotikus kezelése elősegíti az E. coli amelyek klinikailag releváns rezisztenciagéneket hordoznak a mobil elemeken, növelve a rezisztencia elterjedésének kockázatát a mezőgazdasági és az emberi populációkon belül.
Vita
Összességében a fakultatív anaerob antibiotikumok által kiváltott diszbiotikus terjeszkedése E. coli hajlamosíthatja a gazdaszervezetet olyan betegségekre, mint például a bélgyulladás és a rák. Ez is vezethet egy Enterobacteriaceae enterális kórokozó kolonizációja, amely klinikailag releváns transzmisszív antibakteriális rezisztenciákat hordoz. Ezért az egészséges állatok megelőző antibiotikum-kezelésének figyelembe kell vennie az állatok egészségének potenciális veszélyét, valamint a mobil rezisztenciát hordozó kórokozók zoonózis-átvitelének magas kockázatát az emberi populáció számára.
Következmények
A borjak florfenikollal történő kezelése megváltoztatta a bél mikrobiotáját, így étrend-változtatás nélkül hasonlít az elhízott emberek/állatokéhez. Az elhízás világszerte mintegy 400 millió embert érintő fő köz- és klinikai egészségügyi probléma. Míg az étrend hozzájárul a bél mikrobiota sokféleségéhez (Bäckhed et al., 2005), és befolyásolja a testtömeget, azonban kimutatták, hogy ez a növekedés az élelmiszer-fogyasztás változása nélkül is bekövetkezhet (Ley et al., 2006). Ennélfogva az egészséges bélmikrobiota javított energiahordozó képessége az antibiotikumra reagálva hozzájárulhat a fokozott energiafogyasztáshoz, miközben megegyezik az élelmiszer-bevitel. Ezért az elhízásra gyakorolt lehetséges hatását az egészségügyi szakembereknek figyelembe kell venniük a klinikai fertőzések kezelése során.
Kísérleti eljárások
Minták
Genomikus DNS izolálás és szekvenálás
A teljes genomi DNS-t (gDNS) a QIAamp ® DNS széklet kit (QIAGEN®) segítségével extraháltuk. 0,2 g sejtpelletet szuszpendáltunk 180 μl 1 × PBS-ben, és a gyártó utasításainak megfelelően dolgoztuk fel. A tisztított gDNS koncentrációját spektrofotometriával mértük A260-nál. Teljes DNS-t alkalmaztunk az egész (meta) genom sörétes puska szekvenálásához, és templátként a bakteriális 16S kicsi alegység riboszomális RNS génje V3-V4 hipervariábilis régióinak amplifikálásához és szekvenálásához metagenomikus profilozáshoz. A szekvenálási protokollok részleteit, beleértve a primer szekvenciákat is, az S1. Függelék tartalmazza. Az összes szekvenciaadatot benyújtották az Európai Nukleotid Archívumhoz (ENA), a PRJEB33144 (a 16S rRNS adatokhoz) és a PRJEB33145 (a teljes metagenómás sörétes szekvencia adatokhoz tartozó) hozzáférések alatt.
A baktériumközösségek metagenomikus profilozása
A baktériumközösség „ellenállásának” profilozása az egész genom metagenomikus sörétes puska szekvenálásával
Az egyes minták „ellenállásának” meghatározásához a Resfinder-től (https://cge.cbs.dtu.dk/services/ResFinder/) nyertek rezisztenciához kapcsolódó génkészleteket, és ezeket olyan adatbázisok készítéséhez használták, amelyek alkalmasak a BLAT (Kent, 2002). Az olvasásokat úgy dolgoztuk fel, hogy eltávolítottuk a szekvenáló könyvtáradapter-szekvenciákat a cutadapt v1.9.1 (Martin, 2011) segítségével, megtartva csak az 50 bp-nál hosszabb olvasást és a vágás után nem tartalmazott „N” -et. A metszett olvasmányokat FASTA formátumra konvertáltuk és „de-replikáltuk” (az azonos olvasatok egy olvasattá összeomlottak) a vsearch v1.1.1 (Pruesse) használatával et al., 2012). Ezt azért tették, hogy (i) a későbbi elemzést számítási szempontból hatékonyabbá tegyék, és (ii) lehetővé tegyék a műtárgyak, például a PCR-duplikátumok figyelembe vételét a későbbi elemzések során. Az egyes minták replikált leolvasásait az egyes génkészletekhez kerestük BLAT alkalmazásával (Kent, 2002). Minden olvasmányt és célgént lefordítottak mind a hat olvasási keretbe, és fehérjévé igazították annak érdekében, hogy a „referencia” szekvenciáktól távolabbi rokonságban lévő fajok olvasásait rögzítsék. Az egyes „adatbázisokban” a „referencia” szekvenciáknak megfelelő olvasmányokat az egyedi szekvencia-egyezések (azaz a replikált leolvasások) számaként és az egyezések teljes számaként (azaz több azonos olvasatot is beleértve) számként és az összes szám arányaként fejeztük ki. könyvtár mérete.
Félkvantitatív PCR-amplifikáció 16S rRNS és uidA gének
A DNS-szekvencia jelentős növekedése a következőket mutatja: Escherichia spp. T7-nél félkvantitatív PCR-rel validáltuk a uidA gént és a 16S rRNS gént használjuk normalizációs kontrollként. A PCR-körülményeket az S1. Függelék ismerteti.
A PCR, a klónozás és a Sanger szekvenálása mcr ‐ 2 és oqxB gének
A DNS-seq adatok megerősítése a mcr ‐ 2 gén és jelenléte vagy hiánya oqxB a beágyazott PCR sávok vizualizációját, majd klónozást és Sanger szekvenálást végeztünk. A klónozási módszerek részleteit az S1. Függelék ismerteti.
Molekuláris modellezés
Az OqxA és OqxB molekuláris modelljeit az AcrAB-TolC Multidrug Efflux Pump (PDB 5V5S.pdb) kristályszerkezetének felhasználásával állítottuk elő Modeller alkalmazásával (Sali és Blundell, 1993). Száz modellt készítettek, és kezdetben rangsorolták az OPUS_PSP (Lu et al., 2008). Öt legjobb pontszámú modellt finomítottak a Rosetta (Alford, USA) membránfehérje modul segítségével et al., 2015). Pontmutációkat hajtottak végre a vad típusú szekvencián Rosetta alkalmazásával. A szekunder struktúra változását és a szekunder struktúra elemek relatív mozgását egy házon belüli python szkript segítségével elemeztük.
Statisztikai analízis
Az rDNS-szekvencia-leolvasásokat a minták között normalizáltuk a minták összes elolvasott számára, és az összes olvasás százalékában adtuk meg. Annak érdekében, hogy megvizsgáljuk a baktériumok összetételének időbeli különbségeit, valamint a kezelési és kontrollcsoportok között, 2 (injektált vs kontroll, nem gyógyszeres) × 3 (időponttal) módon megismételt ANOVA-méréseket (SPSS v.24) hajtottunk végre, és a Benjamini – Hochberg-teszt, a hamis felfedezési arány (2014 kritikus értéke). Ahol szignifikáns különbségek voltak nyilvánvalóak, post hoc páronkénti összehasonlítást alkalmaztunk annak megállapítására, hogy hol vannak a különbségek, és adott esetben standard hibát alkalmaztunk 95% -os konfidencia intervallummal.
Köszönetnyilvánítás
A DAD-ot az NERC támogatása támogatta az IM számára (NE/N019288/1), az MTFL-t pedig a Coventry Egyetem Egészségügyi Élettudományi Kar Sport-, Testmozgás- és Élettudományi Kutatóközpontja támogatta. Ezúton szeretnénk köszönetet mondani S. Tompsettnek és S. Andrewsnak a technikai segítségért.
Összeférhetetlenség
A szerzők nem jelentenek összeférhetetlenséget.
Szerző hozzájárulás
L.A., J.R. és I.Y.M. tervezett kutatás; D.A.D., M.T.F.L., S.C. és I.Y.M. végzett kutatás; M.D. és I.Y.M statisztikai elemzést végzett; D.A.D., M.T.F.L., G.D.W., J.S., L.A. és I.Y.M. elemzett adatok; és M.T.F.L., G.D.W, J.R. és I.Y.M. írta a lap.
S1. Ábra. A növekedés értékelése E. coli szint a Nuflor-kezelésre adott válaszként. A 16S RNS- és uidA gének ugyanazon gDNS-készleteinek (240 ng, 120 ng vagy 60 ng) hígításainak sorozatát a To és a T7-nél használtuk a félkvantitatív PCR-amplifikációhoz. Az 1. és 3. ábrán az uidA 573 nts-os PCR-fragmense a T7-en és a To-nál, ennek megfelelően; A 2. és 4. ábrán a 16S RNS gén 500 nts-os PCR-fragmense a T7-nél és a To-nál. Ezen elemzés alapján nyilvánvaló volt, hogy a To uidA minta jelet produkált
- Az újrahasznosított gyógyszer segít az elhízott egereknek a fogyásban, javítja az anyagcsere-funkciót Disulfirammal történő kezelés
- Vörös-zsír injekció - Borjak karcsúsító kezelése A szépség legjobbja Koreában az EUNOGO által; Eunogo
- A rövid távú exenatid kezelés jelentős fogyáshoz vezet az elhízott nők egy részénél anélkül
- Az elhízott betegek súlyvesztésével járó pszichológiai változók orvosi kezelésre
- A lövedék hányásának (pylorus stenosis) kockázati tényezői és kezelése BabyCenter