A húgysav urolithiasis epidemiológiája, patofiziológiája és kezelése: Narratív áttekintés
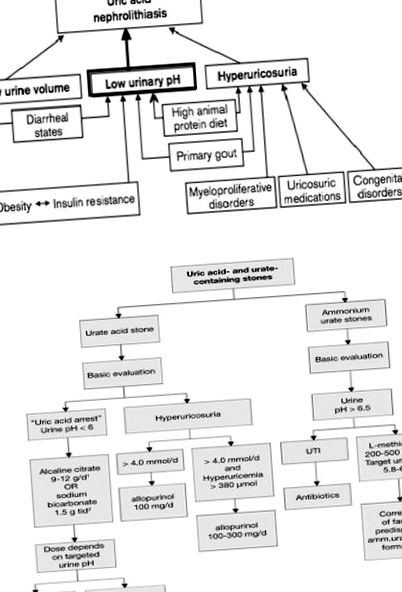
Grafikai absztrakt
Idézi az Urolithiasis - EAU Guidelines 2016 adaptációval.
Absztrakt
Fontos az epidemiológia, valamint a húgysav urolithiasis patofiziológiájának megértése e betegeknél a fogkő azonosításában, kezelésében és megelőzésében. A tartósan alacsony vizelet-pH, a hyperuricosuria és az alacsony vizelettérfogat a legfontosabb tényező a húgysav urolithiasis patogenezisében. A fogkő képződésének egyéb különféle okai a krónikus hasmenés, a vese hyperuricosuria, az inzulinrezisztencia, az elsődleges köszvény, az extra purin az étrendben, a daganatos szindrómák és a veleszületett hyperuricemia. A nem kontraszt-fokozott számítógépes tomográfia a választott radiológiai modalitás a vesekólikában szenvedő betegek korai értékeléséhez. Kivéve azokat az eseteket, amikor akut obstrukció, növekvő vérkémia, súlyos fertőzés vagy megoldatlan fájdalom van, a kezdeti kezelésnek orális kemolízissel történő orvosi oldódásnak kell lennie, mivel ez a módszer az esetek többségében hatékonynak bizonyult.
Háttér
Purin és húgysav anyagcsere
A húgysav (2,6,8-trioxipurin) a purin anyagcseréjének végterméke, és emberben nem ismert fiziológiai funkcióval. Az urikáz enzim hiányzik az emberből, és az emlősök többségében megtalálható, hogy a húgysavat allantoinná alakítja (10–100-szor jobban oldódik). A húgysav vizeletben való koncentrációja függ a vizelet pH-jától, a vizelet térfogatától és a húgysav kiválasztódásától. A vizelet pH-ja a húgysavban való oldhatóság legfontosabb tényezője. A húgysavból egyetlen proton elvesztését és ennélfogva a húgysav disszociációját két disszociációs állandó (pKa) szabályozza. Az első pH 5,5-es pKa szabályozza a húgysav átalakulását oldhatóbb anionos uráttá. A pH 10,3 második pKa értéke klinikailag nem szignifikáns, az átlagos vizelet pH-értéke 5,9, és általában 4,8 és 7,4 között van. 6,5 vizelet-pH mellett a húgysav többsége anionos urát formájában [4].
Endogén források
Normál körülmények között közel 300–400 mg/dL termelődik a de novo szintézissel és a szöveti katabolizmussal. A húgysav szintetikusan magas szintézise köszvény, mieloproliferatív rendellenességek, bizonyos veleszületett anyagcsere-hibák és kemoterápiában részesülő betegeknél fordul elő a gyors sejtforgalom miatt.
Exogén források
Magas purintartalmú étrend pl. hús, állati szervek, hal, édes kenyér és élesztő.
A bélrendszerben purin → szabad nukleinsavak → inozinsav → hipoxantin → xantin (xantin-oxidáz segítségével) → húgysav [5].
A vese kezelése és eltávolítása
A vese a húgysav kétharmadát választja ki. A bőr, a köröm, a haj, a nyál és a gyomor-bél traktus (GIT) kiküszöböli a fennmaradó harmadot. A GIT-ben a baktériumok a húgysav egy részét ammóniává és szén-dioxiddá alakítják, amely gázként távozik. Az ammóniát vagy felszívja és kiválasztja a vizelet, vagy a baktériumok hasznosítják energiaforrásként [6].
A szérum húgysav többsége (95%) nátrium-urát formájában van, és a glomerulusokban szabadon szűrhető, míg a maradék fehérjéhez kötött. A szűrt urát kilencvenkilenc százaléka újból felszívódik a proximális tekercselt tubulusban (PCT) komplex, egymást követő reabszorpció, szekréció és újbóli felszívódás révén, majd 50% -a visszaválasztódik a PCT-be. Ennek az urátnak a szekréciós felszívódása 80% -ban a disztális PCT-ben történik. Ezért a szűrt urát körülbelül 10% -a ürül a vizelettel. Az urát frakcionális kiválasztása koraszülött újszülöttek 60% -ától 3 gyermeknél 12% -ig, felnőtteknél 7% -ig terjed [7], [8].
Gyógyszerek és a húgysav vesekezelését befolyásoló tényezők
A húgysav vesekezelését befolyásoló legfontosabb tényezők közé tartozik a beteg hidratációs állapota és vizeletmennyisége, a szérum urátkoncentráció, a gyógyszerek és a sejten kívüli térfogat-tágulás, amely fordítottan arányos a szérum urátkoncentrációjával. A szalicilátok, a szulfinpirazon és a probenecid urikozurikusak, mivel blokkolják az urát felszívódását a PCT-ben. A tiazidok által okozott hyperuricosuria extracelluláris térfogat-kimerüléssel jár, és ezáltal növeli az urát szekréciót a PCT-ben. A terhesség alatti hyperuricosuria a magzati uráttermelésnek és a megnövekedett intravaszkuláris térfogatnak köszönhető [9], [10].
Járványtan
A húgysav-kő előfordulása földrajzilag változó, a világméretű előfordulás 5 és 40% között mozog. A nephrolithiasis gyakorisága az Egyesült Államokban megközelítőleg évi 0,5% körüli, a prevalencia aránya megmagyarázható, hogy növekszik. Valójában, amikor összefoglaljuk az Egyesült Államok Nemzeti Egészségügyi és Táplálkozási Vizsgálata II. És III. Felmérésének adatait, arról számoltak be, hogy a fogkőbetegségek előfordulási aránya a legfejlettebbeknél az 1976-os 3,8% -ról az 1980-as és 1994-es 5,2% -ra nőtt. országok [11]. Hasonlóképpen, az állapothoz kapcsolódó éves gazdasági kiadások is növekedtek az 1994-ben bejelentett 1,3 milliárd dollárról 2000-re jelentett 2 milliárd dollárra, függetlenül attól, hogy a különféle intézkedések, például a minimálisan invazív folyamatok, csökkennek a kórházi kezelési időszakokban, és a járóbeteg-szakrendelésekben nyújtott változtatásokat elfogadták [12].
Megállapították, hogy a húgysav nephrolithiasis az összes fogkő körülbelül 7–10 százalékát teszi ki. A veteránok adminisztrációs rendszerében lévő betegektől izolált kalkulumok azt találták, hogy körülbelül 9,7% csak húgysavból áll. Egy másik nagy sorozatban arról számoltak be, hogy húgysav-kőzetet mutattak ki a vizsgált kalkulumok 7 százalékában. A legtöbb szerző szerint ez az előfordulás a valódi gyakoriság téves kiszámítása; ugyanakkor jelzi ennek a feltételnek a fontosságát [13], [14].
A húgysavak számának előfordulása eltér a következőktől: életkor, nem, demográfiai adatok, sőt a helyi környezeti szempontok is. Például a hatvanöt évnél idősebb betegeknél beszámoltak arról, hogy hatezer beteget magában foglaló retrospektív kutatás során a húgysavak számának kétszerese volt az ifjúsági betegek prevalenciájánál. A férfiak körülbelül háromszor nőstényeknek tűntek [15], [16].
A húgysavak számarányának eltérései különböző etnikai csoportok között is változhatnak. A Hmong-betegek fele, akiknél vesekövek voltak, húgysav-számítással rendelkeztek, míg nem Hmong-betegeknél; csak 10% -ának volt ilyen állapota. Az előfordulási arány vagy a húgysav kalkulusa a fehéreknél 6, a nem fehéreknél 30 százalék volt. A frekvencia arány más nemzeteknél Indiában kevesebb, mint 1%, Izraelben 440%, Japánban pedig kevesebb mint 4% [17], [18].
Megállapították, hogy a környezet határozottan befolyásolja a húgysav kalkulusának képződését. A számításképződés előfordulási aránya 9% volt azoknál a gyári munkásoknál, akik meleg környezetben dolgoztak, míg a szokásos szobakörnyezetben dolgozóknál 0,9%. Ennek a vizsgálatnak az volt a hátránya, hogy a kutatás során nem számoltak be kalciumtartalomról [18], [19].
Kórélettan
A számképzés egy összetett eljárás, amely a vizelet biokémiai zavarait stimulálja a kristály magképződését, aggregációját és valószínűleg az adhéziót. Különböző kutatások bizonyították, hogy a Randall veseplakkjai szerepet játszanak a kalcium-oxalát képződésében, de nem a húgysav-kalkulumokban. A kutatók a perkután nephrolithotomia során összegyűlt veseszövetet vizsgálták [20], [21]. Valójában a vizelet savtartalmának fejlődését befolyásoló vizeletürítési rendellenességek magukban foglalják az alacsony vizelet pH-értékét (a fő tényezőt), a hipovolémiát és az alacsony vizeletszintet, valamint a hyperuricosuria-t (magyarázat szerint a napi vizelet-húgysav meghaladja a nőknél a 750 mg/napot és a 800 mg/napot férfiaknál) [22], [23].
Tartósan alacsony vizelet-pH
A húgysav urolithiasis általában tartósan alacsony vizelet pH-val társul. Szinte minden húgysav-kalkulációjú betegnek állandóan alacsony a vizelet-pH-ja, míg a többség normális mennyiségű urátot választ ki. [24], [25] Másrészről azok a betegek, akiknek nincsenek veleszületett vagy elért állapotai, amelyek hajlamosítják a húgysav-kalkulumok kialakulását vagy idiopátiás húgysav nephrolithiasis vagy „köszvényes diatézis [25], [26]. Mindkettő az elsődleges köszvény szindrómáját jelenti, és ezt példázza a magas szérum húgysav, a húgysav csökkent frakcionális kiválasztása és a vizelet állandóan alacsony pH-ja. Úgy gondolják, hogy az alacsony vizelet-pH a bázikus sav-bázis kémia és a húgysav oldhatósága révén húgysav-kalkulumokat indukál [9], [27].
Alacsony vizelet-pH-értékű, de rendszeres húgysav-szekrécióval rendelkező betegeknél kialakulhat húgysav-kő, míg másoknak normál vagy megnövekedett vizelet-pH-értékkel, de további urát-szekrécióval nem. Ez a tény a húgysav vízben történő disszociációjával bizonyítható. Az urát N-9 helyzetében lévő nitrogén vízben oldva szabad protont kaphat a húgysav kifejlesztéséhez.
Ennek a reakciónak az első savas disszociációs állandója (pKa) 5,5 pH; a második pKa-nak nincs fiziológiai jelentősége. A húgysav oldhatósági állandója (Ksp) körülbelül 100 mg/l vizes oldatokban 37 ° C-on, míg az urát 20-szor jobban oldódik. Az urát és a húgysav egyenlő arányban léteznek a pKa-val megegyező pH-n (Henderson-Hasselbach-egyenlet) [10], [29]. Következésképpen, ha 200 mg urátot adunk 1 literes vizes oldathoz, amelynek pH-értéke 5,5, 37 ° C-on, 100 mg húgysavvá válik, és a maradék továbbra is urát. Éppen ellenkezőleg, ha 1200 mg urátot adunk azonos térfogatra 6,5 pH-érték mellett, akkor 1100 mg marad oldható urát formájában. Ezek a kölcsönhatások a húgysav-disszociációs görbe felfelé tolódását közvetítik ezen a pH-n, amely majdnem 7,2-es pH-nál fennsíkkal rendelkezik [11], [30].
A húgysav-kalkulációval közölt, folyamatosan savanyított vizelet pontos mechanizmusa azonban még mindig nem világos. Ennek ellenére számos különféle hipotézist javasoltak. Összehasonlítottuk azokat a résztvevőket, akiknek idiopátiás húgysav-nephrolithiasisuk van, és a kontrollált étrendben szokásos alanyokat [31]. Az összehasonlítás azt mutatta, hogy a húgysav-számológépek tartósan savas vizelettel rendelkeznek, valamint savterhelésük kevesebb ammónium formájában ürül ki. Ehelyett a titrálható sav szekréciójának nagyobb mennyiségétől függenek. Ezenkívül ezek a betegek kevésbé hatékonyan reagálnak az ammónium-klorid orális savterhelésére, amit megerősít a vizeletből származó ammónium kiválasztása 7-szer kisebb mennyiségben, mint a szokásos résztvevőknél.
Ezek a megállapítások feltételezték, hogy ezeknek a betegeknek az ammónium-szekréció zavara van, ami jelentős vizelet-puffer elvesztését eredményezi. E puffer nélkül a H koncentrációjának enyhe növekedése jelentősen csökkentheti a pH-t. A kutatók szerint a glutamináz és/vagy glutamát dehidrogenáz enzimek hibái, amelyek a glutamint ammóniává és ketoglutaráttá metabolizálják, károsodhatnak az ammónium szekréciójában. Sőt, azt is elmélete szerint, hogy az út alacsony glutaminfogyasztása megváltoztathatja azt más utakra, amelyek glutamint használnak, ami hiperurikémiát eredményez [8], [32], [33].
Ezt a két feltételt segítik a glutamát megnövekedett plazmaszintjeinek megállapításai azon résztvevőknél, akik húgysav nephrolithiasisban szenvednek, és 15 N-vel jelzett glicin beadása esetén több 15 N-t integráltak a húgysavba, mint az ammónium, szemben a kontrollokkal. Mindazonáltal meg kell említeni, hogy más kutatók nem találtak egyértelmű eltérést a vese glutamináz aktivitása között a köszvényes és a köszvény nélküli résztvevők között.
A vese glutamin katabolizmusának pontos funkciója a vizelet nem megfelelő ammóniumkibocsátásának okaként még nem egyértelmű. A húgysavak képződéséhez a pH-nak tartósan alacsonynak és nemcsak alacsonynak kell maradnia. A nem kalkulus képzőknél a vizelet időnként elég savasságot képes fejleszteni a kristályok kicsapására a normál húgysavkoncentráció ellenére; bár úgy gondolják, hogy az étkezés során bekövetkező átmeneti, vizelet-alkalizálás meggátolja a jóhiszemű kalkulációvá való progressziót. A vizelet időszakos alkalikus dagályai feloldanak minden húgysav-kristályt, amely az átmenetileg savas vizelet következtében jött létre, amely ezt a modellt támogatja. Azok az állapotok, amelyek elméletileg lúgos árapályok hiányához vezethetnek: a bikarbonát vese tubuláris újrafelszívódása, a glomeruláris szűrés csökkenése, a bikarbonát szűrt terhelésének csökkenéséhez vezet, és a gyomorsav szekréciójának hiánya. A rendelkezésre álló információk arra utalnak, hogy egy fel nem ismert veseelégtelenség gyanúja szerint a fiziológiás vizelet alkalikus árapályának kialakulása nem a gyomorsav-szekréció károsodása [9], [34], [35].
Hyperuricosuria
A vizelet rendszeres pH-jával járó hyperuricosuria kevert kalkulus képződést is eredményezhet, amely urátból és kalcium-oxalátból áll. Annak ellenére, hogy az urát legtöbbször jobban oldódik, mint a húgysav, meg kell jegyezni, hogy ez nem számottevően. A mononátrium-urát nagy mennyiségben kicsapódik az oldatból, és úgy gondolják, hogy kalcium-oxalát kristályosodáshoz vezet bármelyikük révén; a litogenezis, a heterogén nukleáció és a kisózás előfordulásának makromolekuláris inhibitorainak csillapítása. A hyperuricosuria legtöbbször táplálkozási indiszkrécióból származik, annak ellenére, hogy az URAT1 csatorna mutációi veleszületett vese hypouricemic hyperuricosuria-t eredményezhetnek [7], [36], [37].
Alacsony vizeletmennyiség
A csökkent vizeletmennyiség megnöveli a litogén oldott anyagok vizeletkoncentrációját. Az urát magas koncentrációja a húgysav korlátozott oldhatósága következtében húgysav- és nátrium-urát-kicsapódást eredményezhet. Következésképpen a húgysav kalkulációja elterjedt a trópusokon és a meleg környezetben [38], [39].
A kristályosodás makromolekuláris inhibitorai
A vizelet olyan tényezőket tartalmaz, amelyek gátolják a kristályképződést, amelyek modulálják a húgysav kristályosodását és a fogkő képződését. A vizelet felületaktív anyagai, a glikoproteinek és a glikozaminoglikánok (GAG) gátló hatást gyakorolnak a húgysav kristályosodására [40]. A vizsgálatok szignifikánsan alacsonyabb GAG-szinteket mutattak ki a húgysavképzők genetikailag és földrajzilag izolált vizeletében. Egyelőre nem világos, hogy az ilyen inhibitorok hiánya hogyan okozhatja a húgysav kalkulus képződését [40], [41], [42].
A családi, genetikai és környezeti tényezők hajlamosak a vizeletkő képződésére. A 10q21-q22 kromoszómán található ZNF365 génről beszámoltak a húgysav urolithiasisával. Annak ellenére, hogy ez a DNS négy különféle fehérjét kódol helyettesítő splicelés útján, csak az egyik kéri a húgysavak számának előrehaladását [43]. Ezen gének pontos szerepe még mindig nem világos.
Másrészt a DNS új homológ génje, amely nem nyilvánvaló az egereknél, miközben általában kifejezhetetlen génként van jelen mind a régi, mind az új világ majmában, úgy tűnik, hogy megjelenik a miocén korszakban, amely abban az időben forog, amikor a majmok véletlenül elvesztették célját urikáz. Ennek a génnek a terméke valószínűleg megvéd a hiperurikémia káros hatásaitól az uricase gén elnémítása miatt, miközben nem veszíti el pozitív hatásait [43], [44].
Jövőbeni vizsgálatokra van szükség annak kiderítéséhez, hogy a géntermék milyen tényleges szerepet tölt be a szervezetben, és hogyan alakul ki a húgysav-kő. Ennek ellenére jelenleg ennek a szerepnek a magyarázata minden erőfeszítés pusztán hipotetikus lesz (1. ábra A, B).
- A húgysav urolithiasis epidemiológiája, patofiziológiája és kezelése Narratív áttekintés -
- A cukorral édesített italok és a szérum húgysavkoncentrációinak szisztematikus áttekintése és
- A kutya és a macska elhízása a patofiziológia, az epidemiológia, a VMRR áttekintése
- Diétás és életmódbeli ajánlások az urolithiasis megelőzésére Szisztematikus szakirodalmi áttekintés -
- Az urolithiasis diétás kezelése (Proceedings) DVM 360