A prenatális hypoxia és a szülés utáni, magas zsírtartalmú étrend szinergetikus hatása a szív- és érrendszeri patológia kialakulásában fiatal patkányokban
Élettani Tanszék,
Női és Gyermekegészségügyi Kutatóintézet,
Kardiovaszkuláris Kutatóközpont,
Mazankowski Alberta Szívintézet, Alberta Egyetem, Edmonton, Kanada
Szülészeti és Nőgyógyászati Osztály,
Női és Gyermekegészségügyi Kutatóintézet,
Kardiovaszkuláris Kutatóközpont,
Mazankowski Alberta Szívintézet, Alberta Egyetem, Edmonton, Kanada
Női és Gyermekegészségügyi Kutatóintézet,
Kardiovaszkuláris Kutatóközpont,
Mazankowski Alberta Szívintézet, Alberta Egyetem, Edmonton, Kanada
Női és Gyermekegészségügyi Kutatóintézet,
Kardiovaszkuláris Kutatóközpont,
Mazankowski Alberta Szívintézet, Alberta Egyetem, Edmonton, Kanada
Élettani Tanszék,
Szülészeti és Nőgyógyászati Osztály,
Női és Gyermekegészségügyi Kutatóintézet,
Kardiovaszkuláris Kutatóközpont,
Mazankowski Alberta Szívintézet, Alberta Egyetem, Edmonton, Kanada
Az újranyomtatási kérelmek és egyéb levelezések címe: S. T. Davidge, Szülészeti és Nőgyógyászati Osztály/Fiziológia, 220 HMRC, Univ., Alberta, Edmonton, AB, Kanada T6G 2S2 (e-mail: [e-mail védett]).
Absztrakt
A hipoxia okozta IUGR rágcsáló modelljének felhasználásával csoportunk korábban részletesen leírta a prenatális hypoxia hosszú távú hatásait az érrendszer működésére (25, 26), valamint a szív morfológiájára, működésére, anyagcseréjére és ex vivo érzékenységére. ischaemia-reperfúziós (IR) sérüléshez (33, 34, 47). Érdekes módon azt figyeltük meg, hogy az IUGR-lel bonyolult terhességből történő születéshez kapcsolódó szív- és érrendszeri patológiák (mint például az endotheliális diszfunkció, a bal kamra diasztolés diszfunkciója és a pulmonalis hipertónia) időskorúaknál (12 hónapos) voltak jelen, de fiataloknál nem, felnőtt (4 hónapos) állatok (33). Ezenkívül a magzati fejlődés során hipoxiának kitett fiatal felnőtt utódokban előforduló kardiovaszkuláris patológiákat (például fokozott érzékenységet az IR sérülésekre) súlyosbítani látszott az öregedés (26). Ezek az eredmények arra utalnak, hogy a hipoxia okozta programozás növelheti az érzékenységet további sértésekre (például HF diétákra).
Csoportunk legújabb tanulmányai azt is leírták, hogy a prenatális hipoxiás sértésnek kitett utódok hajlamosabbak a másodlagos sértésekre, például az étrendbe foglalt elhízásra (15, 32). Például a magas zsírtartalmú étrendek (HF; 45% zsírtartalom) posztnatális fogyasztása az elválasztástól a korai felnőtté válásig a hipoxiának prenatálisan kitett utódok által a metabolikus szindróma (MetS) összetevőinek korábbi és súlyosabb kialakulását eredményezte. . Ezek közé tartozott az inzulinrezisztencia nagyobb szintje, a diszlipidémia, a hasi zsírlerakódás és a keringő gyulladásos markerek (32). Nem ismert azonban a posztnatális táplálkozási sértések (például a HF-étrendnek való kitettség) képessége a szív- és érrendszeri patológiák súlyosbítására/kiváltására a hipoxia okozta IUGR-nek kitett fiatal felnőtt utódokban.
A resveratrol (Resv), más néven 3,5,4′-trihidroxi-transz-stilbene, olyan molekula, amelyről bebizonyosodott, hogy megakadályozza az érelmeszesedést, javítja az érrendszer működését, csillapítja a bal kamra hipertrófiáját és rezisztenciát biztosít a szív iszkémiás károsodásával szemben (14). ). Nemrégiben bebizonyítottuk, hogy a Resv enyhíti az étrend által kiváltott MetS-re való fokozott érzékenységet olyan fiatal felnőtt utódokban, amelyeket méhen belüli hipoxiának tettek ki (15). A Resv hatását a prenatális hipoxiás sértésnek kitett fiatal felnőtt utódok szív- és érrendszerére azonban még nem vizsgálták. Ezért további feltételezésünk volt, hogy a méhen belüli hipoxiának kitett HF-diéták Resv-vel történő kiegészítése megakadályozhatja a korai MetS-szel járó kóros kardiovaszkuláris állapotokat is.
Jelen tanulmány célja annak megvizsgálása volt, hogy a HF-diéta beadása az IUGR-ben született utódok számára előidézheti-e a magas vérnyomás, vaszkuláris diszfunkció és/vagy kóros szívműködés vagy morfológia korábbi kialakulását. A vizsgálat másodlagos célja annak meghatározása volt, hogy a Resv posztnatális beadása javíthatja-e a HF-diéta fogyasztásával járó kardiovaszkuláris állapotokat hipoxia által kiváltott IUGR-nek kitett utódok által.
Állatmodellek és kísérleti beavatkozások
Ebben a vizsgálatban az összes eljárást az Alberta Egyetem Állatvédelmi Bizottsága hagyta jóvá (301/11/09D protokollszám), és összhangban vannak a Kanadai Állatgondozási Tanács irányelveivel és a „Laboratóriumok gondozásának és használatának útmutatójával”. Állatok ”című kiadványt a National Institute of Health kiadta.
Hypoxia által kiváltott IUGR modell (A és B vizsgálatok).
A posztnatális étrend okozta elhízás (A vizsgálat).
Elválasztás után, 3 hetes korban hím utódok minden alomból (IUGR; n = 22 utód 6 alomból és kontrollból; n = 24 utódot 6 alomból) véletlenszerűen kiosztottunk egy LF étrend (-1,1 g száraz wt -1) fogadására, és kiszámítottuk a korábban leírtak szerint (34, 45, 46). A szívműködés méréseit 10 percenként végeztük egy 90 perces protokoll alatt, amely 40 perces stabilizációs periódust (aerob), 10 perc áramlás nélküli iszkémiát és 40 perc reperfúziót (reperfúziót) tartalmazott. Az áramlás nélküli iszkémia sértésének időtartama csoportunk korábbi kísérletein alapult hasonló modell és módszerek alkalmazásával (34). Szívek, amelyek nem reverzibilis szívritmuszavart mutattak (n = 5) kizárták.
Érvizsgálatok (A vizsgálat).
Közvetlenül a szív extrakciója után az érszövetek boncolását jéghideg fiziológiás sóoldatban (PSS) végeztük (mmol/l-ben): 10 HEPES, 5,5 glükóz, 1,56 CaCl2, 4,7 KCl, 142 NaCl, 1,17 MgSO4 és 1,18 KH2PO4, pH 7.4. A kis mesenterialis artériákat elkülönítettük és megtisztítottuk az összes környező zsír- és kötőszövettől. Az artériákat nyomásmérőre (Living Systems, Burlington, VT) szereltük fel, hogy lehetővé tegyük a belső átmérő változásainak izobár mérését.
30 perces egyensúlyi periódus alatt az edényeket fokozatosan növelték a nyomáson 80 Hgmm-re, majd visszatértek 60 Hgmm-re. A kísérlet hátralévő részében az edényeket 60 Hgmm nyomáson tartottuk. A metilkolinra (MCh; 0,1 nmol/l - 100 μmol/l) érkező vaszkuláris válaszok vizsgálatához koncentráció-válasz görbét (CCRC) hajtottunk végre inhibitorok hiányában vagy jelenlétében, a fenilefrinnel való szűkítést követően (PE, 1 μmol/l). Először véletlenszerűen választottak egy fürdőt a nitrogén-monoxid-szintáz (NOS) inhibitor beiktatására N ω -nitro-1 -arginin-metil-észter-hidroklorid (1 -NAME, 100 μmol/l), míg a második fürdőt kontrollként tartottuk. Az MCh CCRC befejezése és az azt követő mosási periódus után a ciklooxigenáz inhibitor meclofenamát (1 μmol/l) mellett 1 -NAME-t alkalmaztunk. Ezután egy második MCh CCRC-t hajtottak végre prosztaglandinok és nitrogén-oxid együttes gátlásának jelenlétében. Végül az erek passzív tulajdonságait úgy értékeltük, hogy a nyomást fokozatosan 0-ról 140 Hgmm-re növeltük Ca 2+ mentes PSS és papaverin (10 μmol/l) jelenlétében.
Statisztikai analízis
Az elemzéshez az egyes gátakból csak egy utódot használtak fel minden meghatározáshoz. Ezért a gátakat tekintették kísérleti egységnek. Az adatokat átlag ± SE-ként adjuk meg, hacsak másként nem jelezzük. Az adatok eloszlását D'Agostino és Pearson normalitás teszt segítségével teszteltük. Két csoport összehasonlítását értékeltük párosítás nélkül t-teszt vagy Mann-Whitney teszt az adatok megoszlásától függően. A táplálkozási beavatkozást követően négy csoportban végzett mérések közötti különbségeket kétirányú ANOVA-val, diétával és IUGR-rel mint variációs forrásként teszteltük. Ezután Bonferroni post hoc tesztet alkalmaztunk a replikációs átlag csoportok szerinti összehasonlítására. A P érték
1. táblázat: Hemodinamikai paraméterek tudatos patkányokban nyugalmi állapotban és akut légfúvás okozta stressz után
Az értékek jelentése ± SE; n = 6 minden csoportban. Resv, resveratrol.
2. táblázat: Echokardiográfiai paraméterek az IUGR-ben és az alacsony és magas zsírtartalmú étrendnek kitett utódok kontrollja
Az értékek jelentése ± SE; n = 6 minden csoportban.
RVET, jobb kamrai kidobási idő; PAAT, a pulmonalis artéria gyorsulási ideje; LV, bal kamra; Ao, aorta; IVRT, izovolumikus relaxációs idő.
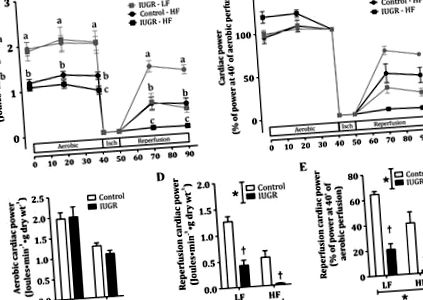
1. ábra.A vizsgálat: a szív teljesítménye stabilizálás (aerob) és reperfúzió után 10 perc áramlás nélküli ischaemia (isch) után kontroll- és intrauterin növekedési korlátozású (IUGR) utódokban, akik alacsony zsírtartalmú (LF) vagy magas zsírtartalmú (HF) étrendet kapnak. Az ex vivo szívteljesítményre vonatkozó adatok a teljes szívteljesítmény átlagának ± SE értékeként jelentve (joule · min -1 -1 g száraz wt -1) (A) (34, 45, 46) és a szív teljesítménye a szív teljesítményéhez viszonyítva 40 perc aerob perfúzió után (B). A Control (körök) és az IUGR (négyzetek) szívek LF (árnyékolt szimbólumok és vonalak) vagy HF (folytonos szimbólumok és vonalak) diétát tápláltak 9 hétig. C és D: az aerob és a reperfúziós időszakban kialakult átlagos maximális szívteljesítmény. E: relatív szíverő helyreállítás reperfúzió alatt. n = 6-10 csoportonként. *P
2. ábra.B. tanulmány: a szív teljesítménye stabilizálás után (aerob) és reperfúzió után 10 perc áramlás nélküli ischaemia (isch) után a kontroll és az IUGR utódok között, akik HF vagy HF + resveratrol (Resv) étrendet kaptak. Az ex vivo kardiális teljesítmény adatok a teljes szívteljesítmény átlagának ± SE értékeként [(szisztolés csúcsnyomás - maximális előfeszítés · szívteljesítmény · 0,13)/g száraz tömeg%]] (joule · min -1 -1 g száraz wt -1) (A) és a szív teljesítménye a szív teljesítményéhez viszonyítva 40 perc aerob perfúzió után (B). A kontroll (körök) és az IUGR (négyzetek) szívek HF diétát adtak (nyitott szimbólumok és szaggatott vonalak) vagy anélkül (folytonos szimbólumok és vonalak) Resv 9 hétig. C és D: az aerob és a reperfúziós időszakban kialakult átlagos maximális szívteljesítmény. E: relatív szíverő helyreállítás reperfúzió alatt. n = 6 csoportonként. *P
Az IUGR és a posztnatális diéta hatása az ex vivo érfunkcióra
Inhibitorok hiányában az összes kísérleti csoport mesenterialis artériájának szegmensei összehasonlítható kontraktilis választ mutattak az 1 μmol/l PE-vel szemben (3. ábraA). Az l -NAME-vel végzett inkubálás az összes kísérleti csoport artériás szegmenseinek a PE-re adott kontraktilis válaszának jelentős növekedését okozta, nevezetesen azok kivételével, akik prenatális hipoxiás sértésnek vannak kitéve és HF diétát kaptak. Nem volt különbség a PE érrendszeri válaszában az l -NAME és az MCh inkubálása után (3. ábraB).
3. ábra.Ex vivo érfunkciós paraméterek. Az érösszehúzódás 1 μmol/l fenilefrinre (PE) reagálva, nitrogén-oxid (NO) szintáz inhibitor hiányában vagy jelenlétében N ω -nitro-1 -arginin-metil-észter-hidroklorid (1 -NAME, 100 μmol/l) (A) vagy l -NAME plusz a ciklooxigenáz inhibitor meklofenamát (Meclo, 1 μmol/l) (B). C: a NO, a prosztanoidok vagy a nem NO, a nonprostanoid mechanizmusok becsült százalékos hozzájárulása a teljes metilkolin (MCh) által indukált értágulathoz. D: passzív válaszok, az ér átmérőjének változása, 0 és 140 Hgmm közötti nyomásnövekedésre. Különböző betűk (a és b) statisztikailag szignifikáns különbségeket mutatnak a kísérleti csoportok között a Bonferroni post hoc tesztet követően minden egyes időpontban. †P
Nem figyeltünk meg különbségeket a csoportok között az MCh-ra adott vaszkuláris válaszokban vagy a fő értágító mechanizmusok (például nitrogén-oxid és prosztanoidok) becsült hozzájárulásában az MCh vaszkuláris válaszában (3. ábra)C). Sem az IUGR, sem a HF nem befolyásolta a mesenterialis artériák kezdeti átmérőjét. Az intraluminalis nyomás változásaira adott passzív válasz azonban azt mutatta, hogy a HF-étrendet kapó utódok artériás szegmensei a vaszkuláris megfelelés növekedését mutatják, a prenatális történelemtől függetlenül (3. ábraD).
Ezeknek a megfigyeléseknek nagyon fontos klinikai vonzata van. Először is azt javasolják, hogy a prenatális hipoxiának való kitettség hosszú távú következményei az élet korai szakaszától kezdve aktívan befolyásolhatják az utódok biológiai rendszereit, annak ellenére, hogy a betegség nyilvánvaló megnyilvánulása nincs. Másodszor, ezek az eredmények arra utalnak, hogy a postnatalis beavatkozások, amelyek bizonyos postnatalis stresszorok expozíciójának csökkentésére irányulnak, hatékonyak lehetnek a nemkívánatos kardiovaszkuláris és anyagcsere-rendellenességek jövőbeni kockázatának csökkentésében, annak ellenére, hogy nincsenek hatással magára a korai programozott állapotra. Ezért a korai beavatkozás azonosítása és a korai beavatkozás lehetősége bizonyos fokú „korai programozással” rendelkező személyeknél óriási potenciállal bír a krónikus betegségek egészségügyi rendszerre nehezedő terheinek csökkentésében.
Vizsgálatunk további érdekes megállapítása az volt, hogy a kiindulási vérnyomás különbségeket egyik kísérleti csoportban sem figyeltek meg. Noha csoportonként csak hat állatot elemeztünk, módszereink eléggé érzékenyek voltak a szisztolés vérnyomás fiziológiailag releváns növekedésének megfigyelésére közvetlenül a HF-étrendben részesülő utódok akut stresszét követően (mind kontroll, mind IUGR). Ezek az eredmények kompatibilisek a metabolikus szindrómát és a magas vérnyomást (36) a kardiovaszkuláris autonóm deregulációval összekötő korábbi jelentésekkel (31).
Vaszkuláris funkcióval kapcsolatos vizsgálatunk során a nitrogén-oxidnak a bazális vaszkuláris tónushoz való hozzájárulásának jelentős csökkenését figyeltük meg az IUGR-csoportban, amely HF-étrendet táplált, amit a PE-szűkület növekedésének hiánya figyelhet meg l -NAME jelenlétében. csoport. Érdekes módon ez a különbség nem volt nyilvánvaló a nitrogén-oxid és a prosztanoidok együttes gátlását követően. Ennek oka lehet azonban az idő alatt csökkent vazokonstriktor kapacitás, mivel csak ebben a csoportban csökkent az idő múlásával az MCh iránti érzékenység. Ezért a növekedés korlátozása és a HF diéta kombinációja károsnak látszott az érrendszer működésére, míg az egyes sértések nem. Ezenkívül jelentősen megnőtt az érrendszeri megfelelés a HF-étrendnek, amelyet nem figyeltek meg az IUGR esetében. Ezért az érrendszer átalakításának változásai csak az étrendtől függtek és függetlenek a növekedés korlátozásától.
Összefoglalva, a jelen tanulmányban bemutatott eredmények összhangban vannak korábbi eredményeinkkel, amelyek igazolják, hogy az IUGR-t okozó prenatális sértések hosszú távú változásokhoz vezethetnek a szív- és érrendszeri funkciókban, és hozzájárulhatnak a felnőtt utódok nagyobb érzékenységéhez a másodlagos sértések iránt. Pontosabban kimutattuk, hogy a zsírban gazdag étrend posztnatális beadása különösen káros volt a prenatális hipoxiás sértésnek kitett utódok szív- és érrendszeri működésére nézve, és a szívbetegségek korábbi kialakulását eredményezte. Ezenkívül kimutattuk, hogy a HF étrendek Resv-vel történő kiegészítése javította az ischaemia iránti szívérzékenységet a magzati fejlődés során hipoxiának kitett utódok HF-étrendjének fogyasztása miatt. Végül bebizonyítottuk, hogy az IUGR-hez vezető prenatális hypoxiás sértések hosszan tartó változásokat okozhatnak a pulzusszámot szabályozó mechanizmusokban felnőtt utódoknál.
Perspektívák és jelentőség
Ez a tanulmány bemutatja, hogy bizonyos posztnatális táplálkozási sértések hogyan működhetnek „második találatként”, káros kardiovaszkuláris hatásokkal a fogékony populációkra (például az IUGR-ben születtekre), és bizonyítékokat szolgáltat arra vonatkozóan, hogy ez a megszerzett érzékenység javítható posztnatális farmakológiai beavatkozásokkal. Összefoglalva eredményeink rávilágítanak a prenatális szakasz fontosságára a szív- és érrendszeri patológiák kialakulásában, és betekintést nyújtanak abba, hogy miért igényelhetik a szorosabb klinikai megfigyelést a nyugati világban élő és IUGR-ben született populációk. Mivel a nyugati népesség 15% -ának növekedése korlátozott, és közel 50% -a túlsúlyos vagy elhízott, eredményeink társadalmunk nagy részének fontos klinikai következményekkel járnak.
Ezt a munkát a Női és Gyermekegészségügyi Kutatóintézet (WCHRI), a kanadai Egészségügyi Kutatóintézet (CIHR) kutatási támogatásával, valamint a kanadai Szív és Stroke Alapítvány (H&S) személyi díjával támogatták. C. F. Rueda-Clausent, J. S. Mortont és V. W. Dolinsky-t a H&S és az Alberta Heritage Foundation for Medical Research (AHFMR) támogatja. S. T. Davidge az Alberta Innovates-Health Solutions (AI-HS) által támogatott AHFMR-tudós és a női szív- és érrendszeri egészséggel foglalkozó kanadai kutatási elnök. J. R. B. Dyck AHFMR Senior Scholar, amelyet AI-HS támogat.
A szerző (k) nem jelentenek be pénzügyi vagy egyéb összeférhetetlenséget.
A szerző hozzájárulása: C.F.R.-C., J.S.M., V.W.D., J.R.D. és S.T.D. a kutatás megtervezése és megtervezése; C.F.R.-C., J.S.M. és V.W.D. elvégzett kísérletek; C.F.R.-C. és J.S.M. elemzett adatok; C.F.R.-C., J.S.M., V.W.D., J.R.D. és S.T.D. értelmezett kísérletek eredményei; C.F.R.-C. elkészített figurák; C.F.R.-C. megfogalmazott kézirat; C.F.R.-C., J.S.M., V.W.D., J.R.D. és S.T.D. szerkesztett és átdolgozott kézirat; C.F.R.-C., J.S.M., V.W.D., J.R.D. és S.T.D. a kézirat jóváhagyott végleges változata.
KÖSZÖNETNYILVÁNÍTÁS
V. W. Dolinsky jelenlegi címe: Manitoba Gyermekegészségügyi Intézet és Manitoba Egyetem, Winnipeg, Kanada.
- Az étrend okozta elhízás és glükóz intolerancia kialakulása C57Bl6 egerekben zsírtartalmú étrenden
- Milyen hatással van az alacsony fehérjetartalmú étrend krónikus vesebetegségben szenvedő, nem cukorbeteg felnőtteknek
- Svédország alacsony szénhidráttartalmú, magas zsírtartalmú étrendet javasol az elhízás elleni természetes termékek elleni küzdelemhez
- A mediterrán étrend hatása a cukorbetegség iránti szükségletre és az újonnan diagnosztizált remisszióra
- Az alacsony szénhidráttartalmú ketogén étrend és az alacsony zsírtartalmú étrend hatása a hangulatra, az éhségre és egyebekre