A táplálkozás hatása a pulmonalis artériás hipertóniára
María Callejo
1 Farmakológiai és Toxikológiai Tanszék, Orvostudományi Kar, Universidad Complutense de Madrid, 28040 Madrid, Spanyolország; se.mcu@ojellac.airam
2 CIBER Enfermedades Respiratorias, Ciberes, 28029 Madrid, Spanyolország; tac.cinilc@arebrabj
3 Instituto de Investigación Sanitaria Gregorio Marañón (IISGM), 28007 Madrid, Spanyolország
Joan Albert Barberá
2 CIBER Enfermedades Respiratorias, Ciberes, 28029 Madrid, Spanyolország; tac.cinilc@arebrabj
4 Tüdőgyógyászati Klinika, Clínic-Institut d'Investigacions Biomèdiques August Pi i Sunyer (IDIBAPS), Universitat de Barcelona, 08036 Barcelona, Spanyolország
Juan Duarte
5 Farmakológiai Tanszék, Gyógyszerészeti Iskola, Universidad de Granada, 18071 Granada, Spanyolország; se.rgu@etraudmj
6 CIBER Enfermedades Cardiovasculares, CiberCV, 28029 Madrid, Spanyolország
7 Instituto de Investigación Biosanitaria (ibs. Granada), 18012 Granada, Spanyolország
8 Centro de Investigaciones Biomédicas (CIBM), 18016 Granada, Spanyolország
Francisco Perez-Vizcaino
1 Farmakológiai és Toxikológiai Tanszék, Orvostudományi Kar, Universidad Complutense de Madrid, 28040 Madrid, Spanyolország; se.mcu@ojellac.airam
2 CIBER Enfermedades Respiratorias, Ciberes, 28029 Madrid, Spanyolország; tac.cinilc@arebrabj
3 Instituto de Investigación Sanitaria Gregorio Marañón (IISGM), 28007 Madrid, Spanyolország
Absztrakt
1. Tüdő hipertónia
1.1. Etiológia
1.2. Kórélettan
1.3. Jelenlegi farmakológiai terápiák
Az elmúlt évtizedekben a sejtszintű és molekuláris mechanizmusok, valamint a jelátviteli utak intenzív kutatása jobb megértést adott a PAH kórélettanában, következésképpen a különböző farmakológiai kezelések azonosításában. Sajnos a PAH-ra nem létezik végleges gyógymód. Jelenleg a PAH számára jóváhagyott öt terápiás osztály a Ca 2+ belépést és a három fő diszfunkcionális endotheliális utat célozza meg: NO, prosztaciklin és endothelin-1 útvonalat [27,28]. Az 5-ös típusú ciklikus nukleotid-foszfodiészteráz (PDE-5) inhibitorai, a szildenafil és a tadalafil fokozzák az endogén NO hatását és elősegítik az értágulatot [5,27,28]. Az oldható guanilát-cikláz (sGC) szintén az NO jelátviteli útban hat, katalizálva a GTP átalakulását cGMP -vé. Az sGC stimulátor riociguat elősegíti a cGMP szintézisét, elősegítve az értágulatot és gátolva a sejtproliferációt. A riociguat hatása független a NO rendelkezésre állásától. A rendelkezésre álló prosztaciklinnel kapcsolatos terápiák közé tartoznak a szintetikus (epoprostenol), a prosztaciklin analógok (treprostinil és iloprost) és a prosztaciklin receptor agonista szelexipag [27,28]. Az endotelin-1 receptor antagonisták (ERA-k) közé tartozik a bozentán, a macitentán és az ambriszentán [5,27,28].
Annak ellenére, hogy a jelenleg jóváhagyott gyógyszerek monoterápiaként kedvező hatást mutattak a klinikai, funkcionális és hemodinamikai kimenetelre, a betegség progresszióját gyakran megfigyelik. A PH 5. világszimpóziumán és számos randomizált, kontrollált vizsgálatból származó magas szintű bizonyítékok alapján javasolták a szekvenciális kombinált terápia alkalmazását, legalábbis a monoterápiára nem megfelelő válaszban szenvedő PAH-s betegeknél, és előrehaladott betegségben szenvedő betegek (New York Heart Association III/IV funkcionális osztály). Ezenkívül a nagyobb terápiás válasz elérése érdekében a diagnózis idején jelenleg a kezdeti kombinált terápia ajánlott. Ezenkívül a hármas kombinációs kezeléseket is figyelembe veszik súlyos PAH esetén, amikor a kettős kezelés sikertelen [27,29].
1.4. Nem gyógyszeres terápiák
Randomizált, kontrollált vizsgálatokban a testgyakorlat javítja a testtűrést, a funkcionális kapacitást és az életminőséget, pozitív hatással van a szociális, érzelmi és pszichológiai szempontokra [3,30]. Ezért ajánlott felügyelt testedzési rehabilitációs programok [3]. Ezenkívül ajánlott, hogy a betegek kerüljék a túlzott fizikai aktivitást, amely szorongó tünetekhez vezet, például a rossz gázcsere vagy a nem megfelelő szellőzés miatt. Ezenkívül az edzésprogramok nincsenek megfelelően kialakítva, és számos korlátozást tartalmaznak az edzés optimális módjának, intenzitásának és időtartamának ismeretében meglévő hiányosságok alapján [31].
Az étrend módosítása az egyik első lépés a szív- és érrendszeri betegségek kezelésében. A szisztémás artériás magas vérnyomás rutinszerű kezelése magában foglalja az étrendi beavatkozásokat minden beteg számára, beleértve a só és az alkohol korlátozását; megnövekedett zöldségfélék, friss gyümölcsök, teljes kiőrlésű gabonák, oldható rostok, halak, diófélék és olívaolaj fogyasztása; alacsony vörös húsfogyasztás; és alacsony zsírtartalmú tejtermékek fogyasztása [32]. Az Európai Kardiológiai Társaság (ESC) és az Európai Légzőszervi Társaság (ERS) irányelvei [3] azonban nem határoztak meg konkrét javaslatokat a PAH táplálkozási szokásaira vagy tápanyag-kiegészítésére vonatkozóan.
Érdekes módon a táplálkozási tényezők és a PAH közötti összefüggésekről nemrégiben számoltak be mind az emberi epidemiológiai vizsgálatok, mind az állatmodellek. Nemrégiben beszámoltak arról, hogy az extra fehérjével, leucinnal, halolajjal és oligoszacharidokkal végzett többcélú táplálkozási beavatkozás új stratégia lehet a patofiziológiai változások, például a szív- és vázizom hipertrófiájának megelőzésében a PAH-ban [33].
Itt arra a tudományos bizonyítékra összpontosítunk, hogy a vas, valamint a C- és D-vitamin, valamint más étrendi összetevők, például a flavonoidok hiánya hogyan befolyásolhatja a PAH progresszióját. Végül a bél mikrobiota szerepe, valamint az étrenddel és a gazda immunrendszerével való kölcsönhatása egyre több kardiovaszkuláris és légzőszervi betegségben, beleértve a PAH-t is, felmerül. Egyéb étrendi tényezők, mint például az n-3 többszörösen telítetlen zsírsavak (PUFA-k), az E-vitamin, a melatonin és a Q10 koenzim elméletileg hatással lehetnek a PAH-ra, de nincs kísérleti vagy klinikai bizonyíték, amely ezt alátámasztaná, és itt nem tárgyaljuk őket.
2. A PAH-t befolyásoló étrendi összetevők
2.1. C vitamin
A C-vitamin, más néven aszkorbinsav, vízben oldódó vitamin, amely több gyümölcsben és zöldségben megtalálható. Számos enzim aktivitásához szükséges, részt vesz a szövetek helyreállításában, fontos az immunrendszer működéséhez, és antioxidánsként működik. A C-vitamin súlyos hiánya skorbuthoz vezet, általános gyengeséget, vérszegénységet, vérzéseket a bőrben, ínybetegségeket és fogvesztést okozva [34,35].
Számos tanulmány kimutatta, hogy az oxidatív stressz szerepet játszik a szív- és érrendszeri betegségekben [36]. A reaktív oxigénfajok által végzett nitrogén-oxid inaktiválás kulcsfontosságú esemény a magas vérnyomáshoz, az érelmeszesedéshez és más érrendszeri patológiákhoz kapcsolódó endotheliális diszfunkcióban [37]. Másrészt az LDL oxidációja az endothel falában ezeket a részecskéket aterogénebbé teszi, és lehetővé teszi, hogy felhalmozódjanak az artéria falaiban [36]. Ez az antioxidánsok, köztük a C-vitamin széles körű használatához vezetett az érelmeszesedés előrehaladásának lassításához. A randomizált, kontrollált vizsgálatok összesített adatainak meta-analízise azonban arra a következtetésre jutott, hogy az antioxidáns vitamin-kiegészítés nincs hatással a súlyos kardiovaszkuláris események, a miokardiális infarktus, agyvérzés, a teljes halál és a szívhalál előfordulására [38].
Számos esettanulmány kimutatta, hogy a pulmonalis hipertónia a skorbut szövődménye [39,40,41,42]. Az emelkedett mPAP reverzibilis volt az aszkorbát beadása után. Két lehetséges mechanizmust javasoltak a C-vitamin hiányának PAH-ban való részvételére [41]. Először is, a C-vitamin növeli az endothel NO elérhetőségét, amelynek értágító és antiproliferatív képessége van [43]. Másodszor, a C-vitamin hiánya inaktiválhatja a prolil-hidroxilázokat, a sejtes oxigénérzékelőket, és leválaszthatja a hipoxia-indukálható faktort (HIF) az oxigénkontrollról [44]. A kontrollálatlan HIF-aktivitás a pulmonalis hipertóniás mechanizmusok aktiválódásához vezethet [45].
Nem ismert, hogy a nyugati társadalmakban ritkán előforduló mérsékelt C-vitamin-hiány és nem a klinikai skorbut szerepet játszik-e a PAH-ban. Sőt, a C-vitamin-kiegészítők PAH-betegekre gyakorolt hatását még nem kezelték megfelelően, és csak előzetes kísérleti bizonyítékok állnak rendelkezésre annak hatékonyságáról. Például egy brojlercsirkékkel végzett vizsgálat kimutatta, hogy a C-vitamin csökkentette a PAH előfordulását és a pulmonalis arteriolák kapcsolódó izomzatát [46].
2.2. D-vitamin
Nincs egyértelmű egyetértés a D-vitamin-hiány meghatározásában; az optimális szint és az étrendi követelmények bizonytalanok [52,53]. A konzervatív küszöbértékek alkalmazása mellett azonban manapság a D-vitamin-hiány világjárványa van [54]. Az alacsony 25 (OH) D3 szint legfőbb okai a nem megfelelő napozás és/vagy a csökkent étrendi bevitel [54].
Klasszikusan a D-vitamin hiány a csontbetegségekkel függött össze. Jelenleg a VDR miatt sok szövet található, például immun- és szív- és érrendszeri sejtek, a D-vitamin-hiány fertőzéssel, rákkal, valamint légzőszervi és szív- és érrendszeri betegségekkel is összefüggésben áll [53,55,56]. Valójában a D-vitamin-hiány az összes ok és a kardiovaszkuláris halálozás megnövekedésével járt [57,58]. A VDR felfedezése számos olyan szövetben, amely nem vesz részt a kalcium- és foszfor-homeosztázisban, a VDR által közvetített sokféle funkció azonosításához vezetett, többek között a sejtproliferáció és differenciálódás, az immunmoduláció és az intracelluláris anyagcsere között [48].
A PAH összefüggésében néhány alapvető és klinikai bizonyíték utal arra, hogy a D-vitamin szerepet játszik a betegség patofiziológiájában. A VDR-t vaszkuláris sejtekben azonosították, beleértve az endotheliális és simaizomsejteket is. Számos kardiovaszkuláris betegségben potenciálisan releváns folyamatban vesz részt, például sejtproliferációban, differenciálódásban és apoptózisban; sejtadhézió; oxidatív stressz; angiogenezis; valamint immunmoduláló és gyulladáscsökkentő aktivitás [53]. Ezért feltételezzük, hogy a D-vitamin szint befolyásolhatja a PAH kialakulását.
Annak tisztázása érdekében, hogy a D-vitamin szintje részt vehet-e a PAH progressziójában, Tanaka és mtsai. 10; 000 UI/kg kolekalciferolt tartalmazó étrenddel kezelt PAH patkányokat [59]. Nevezetesen ebben a tanulmányban azt tapasztalták, hogy a D-vitamin-kiegészítés a PAH patkányokban javította a túlélést és gyengítette a PAH néhány jellemző tulajdonságát, például a jobb kamra átalakulását, amelyet a Fulton-index (a jobb kamra és a bal kamra plusz a septum súly aránya) és mediális az izmos tüdőartériák vastagsága. A D-vitamin ezen előnyei ellenére a kolekalciferol-kezelés nem csökkentette a pulmonalis artéria nyomását [59]. Sőt, in vitro elrendezésben a kalcitriol-kezelés gátolta a hypoxia által kiváltott proliferációt és migrációt patkány pulmonalis artéria endothel sejtekben (PAEC) miR-204/TGFβ/Smad jelátviteli útvonalon keresztül. Pontosabban, a kalcitriol elnyomta a Tgfbr2, a-SMA és Smad7 expresszióját, és miR-204, p21 és Smad2 expressziót indukált [60]. Ugyanebben a vizsgálatban hasonló eredményeket találtak egy in vivo patkánymodellben. Figyelemre méltó, hogy az intraperitoneális kalcitriol adagolása (20 mg/kg) részben megfordította az mPAP és a Fulton-index három hetes hypoxia okozta emelkedését [60].
Az étrend kritikus szabályozója a mikrobiota összetételének és működésének [131]. Több tanulmány foglalkozott a makrotápanyagok (zsír, szénhidrát és fehérje) bél mikrobiomra gyakorolt hatásával. Fontosak lehetnek egyéb étrendi összetevők is, például oldható vagy oldhatatlan rostok [132,133]. Ezenkívül számos élelmiszer-komponens szubsztrátja a bakteriális enzimeknek. Ezek az enzimatikus folyamatok más melléktermékek előállításához vezetnek, amelyek felszívódhatnak a bélben. Fontos, hogy az SCFA-k, különösen a vajsav és az ecetsav, amelyek főleg a rost bakteriális fermentációjából származnak, elősegítik a szív- és érrendszeri egészséget. Ezzel szemben a trimetilamin-N-oxid (TMAO), a bél mikrobiotája által kolinból, betainból és karnitinből előállított metabolit, amely húsban, tojásban és halban bővelkedik, a szívbetegség túlzott kockázatával jár [134].
Ezenkívül beszámoltak arról, hogy egyes étrendi összetevők, például édesítőszerek, ásványi anyagok és vitaminok módosíthatják a mikrobiotát. Figyelemre méltó, hogy a PAH progressziójára a fent leírtak szerint hatással lévő egyes tápanyagok, mint például a vas- és D-vitamin-hiány, valamint a kvercetin és a resveratrol jelentősen befolyásolják a bél mikrobiotáját [135,136,137]. Ezért ezen étrendi összetevők fent említett hatásmechanizmusain kívül a bél mikrobiotájának változásai felelősek lehetnek a vas, a D-vitamin vagy a polifenolok hatásáért is. Éppen ellenkezőleg, a mikrobiota összetétele befolyásolhatja a kalcium, foszfát, vas és cink felszívódását. Sőt, a vízben oldódó vitaminok táplálékforrásai mellett a mikrobiota szintetizálhatja ezeknek a vitaminoknak egy részét [132].
3. Következtetések
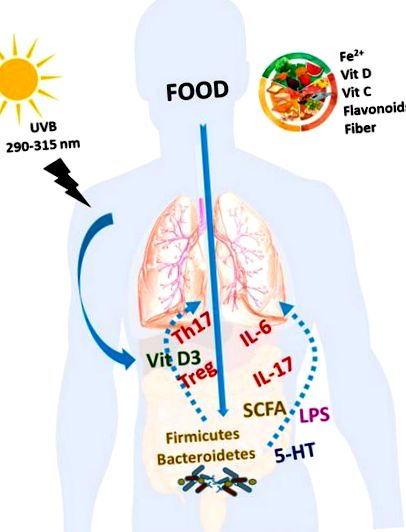
A táplálkozás hatása a PAH-ban. Az olyan étrendi összetevők, mint a Fe 2+, a C- és D-vitamin, a flavonoidok és más rokon polifenolok, a rostok, valamint a napfény hatására nyert D-vitamin pozitív hatással lehetnek a PAH-betegek életminőségére és prognózisára. Minden étrendi tényezőnek meg lehet a maga hatásmechanizmusa. Ezen tápanyagok hatásainak egy része azonban összefüggésbe hozható az immunrendszerre gyakorolt hatásukkal a T-sejtek és citokinek helyreállításával, a mikrobiota és baktériumtermékeik változásával, valamint a baktériumok transzlokációjával.
A polifenolok, a kvercetin, a resveratrol és a genistein lehetséges pozitív hatásait a PAH-ban a klinikai vizsgálatok során még meg kell határozni. Az ilyen polifenolokat tartalmazó kiegészítők alkalmazása ebben a szakaszban nem ajánlható. Tekintettel azonban a gyümölcsök és zöldségek szív- és érrendszeri egészségére gyakorolt biztató hatásaira, különös tekintettel a szisztémás hipertóniára, ésszerűnek tűnik a PAH-ban szenvedő betegeket arra ösztönözni, hogy tartsák be az ilyen ételekben gazdag étrendet.
A bél dysbiosis szerepét a PAH patogenezisében nem határozták meg szilárdan. Jelenleg a bél vagy a tüdő mikrobiota módosítására irányuló ajánlások nem állapíthatók meg. Ha azonban a dysbiosis szerepe beigazolódik, számos beavatkozás valósulhat meg a megváltozott mikrobiális ökoszisztéma kijavítására vagy kompenzálására, ideértve a specifikus baktériumtörzsek (probiotikumok), a rost- és étkezési polifenolok (azaz prebiotikumok) használatát, a széklettranszplantációt, az antibiotikumokat és béta-adrenerg antagonisták vagy specifikus SCFA-k hiányának pótlása (pl. acetát).
Szerző közreműködései
F.P.-V. vázolta a felülvizsgálatot, M.C. írt egy vázlatot, és J.A.B., J.D. és F.P.-V. átdolgozta és kibővítette a végleges verziót. Minden szerző elolvasta és elfogadta a kézirat közzétett változatát.
Finanszírozás
Ezt a tanulmányt a Mineco támogatásai (SAF2016-77222-R és SAF2017-8489-R) támogatták, az Európai Unió (Fondo Europeo de Desarrollo Regionális FEDER) és Fundación Contra la Hipertensión Pulmonar (Empátia-támogatás) forrásaival. M.C. az Universidad Complutense de Madrid finanszírozza.
Összeférhetetlenség
A szerzők kijelentik, hogy nincsenek versengő érdekeik.
- A táplálkozás hatása az agyi keringésre és a megismerésre a metabolikus szindrómában
- Az eliminációs étrendek hatása a táplálékra és a növekedésre a többszörös ételallergiás gyermekeknél -
- Megváltozott az étrend a pulmonalis hipertónia lezárása óta Hírfórumok
- Az elhízás hatása a testmozgásra és a pulmonalis rehabilitációra - DREHER - 2012 -
- Hogyan befolyásolja a táplálkozás az alvászavarokat az alvás felülvizsgálata