Az epigenetikus óra fejlesztési hangolása
Absztrakt
A gerontológia területén végzett kutatás hagyományosan a későbbi életszakaszokra összpontosított. Egyre több bizonyíték van azonban arra, hogy mind az életkorral összefüggő funkcionális hanyatlás mértéke, mind a későbbi életkor egészségi állapota programozható a korai fejlődés során. Kiderült az epigenetikus mechanizmusok (a DNS metilezése, a hiszton módosítások és a nem kódoló RNS-ek által történő szabályozás) szerepe e hosszú távú hatások közvetítésében. Kimutatták, hogy az epigenetikai minták („epigenetikus sodródás”) korhoz kapcsolódó változásának sebessége és iránya nagymértékben függ a korai életkor környezeti viszonyaitól. Az epigenetikai profilokban az egyének közötti eltérések az epigenetikus jelek megőrzésében fellépő sztochasztikus hibák nyomán jelentkezhetnek, de adaptív módon közvetíthetők specifikus környezeti jelzésekkel is. A legújabb kohorsz-vizsgálatok azt mutatják, hogy az epigenetikus óra ketyegési sebessége, amelyet DNS-metiláció-alapú módszerekkel becsülnek meg, fejlõdésileg korrigálható, és hogy az egyén epigenetikai és idõbeli kor közötti eltérései valószínûleg a fejlõdés korai szakaszában programozhatók. Ebben a Perspektíva cikkben összefoglalják és megvitatják a korai élet meghatározóinak fontosságát az epigenetikus sodródás életpálya-dinamikájának fontosságát.
Bevezetés
Az epigenetikus sodródás korai életében meghatározó tényezők
Az állatmodellek bizonyítékai
Az étkezési fehérjetartalmú poszt-eklóziós manipuláció által kiváltott, a Drosophila melanogaster reproduktív aktivitására és hosszú élettartamára vonatkozó transzgenerációs hatásokról Xia és de Belle (2016) számolt be. Ebben a kutatásban mind az alacsony, mind a magas fehérjetartalmú étrend csökkentette az élettartamot, míg a köztes fehérjetartalmú étrend jelentősen meghosszabbította az élettartamot az F3 generációig. Egy későbbi tanulmányban az alacsony fehérjetartalmú étrenddel való táplálkozás az eklózió utáni időszakban az F0 generáció, valamint az F2 utódok várható élettartamának rövidülését eredményezte. Ezeket a hatásokat a H3K27-specifikus metiltranszferáz (E (z)) és a H3K27 trimetilezés, H3K27me3 fokozott szintjének (Xia et al., 2016) fokozott szabályozása kísérte. Érdekes módon mind az E (z) RNSi által közvetített leütése, mind az enzimatikus működését farmakológiai módon gátló specifikus hiszton-metil-transzferáz inhibitorral, a Tazemetostat (EPZ-6438) nemzedékeken át csökkentette a H3K27me3 szintjét. Ezenkívül a Tazemetostat teljesen megszüntette a szülői fehérjeszegény étrend élettartam-rövidítő hatását.
Rágcsáló-modellekben megerősítő bizonyítékokat nyertek olyan tényezők szerepéről is, mint az xenobiotikus expozíció, a stressz és az alultápláltság az utak fejlődési epigenetikai programozásában, hozzájárultak az öregedés és a hosszú élettartam ellenőrzéséhez (az áttekintéseket lásd Vaiserman, 2014; Tarry-Adkins és Ozanne, 2017; Ambeskovic et al., 2018). Például Heo és munkatársai tanulmányában. (2016) szerint a prenatális alultápláltság a DNS (metiláció) és az öregedéssel összefüggő folyamatokban szerepet játszó gének transzkripciós aktivitásának diszregulációjához vezetett, és anyagcserezavarok kialakulásához vezetett fiatal (9 hetes) patkány utódokban. Figyelemre méltó, hogy ezek a szabályozatlan epigenetikai minták hasonlóak voltak az idős (20 hónapos) utódoknál.
Bizonyítékok ikermodellekből
Kvázi kísérleti bizonyítékok
Az epigenetikus óra fejlődési beállítása
Hipotetikus szempontok
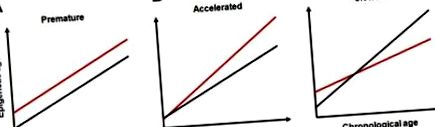
A fenti koncepcionális keretek és kutatási eredmények alapján feltételezhető, hogy az epigenetikus öregedés életút-dinamikája függhet a korai élet eseményeitől, és hogy ennek a függésnek a módja az érintett stádiumtól és a típustól, időtartamtól függően eltérő lehet és az expozíció intenzitása. A kapcsolatról szóló legtöbb adat megfelel az általános intuitív elképzeléseknek. Az élet korai szakaszában jelentkező káros környezeti expozíció az epimutációk felhalmozódásának megnövekedett sebességét eredményezheti, anélkül, hogy felgyorsítaná az epigenetikus öregedés sebességét. Ez növelheti az elfogási paramétert anélkül, hogy megváltoztatná a meredekségi paramétert az ezt a kapcsolatot leíró lineáris regressziós modellben („korai epigenetikus öregedés”, 1.A ábra). 1A). A nem megfelelő fejlődési programozás, például az epigenetikus adaptáció hibája miatt, a meredekség növekedését okozhatja („felgyorsult epigenetikus öregedés”, ábra: 1B 1B ábra).
Az epigenetikus öregedés hipotetikus életmód-dinamikái. (A) korai epigenetikus öregedés; (B) felgyorsult epigenetikus öregedés; és (C) lelassította az epigenetikus öregedést. Az összes panelen a piros vonalak a korai élet hátrányos eseményeinek kitett alanyokat, a fekete vonalak pedig a nem exponált alanyokat jelentik.
Záró megjegyzések
A gerontológia területén végzett kutatások hagyományosan az életciklus későbbi szakaszaira összpontosítottak. Egyre több bizonyíték van azonban arra, hogy az életkorral összefüggő funkcionális csökkenés és az öregedéssel összefüggő betegségek kockázata nagymértékben függhet a fejlődési feltételektől. A felnőttkori élet krónikus kóros állapotainak patogenezisében a fejlesztési programozás tudatosságának növekedése és az érintett mechanizmusok feltárása növekvő érdeklődést eredményezett az ezen a területen folytatott kutatások iránt. A fejlesztési programozási folyamatok valószínűleg különös jelentőséggel bírnak a modern fejlett társadalmakban a jelentős életmódbeli változások (nyugati étrend, ülő viselkedés stb.) Miatt, amelyek gyakran ütközhetnek a fejlesztés során programozott adaptív epigenetikai stratégiákkal.
Két fontos szempont következik ezekből a szempontokból a jövőbeli kutatások és gyakorlati alkalmazások szempontjából. Először is, az epigenetikai módszertan továbbfejlesztése lehetőséget nyújt arra, hogy azonosítsák azokat az egyéneket, akiket jóval a betegség klinikai megnyilvánulása előtt a korai életben előforduló rossz programozás miatt kialakulhat bizonyos életkorral összefüggő kóros állapot. Másodszor, mivel az epimutációk a genetikai mutációktól eltérően potenciálisan reverzibilisek, ezeket speciális táplálkozási és/vagy farmakológiai beavatkozásokkal lehet korrigálni. Az ilyen epigén-célzott beavatkozások lehetővé tennék az epigenetikus élet életdinamikájának befolyásolását, és lassítanák az epigenetikus óra ketyegési sebességét az öregedéssel kapcsolatos folyamatok késleltetésére vagy lassítására.
Szerző közreműködései
A szerző megerősíti, hogy ő a mű egyedüli közreműködője, és jóváhagyta közzététel céljából.
Összeférhetetlenségi nyilatkozat
A szerző kijelenti, hogy a kutatást olyan kereskedelmi vagy pénzügyi kapcsolatok hiányában végezték, amelyek potenciális összeférhetetlenségként értelmezhetők.
- Autizmusban szenvedő gyermekek, fejlődési késések, nagyobb az elhízás kockázata
- A testórájával szinkronban történő étkezés segíthet a zsírgyarapodás visszaszorításában
- Az autizmussal, fejlődési késedelemmel küzdő gyermekek közel 50 százalékkal nagyobb valószínűséggel vannak túlsúlyosak vagy
- A teljes cikk A pubertás fontos fejlődési időszak a zsírszövet létrejöttéhez
- Egyél-e az óra körül