Bilirubin, egy kardiometabolikus jelző molekula
Toledo Egyetem Orvostudományi Főiskola, Élettani és Farmakológiai Tanszékről, OH (T.D.H.)
Levelezés David E. Stec-nek, a Mississippi Egyetem Orvosi Központjának Élettani és Biofizikai Tanszéke, 2500 N State St, Jackson, MS 39216.
Élettani és Biofizikai Tanszék, Mississippi Elhízáskutató Központ, Mississippi Egyetem Orvosi Központ, Jackson (D.E.S.).
A konjugálatlan bilirubin (UCB) magas vérszintjét a sárgaság, a bőr és a szem sárgaságának okozójaként ismerik legszélesebb körben. Az újszülöttkori sárgaságot a 18. század vége óta írják le az orvosi szakirodalom, és ez egy olyan állapot, amely az újszülöttek szérumában az UCB nagyon magas szintjét tükrözi. Az újszülöttek sárgaságának súlyos esetei bilirubin által kiváltott idegrendszeri állapotokat eredményeztek újszülötteknél, kernicterus néven, ami agykárosodást okozhat. A sárgaságban betöltött szerepe ellenére az UCB számos jótékony hatással van a szervezetre. 5 Számos nagyszabású populációs és epidemiológiai vizsgálat eredménye összefüggésbe hozta a szérum bilirubinszint védőhatását a szív- és érrendszeri és anyagcsere-betegségekkel szemben. Ennek molekuláris mechanizmusa azonban nem teljesen ismert. Jelen áttekintés célja kiemelni és megvitatni a BVR bilirubin-generációjának egyedi jelátviteli hatásait, valamint azt, hogy miként jeleznek védelmet a szív- és érrendszeri és anyagcsere-betegségek ellen, amelyek új terápiákhoz vezethetnek.
Bilirubin mint jelző molekula
Az egyik legfontosabb biológiai funkció, amelyet korábban a bilirubinnak tulajdonítottak, az volt, hogy képes antioxidánsként működni. A 6,7 bilirubin közvetlenül képes eltávolítani a reaktív oxigénfajtákat (ROS), valamint gátolhatja a RAD termelését a NADP (H) oxidázok által. A 8–11 A bilirubin kölcsönhatásba lép más antioxidánsokkal, például az E-vitaminnal, hogy tovább védje a fokozott ROS-termelést. 12,13 Bár nem kétséges, hogy a bilirubin erős endogén antioxidáns, továbbra is fennállnak a kérdések arról, hogy a bilirubin antioxidáns hatása képes-e megfelelően megmagyarázni az összes jótékony kardiovaszkuláris és metabolikus hatást. 14–16
Az UCB szerkezetének vizsgálata kimutatta, hogy hasonlóságot mutat más ismert PPARα aktivátorokkal (peroxiszóma-proliferátor-aktivált receptor a), mint például a WY 14 643 és a fenofibrát. 17 A receptor nélküli COS-7 sejteken végzett vizsgálatok, amelyeket átmenetileg PPARα-val vagy üres vektorral transzfektáltak, kimutatták, hogy a biliverdin vagy a bilirubin dózisfüggő növekedése specifikusan aktiválta a PPARα-függő riporter gént. 17 A biliverdint azonban a BVRA gyorsan előállítja bilirubinná (biliverdin reduktáz A), 18 ami azt jelzi, hogy a BVRA bilirubin termelődése közvetíti a PPARα transzkripciós aktivitást. A WY 14 643, a fenofibrát és a biliverdin azonos szintjét összehasonlító hasonló elemzés során Stec és mtsai 17 azt találták, hogy a biliverdin ugyanolyan mértékben növelte a PPARα-függő riporter gént, mint az ismert aktivátor, a fenofibrát. Azonban a WY 14 643-nál ennél a riporternél lényegesen magasabb volt az aktivitás. A fenofibrátnak és a bilirubinnak kardiovaszkuláris védő tulajdonságai vannak.
Fontos, hogy meghatározzuk a szérumkonjugált bilirubint az UCB-ből, mivel a konjugált bilirubin nem megelőzi a szív- és érrendszeri vagy anyagcsere-betegségeket, és csak az emelkedett UCB-szintek korrelálnak a szív- és érrendszeri és anyagcsere-védelemmel. 19 Ezenkívül csak az UCB-ről bizonyították, hogy aktiválja a PPARα-t. 17 UCB-ről kimutatták, hogy az aktív PPARα 50 μmol/L tartományban van, amely a Gilbert-szindrómás betegeknél beszámolt UCB fiziológiai tartományába esik. A 19,20 UCB hasonlóan jelezhet, mint a fenofibrát és más rostosavszármazékok. A bilirubinnak olyan antidiabetikus hatása is van, amelyet tipikusan nem figyelnek meg a fibrát típusú gyógyszereknél. Ennek az összehasonlításnak a bemutatására azonban csak egy tanulmány készült, amelyet még alaposan tesztelni kell.
Bilirubin mint szelektív PPAR modulátor
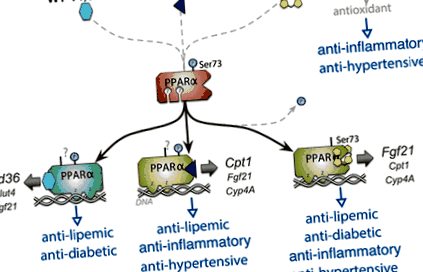
1.ábra. A bilirubin mint szelektív PPARα (peroxiszóma-proliferátor-aktivált receptor α) modulátor (SPPARM). A bilirubin a PPARα ligandumkötő zsebéhez kötődik, hasonlóan más ismert WY-14 643 aktivátorokhoz és a fenofibráthoz. A bilirubin szintén erős antioxidáns. Kimutatták, hogy a bilirubin csökkenti a 73-as szerin (Ser73) foszforilációját, hogy növelje a PPARα transzkripciós aktivitását. 34,36 A PPARα cinkujj (Z) DNS-kötő doménjei megkötik a célgének promótereit. A bilirubin számos PPARα célgén, köztük a fibroblaszt 21-es növekedési faktor (Fgf21), a karnitin-palmitoil-transzferáz I (Cpt1) és a citokróm P450 4A (Cyp4A). A WY 14 643 erősebb a 36-os differenciálódás klaszterének (Cd36) és kisebb mértékben a 4-es glükóz transzporter (Glut4) és Fgf21 promóterek. Az elsődleges cél a fenofibrát Cpt1. Ezek a gének specifikus szerepet játszanak az egyes vegyületek antidiabetikus, antilipémiás, gyulladáscsökkentő és vérnyomáscsökkentő hatásaiban.
Bilirubin jelzése anyagcsere és kardiovaszkuláris betegségek esetén
A bilirubinnak sokféle kardiovaszkuláris hatása van a test számos különböző szervében (2. ábra). A szívben a bilirubin növeli a nitrogén-monoxid (NO) biohasznosulását azáltal, hogy csökkenti a ROS termelést. 35,37 Az érfalban a bilirubin az adhéziós molekulákra gyakorolt hatása, valamint a koleszterin anyagcseréje révén csillapítja az érelmeszesedéses plakkképződést. 38–42 A vesében a bilirubin megőrzi a glomeruláris szűrési sebességet és a vese véráramlását a NO biohasznosulásának növekedése révén. A májban és a zsírban a bilirubin a PPARα-n keresztül hat, hogy fokozza a zsírégetést. 17,36 Ezek a vizsgálatok szerint a bilirubin az anyagcsere és a szív- és érrendszeri betegségek befolyásoló mediátora.
2. ábra. A bilirubin (BR) kardiovaszkuláris és metabolikus hatása. A szívben a bilirubin csökkenti a reaktív oxigénfajtákat (ROS) és növeli a nitrogén-oxid (NO) szintjét a koszorúér-véráramlás (BF) javítása érdekében. A bilirubin a PPARα-n (peroxiszóma-proliferátor-aktivált receptor α) keresztül is felléphet a zsírsav (FA) anyagcseréjének fokozása és a kardioprotekció biztosítása érdekében. Az erekben a bilirubin gyengíti a koleszterin lerakódását és az immunsejtek beszivárgását a plakkképződés csökkentése érdekében. A májban a bilirubin és a BVRA (biliverdin reduktáz A) foszforilálja az AKT-t, amely gátolja a GSK3β (glikogén szintáz kináz 3β) konzerválását, megőrizve a PPARα funkciót a fibroblast növekedési faktor 21 növelése érdekében (Fgf21) és karnitin-palmitoil-transzferáz I (Cpt1) a zsírégetés és a máj steatosis elleni védelem érdekében. Adipocitákban a bilirubin BVRA-termelése aktiválja a PPARα-t a lipidméret csökkentése érdekében. A vesében a bilirubin javítja a glomeruláris filtrációs sebességet (GFR), a vese BF (RBF) és a nitrogén-oxid szintáz (NOS) szintjét, miközben gátolja a ROS szintet.
Számos nagyszabású populációs vizsgálat kimutatta, hogy a túlsúly és az elhízás mértéke negatívan korrelál a férfiak és nők szérum UCB szintjével. 45–48 A szérum bilirubinszint az öregedés során szintén csökken, ami megfelel a testtömeg növekedésének és a szív- és érrendszeri betegségek kockázatának, különösen a nőknél. 49,50 Érdekes, hogy a magasabb szérum UCB-szint a nőknél fiatalosabb megjelenéssel is jár, a férfiaknál azonban nem. 51 Beszámoltak arról is, hogy a szibutramin étrenddel és testmozgással kombinációban történő rövid távú súlycsökkenés növelte a bilirubin szintjét a testsúly változásával arányosan, a hatás nagyobb volt a férfiaknál, mint a nőknél. 52 Ezenkívül a Gilbert-polimorfizmussal összefüggő mérsékelt hiperbilirubinémia alacsonyabb testtömeg-indexhez, csípőkörfogathoz, zsírtömeghez és lipidprofilhoz társult, összehasonlítva az egészséges kontrollokkal és a II-es típusú cukorbetegekkel. Ezek az adatok arra utalnak, hogy a plazma UCB-szintek hatással lehetnek a testtömegre, és hogy maga a fogyás növelheti a szérum bilirubinszintjét.
Az Országos Egészségügyi és Táplálkozási Vizsgálat felmérései azt találták, hogy a magasabb szérum bilirubinszint véd a stroke és a diabetes mellitus kialakulása ellen. 54,55 Hasonló eredményeket kaptak kisebb populációs vizsgálatok is. 56,57 A Gilbert-féle polimorfizmus (UGT1A1 * 28) a Framingham Heart Study-ban a koszorúér-betegség ellen védett. 58 A Gilbert-egyének számára biztosított kardiovédelem egyik mechanizmusa, hogy a magas bilirubinszint csökkenti a ROS termelést. 19,59 A legújabb tanulmányok azt is kimutatták, hogy Gilbert személyeinek metabolikus útvonala megváltozik, például az AMPK (AMP-aktivált protein-kináz) útvonal, hasonlóan a humanizált UGT1A1 * 28 egereknél megfigyeltekhez. 20,36
Számos olyan tanulmány készült, amely megvizsgálta a bilirubin szerepét a magas vérnyomásban. A hiperbilirubinémiás Gunn patkányon végzett vizsgálatok védő szerepet játszottak a deoxikortikoszteron-acetát (DOCA) -só és az angiotenzin-II-függő magas vérnyomásban. 60,61 A bilirubin szérumszintje azonban Gunn patkányban rendkívül magas (~ 30 mg/dl vagy 500 μmol/L), mivel ebben a törzsben a máj UGT1A1 aktivitása teljesen elvesztette. A szérum bilirubin fiziológiásabb növekedésének szerepének meghatározásához, hasonlóan a Gilbert-szabadalmakhoz, kifejlesztettünk egy mérsékelt hiperbilirubinémiás egérmodellt, és bebizonyítottuk, hogy ezek az egerek védettek voltak az angiotenzin-II-függő magas vérnyomástól és a csökkent vese véráramlástól és a glomeruláris szűrési sebesség. A mérsékelt hyperbilirubinemia vérnyomáscsökkentő hatása angiotenzin-II-függő hipertóniában nem annak antioxidáns hatása miatt következtett, hogy a bilirubin egyéb hatásai, például SPPARM-aktivitása felelősek lehetnek a mérsékelt hyperbilirubinemia vérnyomáscsökkentő hatásáért. 14 Ugyanakkor további vizsgálatokra van szükség, amelyek megvizsgálják a bilirubin vérnyomáscsökkentő képességét angiotenzin-II-függő hipertóniában PPARα jelzés hiányában.
A populációs vizsgálatok azt is bizonyították, hogy a szérum bilirubinszint védő szerepet játszik a diabetes mellitus és a kapcsolódó patológiák, például a diabéteszes nephropathia és a végtag amputációk kialakulása ellen. 55,57,62–65 A szérum bilirubinszint emelkedése proteázinhibitorokkal, például atazanavirral szintén javult az érműködésben cukorbetegeknél és javította a vese hemodinamikáját hipertóniás egereknél. Az étrend okozta elhízott és db/db egereken végzett további vizsgálatok azt mutatták, hogy a bilirubin adagolása javítja a hiperglikémiát és az elhízást. 40,67 Bár ezekben a vizsgálatokban a bilirubin szignalizáció specifikus hatását nem értékelték, az UCB kezelés az inzulin szignál útvonalak aktiválódásával járt együtt, és csökkent a gyulladásos citokinek szintje, valamint az endoplazmatikus retikulum stressz markerei. 67 Ezek a tanulmányok kiemelik, hogy a bilirubin számos különböző mechanizmus révén javíthatja az inzulinérzékenységet, beleértve az anti-endoplazmatikus retikulum stresszt, gyulladáscsökkentőt, valamint SPPARM-ként végzett tevékenysége révén (1. ábra).
A plazma lipid- és koleszterinszintjének megváltozása elősegítheti a szív- és érrendszeri betegségeket. A Gilbert-féle polimorfizmusban szenvedő egyéneken végzett vizsgálatok, valamint a mérsékelt hiperbilirubinémia modelljein végzett állatkísérletek bebizonyították a lipidprofilra és a koleszterinszintre gyakorolt hatásokat, amelyek hozzájárulnak az UCB védőhatásaihoz. Beszámoltak arról, hogy Gilbert személyeinek alacsonyabb a szérum koleszterinszintje, az LDL (alacsony sűrűségű lipoprotein) és az oxLDL (oxidált LDL) szintje. 19,59,68,69 Hasonló hatásokat figyeltek meg a szérum koleszterinszintre és az LDL szintre mind a humanizált Gilbert egereknél, mind az étrend által kiváltott, elhízott egereknél, amelyeket UCB-vel kezeltek. Nem ismert, hogy a bilirubin szignalizáció milyen mértékben befolyásolja ezeket a hatásokat a szérum lipidekre; azonban a PPARα agonistákról, mint például a fenofibrátról, régóta ismert, hogy csökkentik a szérum zsírsavak, az LDL és az összkoleszterin szintjét. 70,71
A hiperlipidémia, a szérum zsírsavak és az LDL szintjének emelkedése ismert kockázati tényező a szív- és érrendszeri betegségek kialakulásában. A magas vérnyomás rágcsáló-modelljeivel végzett számos tanulmány kimutatta, hogy a PPARα agonista fenofibrát védő szerepet játszik a vérnyomás csökkentésében és a szervek végső károsodásával szembeni védelemben. 72–75 Nem főemlősökön végzett további vizsgálatok kimutatták, hogy a PPARα agonista képes a plazma lipidek csökkentésére és a szív- és érrendszeri betegségek csökkentésére. 76 A fenofibrát kezelés pozitív hatással van az érrendszer működésére a II. Típusú diabetes mellitusban szenvedő betegeknél; ennek a gyógyszernek a lipidszint-csökkentő hatása azonban nem vezetett jelentős védelemhez a szív- és érrendszeri betegségek ellen az emberi betegcsoportokban. 77–79 A bilirubin-kezelés jobb terápiás potenciált kínálhat, mint a PPARα agonistával végzett kezelés, mivel antioxidáns, antilipémiás és gyulladáscsökkentő tulajdonságokkal rendelkezik, amelyek szintén hozzájárulnak a szív- és érrendszeri betegségek elleni védelemhez (2. ábra).
BVR jelzőműveletek
A BVR a biliverdin bilirubinná történő redukciójáért felelős enzim. A BVRA a legfőbb izoform a felnőtt szövetekben, míg a B izoform (BVRB) a magzati fejlődés során jelenlévő izozim. 1 A BVRA globális knockout egereken végzett legújabb vizsgálatok a plazma bilirubin és a zöld epehólyag közel hiányát mutatják, ami a biliverdin nagyon magas szintjére utal. 84 Ezenkívül a globális BVRA-hiányos egerek magasabb plazma-koncentrációjú koleszteril-észter-hidroperoxidokat mutatnak, ami az endogén oxidatív stressz magasabb szintjét jelzi. 84 A BVRA globális veszteségének az anyagcserére gyakorolt hatását azonban nem vizsgálták.
A BVRA hepatocita-specifikus elvesztése a glikogén raktározásának jelentős steatosis csökkenését és a máj inzulin érzékenységének változását eredményezte. 34 Ezenkívül a hepatocita BVRA elvesztése megnövekedett GSK3β aktivitást eredményez a Ser9 gátló Ser9 foszforilációjának csökkenésével. 85 A BVRA szabályozza a máj GSK3β aktivitását, bár az Akt1 közvetítette Ser9 foszforiláció növekedése. 86 A GSK3β aktivitás növekedése a BVRA által közvetített Ser9 foszforiláció elvesztése miatt megnövekedett Ser (P) 73 PPARα-t és csökkent célgéneket, mint pl. Fgf21 és az 1A karnitin-palmitoil-transzferáz (Cpt1a). 34 Így a BVRA az UCB generálása révén, valamint a GSK3β foszforilezését szabályozó Akt1-gyel való közvetlen kölcsönhatásával szabályozhatja a Ser (P) 73 PPARα-t (2. ábra). A GSK3β foszforilezésének újszerű szabályozása a BVRA-val fontos védelmi útvonal lehet a magas vérnyomás által kiváltott szívkárosodásban, valamint a vese ischaemia-reperfúziós sérülésben, mivel a GSK3β aktivációról számoltak be, hogy jelentős szerepet játszik ezekben a patológiákban. 1,87–89 A közelmúltban a BVRA CRISPR célzása proximális tubulus vesesejtekben azt mutatta, hogy a BVRA elvesztése szignifikánsan magasabb lipidfelhalmozódást és lipotoxicitást okozott. A bilirubin számos előnnyel járhat a vese és a vesekárosodás szempontjából.
Következtetések
- Bilirubinszint, Gilbert-szindróma és a Paleo Keto diéta hatásai
- Egy új mitokondriális jelátviteli út, amelyet a látható-közeli infravörös sugárzás aktivál .¶ - Karu -
- Bilirubin teszt magas vs.
- Online vásárlás Obenyl Tablet fogyás; Megakadályozza a cukorbetegséget; Hipertónia - Általános egészségügyi ellátás
- 01 13 20 a varázslatos fogyókúrás tabletta dr oz okoz-e a tabletta fogyást Diákblog