Elhízás elleni gyógyszerek: múlt, jelen és jövő
R. John Rodgers
1 Behavioral Neuroscience Laboratory, Pszichológiai Tudományok Intézete, Leedsi Egyetem, LS2 9JT, Egyesült Királyság
Matthias H. Tschöp
2 Cukorbetegség és elhízás Intézete, München Helmholtz Center és Müncheni Műszaki Egyetem, Ingolstaedter Landstr. 1, 85764 Neuherberg, Németország
John P. H. Wilding
3 Elhízás és Endokrinológia Tanszék, Öregedés és Krónikus Betegségek Intézete, Klinikai Tudományok Központ, Aintree Egyetemi Kórház, Liverpool, L9 7AL, Egyesült Királyság
Absztrakt
Bevezetés
Az elhízást, amelyet legtöbbször ≥30 kg/m 2 testtömeg-indexként (BMI) határoznak meg, és amelyet az energiafogyasztás és a ráfordítás közötti egyensúlyhiány okoz, széles körben elismerten a legnagyobb és leggyorsabban növekvő népegészségügyi problémaként a fejlett és a fejlődő világban ( https://apps.who.int/infobase/Publicfiles/SuRF2.pdf). A rendellenesség előfordulása felnőtteknél az elmúlt évtizedben több mint háromszorosára nőtt, és az elhízás jelenleg az USA teljes lakosságának körülbelül 30–35% -át, az Egyesült Királyságban pedig 25% -át érinti (National Audit Office, 2001) (http: // www .ic.nhs.uk/statisztikák és adatgyűjtések/egészség és életmód/elhízás/statisztikák az elhízásról-fizikai aktivitás-és-diéta-anglia-2010). Becslések szerint 2005-ben világszerte mintegy 400 millió felnőtt elhízott, összesen 1,6 milliárd túlsúlyos (http://www.who.int/mediacentre/factsheets/fs311/en/index.html). Különös aggodalomra ad okot a gyermekek és serdülők elhízás járványa; az előrejelzések szerint ezekben a populációkban a jelenlegi 7–10% -os prevalencia 2025-re legalább megduplázódik (McPherson et al., 2007), és komoly bizonyítékok vannak a felnőttkorban való kitartásra vonatkozóan (Freedman et al., 2001; Daniels, 2006b).
A műtét alternatív stratégiája olyan terápiás szerek kifejlesztése, amelyek csökkenthetik a testsúlyt az étel fogyasztásának vagy felszívódásának csökkentésével és/vagy az energiafelhasználás növelésével (Cooke és Bloom, 2006; Sargent és Moore, 2009). Sajnos, bár ezt a stratégiát több mint fél évszázadon keresztül folytatták lelkesen, ez a stratégia mindeddig csak korlátozott sikert mutat. Sok új ügynököt, amelyet az elhízás problémájának megválaszolásaként hirdettek, elfogadhatatlan mellékhatások miatt sietve visszavonták. Egy nemrégiben készült áttekintés meglehetősen pesszimistán arra a következtetésre jutott, hogy „az elhízás elleni gyógyszerek kifejlesztésének története korántsem dicsőséges, átmeneti varázslövedékekkel és csak néhány olyan szerrel rendelkezik, amely jelenleg klinikai használatra engedélyezett” (Rodgers et al., 2010). Ezért sürgősen szükség van új, jobban tolerálható és hatékonyabb elhízási kezelésekre (Halford et al., 2010; Kennett és Clifton, 2010; Rodgers et al., 2010; Vickers et al., 2011). Ebben az összefüggésben az étvágy és az energia homeosztázis alapvető neurobiológiájának megértése terén tett közelmúltbeli jelentős fejlemények számos célpontot azonosítottak az elhízás elleni gyógyszerek lehetséges fejlesztésére (Wilding, 2007; Heal és mtsai, 2009; Halford és mtsai, 2010). A kommentár célja, hogy ezeket a fejleményeket összefüggésbe hozza az elhízás farmakoterápiájának áttekintésével múltjának, jelenének és jövőjének szempontjából.
A szakasz meghatározása érdekében fontos felismerni, hogy a potenciálisan fontos új terápiás szerek preklinikai azonosítását követően az emberi gyógyszeres kísérletek a fejlődés több fázisán keresztül haladnak. Az I. fázis jellemzően a tolerálhatóságra, a biztonságra és a farmakokinetikára összpontosít; II. Szakasz a koncepció igazolásáról (mechanizmus, hatékonyság és biztonság); III. Fázis a hatékonyság és a mellékhatások profiljának megerősítéséről nagyszabású, több központú vizsgálatokban; valamint a kormányzati jóváhagyást követő hosszú távú nyomon követésről és adatgyűjtésről szóló IV. szakasz. Az Egyesült Államok Élelmiszer- és Gyógyszerügyi Hivatala (FDA) vagy az Európai Gyógyszerügynökség (EMA) jóváhagyási kérelmét a III. Szakasz után nyújtják be.
A múlt
A központilag ható szimpatomimetikumok, például a dezoxifedrin, a fentermin és a dietil-propion amfetamin-származékai voltak a legkorábbi fogyáshoz használt farmakológiai szerek (Colman, 2005; Wilding, 2007). Az 1950-es és 1960-as években népszerűek voltak, de a kardiovaszkuláris kockázattal és a visszaélések lehetőségével kapcsolatos növekvő aggodalmak az 1970-es évek elejére jelentősen csökkentek használatukban. Noha a fentermin és a dietil-propion még mindig számos országban elérhető, az 1970-es és 1980-as években a fenfluramint és a dexfenfluramint jelentős mértékben felváltotta a szerotonint (5-HT) felszabadító szer. A kezdetektől fogva ismert volt, hogy ennek a sorozatnak az anyagai képesek primer pulmonális hipertónia kialakulására, de a kockázatot kellően alacsonynak ítélték a fogyás előnyeivel szemben. Az 1990-es évek elején az önmagában adott vegyületekkel szembeni jobb hatékonyság bizonyítékai a fenterminnel és fenfluraminnal kombinált kezelés széleskörű alkalmazásához vezettek az Egyesült Államokban (Weintraub et al., 1992). Néhány éven belül azonban a szív valvulopathiáról szóló jelentések (Connolly és mtsai., 1997), különösen akkor, ha ezeket a szereket fenterminnel kombinálták, a gyártókat a fenfluramin és a dexfenfluramin kivonására késztették.
1. rovat.
Szójegyzék:
| Agonista: | olyan anyag, amely egy receptor molekulához kötődik, és olyan ingert produkál, amely mérhető választ eredményez a szövetben. |
| Antagonista: | olyan anyag, amely ugyanahhoz a receptorhoz kötődik, mint egy agonista, de nem vált ki ingert (így nem alakul ki szöveti válasz). Az antagonista azonban blokkolhatja vagy megfordíthatja az agonista vagy inverz agonista hatásait. |
| Fordított agonista: | azokban a szövetekben, amelyekben a receptorok konstitutív aktivitást mutatnak, egy inverz agonista ugyanahhoz a receptorhoz kötődik, mint egy agonista, de a kapott inger ellentétes választ vált ki a szövetben. |
| Antagonista/inverz agonista: | olyan anyag, amely ugyanahhoz a receptorhoz kötődik, mint egy agonista, de hatása az agonista jelenlétének (antagonista hatása) vagy hiánya (inverz agonista hatása) függvényében változik. A semleges antagonistának nincs inverz agonista aktivitása. |
Az FDA 1998-ban hagyta jóvá az orlisztát az elhízás kezelésére. A fent említett többi fogyókúrával ellentétben, amelyek csökkentik az étvágyat és/vagy növelik az energiafogyasztást, az orlisztát gátolja a hasnyálmirigy lipázait, ezáltal ~ 30% -kal csökkenti a bélből történő zsírfelszívódást (Borgstrom, 1988). A súlycsökkenés viszonylag szerény [kb. 3 kg 12 hónapon belül (Li et al., 2005)], de elég nagy ahhoz, hogy jótékony hatással legyen a kardiovaszkuláris kockázatra, amit az alacsony sűrűségű lipoprotein (LDL) koleszterinszint csökkenése is tükröz, vérnyomás és glikémia (Broom et al., 2002; Torgerson et al., 2004). Más szerekkel összehasonlítva a káros hatások korlátozottak, de hasmenést, puffadást, puffadást, hasi fájdalmat és diszpepsziát tartalmaznak (Bray és Greenway, 2007). Az írás idején az orlisztát az egyetlen olyan súlycsökkentő szer, amelyet hosszú távú klinikai alkalmazásra engedélyeztek Európában.
Jelen
A rimonabant visszavonása és számos CB1-receptor-antagonista fejlesztési program megszűnése ellenére okkal feltételezhető, hogy még nem értük el a CB1-receptorokat célzó elhízás elleni kezelések sorának végét (az áttekintéseket lásd Kunos et. al., 2008; Bermudez-Silva és mtsai, 2010). Először is, a rimonabant és a rokon vegyületek nem semleges CB1 receptor antagonisták, de jelentős inverz agonista aktivitással rendelkeznek ezeken a helyeken (Pertwee, 2006) (lásd 1. sz. Keretes szótár). A legújabb preklinikai bizonyítékok arra utalnak, hogy a semleges antagonisták megtarthatják a rimonabant súlycsökkenési előnyeit, de ennek a szernek a káros hatásai nélkül (pl. Cluny és mtsai, 2011). Másodszor ismert, hogy tolerancia alakul ki az akut anorecticus hatással szemben, a rimonabant-szerű vegyületek súlycsökkentő hatásaival szemben azonban nem, és hogy a súlycsökkentő hatás magában foglalhatja a perifériás szövetekben lévő CB1 receptorokat. Ez támogatná a CB1 receptor antagonisták további fejlődését, amelyek nem lépik át a vér-agy gátat; a közelmúltban több ilyen szerről is beszámoltak arról, hogy rágcsáló-modellekben súlycsökkenést okoznak (pl. Chen és mtsai, 2010; Randall és mtsai, 2010).
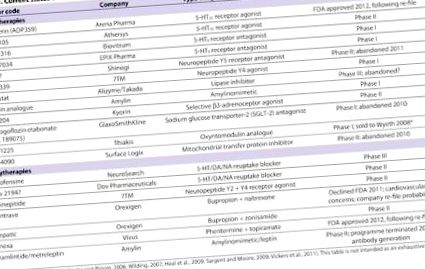
Az 1. táblázat számos olyan hatóanyagot sorol fel, amelyek jelenleg vagy egészen a közelmúltig az elhízás elleni gyógyszerfejlesztési folyamatban vannak (Cooke és Bloom, 2006; Wilding, 2007; Heal és mtsai, 2009; Sargent és Moore, 2009; Vickers és mtsai., 2011). Ezek a kezelések a központi idegrendszer és/vagy periféria különböző molekuláris célpontjaira, és egyes esetekben egyszerre több célpontra irányulnak. A potenciális új terápiák nagy száma nem lehet meglepő, ha egy biztonságos és hatékony elhízás elleni gyógyszerre 3,7 milliárd USD előrejelzett piaci méretet adunk (Vickers és Cheetham, 2007). A cikk keretein kívül esik az 1. táblázatban felsorolt összes lehetséges terápia áttekintése. Ehelyett a legígéretesebb és/vagy legizgalmasabb vizsgálati vonalak egy részére koncentrálunk.
Asztal 1.
Az elhízás elleni gyógyszerek és a gyógyszerkombinációk jelenlegi állapota
A jövő
Az elhízás hagyományos farmakológiai monoterápiái, bár kezdetben sikeresek voltak a fogyás elérésében, gyakran ellenszabályozás alá esnek. Ez nem meglepő, tekintettel az étvágyszabályozásban és az energia homeosztázisban szerepet játszó mechanizmusok sokaságára és redundanciájára (Adan et al., 2008; Vemuri et al., 2008). Ezért helyénvaló megjegyezni, hogy a legutóbb FDA jóváhagyásra benyújtott három kezelés közül kettő (Contrave ® és Qnexa ®) gyakorlatilag „politerápiák” - azaz kombinált szerek, amelyeket egyszerre több biológiai mechanizmus megcélozására terveztek, és amelyek végül hatékonyabbak a tartós fogyás és a társbetegségek javulásában. A politerápia előnyei, amelyek 20 évvel ezelőtt kezdődtek a fentermin és a fenfluramin kombinációjával, magukban foglalják az alacsonyabb gyógyszeradagok alkalmazását, az esetleges szinergikus, de legalább additív súlycsökkenést, a kevésbé súlyos mellékhatásokat és az ellenszabályozás csökkent lehetőségét (Greenway et al. ., 2009; Padwal, 2009; Roth és mtsai, 2010).
Ebben az összefüggésben ésszerűnek tűnik azt sugallni, hogy az ember által előidézett, központi idegrendszerre célzott szerek nagyobb valószínűséggel okoznak káros hatásokat, mint a természetesen előforduló biológiai jelek, amelyek általában szabályozzák a központi CNS-áramkörök aktivitását. Az elmúlt néhány évtizedben az alapkutatások (áttekintésként lásd: Cooke és Bloom, 2006; Field és mtsai, 2009; Halford és mtsai, 2010; Kennett és Clifton, 2010) számos olyan jelet azonosítottak, amelyek a bélből származnak ( pl. CCK, ghrelin, GLP-1, glükózfüggő inzulinotróp polipeptid, oxyntomodulin, PYY), hasnyálmirigy (pl. inzulin, amilin, hasnyálmirigy-polipeptid) és zsírszövet (pl. leptin, adiponektin). Ennek alapján az alapvető és alkalmazott kutatások megkezdték e molekulák kombinációinak terápiás potenciáljának értékelését - akár egymással [pl. amilin egér leptinnel (Trevaskis és mtsai., 2008)] vagy központilag ható szerrel [pl. amilin vagy pramlintid fenterminnel vagy sibutraminnal (Roth és mtsai, 2008; Arrone és mtsai, 2010)]. Amint az 1. táblázat mutatja, egy ilyen kombináció [pramlintide plusz metreleptin (Ravussin et al., 2009)] belépett a II. Fázisú klinikai vizsgálatokba, de a programot az antitestképződés és a bőrreakciók jelentős problémái miatt leállították (http: //www.takeda .com/press/article_42791.html).
Következtetések
Lábjegyzetek
Ez a cikk az elhízásról szóló különszám része: lásd a kapcsolódó cikkeket a Vol. 5. szám, Dis. Modell. Mech. a http://dmm.biologists.org/content/5/5.toc címen.
VERSENY ÉRDEKEK
M.H.T. a Roche Pharmaceuticals tanácsadója. J.P.H.W. tanácsadói és előadói díjakat kapott a Novo Nordisk-től (a liraglutid gyártói), osztályának pedig aktív kutatási támogatásokat kapott a Novo Nordisk és a Sanofi (akik GLP-1 agonistákat fejlesztenek).
FINANSZÍROZÁS
Ez a kutatás nem kapott külön támogatást egyetlen finanszírozó ügynökségtől sem az állami, sem a kereskedelmi, sem a nonprofit szektorban.
- Alekszandr Morozov elmondta, hogy megmentették a drogoktól és az elhízástól; Hírességek Hírek
- Az elhízás-járványt tápláló vérnyomáscsökkentő cikk AMP Reuters
- Az AMPA és a MENA tanácsadók bemutatják a marokkói amerikai hidakat 2015-ben Washingtonban
- 10 teljesítménynövelő gyógyszer, amelyek nem szteroidok a HowStuffWorks
- 10 új, az FDA által jóváhagyott endokrinológiai gyógyszerek endokrinológiai hálózata