Későn megjelenő hipogonadizmus: metabolikus hatás
Orvostudományi Tanszék Austin Health, Melbourne-i Egyetem, Melbourne, Vic., Ausztrália
Endokrinológiai Osztály, Austin Health, Melbourne, Vic., Ausztrália
Orvostudományi Tanszék Austin Health, Melbourne-i Egyetem, Melbourne, Vic., Ausztrália
Endokrinológiai Osztály, Austin Health, Melbourne, Vic., Ausztrália
Orvostudományi Tanszék Austin Health, Melbourne-i Egyetem, Melbourne, Vic., Ausztrália
Endokrinológiai Osztály, Austin Health, Melbourne, Vic., Ausztrália
Orvostudományi Tanszék Austin Health, Melbourne-i Egyetem, Melbourne, Vic., Ausztrália
Endokrinológiai Osztály, Austin Health, Melbourne, Vic., Ausztrália
Orvostudományi Tanszék Austin Health, Melbourne-i Egyetem, Melbourne, Vic., Ausztrália
Endokrinológiai Osztály, Austin Health, Melbourne, Vic., Ausztrália
Orvostudományi Tanszék Austin Health, Melbourne-i Egyetem, Melbourne, Vic., Ausztrália
Endokrinológiai Osztály, Austin Health, Melbourne, Vic., Ausztrália
Levelezés:
Mathis Grossmann, Orvostudományi Tanszék, Austin Health, Melbourne-i Egyetem, 145 Studley Road, Heidelberg, Vic. 3084, Ausztrália.
Absztrakt
Háttér
Az elhízás és a dysglykaemia (beleértve az inzulinrezisztenciát, a metabolikus szindrómát és a 2-es típusú cukorbetegséget), vagyis a cukorbetegség, a csökkent keringő tesztoszteronhoz és egyes férfiaknál az androgénhiányhoz igazodó klinikai jellemzőkhöz társul.
Célkitűzés
A későn megjelenő hipogonadizmus metabolikus hatásának áttekintése.
Mód
Átfogó irodalomkutatás, különös tekintettel a legújabb publikációkra.
Eredmények
Az elhízás az egyik legerősebben módosítható rizikófaktor a későn megjelenő hipogonadizmus szempontjából, és az együttesen fennálló cukorbetegség további hipotalamusz-hipofízis-herék tengelyének elnyomásához vezet. A hipotalamusz-hipofízis-here tengelyének elnyomása funkcionális és ennélfogva reverzibilis, és túlnyomórészt a hipotalamusz szintjén fordul elő. Míg a végleges mechanisztikus adatok hiányoznak, a bizonyítékok arra utalnak, hogy a hipotalamusz-hipofízis-herék tengelyének elnyomását a pro-gyulladásos citokinek diszregulációja közvetíti, ami hipotalamusz gyulladásához vezet. A központi leptin és az inzulinszignalizáció diszregulációja szintén hozzájárulhat. Ezzel szemben a legfrissebb adatok vitatják azt a paradigmát, miszerint az ösztradiol-felesleg a hipotalamusz-agyalapi mirigy-herék tengelyének elnyomásában játszik szerepet. Ehelyett a relatív ösztradiol-szignálhiány hozzájárulhat a metabolikus diszregulációhoz a cukorbetegségben szenvedő férfiaknál. Míg a súlycsökkenés és a társbetegségek optimalizálása megfordíthatja a funkcionális hipotalamusz-hipofízis-here tengely szuppresszióját, a tesztoszteron-kezelés metabolikusan kedvező változásokhoz vezet a testösszetételben és javul az inzulinrezisztencia terén.
Vita
A cukorbetegség és a későn megjelenő hipogonadizmus kapcsolata kétirányú. Az előzetes bizonyítékok arra utalnak, hogy gondosan kiválasztott férfiaknál az életmódbeli intézkedéseknek és a tesztoszteron-kezelésnek additív hatása lehet.
Következtetések
Míg a közelmúltban végzett kutatások új betekintést nyújtottak a cukorbetegséggel összefüggő, későn megjelenő hipogonadizmus mechanisztikus és klinikai aspektusaiba, további bizonyítékokra van szükség a jól megtervezett nagy kísérletekből az ilyen férfiak optimális klinikai megközelítésének irányításához.
Bevezetés
A tesztoszteron és a cukorbetegség társulásai a megfigyelési tanulmányokban
Az SHBG szerepe
Az elhízás tekintetében egyértelmű, hogy míg a szerény elhízás túlnyomórészt a csökkent SHBG-vel párhuzamosan csökkenő teljes tesztoszteronnal társul, a markánsabb elhízás (különösen a BMI> 35–40 kg/m 2) szintén a szabad tesztoszteron csökkenésével jár. Ez arra utal, hogy a markánsabb elhízás valódi biokémiai hipogonadizmussal jár. Összefoglalva, míg az alacsony tesztoszteron-diabétesz társulások némelyike az alacsonyabb SHBG-t tükrözi, a megfigyelési adatok határozottan arra utalnak, hogy az androgén-cukorbetegség kölcsönhatásai függetlenek az SHBG-től.
Tesztoszteron küszöb
Korábbi megfigyelések és kísérleti vizsgálatok férfiakon (Grossmann, 2018) azt sugallták, hogy a káros anyagcsere-hatások, például az inzulinrezisztencia, nagyrészt normálistól alacsonyabb tesztoszteron-koncentrációknál jelentkeznek (2016). Hasonlóképpen egy 70 541 férfit vizsgáló, nagy brit adatbázisban végzett tanulmányban, összehasonlítva a ≥ 20 nmol/l össztesztoszteronszintű férfiak referencia kohorszával, a T2DM jelentősen megnövekedett kockázata már a 15 és 19,99 nmol/l közötti tesztoszteronszintű férfiaknál is nyilvánvaló volt. arány arány = 1,29, 95% CI 1,13; 1.47, o 2019).
Összefoglalva, megfigyelési tanulmányok azt sugallják, hogy az alacsony tesztoszteron összefüggésbe hozható, és megjósolja a jövőbeni káros anyagcsere-eredményeket, mint például az inzulinrezisztencia, a metabolikus szindróma, a T2DM és az elhízás. Míg ezt az asszociációt részben az SHBG közvetíti, a szabad tesztoszteronnal és a tiszta androgén DHT-vel való független asszociációkra vonatkozó bizonyítékok, a módszertani figyelmeztetéseket leszámítva, SHBG-független asszociációkra utalnak. Érdekes, hogy a cukorbetegség kockázata magasabb tesztoszteron-koncentráció mellett nőhet, mint korábban értékelték.
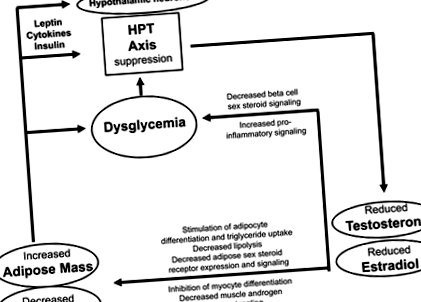
Korábbi megfigyelési tanulmányok, amelyeket a közelmúltban részletesen áttekintettek (Grossmann, 2018; Gianatti & Grossmann, 2019), arról számoltak be, hogy a cukorbetegség (beleértve a metabolikus szindrómát) a tesztoszteron gyorsabb csökkenésével jár, ami kétirányú társulásra utal (lásd alább). A korábbi munkával összhangban egy 141 fiatalabb (átlagéletkor 43 év), többnyire inzulinrezisztens férfinak végzett, nemrégiben készült prospektív tanulmányban az inzulinrezisztencia (oktreotid alapú hasnyálmirigy-szuppressziós teszt alkalmazásával mérve) hipogonadizmust jósolt (a teljes tesztoszteron meghatározása 2018). Egy 1400 svéd férfi (átlagéletkor 58 év) körében végzett nagyobb prospektív vizsgálatban azonban az alacsony tesztoszteron megjósolta az inzulinrezisztenciát (HOMA-IR-vel mérve), de a kiindulási érték magas inzulinrezisztenciája nem jósolta alacsony tesztoszteront a nyomon követés során (Ottarsdottir et al., 2018). Bár a megfigyelési tanulmányok, még akkor is, ha a prospektív nem képes megállapítani az okságot, és nem határozhatja meg az okozati összefüggés irányát, a bizonyítékok összességében összhangban állnak a kétirányú kapcsolattal. Egyrészt az alacsony endogén androgének elősegíthetik a cukorbetegség kockázatát, másrészt a cukorbetegség felgyorsíthatja a tesztoszteron életkorral összefüggő csökkenését. A potenciálisan alacsony endogén androgének és a cukorbetegség kölcsönhatásba lépnek egy önmegőrző ciklusban (1. ábra).
A beavatkozás és a kísérleti vizsgálatok (lásd alább) azt sugallják, hogy a tesztoszteron zsírtömegre és glükóz anyagcserére gyakorolt egyes hatásai függhetnek az ösztradiollá történő aromatizálódástól. Megfigyelési bizonyítékok, amelyek a keringő ösztradiolt és a cukorbetegséget társítják, kevés és ellentmondásos, részben a keringő tesztoszteron (a szubsztrát) és az ösztradiol (a termék) közötti kollinearitás miatt. Továbbá az ösztradiolt a vizsgálatok többségében immunvizsgálattal mértük, amelynek hiánya a pontosság a férfiak viszonylag alacsony keringő ösztradiol-koncentrációinak számszerűsítésében (Russell & Grossmann, 2019).
Az alacsony tesztoszteron-cukorbetegség kapcsolatának irányíthatósága
10% -os testsúlycsökkenés. Bariatrikus műtét (
A testtömeg 30% -os csökkenése) a teljes tesztoszteron 8,73 nmol/l (95% CI 6,51; 10,95) markánsabb növekedésével jár (Corona et al., 2013). Megfelelő testsúlycsökkenés esetén (a testtömeg ≥10% -a) a gonadotropinok és a szabad tesztoszteron szintje is megemelkedik, ami a HPT tengely valódi reaktiválódására utal (Camacho et al., 2013; Korona et al., 2013). Összességében elmondható, hogy az endogén tesztoszteron változásai, amelyek nem sebészeti súlycsökkentő intézkedésekkel érhetők el, viszonylag szerények. A motivált, elhízott férfiak tesztoszteronkezelésének és étrendjének nemrégiben elvégzett RCT-jében egy szigorú, strukturált étrend-program, amely 11 kg-os testsúlycsökkenéshez vezetett, a placebo csoportban csak mérsékelten, 2,9 nmol/l-rel növelte a szérum tesztoszteront (Ng Tang Fui et al., 2016). Ez a hatás nem volt fenn 18 hónappal a vizsgálat befejezése után (Ng Tang Fui et al., 2017a, b, c). A testtömeg változásaira adott HPT tengely reakciókészségével összhangban a biokémiai hipogonadizmus nem állandó állapot; az EMAS-ban átlagosan 4,3 évig tartó követés során a biokémiai hypogonadotrop hypogonadismusban szenvedő férfiak 43% -a gyógyult meg az eugonadizmusban. A kiindulási súlycsökkenés és az elhízás volt a legerősebb előrejelző (Rastrelli et al., 2015).
Ezzel szemben az endogén tesztoszteron koncentrációjának változásai a testtömeg viszonylag szerény változásaival társulnak; még a tesztoszteront nulla közeli szintre csökkentő androgén-deprivációs terápia (ADT) által okozott súlyos tesztoszteronhiánynak is csak csekély hatása van a testsúlyra. Egy lokális prosztatarákban szenvedő idősebb férfiak prospektív vizsgálatában, akik a kiinduláskor eugonadalisak voltak (teljes tesztoszteron 14 nmol/l), 12 hónapos ADT után (a teljes tesztoszteron 0,4 nmol/l-re csökkentve) a BMI csak 0,65 kg/m 2 (95% CI 0,14; 1,15) összehasonlítva az illesztett prosztatarák kontrollokkal, akik nem kaptak ADT-t (Cheung et al., 2016). Az ADT azonban egyértelműen a testösszetételre gyakorolt metabolikusan káros hatásokkal jár. A zsírtömeg 3,5 kg-mal nőtt [95% CI 2,0; 5,0] és a sovány tömeg 1,5 kg-mal csökkent (95% CI 0,2; 1,8), ami az inzulinrezisztencia 30% -os növekedésével jár (HOMA-IR méréssel) (Cheung et al., 2016). A tesztoszteron kezelés klinikai vizsgálatok hatásait az alábbiakban tárgyaljuk, de összhangban vannak a cukorbetegség és az alacsony tesztoszteron közötti kétirányú kapcsolattal, az előbbi dominánsabb hatásokkal.
Az alacsony tesztoszteron-cukorbetegség kapcsolatának lehetséges mechanizmusai
Az alacsony tesztoszteronszintet elősegítő cukorbetegség
Míg a szerény elhízás/inzulinrezisztencia elsősorban az alacsony teljes tesztoszteronszinthez kapcsolódik az alacsonyabb SHBG miatt, a markánsabb elhízás valódi biokémiai hipogonadizmushoz vezet, amit a szabad tesztoszteron csökkenése is bizonyít (Grossmann, 2018). Cukorbetegségben és/vagy elhízásban szenvedő és alacsony tesztoszteronszintű férfiak, amint azt Dandona csoportja (Dhindsa et al., 2018), ritkán vannak megemelkedett gonadotropin koncentrációk. Ezért az endogén tesztoszteron cukorbetegséggel összefüggő csökkenését a központi gonad tengely elnyomásának tekintik. Ez nagyrészt a hipotalamusz szintjén fordulhat elő. Ahogy máshol is áttekintettük, a gyulladáscsökkentő adipocitokinek, a központi idegrendszer inzulinjelének károsodása (CNS) és a szabályozatlan leptinjelzés hozzájárulhatnak a hipotalamusz szuppressziójához, valószínűleg, legalábbis részben, a KNDy-re gyakorolt hatásokon keresztül (kisspeptin/neurokinin B/dynorphin) neuronok a hipotalamusz íves magjában (Dhindsa et al., 2018; Grossmann, 2018; Rastrelli et al., 2018; Gianatti & Grossmann, 2019).
Alacsony tesztoszteron elősegíti a cukorbetegséget
Férfiaknál nem világos, hogy a tesztoszteron kezelés glükóz metabolizmusra gyakorolt hatása mennyiben függ a testösszetétel metabolikusan kedvező változásainak elősegítésétől (azaz a sovány tömeg növekedése és a zsír tömegének csökkenése). Megjegyzendő, hogy a tesztoszteron-kezelés hatással van-e a metabolikusan aktív zsigeri zsírszövetre (lásd alább). Kis tanulmányok arról számoltak be, hogy a tesztoszteron közvetlenül és élesen szabályozhatja az inzulinérzékenységet, mielőtt a testösszetétel változása várhatóan bekövetkezik (Yialamas et al., 2007). Sőt, rövid távú hiperinsulinémiás-euglikémiás clamp vizsgálatok egészséges felnőtt férfiaknál, akiknek farmakológiailag megváltozott az endogén nemi szteroid koncentrációja, az inzulinérzékenység változásáról számoltak be a BMI változásának hiányában (Lapauw et al., 2010; Gibb et al., 2016). Ezek a tanulmányok a tesztoszteron és az ösztradiol inzulinérzékenységre gyakorolt különbségeit is megvizsgálták (további részleteket az alábbiakban tárgyalunk). Egyéb lehetséges mechanizmusok az energiafogyasztás változásai vagy a fizikai aktivitás iránti fokozott motiváció (Ng Tang Fui et al., 2016), de nem létezik határozott bizonyíték.
Az ösztradiol szerepe
A tesztoszteron kezelés metabolikus hatása klinikai vizsgálatokban
A T2DM-ben és/vagy a metabolikus szindrómában szenvedő férfiaknál a 2016 előtt közzétett RCT-ket másutt alaposan átnézték et al., 2018; Grossmann, 2018; Rastrelli et al., 2018; Gianatti & Grossmann, 2019). Összességében a megállapítások azt sugallják, hogy a tesztoszteron-kezelés következetesen és szerény módon növeli a sovány tömeget (kb. 2 kg-mal), csökkenti a zsírtömeget (körülbelül 2 kg-mal), és szerényen javítja az inzulinrezisztenciát a legtöbb, de nem minden vizsgálatban. Ezzel szemben a tesztoszteron-kezelésnek nincs következetes hatása a zsigeri zsírszövet tömegére és a HbA1c-vel mért glikémiás kontrollra. A placebo-kontrollos kettős-vak RCT-kre korlátozott metaanalízis (n = 7) arra a következtetésre jutott, hogy a tesztoszteron-kezelés mérsékelten javította az inzulinrezisztenciát, összehasonlítva a placebóval, az összesített átlag különbség (MD) −1,58 (95% CI −2,25; −0,91, o 2015). A vizsgálatok azonban viszonylag kicsiek voltak (összesen n = 833 férfi) és rövid távú (≤ 12 hónap). A felvételi kritériumok heterogének voltak, és a résztvevők általában jól kontrollált cukorbetegségben szenvedtek. Ráadásul a tesztoszteron eritropoetikus hatásai miatt a HbA1c nem tükrözi pontosan a környezeti glikémiát. A Corona egy későbbi nagyobb metaanalízise et al. (2016) 59 vizsgálatot tartalmazott, összesen csaknem 5100 idősebb férfi (átlagéletkor 62 év), amelyek a tesztoszteron testösszetételre és glükometabolikus kimenetelre gyakorolt hatásáról számoltak be. A vizsgálatokat a tesztoszteron kiindulási koncentrációjától vagy a metabolikus betegség jelenlététől függetlenül vonták be. A placebo csoport nélküli kontroll nélküli vizsgálatok szintén alkalmasak voltak. Míg a tesztoszteron-kezelés nem csökkentette a testsúlyt, a derékbőséget vagy a BMI-t, a zsírtömeg csökkent (standardizált átlagérték: -0,34, 95% CI -0,48; −0,20, o 2016).
Számos közelmúltbeli, placebo-kontrollos kettős-vak RCT-ből számoltak be glükometabolikus eredményekről. Egy kis 12 hónapos RCT-ben 55 elhízott, T2DM-es szájüregi antidiabetikus mediáció mellett, a hosszú hatású intramuszkuláris undecanoát 4,64-rel csökkentette a HOMA-IR-t és 0,94% -kal a HbA1c-t a placebóhoz viszonyítva, a BMI vagy a derék között nem volt szignifikáns különbség kerület (Groti et al., 2018). Egy 134 nem cukorbeteg férfi alcsoportjának másodlagos elemzésében vettek részt a tesztoszteron-hatások időskorú férfiak ateroszklerózisára (TEAM) vizsgálatban, átlagos kiindulási életkoruk 66 év volt, a BMI 28 kg/m 2 és az összes tesztoszteron 11,4 nmol/L, 3 éves topikális tesztoszteron gél (az átlagos szérum tesztoszteron 16,6 nmol/l elérése a tesztoszteron csoportban) az oktreotid inzulin szuppressziós teszteléssel értékelve nem volt hatással a testtömegre vagy az inzulinérzékenységre (Huang et al., 2019). A nagy tesztoszteron-vizsgálatban, amelybe 788 65 évnél idősebb férfit vontak be (a kiinduláskor 72% elhízott, 37% -uk cukorbeteg volt), 2018-as szérum tesztoszteronnal).
| Testsúly | Nincs változás a Nem randomizált, nem vak vizsgálatokban csökkenést jelentettek. |
| Zsírtömeg | Csökken |
| Sovány tömeg | Növekedés |
| Májzsír | Nincs változás |
| Zsigeri zsír | Csökken vagy nincs változás |
| Inzulinrezisztencia (HOMA ‐ IR) | Csökken vagy nincs változás |
| Inzulinrezisztencia (hiperglikémiás-euglikémiás bilincsek) | Csökken, vagy nincs változás |
| HbA1c | Nincs változás a Nem randomizált, nem vak vizsgálatokban csökkenést jelentettek. |
| Teljes koleszterinszint | Csökken |
| LDL-koleszterin | Csökken |
| HDL koleszterin | Csökken |
| Trigliceridek | Csökken vagy nincs változás |
- a Nem randomizált, nem vak vizsgálatokban csökkenést jelentettek.
Következtetések
KÖSZÖNETNYILVÁNÍTÁS
Az MNTF-et egy ESA-RACP kutatóintézeti ösztöndíj és MG támogatásával az NHMRC karrierfejlesztési munkatársa (1024139) támogatta.
Közzétételek
Az MG kutatási támogatást kapott a Bayertől, a Novartistól, a Súlyfigyelőktől, a Lillytől és az előadó honoráriumait a Besins Health Care-től. Az MNTF kutatási támogatást kapott a Bayer Pharma-tól. Az ASC megkapta az előadó tiszteletdíját az Astra Zenecától és a Merck Sharp & Dohme-tól (Ausztrália).
- Antonio L, Wu FC, O'Neill TW, Pye SR, Carter EL, Finn JD, et al. (2015) A nemi szteroidok és a metabolikus szindróma kialakulása közötti összefüggések: longitudinális vizsgálat európai férfiaknál . J Clin Endocrinol Metab 100, 1396-1404 .
A CrossRef szerint idézett alkalmak száma: 12
- Omer Faruk Kirlangic, Didem Yilmaz-Oral, Ecem Kaya-Sezginer, Gamze Toktanis, Aybuke Suveyda Tezgelen, Ekrem Sen, Armagan Khanam, Cetin Volkan Oztekin, Serap Gur, Az androgének hatása a kardiometabolikus szindrómára: Jelenlegi terápiás koncepciók01, szexuális orvoslás /j.esxm2020.02.006, (2020).
Az előrehaladott krónikus vesebetegség a hipogonadizmus erős előrejelzője, és társul a csökkent sovány szöveti tömeggel
- A magas energiájú étrend veszélyezteti a férfi termékenységet Rato - 2014 - Elhízási vélemények - Wiley Online Könyvtár
- Az élelmi rostok egészségügyi előnyei - Anderson - 2009 - Táplálkozási vélemények - Wiley Online Könyvtár
- Az elhízás hatása a török ország egész területén a 2-es típusú cukorbetegség metabolikus kontrolljára
- Tömegspektrometrián alapuló metabolomika - Dettmer - 2007 - Tömegspektrometriai vélemények - Wiley Online
- A magas zsírtartalmú étrend megváltoztatja a szérum citokineket az elhízás megjelenése előtt - Song - 2020 - The FASEB Journal