Az inzulinszerű növekedési faktor I. stimulálja a csontok kirakodása után elveszett csontok helyreállítását
Absztrakt
a csontváz kirakodása osteopeniát vált ki (3, 4, 10, 19, 26, 29–31). A kirakodás során bekövetkező progresszív csontvesztés nagyrészt az oszteoblaszt toborzás és aktivitás csökkenésének következménye (8, 9, 11, 18, 30).
Az inzulinszerű növekedési faktor (IGF) -I, a csontok hatékony anabolikus ágense, elősegíti az osteoprogenitor proliferációt, az osteoblast képződést és az osteoblast túlélést, és serkenti a csontképződést (6, 7, 25). Az oszteoblaszt aktivitás csökkenése és a csontok kirakodása által kiváltott csontvesztés az IGF-I anabolikus hatásaival szembeni csontreakció csökkenésével jár (5, 12, 20, 22). A csontváz kirakodása a patkány hátsó szárának emelkedési modelljével rontja az IGF-I receptor aktiválódását, megzavarja az IGF-I jelátvitelt, és gátolja az oszteoblaszt képződését és aktivitását (5, 20, 22).
Jóllehet a csontváz kirakodását és a csontvesztésért felelős mechanizmusokat jól tanulmányozták, mi történik a csontokkal, ha a csontváz újratöltése után egy kirakodási időszak kevesebb figyelmet kapott. Az űrrepülés során vagy az űrrepülés súlytalanságát utánzó modellekben elvesztett csontok legalább részben helyreállnak a normál terheléshez vagy a súlyviseléshez való visszatérés után, de a folyamat rendkívül lassú (1, 2, 14, 15, 23, 28). A teljes gyógyulás soha nem fordulhat elő. A 14 napos űrrepülési küldetéseknél a csontváz tömege a patkányban csökken. Tizennégy nappal azután, hogy visszatér a normális ambulációhoz, a csontképződés megnövekedett, de a csonttömeg teljes helyreállítása még nem történt meg (14, 32). Az emberi ágynyugalmi vizsgálatok során a csont is elveszett, és a gyógyuláshoz 6 hónapos vagy annál több normális ambulációra lehet szükség (16). Ezek a tanulmányok azt mutatják, hogy a csontváz kirakodása során elvesztett csont legalább részben helyreállhat a normális testsúly visszatérésével, de a folyamat lassú, és ebben az időszakban megnőhet a törés kockázata.
Arra a megfigyelésre alapozva, hogy a csontváz kirakodása rezisztenciát vált ki az IGF-I-vel szemben, feltételeztük, hogy egy kirakodás utáni újratöltés növeli a csont reakcióképességét az IGF-I iránt és elősegíti a csontok helyreállítását. Ennek a hipotézisnek a teszteléséhez megvizsgáltuk a csont szerkezetét és kialakulását az IGF-I hatására terhelt (normál ambuláns), terheletlen (hátsó lábszár emelkedés) és terheletlen/újratöltött patkányokban.
Állatok
Negyvennyolc hím Sprague-Dawley patkányt (Charles River Laboratories, Wilmington, MA; 3 hónapos) használtunk erre a vizsgálatra. A csontváz kirakodását a hátsó szár emelkedésének vagy a farok felfüggesztésének modelljével indukáltuk (10, 19, 31). Az állatokat hat, egyenként nyolc állatból álló csoportba osztottuk. Vagy normálisan 4 hétig, 4 hétig vagy 2 hétig, majd 2 hétig újratöltik őket. Mindegyik csoportot vivőanyaggal vagy IGF-I-vel (2,5 mg · kg –1 · nap –1) kezeltük ozmotikus minipumpákkal (Durect, Cupertino, CA) az utolsó 2 héten keresztül. A kirakodáshoz és az újraterheléshez választott időintervallumok korábbi vizsgálatokon alapultak, amelyek azt mutatták, hogy 2 hetes kirakodás egyértelmű csökkenést eredményez a csontképződés sebességében és a szivacsos csontmennyiség csökkenésében, és hogy 2 hét újratöltés megindítja a csontképződés növekedését és a csontmennyiség helyreállítását (23) Az állatokat páronként etették és naponta lemérték. A csontképződés mérésére 2 hét és 2 nappal az eutanázia előtt a patkányokat szubkután kalceinnel (15 mg/kg) és demeclociklinnel (20 mg/kg) injektálták az mineralizáló felületek jelölésére.
Az eutanázia idején vért gyűjtöttünk a hasi aortából, és szérumot gyűjtöttünk az IGF-I meghatározásához. A bal lábszárcsontot és a második ágyéki csigolyát kaptuk a zsírmentes tömeg mérésére és a mikro-komputertomográfiára. A jobb sípcsontot a periostealis csontképződési sebesség mérésére kaptuk. Ezeket a vizsgálatokat a San Francisco Veterans Affairs Medical Center állatgondozási és felhasználási bizottsága hagyta jóvá.
Mikroszámítógépes tomográfiai letapogatási eljárás
A sípcsontokat és a csigolyákat megtisztítottuk a tapadó lágyrészektől, és etanollal (24 óra) és dietil-éterrel (24 óra) extraháltuk egy soxhlet-készülék segítségével (Fisher Scientific, Pittsburg, PA). A csontokat 100 ° C-on szárítottuk, és megmértük a zsírmentes tömeg meghatározásához. Ugyanezeket a csontokat mikroszámítógépes tomográfiával elemeztük (Scanco Medical, Zürich, Svájc).
Elsődleges spongiosa.
A sípcsontok proximális végeit az epiphysis tetejétől disztálisan, a szekunder spongiosa közepéig pásztáztuk, hogy az magában foglalja a teljes primer spongiosa-t. Az izotróp voxel (volumetrikus pixel) mérete névlegesen 10,5 μm volt. A röntgenenergia 55 kV volt. Az elsődleges szivacs belső szerkezete a mineralizált szövet, a velő és a porc összetett keveréke. E különbözõ struktúrák jobb megkülönböztetése érdekében 1 másodpercre állítottuk az integrációs idõt a jel-zaj arány optimalizálása érdekében.
A csont keresztmetszeteit hosszanti metszetekké alakítottuk át, hogy a felhasználó vizuálisan felismerhesse és izolálhassa az elsődleges szivacsot, az érdekes régiót (ROI). A ROI határa a növekedési lemez volt a proximális felületen és a csont spiculák vége a disztális oldalon. A kéreg volt az oldalsó határ.
Másodlagos spongiosa.
A proximális sípcsont elemzési régióját a következőképpen határoztuk meg. Háromszáz szeletet (16 μm voxelt) pásztáztunk a növekedési lemez aljától distálisan. Az első 100 szeletet (1,6 mm) eldobtuk, és elemeztük a növekedési lemez alatti 1,6 és 4,8 mm közötti régiót. A csigolyák elemzési régiója a teljes csigolyatestet magában foglalta, a kortikális csont kivételével.
Mikroszámítógépes tomográfiai letapogatás elemzése
Globális küszöbértéket alkalmaztunk a lágy szövetekből (sovány és zsírvelő) mineralizált szegmensre. A szekunder spongiosa esetében a küszöbértéket a lehetséges maximális érték 22% -aként határozták meg, ami a 220-as küszöbértéknek felel meg a „promillus” egységben. A trabekuláris szám (Tb.N; 1/mm), vastagság (Tb.Th; μm) és távolság (Tb.Sp; μm); szoftverrel számoltuk a kapcsolódási sűrűséget (Conn-dens; 1/mm 3), a struktúra modell indexét (SMI; 0 és 3 közötti tartományban, 0 = platelikus és 3 = rúdszerű) és a csont ásványi sűrűséget (BMD; mg hidroxi-apatit/cm 3). a Scanco (Scanco Medical) nyújtotta. A BMD a ROI (csont) szegmentált frakciójának átlagos sűrűsége, a velő frakciót nem beleértve. A BMD a röntgensugár lineáris csillapítási együtthatójából származik, miután ismert hidroxiapatit sűrűségű fantommal kalibrálták.
Az ásványosodott szövet átlagos sűrűsége az elsődleges szivacsokban átlagosan alacsonyabb, mint a szekunder csont sűrűsége a másodlagos szivacsokban, és széles tartományt ölel fel a hipertrófiás kondrocita zóna szomszédságában található legalacsonyabbtól a legmagasabbig a csont spiculákban. Az elsődleges spongiosa alacsonyabb sűrűségének kielégítése érdekében a küszöbértéket a maximális lehetséges érték 20% -aként rögzítették, ami a promillus egység 200-as küszöbének felel meg. Az előre meghatározott küszöbértéket az operátor ellenőrizte az mineralizált szövetek összehangolása érdekében, amint azok a mikro-komputertomográfiás felvételen hosszanti metszetekben megjelennek.
Csont hisztomorfometria
A periostealis csontképződési sebességet a tibiofibularis csomópontnál (TFJ) (modellünkben terheletlen csont) és a midhumerusnál (modellünkben terhelt csont) mértük. A sípcsontokat és a humerit 4% foszfáttal pufferolt formalinban rögzítettük 24 órán át, növekvő koncentrációban etanolban dehidráltuk, és abszolút acetonban, majd éterben zsírtalanítottuk. A csontokat bioplasztikus műanyagba ágyazták (Tap Plastics, Dublin, Kalifornia). Egy éjszakán át 60 ° C-on végzett polimerizáció után a metszeteket (100 μm) egy Leica SP 1600 körfűrésszel (Leica, Deerfield, IL) vágtuk, és a csontképződési sebességet a kereskedelemben kapható képelemző programmal (BIOQUANT Image) korábban leírt módon mértük. Elemzés, Nashville, TN) (11).
Szérum IGF-I
A szérum IGF-I szinteket az American Laboratory Products (ALPCO, Windham, NH) által gyártott IGF-I (IGF-kötő fehérje blokkolva) RIA alkalmazásával határoztuk meg, a korábban leírtak szerint (20). A vizsgálat számított érzékenysége 0,02 ng/ml. Az IGF-II-vel való keresztreaktivitás kicsi ( 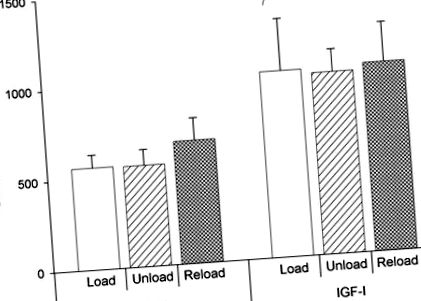
1. ábra.Az inzulinszerű növekedési faktor I (IGF-I) szérumkoncentrációja 28. nap. Az értékek átlag ± SD. Az IGF-I kezelés a hordozóval kezelt állatokban 599 ± 43 ng/ml-ről az IGF-I-vel kezelt állatokban 1024 ± 41 ng/ml-re növelte a szérumkoncentrációt. §P
A sípcsont zsírmentes súlya (testtömegre normalizálva) nem különbözött a csoportok között (2. ábra), bár volt tendencia, hogy a hordozóval kezelt, terheletlen állatok szintje alacsonyabb volt (P = 0,06). A zsírmentes súlyokat normalizálták, hogy korrigálják a testtömeg kis különbségét 28. nap.
2. ábra.A sípcsont zsírmentes súlya a testtömegre normalizálódott 28. nap. Az értékek átlag ± SD. A csontsúlyokat normalizáltuk, hogy korrigáljuk a testtömeg kis különbségét 28. nap. A csoportok között nem volt szignifikáns különbség (2-utas ANOVA).
A periosztealis csontképződés sebességét a TFJ-nél és a midhumerusnál a 3. ábra mutatja, A és B, illetőleg. Hordozóval kezelt állatokban a csontváz kirakodása 17 ± 6-ról 6 ± 3 × 10 3 μm 2/napra csökkentette a TFJ képződését (P 3 μm 2/nap (P 3 μm 2/nap vagy 238% (P 3 μm 2/nap) és az IGF-I-vel kezelt állatok (16 × 10 3 μm 2/nap)> 700%. A periostealis felület fluorokróm jelölését a 3. ábra mutatja, C és D, hordozóval vagy IGF-I-vel kezelt újratöltött állatok esetében. A humerus, amely normálisan terhelt és modellünkben kontrollcsontként működik, reagált az IGF-I-re, de a terhelési állapot nem befolyásolta (3. ábraB). A képződési arány az IGF-I-vel kezelt állatokban ~ 60% -kal volt magasabb (P
3. ábra.Az IGF-I kezelés és a csontváz kirakodásának hatása a periostealis csontképződési sebességre (BFR) a tibiofibularis csomópontban (TFJ, modellünkben egy terheletlen csont) (A) és a humerus középső tengelye (modellünkben normálisan terhelt csont) (B). Az értékek átlag ± SD. A periostealis csontképződés mértékének mérésére 2 héttel, illetve 2 nappal az eutanázia előtt kettős fluorokróm jelzést (kalcein és demeclociklin) adtunk. C és D mutatják be az újratöltött jármű fluorokróm-jelölési mintáit (C) és újratöltött IGF-I-vel kezelt állatok (D). Ban ben A: *P
A csontváz kirakodása a proximális sípcsontban a csontritkulás csökkenését eredményezte (4. ábraA) és a csigolya (4. ábraB) mind a vivőanyaggal, mind az IGF-I-vel kezelt állatokban. A sípcsontban 2 hét múlva történő újratöltés növelte a rákos csontmennyiséget az IGF-I-vel kezelt, de nem vivőanyaggal nem kezelt állatokban. A csigolyákban az újratöltés nem eredményezett szignifikáns növekedést a csontmennyiségben sem vivőanyaggal, sem IGF-I-vel kezelt állatokban.
4. ábra.Az IGF-I kezelés és a csontváz kirakodásának hatása a proximális sípcsont szivacsos csontmennyiség/teljes szövet térfogat arányára (BV/TV) (A) és az ágyéki csigolya (B). Az értékek átlag ± SD. A csontmennyiséget mikroszámítógépes tomográfiai elemzéssel értékeltük, az anyagok és módszerek szerint. *P
Az IGF-I kezeléssel és a csontváz kirakodásával kiváltott csontmennyiség változásai a csont szerkezetének specifikus változásaival társultak (1. és 2. táblázat). A sípcsont másodlagos szivacsos részén a Tb.Th a kirakodáskor csökkent, majd az újratöltéssel nőtt az IGF-I-vel kezelt állatokban (1. táblázat). A Tb.Th nem változott szignifikánsan a vivőanyaggal kezelt állatok kirakodásakor, de az újratöltés során jelentősen megnőtt a kirakodott állapothoz képest. A csigolyákban a Tb.Th csökkent mind a vehikulummal, mind az IGF-I-vel kezelt állatokban, de az újratöltéssel nem nőtt (2. táblázat). A csatlakozási sűrűség a sípcsontok tehermentesítésével csökkent, de a csigolyákban nem. Az SMI növekedett (a trabeculák szerkezete rúdszerűbbé vált) mind a járművekkel, mind az IGF-I-vel kezelt állatok sípcsontjaiban és csigolyáiban a kirakodás során, és az újratöltés során platósabb struktúrába került, kivéve a járművekkel kezelt állatok csigolyáit. A szegmentált BMD-ben változás nem volt megfigyelhető.
Asztal 1. Az IGF-I kezelés és a csontváz kirakodásának hatása a proximális sípcsont szivacsos csontszerkezetére
Az értékek átlag ± SD. Terhelés, általában 4 hétig terhelve; 4 hét múlva kirakodva; Töltsük be, 2 hét múlva és 2 hét múlva újratöltve. A kezelést szubkután minipumpákkal végeztük az utolsó 2 héten. [Vivőanyag vagy inzulinszerű növekedési faktor I (IGF-I).] Tb.N, trabekuláris szám; Tb.Th, trabekuláris vastagság; Tb.Sp, trabekuláris távolság; Csatlakozási sűrűségek, csatlakozási sűrűség SMI, struktúra modell index; szegmentált BMD, a trabekulák átlagos sűrűsége, HA, hidroxi-apatit. A szignifikáns különbségeket egy egyutas varianciaanalízissel értékeltük, amelyet Holm-Sidac post-hoc teszt követett.
* Jelentősen különbözik a terhelés szabályozásától, P † Jelentősen különbözik a kirakodástól, P
2. táblázat. Az IGF-I kezelés és a csontváz kirakodásának hatása a második ágyéki csigolyák szivacsos csontszerkezetére
Az értékek átlag ± SD. A szignifikáns különbségeket egy egyutas varianciaanalízissel értékeltük, amelyet Holm-Sidac post-hoc teszt követett.
* Jelentősen különbözik a terhelés szabályozásától, P † Jelentősen különbözik a kirakodástól, P
5. ábra.A proximális sípcsont elsődleges szivacsos mikroszámítógépes tomográfiájának háromdimenziós ábrázolása (A) és a proximális sípcsont kétdimenziós mikroszámítógépes tomográfiai szakasza (B). A tenyészlemez nincs lezárva (nyílhegyek), és az elsődleges spongiosa lényegesen nagyobb (nyilak) az IGF-I-vel kezelt újratöltött patkányokban.
6. ábra.Az IGF-I kezelés és a csontváz kirakodásának hatása a teljes értékre (A) és meszesített (B) az elsődleges spongiosa mennyiségei. Az értékek átlag ± SD. A mennyiségeket mikrokomputertomográfiával értékeltük, az anyagok és módszerek szerint. *P
A testtömeg hasonlósága a vivőanyaggal kezelt és az IGF-I-vel kezelt csoportokon belül arra utal, hogy a kirakodáshoz kapcsolódó csontváltozások nem a testtömeg változásainak következményei voltak. Azok az állatok, akik IGF-I-t kaptak együttesen, szignifikánsan nehezebbek voltak, mint a hordozóval kezelt állatok. Ezek a megállapítások összhangban vannak a kezelt állatok szérum IGF-I emelkedésével és az IGF-I anabolikus hatásaira várható válaszsal.
Bár a csoportok között nem történt jelentős változás a zsírmentes tömegben, a kirakodás általában a csonttömeg kismértékű (9%) csökkenését eredményezte. Ezt figyelték meg 6 hónapos patkányokban is, ahol a csontváz 4 hét múlva történő kirakodása ~ 10% -kal csökkentette a csonttömeget (9). Fiatal patkányokon (6 hetes idősek) végzett vizsgálatokban a csontváz kirakodása sokkal nagyobb csonthiányt (12-25%) eredményez sokkal rövidebb idő alatt (2 hét) (10, 23). Ez magyarázható a fiatal állatok magas anyagcseréjével és gyors csontforgalmával. A magas csontforgalom várhatóan nagyobb lehetőséget nyújt a csonttömeg elvesztésére vagy gyarapítására, és ez megmagyarázhatja, hogy az idősebb állatok miért reagálnak lassabban a kirakodásra a zsírmentes súly és a csonttartalom változása tekintetében.
- Anyagtudomány és a növekedési faktor szállító rendszerek tervezési alapelvei a szövetmérnöki és
- Elvesztettem a menstruációmat
- A hepatocita nukleáris faktor ‐ 1 béta mutációi újszülöttkori cukorbetegséget és intrauterin növekedést okoznak
- Hogyan fogytam 40 kg-ot a terhességem után - a Chriselle-faktor
- Hogyan fogyott Seth Rogen 30 kilót az 5 faktoros étrenddel; Tom Corson-Knowles