Bélmikrobiota a korai életben és következményei a gyermekkori egészségre
Lu Zhuang
1 Társult Bayi Gyermekkórház, a PLA Általános Kórház hetedik orvosi központja, Peking 100700, Kína
4 Országos mérnöki laboratórium a születési rendellenességek megelőzésére és a legfontosabb technológia ellenőrzésére, Peking 100700, Kína
5 Pekingi kulcsfontosságú gyermekszervi kudarc laboratórium, Peking 100700, Kína
Haihua Chen
1 Társult Bayi Gyermekkórház, a PLA Általános Kórház hetedik orvosi központja, Peking 100700, Kína
2 A Dalian Orvostudományi Egyetem Első Klinikai Akadémiája, Dalian 116011, Kína
Sheng Zhang
1 Társult Bayi Gyermekkórház, a PLA Általános Kórház hetedik orvosi központja, Peking 100700, Kína
4 Országos mérnöki laboratórium a születési rendellenességek megelőzésére és a legfontosabb technológia ellenőrzésére, Peking 100700, Kína
5 Pekingi kulcsfontosságú gyermekszervi kudarc laboratórium, Peking 100700, Kína
Jiahui Zhuang
3 Környezetvédelmi Főiskola, Northeast Normal University, Changchun 130117, Kína
Qiuping Li
1 Társult Bayi Gyermekkórház, a PLA Általános Kórház hetedik orvosi központja, Peking 100700, Kína
4 Országos mérnöki laboratórium a születési rendellenességek megelőzésére és a legfontosabb technológia ellenőrzésére, Peking 100700, Kína
5 Pekingi kulcsfontosságú gyermekszervi kudarc laboratórium, Peking 100700, Kína
Zhichun Feng
1 Társult Bayi Gyermekkórház, a PLA Általános Kórház hetedik orvosi központja, Peking 100700, Kína
4 Országos mérnöki laboratórium a születési rendellenességek megelőzésére és a legfontosabb technológia ellenőrzésére, Peking 100700, Kína
5 Pekingi kulcsfontosságú gyermekszervi kudarc laboratórium, Peking 100700, Kína
Absztrakt
Milliárd mikroba él az emberi testben, és részt vesz több olyan fiziológiai és patofiziológiai folyamatban, amelyek az egész életciklus alatt befolyásolják a gazdaszervezet egészségét. A mikrobiomot jellegzetes kompozíciós és funkcionális jellemzők jellemzik a különböző életszakaszokban. A halmozódó bizonyítékok azt mutatták, hogy az emberi testben élő mikrobák alapvető szerepet játszhatnak a csecsemők fejlődésében és az immunrendszer érésében. A bélmikrobákat elengedhetetlennek tartják az infantilis és gyermekkori fejlődés megkönnyítésében és immunitás azáltal, hogy segíti az élelmiszer-anyagok lebontását a tápanyagok felszabadítása érdekében, védelmet nyújt a kórokozókkal szemben, stimulálja vagy módosítja az immunrendszert, és ellenőrzést gyakorol a hipotalamusz – hipofízis – mellékvese tengely felett. Ez az áttekintés a bél mikrobiota kolonizációjának és fejlődésének jelenlegi megértését kívánja összefoglalni korai élet, kiemelve a bélmikrobák gyermekkorban betöltött szerepével kapcsolatos legújabb megállapításokat betegségek. Ezenkívül megvitatjuk azokat a mikrobiota által közvetített terápiákat is, amelyek képesek a baktériumok közösségének újrakonfigurálására a dysbiosis kezelésére.
Bevezetés
A következő szakaszok összefoglalják a közelmúltban megszerzett bizonyítékokat az emberi infantilis bél mikroflóra kialakulásáról és fejlődéséről, megvitatják az emberi bél mikrobiómájának változásait gyermekbetegségekben, és bemutatják azokat a stratégiákat, amelyek felhasználhatók a bél mikrobiota közvetlen manipulálására a korai életszakaszokban. emberek.
A bél mikrobiota kolonizációja és fejlődése a korai élet során
A bél mikrobiota kolonizációja születés előtt
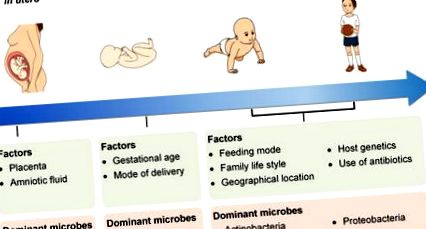
A bél mikrobiotáját alakító tényezők a korai élet és fejlődés során
A mikrobák jelenléte a méhlepényben és a magzatvízben arra utal, hogy a magzat méhen belül kolonizálódik egy proteobaktériumok által uralt mikrobiommal. Az újszülött korában a terhességi kor és a szülés módja befolyásolja az újszülött mikrobiális kolonizációját. Az életkor és az etetési mód, a családi életmód, a földrajzi elhelyezkedés, a csecsemő genetikája, valamint az antibiotikumok alkalmazása megváltoztatja a mikrobiómát a korai életben. A mikrobiota idővel változatosabbá válik, és a domináns mikrobák az Actinobacteriumok és a Proteobacteriumok.
Bár a felhalmozódó bizonyítékok azt mutatják, hogy a magzat már születése előtt is örökölheti az anya mikrobáit, viták alakultak ki a születés előtti mikrobiális kolonizációval kapcsolatban. Szükség lehet a „méhen belüli kolonizáció” hipotézisének újragondolására, mivel ezeket a vizsgálatokat többnyire molekuláris módszerekkel végezték, amelyek nem megfelelőek az alacsony bőségű mikrobaközösségek vizsgálatához, mivel a szennyeződés értékelésére nem állnak rendelkezésre megfelelő kontrollok [16], [17].
A mikrobiota fejlődése születés után
A szülés és az etetési módok mellett egyéb tényezők, beleértve a születési terhességi életkorot, a földrajzi elhelyezkedést, a családi életmódot, a gazda genetikáját és az antibiotikumok használatát, szintén felelősek a csecsemő bél mikrobiota kolonizációjáért (1. ábra). Koraszülötteknél általában éretlen gasztrointesztinális, légzőszervi, neurológiai és immunológiai rendszerek vannak jelen. Ezért a koraszülöttek gyakran vannak kitéve gyógyszeres kezeléseknek, különösen az antibiotikumok széleskörű alkalmazásának. Ezek az újszülöttek általában hosszú távú kórházi kezelésre szorulnak, parenterális táplálást és mechanikus szellőztetést kapnak, ami befolyásolhatja a kolonizáció és a mikrobiota fejlődésének természetes folyamatát, és esetleg eltérést eredményezhet a bél mikrobiota kialakulásában vagy a test rendellenes összetételében. bél mikrobiális flóra [39]. Koraszülötteknél a kommensális anaerob mikrobák bélkolonizációja késik. Ezért a koraszülöttek székletanyaga lényegesen magasabb Enterococcus, Enterobacteriaceae és opportunista kórokozókat tartalmaz, mint a koraszülöttek székletanyaga [25], [40], [41], [42], [43], [44].
A földrajzi elhelyezkedés befolyásolhatja a csecsemő bél mikrobiota kolonizációját [37] az eltérő kulturális gyakorlatok és a regionális étrend miatt. Egy tanulmány beszámolt egy „földrajzi gradiens” jelenlétéről az európai csecsemők bélmikrobiális flórájában. Vagyis az észak-európai országokból származó csecsemőknél magasabb a bifidobaktériumok szintje, míg a dél-európai országokból származó csecsemők mikrobiotája változatosabb, a Bacteroides nagyobb gyakorisággal fordul elő [45].
Továbbá egy Hollandiában végzett tanulmány bizonyítékai azt mutatják, hogy a Bifidobacterium spp. a testvéres csecsemőknél magasabb, mint a testvér nélküli csecsemőknél [46]. Ezenkívül a háziállatok jelenléte a háztartásban hatással van a bél mikrobiota összetételére [47].
Érdekes módon egy nagy kohortos vizsgálat, amely 1514 vizsgálati alanyot vesz fel, hogy értékelje a gazda genetikájának a bél mikrobiotájára, útvonalaira és gén ontológiai kategóriáira gyakorolt hatását, összefüggést tár fel a gazda genotípus és a bél mikrobiota taxonómiája között felnőttkorban [48]. Ezért figyelembe kell venni a gazda genotípusának a csecsemő bél mikrobiális flórájának kolonizációjára és fejlődésére gyakorolt hatását. Azt is megállapították, hogy a laktáz-florizin-hidrolázt (LCT) kódoló génben funkcionális egy nukleotid polimorfizmus (SNP) jelenléte korrelál a Bifidobacterium bőségével, ezáltal bizonyítékot szolgáltat a gén – diéta kölcsönhatásra a Bifidobacterium bőség szabályozásában.
Végül a fág predáció egy másik hatalmas erő, amely befolyásolja a mikrobiota összetételének szerkezetét és dinamikáját [39].
Bél mikrobiota és gyermekbetegségek
Az újszülött patológiáinak kockázata
A nekrotizáló enterocolitis (NEC) és a későn megjelenő szepszis (LOS) két fő veszélyt jelentenek az újszülöttek életére, és előfordulásuk szorosan összefügg a bél mikrobiotájával (2. ábra). Koraszülötteknél a NEC és a szepszis kialakulásának kockázata fokozódik [49], [50]. Továbbá a NEC-ben szenvedő csecsemőknél nagyobb valószínűséggel alakul ki LOS, elsősorban a bélbaktériumok, például az enterobaktériumok transzlokációja miatt [42], [43]. Feltételezik, hogy a magas szintű Enterobacteriaceae elleni fokozott immunválasz elősegítheti a baktériumok transzlokációját, és növelheti a NEC, a szepszis és más gyulladásos állapotok kialakulásának kockázatát [51]. Számos metagenomikai vizsgálat kimutatta, hogy az egészséges csecsemőkhöz képest azok a csecsemők, akiknél a LOS kialakult, kevésbé változatos mikrobiotával rendelkeznek, és alacsonyabb a Bacteroides és Bifidobacterium szintjük, és a belükben túlsúlyban vannak az enterobaktériumok [52], [53], [54]. Ezenkívül az a megállapítás, hogy a LOS-ban szenvedő csecsemők nagy hányada ugyanazt a baktériumot osztja meg a presepszis székletében, erős érvet ad a baktériumok transzlokációja mellett [55], [56]. Ezenkívül néhány tanulmány kimutatta, hogy a bélflóra sokfélesége csökken, míg a specifikus kórokozók száma megnő azoknál a csecsemőknél, akiknél NEC alakult ki [57], [58]. Jelenleg azonban nincs egyetértés ebben a kérdésben.
A bél mikrobioma és az agy kapcsolatának sematikus bemutatása-béltengely
A bél mikrobiota részt vesz a bél immunrendszerének stimulálásában vagy modulálásában, és közvetett módon gyakorolja a hipotalamusz – agyalapi mirigy – mellékvese tengely feletti irányítást. A bélmikrobiota diszbiózisa feltehetően számos gyermekbetegségért felelős, beleértve a nekrotizáló enterocolitist, a későn megjelenő szepszist, az ekcémát, az asztmát, az ételallergiát, a T1DM-t, az elhízást, az irritábilis bél szindrómát, a gyulladásos bélbetegségeket és a neuropszichiátriai rendellenességeket. T1DM, 1-es típusú diabetes mellitus.
Koraszülötteknél a NEC-et megelőző mikrobiális diszbiózist a proteinobaktériumok megemelkedett szintje, valamint a Firmicutes és Bacteroidetes csökkent szintje jellemezte [59]. Stewart és mtsai. számoltak be arról, hogy nincs szignifikáns különbség az összes baktériumfaj átlagos számában az NEC nélküli és az egészséges csecsemők között. A baktériumok összetétele azonban különbözik e két csecsemőcsoport között, és a Sphingomonas dominánsnak bizonyult azoknál a csecsemőknél, akiknél később NEC-t diagnosztizáltak [60], [61]. Ezenkívül az alacsony mikrobiális sokféleség a patogén baktériumok túlszaporodását idézheti elő, amelyet szintén fontos tényezőnek tekintenek, amely hozzájárul a NEC kialakulásához. Úgy tűnik azonban, hogy a bél mikrobiotájának nincs olyan különleges összetétele, amely hajlamosítaná az újszülöttet a NEC-re.
Ekcéma
Asztma
Ételallergia
1-es típusú diabetes mellitus
Elhízottság
Az elhízás nemcsak az anyagcsere-betegségek, például a szív- és érrendszeri megbetegedések, a II. Típusú diabetes mellitus (DM2), a rákos megbetegedések és az osteoarthritis kialakulását befolyásolja [101]. A legutóbbi, emberi alanyokkal és állatmodellekkel végzett vizsgálatok kimutatták, hogy a bél mikrobiota diszbiózisa részt vesz az elhízás kialakulásában (2. ábra). A bifidobaktériumok száma a székletmintákban csecsemőkorban normál testsúlyú gyermekeknél magasabb, míg a Staphylococcus aureus mennyisége nagyobb a túlsúlyos gyermekeknél [102]. Ezenkívül egy kohorszos vizsgálat, amelybe 909 egy hónapos gyermeket vontak be, akiket egy hónapos kortól 10 éves korig követtek nyomon, feltárja, hogy a Bacteroides fragilis egy hónapos korban bekövetkezett kolonizációs szintje összefügg a megnövekedett testtömeg-indexgel (BMI). ) z-pontszámok 10 éves korig [103]. A kísérleti modellek számos mechanizmust javasoltak a bélmikrobák elhízással és más anyagcserebetegségekkel való összefüggései mögött. Ezek közé tartozik az étrend fokozott energiaszerzése, a zsírlerakódás elősegítése, a mozgásszervi aktivitás módosítása, a jóllakottsági hatások és a szisztémás gyulladás aktiválása [104], [105], [106], [107]. A mikrobiota szerepe az elhízás kialakulásában kiszélesítheti a súlykontroll és az elhízás kezelésének nézeteit.
Irritábilis bél szindróma
Gyulladásos bélbetegség
Neuropszichiátriai rendellenességek
A bélmikrobák kezelése
Antibiotikumok
Az antibiotikumok, amelyeket általában olyan fertőzések megelőzésére vagy kezelésére használnak, amelyeket nem feltétlenül egy adott kórokozó okoz, hatékonyan kimeríthetik a bél mikrobiotáját. A NEC-ben szenvedő újszülötteknél magas a bél mikrobái által okozott fertőzés kockázata, és gyakran antibiotikumokat alkalmaznak ezeknek a fertőzéseknek a megelőzésére vagy kezelésére [141]. A gyermekkori IBD kezelésében az egyetlen antibiotikum beadása előnyös a szövődményekkel, például fisztulákkal és tályogokkal küzdő betegek számára, míg a széles antibiotikum-kombinációk javíthatják a klinikai eredményeket [142], [143]. Nagy kockázattal jár azonban az antibiotikumok kisgyermekek általi alkalmazása. Számos bizonyíték bizonyította, hogy az antibiotikumok befolyásolják a fertőzésekkel szembeni ellenállóképességünket, az immunrendszer működését és az élelmiszer-feldolgozás képességét [144]. A bél mikrobiota megzavarása hosszú távú egészségügyi következményekkel járhat, beleértve a csökkent vitamintermelést, a tápanyagok felszívódásának csökkenését, valamint a cukorbetegség, az asztma, az elhízás és a fertőzések fokozott kockázatát [145].
Prebiotikumok és probiotikumok
Az étrend módosítása
Széklet mikrobiota transzplantáció
Perspektívák
A bél mikrobiota kiegyensúlyozott szimbiózisa szorosan összefügg az emberi egészséggel, bár ezt a nagy, sokszínű és dinamikus populációt régóta elhanyagolták. A megfigyelési és vizsgálati technikák fejlődésével felismerték, hogy a szimbiotikus mikrobaközösségek kölcsönhatásba lépnek a legtöbb gazdaszervvel, és egyedi összetételűek és funkcionális jellemzőkkel rendelkeznek az élet különböző szakaszaiban. A bél mikrobiota fontos szerepet játszik az immunrendszer érésében, különösen az élet korai szakaszában, valamint a csecsemők növekedésének és fejlődésének során.
Feltételezzük, hogy a bél mikrobiota kolonizációjának és fejlődésének folyamata a korai életben a későbbi élet betegségeihez kapcsolódik. Különböző vizsgálatokból származó bizonyítékok felhalmozódása azt mutatta, hogy egy betegség előfordulását gyakran megelőzi a mikrobiota korai megváltozása. Tekintettel a potenciális egyénspecifikus fiziológiai szerepre, a mikrobiom a betegség kockázatának jó előrejelzője. Úgy képzeljük el, hogy számos összetett életmóddal és életkorral összefüggő emberi rendellenesség, például anyagcsere-, gyulladásos és neurodegeneratív betegségek kockázatát lehet megjósolni és rétegezni a megszakadt mikrobiota jellemzésével. Jobban meg kell érteni azt a természetet és mechanizmusokat, amelyek révén a mikrobiota megváltozik az élet során, valamint azokat a módszereket, amelyek révén ezek a változások befolyásolják a biológiai útvonalakat.
Versenyző érdekek
A szerzők kijelentették, hogy nincsenek versengő érdekeik.
Köszönetnyilvánítás
Ezt a tanulmányt a Kínai Nemzeti Természettudományi Alapítvány (81671504 és 81401248 számú támogatások) és a kínai Sanming-i Sanming Projekt (SZSM201606088 támogatás) támogatta. Köszönetet mondunk Shunxing Zhang professzornak és Abhay K. Lodha professzornak a kézirat csiszolásáért.
Megjegyzések
Kang Ning kezeli
Lábjegyzetek
Szakértői értékelés a Pekingi Genomikai Intézet, a Kínai Tudományos Akadémia és a Kínai Genetikai Társaság felelőssége alatt.
- A magas steakek marhahús fogyasztásának hatalmas egészségügyi előnyei - Paleo életünk
- Nőgyógyászati rák tudatossági hónap A korai diagnózis jobb életminőséget biztosít a betegeknek,
- Az alacsony fehérjetartalmú étrend a korai életkorban megnöveli a gyümölcslégyek élettartamát
- Bélhang az Life Force International Review Body Balance folyékony vitamin teljes étrend-kiegészítők
- Az egészség számomra a bélsaga, 5. rész: Monastyrsky és Kwasniewski