Gyulladásos bélbetegség a kutyánál: Különbségek és hasonlóságok az emberrel
Levelezés: Gabrio Bassotti, professzor, Gasztroenterológiai és Hepatológiai Szakosztály, Klinikai és Kísérleti Orvostudományi Tanszék, Santa Maria della Misericordia Kórház, Piazzale Menghini, 1, 06153 San Sisto (Perugia), Olaszország. ti.nit@tossabag
Telefon: + 39-75-5784423 Fax: + 39-75-5847570
Absztrakt
A gyulladásos bélbetegségek (IBD) fontos krónikus állapotokat jelentenek az ember gyomor-bél traktusában. Ugyanakkor számos állatfajnál hasonló rendellenességek találhatók, és a kutyákat érintő IBD különösen fontos. Ezeket valószínűleg több különböző entitás esernyője öleli fel, amelyeknek közös tünetei vannak, amelyek közül úgy tűnik, hogy meglepő hasonlóságok vannak az emberi feltételekkel. Ez az áttekintés a kutyák IBD-jének tényleges ismeretére összpontosít, és megkísérli azonosítani az emberi IBD-betegség különbségeit és hasonlóságait.
BEVEZETÉS
A gyulladásos bélbetegségek (IBD) jól ismert gyomor-bélrendszeri rendellenességek; ezek a rendellenességek azonban állatokban is jelen vannak, és gyakran vizsgálják őket [1]. Az IBD emberben [Crohn-betegség (CD) és fekélyes vastagbélgyulladás (UC)] krónikus idiopátiás multifaktoriális betegségként határozható meg [2,3]. A CD tipikusan az ileum és a vastagbél betegsége, de az emésztőrendszer más területeire is hatással lehet [4], granulómákat képez és az egész bélfalra kiterjed, míg az UC fekélyes és gyulladásos betegség, általában felületes rétegekre (nyálkahártya, felszíni a vastagbél submucosa része) [5].
A kutyáknál IBD is kialakulhat [6], amely a krónikus enteropathiák része, ha három hétnél hosszabb ideig tart [7], és megfelelően meghatározhatók, ha a nyálkahártya gyulladásának szövettani kimutatása van, és az enteritis/infiltrátumok minden egyéb lehetséges okát megvizsgálták és kizárt [7-10]. Az enteritis osztályozása attól függően, hogy mely domináns sejtek hatolnak be a bélfalba, és hol tart ez a beszűrődés [11].
Tehát a vékonybél krónikus betegségei, amelyek az IBD közé sorolhatók, a limfocita-plazmaciás enteritis (LPE), az eozinofil enteritis és az eozinofil gyomor-enteritis (EGE) [10]. A vastagbél tekintetében négy fő kórállapotot ismerünk el IBD-ként kutyákban: limfocita-plazmaciás kolitisz, eozinofil kolitisz, histiocytás fekélyes vastagbélgyulladás (HUC) (főleg PAS-pozitív makrofágok) és regionális granulomatózus vastagbélgyulladás (főleg PAS-negatív makrofágok) [10,12-16]. Érdemes azonban megjegyezni, hogy az ilyen betegségek gyakran előfordulhatnak a vékonybélben és a vastagbélben, vagy akár a gyomrot is magukban foglalhatják: limfocita-plazmaciás enterocolitis, eozinofil enterocolitis (EEC) vagy gastroenterocolitis (EGEC) és granulomatous gastroenteritis [8,10,13, 15].
A kutyáknál egy másik fontos krónikus bélgyulladás, amelynek okait még nem határozták meg egyértelműen, de széleskörűen megvizsgálták, és amelyek mögött feltételeztek allergiás tényezőket, az úgynevezett ételre reagáló hasmenés (FRD) [6]. Ez a betegség különösen fontos, mert gyakran szerepel az IBD differenciáldiagnózisában.
Úgy gondolják, hogy az IBD ugyanolyan gyakorisággal rendelkezik a férfiaknál és a nőknél, és úgy tűnik, hogy a középkorú kutyák jobban érintettek [10]. A fajta hajlamát illetően ezt javasolják az IBD egyes specifikus formáira, mint például az immunproliferatív enteropathia Basenjis-ben, a fehérjét vesztő enteropathia és a kapcsolódó fehérjét vesztő nephropathia a lágyrétegű búzás terriereknél, és a HUC az ökölvívóknál [10,11]. Bár a HUC nagyobb hajlandóságot mutat a bokszolókban [17], más kutyafajtáknál is leírtak, mint például a francia bulldog, doberman pinscher, masztiff és alaszkai malamut [16,18].
PATOGENEZIS
Információ kutyáknál
Kutyáknál az IBD kialakulása vélhetően a hajlamos állatok nyálkahártya-immunitásának deregulációjának következménye lehet [14]. Az antigének (táplálék, bélbaktériumok stb.) Toleranciájának elvesztése az egyik legtöbbet vizsgált mechanizmus, amely igazolhatja a krónikus bélgyulladás kialakulását [8,11,19]. A betegség immunmediált alapja az immunmoduláns gyógyszerek beadására adott válaszból következtethet; a megnövekedett IgE-pozitív sejtek jelenléte a beteg kutyákban az egészséges kutyákhoz képest egy másik szempont, amely szintén utal a túlérzékenységi reakciók bevonására a kutya IBD patogenezisében [20], valamint az eozinofilek és a hízósejtek megnövekedett koncentrációjával sok kutyában EGE-vel [8]. A nyálkahártya gátjának megszakadása az elsődleges októl (bakteriális, kémiai stb.) Függetlenül további antigén expozícióhoz is vezethet, lehetővé téve a folyamat krónikussá válását [21], és ezt a limfociták csökkent apoptózisa hajtja végre, amint azt a IBD-s kutyák a kontroll kutyákhoz képest [22].
Az emésztőrendszer belsejében a homeosztázist a kórokozókra és a kommenzális baktériumokra vagy más inenzív luminalis antigénekre (tolerancia) adott reakciók egyensúlya tartja fenn, amelyeket különböző molekulák közvetítenek [23]. Az ártalmatlan antigének iránti nyálkahártya-tolerancia jelenléte nagyon fontos, mivel annak hiányától függően a későbbi gyulladásos válasz túlzó lehet, sőt káros is lehet. Az ilyen tolerancia valószínűleg azon a tényen alapul, hogy az antigén bemutatásra kerül vagy sem, összefüggésben más veszélyjelekkel [10,24]. A tolerancia és a reakció közötti különbség a mintázatfelismerő receptorokon (PRR) is alapszik [25], amelyek képesek felismerni a mikroflóra kórokozóhoz kapcsolódó molekuláris mintázatuk vagy mikrobához kapcsolódó molekuláris mintázatuk szerint [26].
Az emberhez hasonlóan az IBD vizsgálata az érintett kutyákban arra a hipotézisre vezetett, hogy a genetikai tényezők és az enterális baktériumok kulcsfontosságú szerepet játszhatnak e rendellenességek patogenezisében, a kommensális mikroflóra rendellenes bélreakciójának köszönhetően [26]. Miután stimulálták, a PRR-ek, például a Toll-szerű receptorok (TLR) [27], megkezdik gyulladásgátló aktivitásukat, és egy nemrégiben készült tanulmány kimutatta, hogy a baktériumok által stimulált három TLR-t (2, 4 és 9) az IBD-ben szenvedő kutyák szabályozzák. [26]. Ezek az eredmények hasonlóak a TLR4 aktiválását követő eredményekhez, amelyet IBD-ben szenvedő embereknél bizonyítottak [28]. Ezekben a betegeknél mind a genetikai hajlam, mind a környezeti tényezők fontos elemnek számítanak a betegség kialakulásában. Ezenkívül, amint az embereknél már jól ismert [29,30], egy nemrégiben elvégzett tanulmány kimutatta, hogy az IBD kutyáknál a vékonybél baktériumok eltérnek az egészséges kutyáknál tapasztaltaktól [31], megerősítve a mikroflóra és az IBD közötti összefüggés gondolatát.
Így még kicsi állatoknál is, és hasonlóan az emberéhez, a bél limfocita részhalmazának eloszlása és a fő hisztokompatibilitási komplex II. Osztályú antigének, valamint a citokin gén expresszió és egyéb markerek érdekes és néha átfedő eredményeket hoztak [9,32-36] . Például egy tanulmány kimutatta, hogy az IBD-ben szenvedő kutyák nagyobb számú IgE-pozitív sejtet mutatnak, mint az egészséges kutyák, hasonló módon, mint az interleukin 4 (IL-4) expressziója az IBD-ben szenvedő embernél [20]. Ezenkívül úgy tűnik, hogy a béllamina propria limfociták P-glikoprotein (P-gp) expressziójának modulációja hasonló szerepet játszik mind az emberi, mind a kutya IBD-ben. Valójában az IBD-ben szenvedő betegeknél, akik alig reagálnak a szteroid kezelésre, a P-gp erősen expresszálódik, és a kezelésre jó választ mutató kutyáknál ez a fehérje szerényen képviselteti magát [37].
Amint azt az embereknél korábban dokumentálták, IBD kutyákban a sejtszintű populációk specifikus részhalmazainak vizsgálata a hízósejtek (MC) számának csökkenését, valamint a CD3 + sejtek és az IgG + plazma sejtek növekedésének kimutatásához vezetett [38].
Az állatgyógyászatban biztató eredmények származnak a nukleáris receptorok (NR-k, feltehetően az emberben az IBD genezisében is részt vevő), például a peroxiszóma proliferátorhoz kapcsolódó α (PPARα) és különösen az NR célgének [például multi -drogrezisztencia-gén-1 (MDR1)], többszörös gyógyszerrezisztencia-társított fehérje (MRP2), citokróm P450 (CYP3A12) és fenol-szulfatáló fenolszulfotranszferáz (SULT1A1) [39,40]. Egy nemrégiben készült tanulmányban kiemelték, hogy az MRP2, a CYP3A12, a SULT1A1 és a PPARα jobban expresszálódik FRD és/vagy IBD kutyákban, és hogy az MDR1 is meg tudja különböztetni őket [21]. Ezenkívül egy IBD-ben szenvedő német juhászkutya vizsgálatában számos citokin, például IL-2, IL-5, IL-12p40, interferon-y (IFN-γ), tumor nekrózis-faktor α (TNF-α) mRNS-expressziója ), és a transzformáló növekedési faktor-β1 (TGF-β1) magasabbnak bizonyult beteg állatokban a kontrollokhoz képest [34]; mindazonáltal azt is szem előtt kell tartani, hogy más vizsgálatok újragondolták egyes citokinek fokozott expresszióját IBD-ben szenvedő kutyáknál [35,36].
Információ emberekről
Az emberben az IBD, különösen a CD, valószínűleg felismeri a genetikai hajlamot, és számos olyan gént, mint a NOD2/CARD15, HLA és IL-1-Ra géneket vizsgáltak, és feltételezhetően szerepet játszanak a CD fejlődésében [41-43]. Ugyanakkor környezeti tényezők [44,45] és a bél mikrobiota is szerepet játszhatnak az IBD-ben [46-49], amint azt az a tény is mutatja, hogy az antibakteriális gyógyszerek segíthetnek a tünetek kezelésében [50-52]. Az emberi IBD károsodásának fennmaradásának fontos pontja, hogy miután stimulálta, a limfociták hajlamosak felhalmozódni a lamina propriában, mert úgy tűnik, hogy jobban ellenállnak az apoptózisnak [53]. Sőt, szerepet játszhat a gyulladáscsökkentő és gyulladáscsökkentő citokinek egyensúlyhiánya is [54].
Emberben a nukleáris faktor-κB (NF-κB) szintén összefüggésbe hozható az IBD-vel [55], és bebizonyosodott, hogy az IL-23 az IL-17-et termelő Th17 limfociták differenciálódásához vezethet az NF-κB későbbi aktiválásával. gyulladásgátló jelek [56]. Egy nemrégiben végzett kutatás során feltételezték az IBD és az NF-κB közötti kapcsolatot kutyáknál is, ahol az IBD-ben szenvedő kutyák biopsziás mintái azt mutatták, hogy az NF-κB aktiváció jelenléte a lamina propria makrofágokban magasabb volt, mint a kontroll csoportban [23].
A fajok közötti különbségek
A humán orvostudomány egyik fontos fejleménye megmutatta a limfocita altípusok (Th1 és Th2) eltérő részvételét az IBD-ben, a Th1 főként a CD-vel, míg a Th2 túlsúlyban van az UC-ben [57], és ezt követően különböző citokinaktivációval [23]. Az embertől eltérő kutyáknál a Th1 és a Th2 vegyesen aktiválódik az IBD-ben [6,23,38], ami egyes citokinek eltérő expressziójához vezet, annak ellenére, hogy nemrégiben feltételezték, hogy a különböző IBD-kben különböző Th-sejtek vehetnek részt. típusok [8]. Egyes szerzők kimutatták, hogy az MC az uralkodó sejtes infiltrátumtól függően megnövekedhet vagy csökkenhet, és ezek főleg az LPE-ben csökkentek és az EGE-ben megnőnek, ezáltal feltételezve az IBD két típusának (Th1 az LPE és Th2 az EGE esetében) [8].
Annak ellenére, hogy a fenti tanulmányok aktív érdeklődést mutatnak az IBD patogenezise iránt, az is nyilvánvaló, hogy a betegség hátterében álló mechanizmusok emberben és kutyában egyaránt korántsem értettek. HUC, egy különös állapot, amelyben a baktériumok központi szerepét javasolták az intraléziós mikrobák és a PAS + makrofágok jelenléte miatt, hasonlóan az ember Whipple-kórjához [7].
KLINIKAI ÉS DIAGNOSZTIKAI SZEMPONTOK
Az IBD klinikai megnyilvánulása kutyákban számos és nem specifikus; a leggyakoribb klinikai tünetek a fogyás, a tartós vagy visszatérő hányás és/vagy hasmenés [8], amelyek gyakran olyan tünetekkel társulnak, amelyek a lehetséges szövődmények kifejeződését jelentik, mint például az ascites (ha hipoalbuminémia van jelen) vagy a nyálkahártya sápadtsága krónikus gasztrointesztinális vérzés esete) [11,58].
Az IBD diagnózisának elérése előtt fontos kizárni a krónikus enteritis minden egyéb lehetséges okát [6,59] teljes klinikai vizsgálattal, laboratóriumi vizsgálatokkal és műszeres vizsgálatokkal, beleértve a szövettani értékeléshez szükséges biopsziás mintákat is. A diéta korrekció szintén fontos eszköz az FRD kizárására vagy végül megerősítésére [23].
Mivel kutyáknál az IBD diagnózisa kizárással történik, nyilvánvaló, hogy a diagnosztikus iter során végzett számos vizsgálatra (például vér-, vizelet- és székletvizsgálatok) szükség van a gyulladás egyéb okainak kizárására, és ritkán specifikusak az IBD-re, nem becsülve túl egy ilyen diagnózis előfordulását [10]. Ez a szempont nagyon fontos, mert ha a krónikus enteritis okát hibásan diagnosztizálják és IBD-ként kezelik, akkor nem valószínű, hogy megoldódjon [58].
Az IBD diagnosztizálásakor az instrumentális diagnosztika fontos és gyakran kiemelkedő fontosságú, annak ellenére, hogy a három leggyakrabban alkalmazott technika, azaz a radiológia (XR), az ultrahangvizsgálat (USA) és az endoszkópia közül csak ez utóbbi szolgáltat specifikusabb információkat az IBD diagnózisához (ábra (1. ábra), 1), különösen, mivel biopsziás mintákat tesz lehetővé, amelyek nélkülözhetetlenek a nyálkahártya-beszivárgás különböző altípusainak megkülönböztetéséhez [60]. Az XR és az USA (amelyek fontos információkat adnak a bélrétegről és a falvastagságról) hasznosabbnak tűnnek más lehetséges okok kizárásában [61], és mivel az IBD-ben szenvedő kutyáknál a közelmúltban átértékelték a bélfal megvastagodásának fontosságát [10, 62,63].
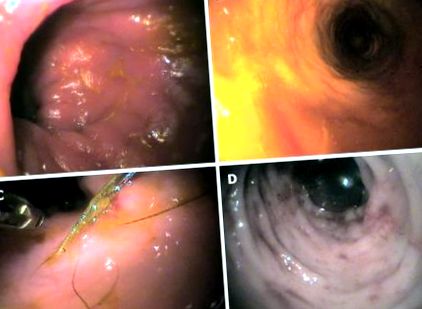
Reprezentatív endoszkópos képek a kutyában. V: Limfocita-plazmaciás kolitisz; B: Makrofollikuláris és diffúz intersticiális limfocita vastagbélgyulladás; C: hiszticita vastagbélgyulladás; D: Neutrofil-eozinofil vastagbélgyulladás.
A krónikus enteropathiák leggyakoribb okainak kizárása után a bélbiopsziák, amelyeket a körülményektől függően műtéti úton vagy endoszkópos úton kapnak (az endoszkópia kevésbé invazív, de a mintavétel korlátozott a végrehajtás helye és/vagy dimenziója szempontjából), lehetővé tehetik az IBD diagnosztizálását. [10] (ábra (2. ábra). 2). Fontos azonban hangsúlyozni, hogy a biopsziás minták nem egyértelműen értelmezhetők [6,10,64], annak ellenére, hogy a közelmúlt munkája segített az ilyen értelmezés tisztázásában azáltal, hogy hisztopatológiai pontszámot adott kutyák nyálkahártya-változásaira [65].
Reprezentatív szövettani képek a kutyán (HE, bar = 50 μm). V: Limfocita-plazmaciás kolitisz. Figyeljük meg az infiltrátum intersticiális diffúz mintázatát, amelyet nagy mennyiségű limfocita képvisel plazma sejtekkel és néhány makrofággal keverve; B: Limfocita-plazmaciás colitis (follikuláris variáns); C: hiszticita vastagbélgyulladás. Súlyos nyálkahártya-rendellenességek, a kripták elvesztésével és a nagy makrofágok (nyilak) diffúz beszivárgásával, amelyek az inszertben (PAS-folt) a lamina propriába beszivárgó fő sejtekként vannak feltüntetve; D: Eozinofil vastagbélgyulladás. Vegye figyelembe, hogy nagy számban vannak eozinofilek (nyilak).
Emberben az IBD diagnosztizálására és/vagy monitorozására számos szerológiai marker, például anti-neutrofil citoplazmatikus antitest (p-ANCA), anti-Saccharomyces cerevisiae (ASCA), külső membrán porin C antitest (anti-OmpC), anti-laminaribiosid antitest, anti-mannobiosid antitest és anti-chitobioside antitest, hasnyálmirigy-ellenes Ab és anti-caliciform bélsejtek Ab, széklet-kalprotektin, laktoferrin és polimorfonukleáris neutrophil-elasztáz állnak rendelkezésre és tesztelték őket, bár a klinikai gyakorlatban nem mindet alkalmazzák [66-68].
Ha a betegség diagnosztizálása hosszú és teljes diagnosztikai tervet igényel, az IBD klinikai értékelésének fontos eszközei a kutya krónikus enteropátia aktivitási indexe és a kutya IBD aktivitási indexe (CIBDAI) (hasonlóan az ember Crohn-betegség aktivitási indexéhez [74]). ), amely szintén lehetővé teszi a páciens nyomon követését a kezelés alatt [75-77], annak ellenére, hogy a CIBDAI nem tűnik összefüggésben a hisztopatológiai fokozattal [73]. Az IBD kezelésének egyik fontos szempontja, hogy nagyon nehéz előre látni a beteg eredményét; szerencsére a közelmúltban számos fontos markert vizsgáltak prognosztikai indikátorként, mint például a kutya hasnyálmirigy-lipáz immunreaktivitása (cPLI), a kobalamin és az albumin koncentrációja [78-80].
KEZELÉS
Az emberi orvosláshoz hasonlóan az IBD-s kutyák kezelésének fő nehézségei e betegségek patofiziológiai alapjainak hiányos megértéséből fakadnak; így nem meglepő, hogy sok esetben a terápiás protokollokat részben kölcsönözik az emberben elfogadottaktól [23,78]. A kutyák IBD-jének megválasztott terápiás protokollja általában a betegség súlyosságától és végül egyes gyógyszerekkel szembeni rezisztenciától függ. Egyes betegek, mint például az FRD-ben szenvedők, javíthatják, vagy akár megoldhatják állapotukat egy speciális étrend egyszerű beadását követően, például a hidrolizált fehérjéken alapuló betegek [58].
Általában az IBD-ben szenvedő kutyáknál az első megközelítés általában bizonyos étrend-módosításokat, prebiotikumok-probiotikumok [10,11], antimikrobiális szerek és végül kortikoszteroidok (prednizolon vagy újabban budesonid) alkalmazását foglalja magában [58]. A metronidazol fontos terápiás szer, mivel egyidejű antimikrobiális és immunmoduláló hatása van [10,58]. Más immunmoduláló vagy gyulladáscsökkentő gyógyszerek, például azatioprin, ciklosporin, klorambucil, ciklofoszfamid és 5-amino-szalicilátok adhatók alternatívaként vagy a szteroidokkal együtt, a molekulától függően [10,12,58,78]. Az IBD-ben szenvedő kutya kezelésénél fontos olyan tüneti terápiás intézkedéseket is bevezetni, mint a gasztroprotektorok, antiemetikumok, mozgásmodulátorok stb., Valamint korrigálni az esetleges egyensúlyhiányokat (például kobalamin vagy elektrolit kiegészítéssel) [10,58].
Figyelembe véve, hogy az IBD-ben szenvedő betegeknél a citokinminták ismerete fontos eszközt jelent az új terápiás stratégiák kidolgozásában [61], ez új terápiás eszközöket is kínálhat az állatorvoslásban [10,58]; az IBD-ben szenvedő kutyák bélbiopsziáiról szóló, a növekedési hormon receptor és az inzulinszerű növekedési faktor (IGF-1/-2) mRNS expresszióját értékelő nemrégiben végzett tanulmány eredményei további perspektívákat adtak az IBD kezelésére [82].
KÖVETKEZTETÉS
A mai napig az emberek és a kutyák IBD közötti kapcsolatát nem határozták meg teljesen, különös tekintettel a patofiziológiára és a terápiás protokollokra; így az emberen vizsgált szempontok közül valószínűleg csak néhányat sikerült sikeresen lefordítani kutyáknak. Valójában az IBD több és néhány feltűnően eltérő formát mutat az emberek tekintetében, akiknél ezek a betegségek standardizáltabb klinikai, endoszkópos és kóros szempontokat mutatnak.
Egyes szerzők [83,84] javaslata szerint azonban az IBD állatokon végzett párhuzamos vizsgálata az embereknél is fontos információkhoz vezethet [85], és remélhetőleg jobb terápiás intézkedéseket dolgozhat ki e bajok enyhítésére kutyás barátainkban és társainkban.
Lábjegyzetek
Szakértői vélemény: Dr. Pingchang Yang, MD, PhD, Pahtológiai és Molekuláris Orvostudományi Tanszék, McMaster Egyetem, BBI-T3330, 50 Charlton Ave East, Hamilton, L8N 4A6, Kanada
S- szerkesztő Tian L L- szerkesztő Webster JR E- szerkesztő Lin YP
- Gyulladásos bélbetegség Macska orvos
- Gyulladásos bélbetegség Klinika, Emésztési Egészségügyi Szolgáltatások UW Health Madison, WI
- Gyulladásos bélbetegség Okai, tünetei és kezelése
- Az egészségtelen ételekhez kapcsolódó gyulladásos bélbetegség MinnPost
- Bélgyulladás (IBD)