Hiperinzulinémia és autonóm idegrendszeri diszfunkció az elhízásban
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Metabolizmus és koszorúér osztálytól, a CNR Klinikai Élettani Intézet és a Pisai Egyetem Belgyógyászati Klinikája, Pisa, Olaszország.
Absztrakt
Háttér—Mivel a hiperinsulinémia akutan serkenti az adrenerg aktivitást, feltételezték, hogy a krónikus hiperinsulinémia fokozott szimpatikus tónushoz és kardiovaszkuláris kockázathoz vezethet.
Az elhízás hemodinamikája szintén nem egyeztethető össze önmagában az adrenerg túlműködés jelenlétével. Valójában, míg a szívteljesítmény megnövekszik, a normotenzív elhízottaknál a perifériás érellenállások általában csökkennek. 9 Bár ez a nagy teljesítményű, alacsony ellenállású állapot részben a megnövekedett testtömeg következménye, 10 regionális hemodinamikai tanulmány megerősítette, hogy a végtag érellenállása vagy normális, vagy csökkent normotenzív elhízott egyéneknél. 10.
Javasolták a hiperinzulinémia szerepét az elhízás szimpatikus túlműködésében. Az állatokon végzett vizsgálatok alapján Landsberg 11 eredetileg azt feltételezte, hogy az elhízás kialakulása során a hiperinsulinémia szimpatikus aktivitást gerjeszt, ezáltal növelve az oxigénfogyasztást és az energiafelhasználást. Ez az inzulinhatás hosszú távon rosszul alkalmazkodó lenne, mivel a további súlygyarapodás korlátozása mellett előkészíti a talajt a magas vérnyomás (és más anyagcserezavarok) megjelenéséhez. Az embereknél a jelenség hiányos. Egészséges önkéntesekben az akut euglikémiás hiperinsulinémia a keringő NE-koncentrációk dózisfüggő növekedését okozza. 12 Másrészt megállapították, hogy az elhízott inzulinrezisztens egyéneknél a szívaktivitás inzulinérzékenysége megmaradt. 13 Ezért nem világos, hogy az elhízott állapot hemodinamikai és autonóm idegrendszeri (ANS) változásai a tartós hiperinsulinémia vagy az inzulinrezisztencia következményei.
Ennek a hipotézisnek a teszteléséhez az ANS funkciót vizsgáltuk az elhízásban, kombinálva az időzített vizelet katekolamin kiválasztásának mérését a pulzusszám változékonyságának (HRV) monitorozásával 24 órás szabad élet alatt. A szívverés (HR) ütés-ütés ingadozásainak spektrális elemzése lehetővé teszi a szívaktivitás spontán autonóm szabályozásának dinamikus értékelését. 14 Súlycsökkentéssel tesztelték, hogy az elhízottakban talált ANS-rendellenességek reverzibilisek-e és ezért funkcionálisak-e, és nem strukturális eredetűek.
Mód
Tanulmány a népességről
Huszonegy elhízott alanyot (testtömeg-index [BMI]> 30,5 kg/m 2 férfiaknál és> 27,3 kg/m 2 nőknél, az Olasz Konszenzus Konferencia 15. kritériuma szerint) és 17 sovány alanyot vizsgáltak. Mindegyikük normális orális glükóz toleranciával rendelkezett 16 és nyugalmi vérnyomásszinttel (17); egyik sem szedett gyógyszereket. Valamennyi alanynak normál máj-, vese- és endokrinfunkciós tesztje volt, és a vizsgálatot megelőző 6 hónapban egyikük sem fogyott vagy megváltozott az étkezési szokások. Az etikai bizottság jóváhagyta a vizsgálatot, és minden alany megalapozott beleegyezést adott.
Kísérleti protokoll
A kezdeti vizsgálatok után az elhízott betegeknek hipokalorikus étrendet írtak elő (4,9 ± 0,1 MJ/d; 55% szénhidrát, 25% zsír és 20% fehérje). 8 ± 1 hónapos időszak alatt 9 beteg (7 nő és 2 férfi; életkor: 35 ± 3 év) 8–12 kg-ot fogyott (kezdeti súlyának 10–18% -a). Ezekkel a betegekkel a vizsgálatokat megismételték, amikor új súlyuk ~ 4 hétig stabil volt.
Klinikai autonóm funkció tesztek
Az ANS-t a Valsalva manőver, a mély légzési teszt és az fekvő-álló teszt segítségével vizsgálták, ebben a sorrendben, Ewing módszerével. 21 Az összes mérést ugyanabban a helyiségben végezték, amelyet állandó hőmérsékleten tartottak; 1 kezelő (M. E.) elvégezte az összes tesztet.
Frequency-Domain HRV
Az EKG-t 250 Hz-en digitalizálták. Az RR intervallumok idősorait a 24 órás periódus alatt kiszámoltuk, és egymást követő 256 adatpontos intervallumokban elemeztük a leírt autoregresszív technikával. 13 A konszenzusos előírások szerint az RR teljesítményspektrumban 14 3 fő frekvenciakomponens került figyelembe vételre: nagyon alacsony frekvenciájú (VLF) komponens (0,003–0,03 Hz), alacsony frekvenciájú (LF) komponens (0,03–0,15 Hz) és nagyfrekvenciás (HF) komponens (0,15–0,40 Hz). 22 Minden spektrum esetében az átlagos RR intervallumot, a teljes spektrum teljesítményt, az LF és HF komponensek teljesítményét (abszolút és normalizált egységekben, nu), az LF és HF sávok központi frekvenciáját és az LF/HF arányt tároltuk a statisztikai adatokhoz. elemzés. A légzési frekvenciát mind a HF komponens központi frekvenciájából, mind az R-hullám amplitúdó-variabilitásának külön spektrális elemzésével kaptuk (ez utóbbi a mellkas és a szív mozgásainak köszönhető a légzés során).
Analitikai eljárások
A plazma glükózszintet glükóz-oxidáz technikával mértük (Beckman Glucose Analyzer, Beckman). A plazma inzulin koncentrációit (InsKit, Sorin) radioimmun vizsgálattal mértük, míg a plazma és a vizelet epinefrin és NE koncentrációit nagy teljesítményű folyadékkromatográfiával (HLC 725 készülék), elektrokémiai detektálással (Eurogenetika) határoztuk meg.
Adatelemzés
A zsír tömegét a testtömeg és a zsírmentes tömeg különbségeként számoltuk ki. Az idő-koncentráció görbék alatti területeket a trapéz szabály szerint számítottuk ki. Minden adatot átlag ± SEM értékként adunk meg. Nem normális eloszlásuk miatt az inzulin és a katekolamin plazmakoncentrációi, a vizelet katekolamin kiválasztási értékei és a spektrális paraméterek log transzformációval készültek statisztikai vizsgálatokhoz; ezeket a változókat geometriai átlagként [interkvartilis tartomány] foglaljuk össze. A csoportok közötti összehasonlítást a Mann-Whitney végezte U teszt; páros összehasonlításokat végeztünk a Wilcoxon jel-rang teszt segítségével. Az ismételt mérésekhez kétirányú ANOVA-t használtunk, hogy összehasonlítsuk a csoport átlagát a különböző időszakokban. A regresszióanalízist általános lineáris modellekkel végeztük, folyamatos és kategorikus változókat is beleértve.
Eredmények
Klinikai, metabolikus és hemodinamikai jellemzők
Az elhízott csoport túlsúlya átlagosan 50% volt, és mind zsírból, mind sovány tömegből állt (1. táblázat). Bár minden alany normál glükóz toleranciával rendelkezett a hagyományos kritériumok szerint, a glükóz területe szignifikánsan magasabb volt elhízott, mint sovány alanyoknál. Éhomi állapotban és a glükózra reagálva a plazma inzulinszintje 40–80% -kal magasabb volt az elhízottaknál, és közvetlenül összefügg a BMI-vel (r= 0,48, illetve 0,65; P pm és 3:00, de alacsonyabb HR 7 és 10 óra között (1. ábra). Míg az LF teljesítmény lényegében a 24 órás periódus alatt lecsökkent, a HF teljesítmény késő délutánon át az éjszaka első feléig csökkent (2. ábra). Ennek eredményeként a délután folyamán az LF/HF arány az elhízott csoportban észrevehetően megnőtt.
A teljes adatsorban magasabb nappali LF/HF arányok társultak magasabb éhomi plazma inzulin koncentrációktól, nemtől, kortól, HR-től és BMI-től függetlenül; mennyiségileg az éhomi inzulin megháromszorozása megjósolta az LF/HF arány megduplázódását (3. ábra).
A fogyás hatásai
A súlycsökkentett betegeknél a testtömeg és a zsíreloszlás indexei jelentősen javultak, a szívteljesítmény csökkent és a TPVR emelkedett (4. táblázat). A katekolamin vizelettel történő kiválasztása általában csökkent (bár a változás statisztikailag nem volt szignifikáns). A kiindulási 24 órás LF teljesítmény (608 [420] ms 2) visszatért a normál tartományba (824 [799] ms 2-ig; P 2), az ezen állapotra jellemző összes anyagcsere-változással együtt. A strukturális érrendszeri változások zavaró hatásainak elkerülése érdekében az elhízott alanyokat normál glükóztoleranciával és vérnyomásszinttel választották ki. Ezenkívül az autonóm funkció klinikai tesztjei normális határokon belül voltak. Eredményeink tehát a komplikáció nélküli elhízásra vonatkoznak.
Szimpatikus tevékenység
További megállapítás volt, hogy a vizelet NE kimenetének normális éjszakai süllyedése elhízott. Az NE-kibocsátás időeltolódása a késő délután és a kora éjszaka felé egyértelműen követhető a HR időbeli lefutásával: A késő esti órák magasabb HR-je a kora éjszakáig terjedt, átfedve ezzel az éjszakai vizeletgyűjtést. Így a vizelet NE kiválasztásának mintázata és a HR időbeli lefutása koherensen jelezte az epizódos adrenerg aktivációt és a paraszimpatikus megvonást elhízottakban, egybeesve az étkezés utáni állapottal.
ANS funkció
A cirkadián HR és HF oszcillációk jól látszottak a kontrollcsoportban, és elhízottak; utóbbiban azonban a HF teljesítménye késő délutántól kora éjszakáig csökkent (2. ábra). Ennek eredményeként az LF/HF arány, a szimpatovagális egyensúly indexe, 28 szintén megváltozott ebben az időszakban, ami elmozdulást jelent a szimpatikus dominancia felé. Ez a megállapítás tükrözheti a sinuscsomópont-aktivitás központi autonóm szabályozásának zavarát. 13.
Értelmezés
Ennek az értelmezésnek a meggyőző bizonyítéka csak a preobese állapot tanulmányozásából származhat; ezt azonban csak utólag határozzák meg. Egy tanulmányban, amely egészséges önkéntesek rövid távú, kicsi (10%) testtömeg-változásainak elemzését elemezte, Hirsch és mtsai 32 dokumentálták a HR növekedését és a spektrális erő csökkenését a súlygyarapodás során és ellentétes változásokat a fogyás során.
Ki kell emelni, hogy korábbi tanulmányunkban 13 bebizonyítottuk, hogy az inzulin akkus hatása a sinus csomópont aktivitására hasonló volt a sovány és elhízott inzulinrezisztens alanyok között; azaz nem voltak összefüggésben a glükóz metabolizmus inzulinrezisztenciájával. Ezért úgy tűnik, hogy az elhízottak ANS-diszfunkciója egy napos hiperinsulinémia közvetlen következménye, amelyet nem inzulinrezisztencia vált ki. Hangsúlyozni kell azt is, hogy bár az elhízott és sovány egyének közötti megfigyelt különbségeket megfelelően meg tudja magyarázni, a hiperinsulinémia nem feltétlenül az egyedüli meghatározó tényező, és a mögöttes, de nem mérhető tényezők mellett állhat. Mindazonáltal lényeges, hogy az inzulin képes közvetlenül befolyásolni a sejtek ingerlékenységét (a transzmembrán ioncserére gyakorolt hatásai révén 33), és áthatja a vér-agy gátat, hogy modulálja a középagy neuronális aktivitását. 34
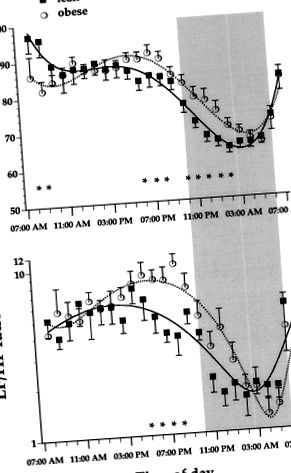
1.ábra. Óránkénti HR (felső) és LF/HF arány (alsó) karcsú és elhízott személyeknél. Az adatok átlag ± SEM. Az árnyékolt terület kiemeli az éjszakai időszakot. * Olyan időpontok, amikor a 2 csoport közötti különbség statisztikai szignifikanciát ért el (P
2. ábra. Az LF (felső) és a HF (alsó) teljesítmény óránkénti profilja sovány és elhízott alanyokban. Az árnyékos terület kiemeli az éjszakai időszakot. * Olyan időpontok, amikor a 2 csoport közötti különbség statisztikai szignifikanciát ért el (P
3. ábra. Összefüggés a nappali LF/HF arány (a nem, az életkor, a HR és a BMI kiigazítását követő maradványok) és az éhomi plazma inzulin koncentráció között. Az Inset az LF/HF arány modell által előre jelzett változását mutatja, amely az éhomi plazma inzulinszint háromszorozásához kapcsolódik ([I]). resds jelzi a maradványokat.
4. ábra. A HR (felső) és az LF teljesítmény (alsó) óránkénti profilja 9 elhízott alanynál fogyás előtt és után.
Asztal 1. Klinikai, metabolikus és hemodinamikai jellemzők
A WHR a derék-csípő arányt jelzi. A zárójelben lévő értékek interkvartilis tartományok.
1 Mann-Whitney-teszt.
2 A nemhez igazítva.
2. táblázat. Vizelet katekolamin kiválasztás 1
1 A bejegyzések geometriai átlaga (interkvartilis tartomány). A valószínűségi értékek a kétirányú ismételt ANOVA értékekre vonatkoznak a csoport (elhízás) és az idő hatására.
3. táblázat. Spektrális elemzés az 1. nap időtartama szerint
1 A bejegyzések geometriai átlaga (interkvartilis tartomány).
2 Az elhízott és a sovány alanyok közötti különbségre a nem, az életkor és a HR szempontjából többszörös regresszióval igazítva.
3 A nappali és éjszakai különbségért kétirányú ANOVA-val az ismételt intézkedések érdekében.
4. táblázat. A fogyás hatásai
A WHR a derék-csípő arányt jelzi. A zárójelben lévő értékek interkvartilis tartományok.
1 Wilcoxon aláírt rangú teszttel; az adrenalin és az NE esetében a kétirányú, ismételt intézkedések az ANOVA-t a fogyás hatására.
- Magnézium a neurózisokban és a neurotikumban - Magnézium a központi idegrendszerben - NCBI könyvespolc
- Kapcsolat a merevedési zavar és az elhízás között az elhízás és a súly kezelésében -
- Kim 8 fogyókúrás rendszer áttekintése 🍑 Vényköteles gyógyszerek a túlsúly és az elhízás kezelésére
- Az elhízás mérése Az elhízás megelőzése Forrás Harvard T
- Hogyan segíthet egy kövér macska fittségben - Tippek a macskák elhízásával járó Kellemes síkság állatkórházában