Kombinált terápia cachexiában
Egidio Del Fabbro
Kulcsszavak: Multimodális terápia; rák; cachexia
Beküldve 2018. június 27-én. Elfogadva közzétételre 2018. augusztus 06.
Bevezetés
Ken Fearon felismerte, hogy az embereknél a cachexia meghatározó jellemzői (súlycsökkenés, csökkentett táplálékfogyasztás és krónikus gyulladás) keretet nyújthatnak a cachexia osztályozásához és a több terápiás célpont azonosításának indoklását (1). A farmakológiai és a nem farmakológiai beavatkozások kombinálásával ennek a komplex szindrómának a sokrétű mechanizmusait egyszerre lehetne kezelni, ami jobb fehérje- és kalóriabevitelt, izom- és zsírgyarapodást, valamint jobb fizikai funkciókat eredményezhet. Továbbá értékelték a társbetegségek, például az életkorral összefüggő szarkopénia és a mozdulatlanság szerepét az izomsorvadás elősegítésében, igazolva a fizikai aktivitás és a táplálkozási támogatás bevonását az átfogó cachexia terápia kialakításába az „egész beteg” számára. A rákos kachexia komplex molekuláris mechanizmusait feltáró preklinikai kutatások további támogatást mutattak a specifikus egyedi beavatkozások multimodalitási kezelési stratégiákba történő beépítésére és a genetikai variációk miatt fokozott hajlamra a cachexia iránt.
Azonban több mint két évtizede, a siker ismétlődő pillantásai ellenére, a „multimodális terápia egy multidimenzionális problémára” koncepciójának erős bizonyítékai megfoghatatlannak bizonyultak. Ez az áttekintés kiemeli azokat a kutatásokat, amelyek támogatást nyújtanak a táplálkozási, testmozgási és farmakológiai beavatkozások változó kombinációjának alkalmazásához. A felülvizsgálat a múltbeli klinikai vizsgálatokra is összpontosít, amelyek nem szteroid gyulladáscsökkentő gyógyszereket (NSAID) és omega-3 kiegészítőket tartalmaznak kombinált terápiában - a szupportív kezelés mellett az egyik legfontosabb szer, amely szerepel a MENAC-ban (Multimodal-Exercise, Nutrition and Anti gyulladásos gyógyszer a Cachexiára), egy több központú vizsgálat, amelyet néhai Ken Fearon fejlesztett ki (2).
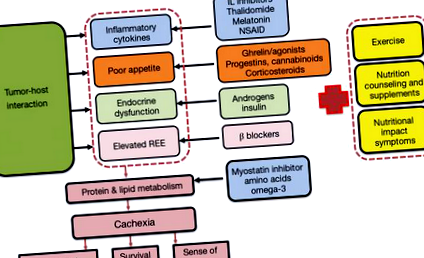
A cachexia multimodális terápiájának elméleti modelljét az 1. ábra mutatja. Bár vita merülhet fel az egyes egyedi beavatkozások összetételéről vagy relatív fontosságáról, a modell bemutatja a különféle cachexia mechanizmusokra irányuló multimodalitás kezelésének indoklását.
Egyénre szabott multimodális modell
A beteg preferenciája alapján
További klinikai és biológiai markerekre van szükség annak érdekében, hogy jobban azonosíthassuk azokat az egyéneket, akik adott beavatkozásokra reagálhatnak. A cachexia biomarkerei még gyerekcipőben járnak, de a jövőben megkönnyíthetik a korábbi beavatkozást, hatékonyabb egyénre szabott terápiás rendet és kevesebb felesleges mellékhatást. A gyulladásgátló citokinek, a reaktív oxigénfajok (ROS) (8,9) és az egy nukleotid polimorfizmusok (10, 11) példák olyan markerekre, amelyek segíthetnek a kachektikus betegek biológiai profiljának kialakításában.
Farmakológiai kombinációk
Egyedül a monoterápia nem valószínű, hogy kijavítja a cachexiával járó többszörös rendellenességeket, például az izom-, zsír- és fizikai funkciók csökkenését, a negatív fehérje- és energiaegyensúly miatt, amelyet a csökkent táplálékfelvétel és az anyagcsere-diszfunkció vezet. Még egy hatékony farmakológiai hatóanyagot is össze kellene kapcsolni étrendi tanácsadással, kiegészítéssel, a tünetek kezelésével és a testmozgással. A kombinált terápiának ideális esetben additív vagy akár szinergetikus hatása is lehet. Sajnos egyes jelenlegi gyógyszerek, például a megestrol-acetát (MA) vagy a medroxiprogeszteron kedvezően modulálhatják az egyik utat, miközben más potenciálisan káros mechanizmusokat ösztönöznek. Például, bár a progesztinek csökkenthetik a gyulladásgátló citokineket és javíthatják az étvágyat, ezek endokrin rendellenességekkel, például hipogonadizmussal és hipoadrenalizmussal társulnak (12). Más gyógyszerek, például a kortikoszteroidok, hatékony étvágygerjesztők, de káros hatással vannak az izom működésére, beleértve a myopathiát is. Néhány vizsgált cachexia-beavatkozás, például a ghrelin, a ghrelin agonisták, a béta-blokkolók és a testmozgás, különösen ígéretesnek tűnik, mivel több mechanizmust is kedvezően befolyásolhatnak (pl. Gyulladásos és neurohormonális utak).
NSAID-ok
Számos nem szteroid gyulladáscsökkentőt, köztük celekoxibot, ibuprofent, indometacint és etodolakot (13), önmagában vagy más szerekkel kombinálva alkalmaztak a rákos kachexiával kapcsolatos különféle klinikai eredményekhez. Szisztematikus szakirodalmi áttekintés 13 vizsgálatból 11-et azonosított, amelyek javulást vagy stabilizálódást mutattak a súly vagy a testtömeg (LBM) terén (14). A szerzők azonban arra a következtetésre jutottak, hogy a klinikai vizsgálatokon kívül a bizonyítékok nem voltak elegendők az NSAID-k cachexiához történő ajánlásához, mivel hét nem volt összehasonlító, többségük kis mintamérettel rendelkezett, és néhány módszertanilag hibás volt. A nem szteroid gyulladáscsökkentők és más szerek kombinációját használó vizsgálatok két olyan vizsgálatot tartalmaztak, amelyben az NSAID-ket MA-val, illetve NSAID-okat halolajjal kombinálták.
Az ibuprofen (1200 mg/nap) prospektív randomizált vizsgálata MA-val kombinálva szignifikánsan javított életminőséget (QoL) és 2,3 kg-os átlagos súlygyarapodást mutatott, szemben a kizárólag MA-ban szenvedő, gyomor-bélrendszeri betegek 2,8 kg-os fogyásával. GI) rák (15). Nevezetesen az ibuprofennel kombinált terápiában részesülő egyéneknél nem látszott, hogy a nagyobb vérzés kockázata nagyobb, mint az egyedül MA-t kapó betegeknél (napi 480 mg). A III. Fázisú vizsgálat 104 előrehaladott stádiumú nőgyógyászati daganatos betegnél megállapította, hogy az MA plusz az L-karnitin, a celekoxib és az antioxidánsok javították az LBM-t a kettős energiájú röntgenabszorpciósometriával (DEXA), a REE-vel, a fáradtsággal és a QoL-vel mérve, egyedül a MA-hoz képest ). A gyulladás és az oxidatív stressz mértéke, beleértve az IL-6-ot, a TNF-α-t, a CRP-t és a ROS-t, jelentősen csökkent a kombinált terápiával.
Egy 6 hetes prospektív vizsgálatban 22 előrehaladott tüdőrákos beteg vett részt összehasonlítva a celekoxibot (napi 200 mg naponta kétszer) a halolajjal kombinálva a csak a halolajjal (napi 6 g osztott adagokban). A kombinált terápiában részesülők CRP-szintje szignifikánsan alacsonyabb volt (17) (21,3 mg/L; standard hiba 7) és nagyobb a markolat ereje (3,12; 0,98), mint a monoterápiában részesülő betegeknél (6,7 mg/L; 4,5 és 1,16; 0,3). Mindkét csoport számára az alapanyagcsere (BMR) 20% -ának megfelelő étrend-kiegészítést kaptak, a BMR-rel egyenértékű kalóriabevitel fenntartását célzó étrendi tanácsok mellett.
Végül egy svéd központ, amelynek kórtörténetében kombinációs terápiát alkalmaztak a rákos cachexiában, összehasonlította a központban lévő cachexia szokásos ellátását (SC) az SC-vel és az alacsony dózisú inzulinnal 138 előrehaladott GI rosszindulatú daganatos betegben (18). Az SC tartalmazta az indometacint az emelkedett CRP-s betegek számára, valamint az eritropoietint a vérszegénységért, valamint az enterális vagy parenterális táplálékot a csökkent ételfogyasztásért (
A tünetek kezelésének és a szupportív kezelésnek alapvető szerepe van a csökkent orális bevitel sok közreműködőjének kezelésében. Ide tartoznak a korai jóllakottság, az íz- és illatváltozások, a mucositis, az émelygés, a székrekedés, a fájdalom, a dysphagia, a fáradtság és a depresszió (32). Ezek a tünetek gyakoriak (33), csökkentik az energiafogyasztást (34), és reagálnak a könnyen elérhető, olcsó gyógyszerekre, növelve az orális bevitelt és a súlygyarapodást a betegek legfeljebb egyharmadánál (32). Egyéb anyagcsere-rendellenességek, például hipogonadizmus, B12-vitamin-hiány, hipotireózis és hipoadrenalizmus szintén hozzájárulhatnak az anorexiához és az izmok kimerüléséhez a betegeknél; azonban a férfiak alacsony tesztoszteronszintje és a D-vitamin-hiány (35) a leggyakoribbnak tűnik. A NIS jelentőségét egy olyan tanulmány hangsúlyozta, amely 17 tünet hatását értékelte a fej- és nyakrákos betegek klinikai eredményeire. A tünetek összesített terhe jelentős független előrejelzője volt a csökkent bevitelnek, a fogyásnak és a túlélésnek (36). Fontos, hogy ezek a NIS hatással lehetnek a szájon át történő bevitelre a betegség egész pályáján, ami az előrehaladott rák, a rákellenes kezelés vagy akár az orvosi kísérő betegségek tüneteinek és szövődményeinek következménye lehet.
Pszichoszociális beavatkozások
Táplálékkiegészítők és étrendi tanácsadás
A megnövekedett kalória- és fehérjebevitel szükségességét hangsúlyozó multimodális megközelítést alátámasztják olyan vizsgálatok, amelyek az ONS-t a beavatkozás részeként tartalmazzák, és tanulmányok arról számoltak be, hogy az előrehaladott daganatos és súlycsökkentő betegek többsége olyan étrendet fogyaszt, amely nem elégséges a testsúly fenntartásához még egészségesekben egyének. Szisztematikus áttekintés szerint az idősebb betegek különösen érzékenyek lehetnek, a kemoterápia során akár 90% -uk is fogyhat. Az étrendi tanácsadás, amely magában foglalja az energiasűrűségű ételek növelését, az étkezési gyakoriságot és az orális folyékony táplálékkiegészítők használatát, javíthatja az energiafogyasztást és a testsúlyt. Kevés publikált tanulmány létezik, és egy szisztematikus áttekintés arra a következtetésre jutott, hogy nem volt elegendő bizonyíték az előnyökre azoknál a betegeknél, akik rákos kachexiában szenvedtek (42–44). Azonban az onkológiai betegek táplálkozási beavatkozásainak szisztematikus áttekintése (45) és metaanalízise (46) megállapította, hogy ONS-sel vagy anélkül tanácsadás társult a súly, a BMI, az energiafogyasztás és a PG-SGA pontszám javulásával.
Gyakorlat
A testmozgás javíthatja az izomtömeget és az erőt, a fizikai funkciókat (47), a fáradtságot és a QoL-t rákos cachexiában szenvedő betegeknél. A testmozgás az izomanyagcsere, az inzulinérzékenység, a daganat növekedésének mérséklése és a gyulladás szintjének csökkenése révén fejtheti ki hatásait (48). A rezisztencia-edzés és az aerob testgyakorlás erős igazolása ellenére (49) egy szisztematikus áttekintés nem talált elegendő bizonyítékot a rákos cachexiában szenvedő betegek biztonságosságának és hatékonyságának meghatározásához (50). A testmozgást kis kísérletek során sikeresen kombinálták más módozatokkal. A tesztoszteronnal kombinált ellenállási gyakorlat nagyobb anabolikus hatást fejt ki, mint bármelyik önmagában végzett beavatkozás az életkorral összefüggő cachexia esetében, és hasonló előnyöket mutatott a HIV és a COPD esetében (51). A HIV-vel összefüggő pazarlás esetén az eugonadal férfiaknál a rezisztencia edzés és a tesztoszteron kombinációja növeli az izomtömeget (52). A testmozgás a multimodális terápia fontos elemének ígérkezik, mivel modulálja a citokinek expresszióját, és talán együtt működik az anabolikus hormonokkal az erő, a funkció és a QoL javítása érdekében (53).
Jelenlegi multimodális vizsgálatok
A multimodalitási beavatkozás fent vázolt kerete beépült két randomizált vizsgálat tervezésébe. A cachexia testmozgásának, táplálkozásának és gyulladáscsökkentő kezelésének II. Fázisú multimodális vizsgálata megvalósíthatóságot és biztonságot mutatott azoknál a betegeknél, akik kemoterápiában részesültek gyógyíthatatlan tüdő- vagy hasnyálmirigyrák miatt. A III. Fázisú MENAC-beavatkozás egy multimodális, több helyszíni kísérlet, amely ibuprofent (1200 mg/nap), omega-3 zsírsavakat (2 g EPA és 1 g DHA), ONS-t tartalmaz, 542 kcal és 30 g fehérje, és otthoni testedzési program, amely hetente háromszor ellenállóképzést és heti 2 alkalommal aerob edzést tartalmaz. Mivel a cachexia korai szakaszában lévő betegek nagyobb valószínűséggel reagálnak a terápiára, a beavatkozásokat a kemoterápia és az egyidejű tünetkezelés mellett kezdik meg (54).
Következtetések
Köszönetnyilvánítás
Lábjegyzet
Érdekkonfliktusok: A szerzőnek nincs kijelentendő összeférhetetlensége.
- A normobact l sinbiotic klinikai alkalmazásának tapasztalata az akut bél kombinált terápiájában
- Endoszkópos bariatrikus terápia (EBT) Michigan Medicine
- Zsír; s Az érzelmi szorongás elleni védőszigetelés funkciója - terápiás blog
- Zsírvesztés program specialistája - San Jose, CA Excel Medicine Internal Medicine
- Zsír; Fogyás; Vörös fényterápia Amit tudnia kell Greenspan Wellness Center