LEAP2: Az élelmiszer-bevitel és a testsúly új szabályozója?
Tárgyak
Egy új tanulmány elsőként vizsgálja a májban dúsított antimikrobiális peptid-2 (LEAP2) és a különböző anyagcsere-állapotok kapcsolatát, és kiemeli a LEAP2 és a ghrelin (az étvágygerjesztő szerepe miatt „éhséghormonként” ismert) kölcsönös kapcsolatot. . Ezeknek a megállapításoknak fontos következményei lehetnek, tekintve az elhízás világméretű növekedését 1975 óta.
Utal rá Mani, B. K. és mtsai. A LEAP2 változik a testtömeggel és a táplálékfelvétellel emberben és egérben. J. Clin. Invest. 129, 3909–3923 (2019).
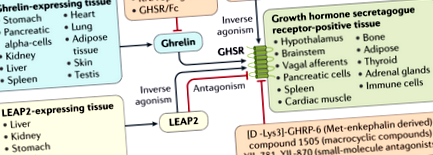
A Ghrelin egy orexigén peptidhormon, amely periférián (főleg a gyomorból) választódik ki, és jelzi az agy számára, hogy ösztönözze az ételbevitelt. 1999-ben a ghrelint a növekedési hormon szekretagóg receptor (GHSR) endogén ligandumaként azonosították, amely serkenti az agyalapi mirigy növekedési hormon felszabadulását 1. 19 évvel később, 2018-ban, májban dúsított antimikrobiális peptid-2-ről (LEAP2) írták le a ghrelin által kiváltott GHSR-aktiváció gátlását, megakadályozva ezzel a ghrelin hatásait a növekedési hormon felszabadulására, az élelmiszer-bevitelre és az éhezés alatti glükózszint-szabályozásra 2. A LEAP2 táplált állapotban a májból, a veséből, a gyomorból, a nyombélből és a jejunumból választódik ki, ami feltételezi, hogy a LEAP2 egy endogén ghrelin antagonista vagy inverz agonista. Mani és munkatársai új tanulmánya. A 3. ábra a LEAP2 és a különböző anyagcsere-viszonyok kapcsolatát vizsgálja.
Egerekben a LEAP2 plazmaszintje pozitívan korrelált a zsír tömegével és testtömegével (vagyis a LEAP2 szintje a súlygyarapodás növekedésével, a súlycsökkenéssel pedig ismét csökkent) 3. Az elhízott és a sovány egerek nem különböztek a máj vagy a jejunális LEAP2 mRNS expressziós szintjét tekintve, ami arra utal, hogy a LEAP2 szintjének változásai nem a transzkripciós szabályozásból származnak. Nevezetesen más szöveteket, mint például a vese, a nyombél és a gyomor, nem vizsgálták, felvetve a kérdéseket, hogy ezek az expressziós helyek stimulálódnak-e az elhízás körülményei között, és ha nem, milyen mechanizmusok szabályozzák a plazmaszint növekedését.
Ez a tanulmány azt is kimutatta, hogy sovány egerekben a 24 órán át tartó akut böjt csökkentette a LEAP2 plazmaszintjét anélkül, hogy megváltoztatta volna a máj LEAP2 mRNS szintjét 3. Ezenkívül az orális glükóz beadása (a vércukorszint növelése érdekében) a LEAP2 plazmaszintjének emelkedését eredményezte 1 óra múlva 3. Hasonlóképpen, az 1-es típusú diabetes mellitus egérmodelljében a hiperglikémia növelte a LEAP2 plazmaszintjét 3. Összességében egyértelmű pozitív korrelációt mutattak ki a glükóz és a LEAP2 szint között. Érdekes módon a sovány egereknél tapasztalt LEAP2 kalória-bevitel által kiváltott uregegulációját sovány nőknél nem figyelték meg 3, megkérdőjelezve az egereken végzett vizsgálatok eredményeinek az emberekre történő átvitelét és hangsúlyozva az emberi adatok bevonásának fontosságát is.
Amint fentebb említettük, az éhgyomri nők étkezés (337 kcal) bevitele nem növelte szignifikánsan a LEAP2 plazmaszintjét 1,5 óra elteltével sem sovány, sem elhízott egyéneknél 3. Azonban a magas kalóriatartalmú folyékony étkezés (600 kcal) a nem koplalt felnőttek vegyes nemű csoportjában, amelynek BMI-értéke> 35 kg/m 2, 2 óra elteltével lényegesen megemelte a LEAP2 plazmaszintjét, ami pozitívan korrelált a plazma glükózszintjével 3. Hogy ezt az eltérést a két kohorsz között a metabolikus állapot, a nem, az elemzés időzítése, az étkezés kalóriamennyisége vagy konzisztenciája okozza-e, további vizsgálatot igényel.
A Roux-en-Y gyomor bypass csökkentette az étkezés utáni szintet 3 hónap elteltével, az éhomi LEAP2 plazmaszint pedig 2 év után embernél 3. Hasonlóképpen, a függőleges hüvelyes gastrectomia csökkentette az étkezés utáni plazma LEAP2 szintjét, és tompította az étkezés okozta LEAP2 növekedést
12–18 hónappal a műtét után 3. Különösen úgy tűnik, hogy a fogyás megelőzi a LEAP2 csökkenését (3. hivatkozás), ami arra utal, hogy a fogyás független a LEAP2-től. Mindazonáltal egyelőre nem világos, hogy az elhízott betegek számára előnyös-e az exogén LEAP2 alkalmazás, mint konzervatív kezelési módszer.
Kevés kivételtől eltekintve a LEAP2 és az acil-ghrelin szint kölcsönös kölcsönhatását bizonyították egerekben és emberekben is. Ezenkívül a receptortanulmányok kimutatták, hogy a LEAP2 képes kiszorítani a ghrelint a GHSR 5-höz kötődési helyéről. Tekintettel arra, hogy a LEAP2 potenciálja és affinitása a GHSR iránt majdnem megegyezik a ghrelinével, és a LEAP2 koncentrációja 20-szor magasabb, mint az ac lib-grelin koncentrációja az ad libitum táplált egerek és az emberek 3 plazmájában, feltételezhető. hogy a LEAP2 a táplált állapotban a domináns endogén GHSR ligandum, ami megakadályozhatja a további (túl) evést.
A LEAP2 szekréciójának modulálása ígéretes célpont olyan körülmények között, mint az elhízás.
Összességében ez a tanulmány az első, amely részletesebben megvizsgálja a LEAP2 emberben történő szabályozását, mivel a korábbi vizsgálatok csak az emberi LEAP2 molekulaszerkezetét és in vitro hatásait vizsgálták. Ezek az adatok átfogóak és egyértelműen erős kapcsolatot mutatnak a LEAP2 és az egerek és az emberek metabolikus állapotának akut, valamint krónikus változásai között. Ezek a vizsgálatok különösen relevánsak az elhízás világszerte növekvő gyakorisága fényében 10, és új gyógyszerészeti stratégiákhoz vezethetnek.
Hivatkozások
Kojima, M. és mtsai. A Ghrelin egy növekedési hormont felszabadító acilezett peptid a gyomorból. Természet 402, 656–660 (1999).
Ge, X. és mtsai. A LEAP2 a ghrelin receptor endogén antagonistája. Sejt. Anyagcsere 27., 461–469.e6 (2018).
Mani, B. K. és mtsai. A LEAP2 változik a testtömeggel és a táplálékfelvétellel emberben és egérben. J. Clin. Invest. 129, 3909–3923 (2019).
Cornejo, M. P. és mtsai. A növekedési hormon szekretagóg receptor jelátvitel 4 napos falatozási modellben befolyásolja a magas zsírbevitelt, függetlenül a ghrelin és az ugrás plazma szintjétől. J. Neuroendocrinol. https://doi.org/10.1111/jne.12785 (2019).
M’Kadmi, C. és mtsai. Az N-terminális máj-expresszált antimikrobiális peptid 2 (LEAP2) régió fordított agonista aktivitást mutat a ghrelin receptor felé. J. Med. Chem. 62, 965–973 (2019).
Wang, J. H. és mtsai. A LEAP2 és a GHSR1a receptor kötődési mechanizmusának azonosítása. FEBS J. 286, 1332–1345 (2019).
Schalla, M. A. & Stengel, A. A ghrelin farmakológiai modulációja a fogyás kiváltására: sikerek és kihívások a jelenlegi cukorbetegségről. Curr. Diabetes Rep. 19., 102 (2019).
Schalla, M. A. & Stengel, A. A ghrelin szerepe az anorexia nervosában. Int. J. Mol. Sci. 19., 2117 (2018).
Henriques, S. T., Tan, C. C., Craik, D. J. & Clark, R. J. Az emberi májban expresszált antimikrobiális peptid 2 szerkezeti és funkcionális elemzése. Chembiochem 11., 2148–2157 (2010).
Köszönetnyilvánítás
A szerzők munkáját a Német Kutatási Alapítvány (STE 1765/3-2) és a Charité Egyetemi Finanszírozás (UFF 89/441-176, A.S.) támogatásával támogatják.
Szerzői információk
Hovatartozások
Charité Belgyógyászati és Bőrgyógyászati Központ, Pszichoszomatikus Orvostudományi Osztály, Charité-Universitätsmedizin Berlin, a Freie Universität Berlin, a Humboldt-Universität zu Berlin és a Berlini Egészségügyi Intézet vállalati tagja, Berlin, Németország
Martha A. Schalla és Andreas Stengel
Pszichoszomatikus Orvostudományi és Pszichoterápiás Tanszék, Tübingeni Orvosi Egyetemi Kórház, Tübingen, Németország
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
- Az étkezés megtervezése nagyban összefügg az ételek változatosságával, az étrend minőségével és a testsúly állapotával
- Keto diéta Hogyan találhatom meg a test zsírszázalékát és a múmia varázslatos fogyókúrás teait
- Hogyan segíti elő a lorcaserin a fogyást, és ki részesül a Nature Reviews Endocrinology
- Keto diéta napi kalóriabevitel fogyás kalkulátor és fogyás kiegészítők vélemények
- Linda fogyókúrás tabletták vélemények a test egészségéről a vény nélkül Fogyás gyógyszeres terápiás