Mitokondriális diszfunkció elhízás esetén: a Q10 koenzim kiegészítésének potenciális előnye és mechanizmusa metabolikus szindrómában
Md Ashraful Alam
1 Orvosbiológiai Orvostudományi Kar, Queensland Egyetem, Brisbane, Ausztrália
2 Gyógyszerésztudományi Tanszék, Észak-Dél Egyetem, Dhaka, Banglades
Md Mahbubur Rahman
2 Gyógyszerésztudományi Tanszék, Észak-Dél Egyetem, Dhaka, Banglades
Absztrakt
A Q10 koenzim (Co-Q10) a mitokondriális elektrontranszportlánc alapvető eleme. A legtöbb sejt érzékeny a Q10 koenzim (Co-Q10) hiányára. Ez a hiányosság számos klinikai rendellenességben szerepet játszik, mint például szívelégtelenség, magas vérnyomás, Parkinson-kór és elhízás. A lipidszint-csökkentő gyógyszer sztatin gátolja a HMG-CoA átalakulását mevalonáttá, és csökkenti a plazma Co-Q10 koncentrációját. A Co-Q10 kiegészítése azonban javítja a sztatin terápia patofiziológiai állapotát. A legújabb bizonyítékok arra utalnak, hogy a Co-Q10 kiegészítés hasznos lehet az elhízás, az oxidatív stressz és a metabolikus szindróma gyulladásos folyamatainak kezelésében. A Co-Q10 gyulladáscsökkentő reakcióját és lipidmetabolizáló hatását valószínűleg a gyulladás és a lipidanyagcsere transzkripciós szabályozása közvetíti. Ez a tanulmány áttekinti a Co-Q10 kiegészítés jótékony szerepét és annak lehetséges hatásmechanizmusát a metabolikus és kardiovaszkuláris szövődmények járulékos tényezőinél.
Bevezetés
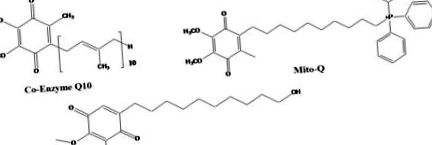
A Co-Q10, Mito-Q és Idebenone sematikus diagramja.
A Co-Q10 eredete, kémiája és abszorpciója
Mitokondriális biogenezis és Co-Q10
A mitokondriális biogenezist számos, a sejtben jelenlévő transzkripciós szabályozóval lehet modulálni. A peroxiszóma proliferátorral aktivált receptor (PPAR) család a mitokondriális biogenezis ilyen szabályozója [23]. Három típusú PPAR fehérjét azonosítottak eddig, a PPAR-α, PPAR-γ és PPAR-δ [24]. A PPAR-aktiváció szintén fontos a lipid anyagcsere, az adipocita differenciálódás és a gyulladás megelőzése szempontjából [24]. Sőt, a PPAR-ok a mitokondriális biogenezist is szabályozzák egy peroxiszóma proliferátorral aktivált receptor gamma koaktivátor-1α (PGC-1α) nevű aktivátor révén [25,26]. A PGC-1α fiziológiásan szabályozható testmozgással [27,28] és kalória-korlátozással [29]. Ezeken a testmozgáson és kalória-korlátozási eszközökön kívül olyan farmakológiai szerek, mint a fenofibrátok [30] és a resveratrol [31] stimulálják a PGC-1α-t és helyreállítják a mitokondriális funkciót. A PPAR-k Co-Q10 által közvetített aktivációja csak a közelmúltban derült ki, amely az energia homeosztázis lehetséges mechanizmusa lehet a kudarcos szövetekben és az elhízásban [32].
Metabolikus rendellenesség Co-Q10 hiány miatt
Ogashara és mtsai. leírta az első, elsődleges Co-Q10-hiányos betegeket (két nővér) 1989-ben [33]. Korai gyermekkoruktól kezdve progresszív izomgyengeség, rendellenes fáradtság és központi idegrendszeri diszfunkció volt, amelyet izmaikban alacsony Co-Q10 koncentráció jellemzett. Mindkét beteg figyelemre méltóan javult az orális Co-Q10 alkalmazásával [33]. Megfelelő Co-Q10 szint fenntartása az egész testben fontos a normális működés és az egészség szempontjából. A Co-Q10 plazmakoncentrációja egészséges csecsemőben és gyermekben magas, és az életkor előrehaladtával csökken [34,35]. Metabolikus rendellenesség léphet fel a Co-Q10 hiány miatt. A növekvő bizonyítékok azt jelzik, hogy az oxidatív stressz kritikus szerepet játszik a 2-es típusú diabetes mellitus és annak szövődményeinek patogenezisében [36]. Alacsony plazma Co-Q10 koncentrációt találtak rossz glikémiás kontrollban és diabéteszes szövődményekben szenvedő betegeknél [37-40].
A HMG-CoA reduktáz inhibitorok (sztatinok) csökkentik az emberi Co-Q10 szintjét [41,42]. Alternatív megoldásként az orális Co-Q10-sel történő kiegészítés helyreállíthatja a plazma Co-Q10 szintjét a statin-terápiában részesülő betegeknél [41-43]. A statin által közvetített Co-Q10 kimerülés befolyásolja az izom működését. Azok a betegek, akik statint szedtek a plazma lipidek csökkentésére, myalgiában és myopathiás fájdalomban szenvedtek [44-46]. A Co-Q10 szívizom-kimerülését kardiomiopátiában szenvedő szívelégtelenségben szenvedő betegeknél is kimutatták, amelyet Co-Q10 terápia javított [47]. A statinnal kapcsolatos myopathiához hozzájáruló fontos tényező lehet az izomzavarokra való genetikai hajlam és az alapvető metabolikus mechanizmusok [48,49]. A sztatinterápia miatt genomiális variációt találtak a COQ2 génben, amely para-hidroxi-benzoát-poliprenil-transzferázt kódol a CoQ10 bioszintézis számára [48]. Egy másik jelentés azt sugallja, hogy a sztatinok befolyásolhatják az energia-anyagcserét (karnitin-palmitoil-transzferáz II-hiány) kombinálva genetikai érzékenységgel, amely kiválthatja a myopathiás kimenetelt bizonyos magas kockázatú betegeknél [49].
A Co-Q10 antioxidáns hatása
A Co-Q10 hatása a gyulladásra és a metabolikus szindrómára
Az alacsony sűrűségű lipoprotein (LDL) koleszterin oxidációja a legfontosabb szabályozó a gyulladás kialakulásához az endothel sejtekben és más szövetekben [78]. Az LDL receptor létfontosságú szerepet játszik a koleszterin felvételének fokozásában a plazmából a sejtekbe, valamint az apoB és az apoE-tartalmú lipoproteinek clearance növelésében [79]. Cukorbetegség és elhízás esetén az LDL-R populációk csökkentik és növelik az LDL szintjét a plazmában [80]. Az LDLR -/- egerek fokozott plazma lipidprofilt és növekedést mutattak a gyulladásos markerekben a magas zsírtartalmú étrendre reagálva [79,81,82]. Az LDLR -/- hím egerekben a PPARγ agonista anti-atherogén hatását tapasztalták, amely összefüggésben van a javuló inzulinérzékenységgel és a TNF-α és a zselatináz B csökkent szöveti expressziójával [83]. A peroxiszóma-proliferátor által aktivált receptor-y (PPAR-y) azonban beszámolók szerint csillapítja a gyulladást az aktivált makrofágokban azáltal, hogy zavarja az NF-κB jelátvitelt [84]. A PPAR-α egy másik analógja a PPAR családnak, és szabályozza a gyulladásgátló géneket is (2. ábra) [85].
A Co-Q pótlásának javasolt mechanizmusa a szövetek gyulladáscsökkentő és lipid anyagcsere útjain metabolikus szindróma esetén. AMPK, adenozin-monofoszfát-aktivált protein-kináz; PPAR, peroxiszóma proliferátor által aktivált receptor; PGC-1α, peroxiszóma proliferátor-aktivált receptor gamma koaktivátor-1; oxLDL, oxidált kis sűrűségű lipoprotein; NRF, nukleáris légzési tényező; LXR, máj X receptor; PPRE PPAR válaszelem.
A Co-Q10 gyulladáscsökkentő aktivitása jól dokumentált. A sejtek LPS-sel történő stimulálása a TNF-α, a makrofág gyulladásos fehérje-1 alfa (MIP-1α) és a monocita kemo-attraktáns protein-1 (MCP-1) egyértelmű felszabadulását eredményezte, amelyeket jelentősen gyengített a sejtek előzetes inkubálása. a Co-Q10 redukált formája [86,87]. A CoQ10-gyel végzett kezelés szintén csökkentette a megemelkedett plazma lipidprofilokat és csökkentette a pro-gyulladásos citokin TNF-α expresszióját ob/ob egerek zsírszöveteiben [88]. A CoQ10-kiegészítés javította a magas zsírtartalmú fruktóz-táplálékkal táplált patkányok májának gyulladásos állapotát is [89]. A legújabb bizonyítékok arra utalnak, hogy a Co-Q10 a PPAR-k agonistájaként szolgálhat, és aktiválja a PPAR által közvetített gyulladáscsökkentő választ (2. ábra) [90,91].
A Co-Q10 hatása az endothel diszfunkcióra és a magas vérnyomásra
A Co-Q10 hatása a szívműködési zavarokra
A Co-Q10 hatása a cukorbetegségre és az inzulinrezisztenciára
Máj steatosis és a Co-Q10 hatása a máj diszfunkciójára
A Co-Q10 kiegészítés májvédelmet mutatott a májműködési zavarok más modelljeiben is. A Co-Q10 kezelés májvédelmet mutatott patkányokban az acetaminofen által kiváltott máj-toxicitások ellen [59]. A Q10 koenzim-kezelés javította az extenzív centrilobularis nekrózist, a citoplazmatikus vakuolizációt és a hepatociták ballonos degenerációját torlódott sinusoidokkal patkányok májában [59]. Ezeknek a patkányoknak a májvédelme az blokkoló NF-kB által közvetített gyulladásos jelutaktól és a kaszpáz aktivitás inaktivációjától függ [59]. A Co-Q10 kiegészítés hatékonyan megakadályozza a toxin által kiváltott májkárosodást is [130]. Az étrendben a Co-Q10 kiegészítés májvédelmet is mutatott idős patkányokban a fokozott celluláris antioxidáns hatás miatt [131].
A Co-Q10 hatása az elhízásra és a zsíranyagcserére
A jövő perspektívái és következtetés
A Co-Q10 gyulladáscsökkentő tulajdonságokkal rendelkező antioxidáns molekulaként bizonyított. A legújabb bizonyítékok arra is utalnak, hogy a Co-Q10 AMPK és PPAR aktivátoroként szolgálhat, és növeli a sejtek zsírégető képességét (1. táblázat). Használata a gyenge vízoldékonyság és a lipofil természet miatt még mindig korlátozott. Számos analógot szintetizáltak eddig, például a mito-Q-t és az idebenont.
Asztal 1
A Co-Q10 kiegészítés hatása a lipid anyagcserére metabolikus szindrómában
| Lipid anyagcsere | 3 T3-L1 pre-adipocita | -Növeli a zsírsav-béta oxidációt. | [32] |
| - ↑ Ca ++ Influx; ↑ AMPK; ↑ PPAR-α. | |||
| -Megakadályozza az adipociták differenciálódását | |||
| Fruktóz táplált patkány | -↓ összkoleszterinszint; ↓ LDL-koleszterin; ↓ trigliceridek | [93] | |
| ob/ob egerek | - ↓ összkoleszterinszint; ↓ trigliceridek; ↓ NEFA | [88] | |
| - ↓ a lipogén enzimek, például a zsírsav szintáz (FAS) és az acetil-CoA karboxiláz 1 (ACC1) mRNS expressziója. | |||
| C57BL6J egerek | - Növeli a zsírsav-béta oxidációt | [90] |
Rövidítések
AMPK: Adenozin-monofoszfát-aktivált protein-kináz; ATP: adenozin-trifoszfát; CAT: kataláz; ERK: Extracelluláris receptor kináz; GPx: glutation-peroxidáz; GST: glutation-S-transzferáz; HUVEC: Emberi köldökvénás endothelsejt; IL-6: Interleukin 6; IRS: Inzulinreceptor szubsztrát; LDL: alacsony sűrűségű lipoprotein; LXR: Máj X receptor; MAPK: mitogénnel aktivált protein-kináz; MCP-1: monocita kemotaktikus protein-1; mtTFA: A mitokondriális transzkripciós faktor; NO: Nitrogén-oxid; NRF: Nukleáris légzési tényező; PGC-1α: peroxiszóma proliferátor-aktivált receptor gamma koaktivátor-la; PPAR: Peroxisoma proliferátor által aktivált receptor; PPRE: PPAR válaszelem; ROS: Reaktív oxigén szubsztrát; SOD: Szuperoxid-diszmutáz; STZ: sztreptozotocin; TNF: Tumor nekrózis faktor; VSMC: vaszkuláris simaizom sejt; oxLDL: Oxidált kis sűrűségű lipoprotein; VCAM-1: Vaszkuláris sejtadhéziós molekula-1; UCP-1: Fehérje szétkapcsolása - 1.
Versenyző érdeklődés
A szerzők kijelentik, hogy nincsenek versengő érdekeik a kézirattal kapcsolatban.
A szerzők hozzájárulása
A MAA generálta az ötletet, a szakirodalom felkutatását és elkészítette a kéziratot. Az MMR elkészítette a rajzokat, ábrákat és elkészítette a kéziratot. Mindkét szerző elolvasta és jóváhagyta a végleges kéziratot.
Köszönetnyilvánítás
Md. Ashraful Alamot az Islamic Development Bank Merit PhD ösztöndíj és a Queenslandi Egyetem tandíj ösztöndíja támogatta.
- A hipotalamusz gyulladásának markere vagy az elhízás mechanizmusa Patogenezis Diabetes
- Az elhízás oka-e az ízületprotézisek elkerülésére Harvard Health Blog - Harvard Health
- A föld alatti rágcsálók hogyan védekeznek a rák ellen A második vakond patkányfajok mechanizmusa eltérő
- Hogyan segíthet a csal étkezés valóban az étrendedben - Aaptiv
- Az elhízás genetikai-e, mit kell tudni a genetikáról és a testsúly alakjáról