A kezdeti intravénás immunglobulin-dózist az elhízott, elsődleges immunhiányos betegségben szenvedő betegek testtömegén kell alapulnia
Absztrakt
Háttér
Az immunglobulin terápia kritikus szerepet játszik az immunhiányos rendellenességek, valamint az autoimmun és gyulladásos állapotok kezelésében. Immunhiányos betegeknél vita merült fel arról, hogy az intravénás (IVIG) kezdeti terhelő dózisoknak a tényleges testtömegen vagy egy olyan számított paraméteren kell-e alapulniuk, mint például az elhízott betegeknél beállított testtömeg.
Eset bemutatása
Leírok egy gyakori változó immunhiányos rendellenességet (CVID) szenvedő beteget, akinek bariatériás műtéten esett át kóros elhízás miatt. Súlya 50% -kal csökkent a számított ideális testtömeg (IBW) alá, míg immunglobulinigénye körülbelül 20% -kal csökkent. Állandó állapotú szérum IgG-je súlycsökkenéssel egyidejűleg körülbelül 7 g/l-ről 11,7 g/l-re nőtt.
Következtetések
Ezt a megfigyelést alátámasztom annak az ajánlásnak, miszerint az immunhiányos állapotban a SCIG/IVIG kezdeti terhelési dózisának a beállított testtömegen (AjBW) kell alapulnia, és nem az elhízott betegek tényleges testtömegén. Ennek fontos költségvetési vonzatai vannak az elhízott, immunhiányos rendellenességekben szenvedő betegek kezelésében.
Háttér
Az immunoglobulin helyettesítés a legtöbb tüneti primer immunhiányos betegségben (PID) szenvedő beteg ellátásának szokásos standardja. Az immunglobulin pótlása történhet szubkután (SCIG) vagy intravénás (IVIG) úton. A jelenlegi adatok az egészség fokozatos javulását sugallják a szérum IgG szintjének fokozatos emelkedésével [1]. Általában a legtöbb beteg kevésbé válik tünetessé, ha egyensúlyi állapotát/minimális IgG-szintjét 7–8 g/l felett tartják [2]. Számos betegtényező befolyásolja a SCIG/IVIG-t követő egyensúlyi állapot/minimális szérum IgG-szintet. Ide tartozik az FcRn receptor genotípusa, a fertőző vagy gyulladásos állapotok, például a bronchiectasis jelenléte. A legtöbb esetben a fenntartó immunglobulin dózist utólag módosítják a klinikai válasz alapján [3, 4]. Ezt nevezték biológiai vályúszintnek [5, 6].
Mélységesen alacsony IgG-szinttel rendelkező primer immunhiányos rendellenességekben (PID) szenvedő betegeknél gyakran alkalmaznak kezdeti IVIG töltőadagot (1 g/kg), amelyet havonta 400–800 mg/kg fenntartó dózis követ. A telítő dózis lehetővé teszi a beteg számára, hogy gyorsan elérje az egyensúlyi állapotú terápiás IgG-szintet, ami egyébként több hónapig is eltarthat, ha tipikus fenntartó dózisokat adnak be. Viták folynak arról, hogy az IVIG kezdeti terhelő dózisának morbid elhízott PID-es betegeknél a tényleges testtömegen vagy a módosított testtömegen kell-e alapulnia [7]. Az IVIG-terápia legtöbb klinikai vizsgálata kizárta ezeket a betegeket.
Ha telítő dózist adnak, a legtöbb szakértő azt javasolja, hogy a kezdeti SCIG/IVIG dózist a tényleges testtömeg helyett a beállított testtömegen (AjBW) kell alapulnia. Ennek az ajánlásnak az az alapja, hogy a beadott immunglobulin nem oszlik el a testzsírban, és csak az intravaszkuláris térben és az extracelluláris folyadékokban van jelen. A kiigazított testtömeg alkalmazása az ideális testtömeg (IBW) vagy a sovány testtömeg (LBW) helyett azon a feltételezésen alapul, hogy az extracelluláris folyadék megnövekszik a megnövekedett zsírszövetben szenvedő betegeknél [8]. Ezeknek a levezetett testtömeg-paramétereknek a leírását és számítását az 1. táblázat jelmagyarázata mutatja.
Itt jelentek egy gyakori változó immunhiányos rendellenességben (CVID) szenvedő beteget, akinek kórházi elhízás miatt bariatrikus műtéten esett át. A progresszív fogyás a szérum immunglobulin szintjének fokozatos emelkedésével járt, ami lehetővé tette az adag csökkentését. Amint itt bemutatjuk, ez a megfigyelés alátámasztja azt az ajánlást, hogy az IVIG kezdeti terhelési dózisa a legalkalmasabban a PID-betegek beállított testtömegén és nem a tényleges testtömegén alapul.
Eset bemutatása
Az 50 éves beteg 2011-ben bronchiectasissal jelentkezett és csökkentette az immunglobulinszintet 2011-ben. IgG-je 3,5 g/l (7–14), IgA®, diftéria, H. influenzae és tetanus toxoidok voltak (2. táblázat) [9]. Csökkent a memória B-sejtjeinek száma, és találkozott Ameratunga et al. a CVID kritériumai [10, 11] és képesek intravénás immunglobulinra (IVIG). [12] Egyik lányának CVID-je van, de a teljes exomszekvenálás (WES) nem tudta azonosítani az okozó mutációt a családban [13, 14]. Az IVIG előtt kezdetben profilaktikus antibiotikumokkal kezelték, de továbbra is áttörő fertőzései voltak. [12].
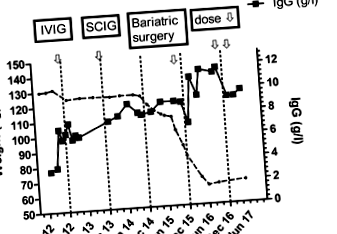
A csúcssúlya 132 kg volt, és a kezdeti immunglobulin-dózist a beállított testtömegnek megfelelően számították ki. Ezt követően a dózist a tünetei szerint titrálták, ami kb. 7 g/l minimális IgG-nek felelt meg. Az immunglobulin-pótlást követően a köpet termelése jelentősen csökkent, a bronchiectasisban pedig kevesebb exacerbáció lépett fel. Életmódbeli okokból később SCIG-kezelésre váltott, és jól maradt (1. ábra).
A beteg csúcssúlya 132 kg volt. Súlyát 110 kg-ra tudta csökkenteni a műtét idején, 2015 decemberében. Kezdetben IVIG-vel kezelték 2012 októberében, majd 2013 októberében SCIG-re változtatták. SCIG-adagja minden héten 14,4 g volt. 2016 novemberében heti 13,6 g-ra, 2017 januárjában pedig heti 12,8 g-ra csökkent. A súlycsökkenést megelőzően minimális immunglobulin-szintje körülbelül 7 g/l volt. Legutóbbi IgG-je 2017 májusában 9,2 g/l volt, annak ellenére, hogy a SCIG dózisa 20% -kal csökkent. A nyilak a kezelés változásait ábrázolják
A kóros elhízás ellenére sem felelt meg a szigorú kritériumoknak a közfinanszírozású bariatrikus műtétek terén Új-Zélandon, mivel nem alakult ki 2-es típusú cukorbetegség. A bariatrikus sebészeti csoporttal folytatott megbeszélést követően felvették súlycsökkentő műtétre az immunoglobulin-szükséglet csökkenése miatt várható költségmegtakarítás alapján. A bariatrikus műtét előtt 10 kg-ot tudott lefogyni (1. ábra). Roux-en-Y eljáráson esett át, és bonyolult posztoperatív tanfolyama volt.
A bariatrikus műtétet követően progresszív súlycsökkenést tapasztalt (1. ábra), amely 63 kg-on stabilizálódott, ami valamivel alacsonyabb, mint az előre jelzett ideális testtömeg (1. táblázat). Súlycsökkenéssel egyidejűleg a minimális IgG-szintje növekedni kezdett, lehetővé téve az adag csökkentését (1. ábra). Valószínűleg a jövőben a SCIG adagjának további csökkentése lehetséges. Egészségi állapota továbbra is jó, a köpettermelés jelentősen javult, és képes volt abbahagyni a profilaktikus antibiotikumokat.
Megbeszélés és következtetések
Megfigyelésem közvetlen bizonyítékot szolgáltat arra vonatkozóan, hogy az SCIG-követelmények jelentős súlycsökkenést követően csökkennek (1. ábra). A beteg tényleges súlya 50% -kal csökkent, de immunglobulinigénye körülbelül 20% -kal csökkent. Minimális IgG-szintje a műtét előtt körülbelül 7 g/l volt, de 11,7 g/l-re emelkedett, ami lehetővé tette a SCIG dózisának csökkentését. Amint az az 1. táblázatból látható, látszólagos SCIG-dózisa/kg majdnem megduplázódott 0,44 g/kg/hó-ról 0,81 g/kg/hó-ra súlycsökkenéssel együtt. A zsírszövet elvesztését követően az extracelluláris folyadék csökkenése feltehetően a csökkent immunoglobulin szükséglet és a szérum IgG növekedésének magyarázata. Más tényezők is hozzájárulhatnak a csökkent SCIG-követelményekhez, beleértve az elhízással járó gyulladásos állapot enyhülését és a bronchiectasis jobb szabályozását [7].
Számított IgG indexet (szérum IgG/SCIG dózis/kg) használtam annak meghatározására, hogy a műtét előtt melyik levezetett testtömeg-paraméter korrelál a legjobban a későbbi súlycsökkenés utáni SCIG-követelményekkel. Ez az index figyelembe veszi az egyensúlyi állapotú szérum IgG változását, valamint a SCIG/IVIG/kg dózis változását [7]. Ennek az IgG-indexnek egy változatát alkalmazták a minimális IgG-szint változásainak kiszámításához, amikor elhízott betegeknél módosították a SCIG/IVIG-dózist [15]. Betegem esetében a SCIG adagját kezdetben stabilan tartották, míg a súlya csökkent.
A fogyást követően tényleges testtömeg-IgG-indexe (szérum IgG/SCIG-dózis/kg) 11,35 volt, amely szorosan korrelált a korrigált testtömegből (11,2) a súlycsökkenés előtt megjósolt IgG-indexgel (1. táblázat). A súlycsökkentés utáni IgG index (11,35) figyelembe veszi a megnövekedett szérum IgG-t és a súlycsökkenést követően csökkent SCIG-dózist. Mint fentebb említettük, a zsírszövet elvesztését követően az extracelluláris folyadék rekesz csökkenése feltehetően megmagyarázza a szérum IgG szintjének növekedését (1. ábra). Más származtatott testtömeg-paraméterek, például a sovány testtömeg és az ideális testtömeg, nem hatékonyan modellezik ezt a megnövekedett extracelluláris folyadékteret az elhízásban. Nem szorosan korreláltak a testsúlycsökkenés utáni IgG indexszel (1. táblázat).
Az IgG-index kiszámítása ennél a páciensnél támogatja az elhízott PID-betegeknél az IVIG kezdeti terhelési dózisainak alapját a beállított testtömegre, nem pedig a tényleges testtömegre vagy az ideális testtömegre (1. táblázat). Amint azt a fentiekben megjegyeztük, a későbbi fenntartó SCIG/IVIG dózisok a beteg klinikai válaszán alapulnak. Az elhízott PID-ben szenvedő betegeknél az alacsonyabb IVIG-töltő dózis sok előnnyel jár. Nyilvánvaló fiskális előny. A kórházi tartózkodás az első látogatás alkalmával lerövidül, és más előnyök is vannak, többek között a trombózis és a szív- és érrendszeri nemkívánatos események alacsonyabb kockázata a nagy kezdeti infúzió miatt [7].
Kevésbé biztos, hogy ez a megfigyelés alacsonyabb IVIG-dózist alkalmazhat-e elhízott, autoimmun vagy gyulladásos rendellenességekben szenvedő betegeknél. A világ más részeihez hasonlóan Új-Zélandon ma is az autoimmun és gyulladásos rendellenességek teszik ki az IVIG használatának többségét [16]. Az immunmoduláló IVIG dózis általában 2 g/kg, 2-5 nap alatt adva. A magas csúcs IgG-szint fontos lehet a hatékonyság szempontjából autoimmun és gyulladásos rendellenességekben, összehasonlítva a PID-kkel, ahol a fenntartás alatti egyensúlyi állapot relevánsabb lehet. A legfrissebb kanadai tanulmányok arról szolgáltattak adatokat, hogy a módosított testtömeg használata jelentős költségmegtakarítást eredményezhet [8, 17]. Azonban nem nyújtottak be hatékonysági adatokat, ami fontos szempont az IVIG-dózisok kiigazításakor. Noha az IVIG alacsonyabb dózisával azonnali költségmegtakarítás érhető el, fennáll a csökkent hatékonyság kockázata, ami az egészségügyi rendszer downstream költségeihez vezethet [7]. Az autoimmun és gyulladásos rendellenességek esetén a beállított testtömeg alapján az alacsonyabb IVIG-dózisokat a jövőbeni vizsgálatok során validálni kell.
Az elhízás jelenleg globális közegészségügyi probléma. A bariatrikus műtétet egyre inkább felajánlják a kóros elhízásban szenvedő betegeknek, amikor más beavatkozások nem jártak sikerrel. Ezekben a betegeknél számos egészségügyi előnye van a testsúlycsökkenésnek, beleértve a cukorbetegség, a magas vérnyomás, a koszorúér-betegség és az osteoarthritis kockázatának csökkenését [18]. Általában a 30-as BMI-vel rendelkező betegeket, akiknek társbetegségei vannak, megfelelő jelöltnek tekintik a bariatrikus műtétre. A bariatrikus műtétnek megfelelő társbetegségek közé tartozik a cukorbetegség, a magas vérnyomás és az ízületi tünetek. Sok országban vannak életkorhatárok is. A konszenzus kritériumai kizárják az endokrin rendellenességek miatt másodlagos elhízást, valamint azokat, akik súlyos pszichés rendellenességekkel küzdenek.
A bariatrikus sebészeti beavatkozások fejlődnek [18]. Számos műtéti lehetőség létezik, beleértve a Roux-en-Y gyomor bypass-ot, hüvelyes gastrectomiát, duodenum kapcsolót és állítható gyomorszalagot. Ezen eljárások mindegyikének megvannak a maga előnyei és hátrányai. A legtöbb eljárást laparoszkóposan végzik, amelynek számos előnye van, beleértve a csökkent műtéti morbiditást is. Amint itt látható, a bronchiectasisban szenvedő PID-betegek jól tolerálják ezt az eljárást.
Bár a testsúlycsökkenésnek számos előnye van, jelentős műtéti kockázatok és anyagcsere-komplikációk vannak, amelyeket figyelembe kell venni ennek a lehetőségnek a mérlegelésekor. Jelenleg az operatív mortalitás körülbelül három eset/1000 [18]. Az ilyen műtéti beavatkozásokra befogadott betegek intenzív tanácsadáson esnek át, és arra ösztönzik őket, hogy végezzék el az elősebészeti súlycsökkenést a Bariatric sebészeti csoport dietetikusának felügyelete alatt. Betegem a műtét előtt csaknem 10 kg-ot tudott leadni (1. ábra). A műtét után rendszeresen látta táplálkozási tanácsokkal és monitorozással a bariatrikus sebészeti csoport. Súlya körülbelül 63 kg-ra stabilizálódott, és már nem szenved magas vérnyomásban vagy pre-diabéteszben.
Megfigyelésem azt mutatja, hogy az abszolút SCIG/IVIG követelmények lényegesen csökkenni fognak egy bariatrikus műtét után. A csökkent SCIG követelmények alapján évente 10 400 USD közvetlen költségmegtakarítást számoltam ki. 30 év alatt ez a megtakarítás önmagában meghaladja az eljárás költségeit. Nem felelt meg a szigorú NZ kritériumoknak a közfinanszírozású bariatrikus műtétek esetében, de az itt bemutatott gazdasági érv fontos tényező volt az eljárásban való részvétel szempontjából. A várható költségmegtakarítás megvalósul. Költség-haszon elemzés során figyelembe kell venni az immunoglobulin szükséglet csökkenését a jövőben PID-ben szenvedő betegeknél.
Noha ez egyetlen megfigyelés, a beteg saját történelmi kontrolljaként szolgált. Ez ellenőrzi a betegekkel kapcsolatos tényezőket, beleértve a bronchiectasist, az FcRn receptor genotípusát stb. Az elhízás növekvő prevalenciája miatt más SCID/IVIG-ben részesülő PID-betegek is súlycsökkentő műtéten esnek át a jövőben. Fontos lesz gondosan dokumentálni a fogyásukat, és összehasonlítani a SCIG/IVIG követelményeikkel. Az ilyen betegek megfigyelései lehetnek a legmeggyőzőbb bizonyítékok arra, hogy a korrigált testtömeg a legjobb paraméter az IVIG kezdeti terhelő dózisainak megalapozásához PID-ben szenvedő betegeknél.
Hivatkozások
Orange JS, Belohradsky BH, Berger M, Borte M, Hagan J, Jolles S és mtsai. A dózis és a klinikai eredmények közötti korreláció értékelése a szubkután immunoglobulin helyettesítő terápiában. Clin Exp Immunol. 2012; 169 (2): 172–81.
Orange JS, Grossman WJ, Navickis RJ, Wilkes MM. A minimális IgG hatása a tüdőgyulladás előfordulására az elsődleges immunhiányban: a klinikai vizsgálatok metaanalízise. Clin Immunol. 2010; 137 (1): 21–30.
Hodkinson JP, Lucas M, Lee M, Harrison M, Lunn MP, Chapel H. A terápiás immunglobulint elhízott betegeknél a klinikai eredmény helyett a testtömeg alapján kell adagolni. Clin Exp Immunol. 2015; 181 (1): 179–87.
Berger M. Choices in IgG helyettesítő terápia primer immunhiányos betegségek esetén: szubkután IgG vs. intravénás IgG és az optimális dózis kiválasztása. Curr Opin Allergy Clin Immunol. 2011; 11 (6): 532–8.
Bonagura VR. Dózis és eredmények primer immunhiányos rendellenességekben. Clin Exp Immunol. 2014; 178 (1. kiegészítés): 7–9.
Bonagura VR. Intravénás immunglobulin (IVIG) alkalmazása primer immunhiányos betegségben szenvedő betegek kezelésére. J Clin Immunol. 2013; 33 (2. kiegészítés): S90–4.
Hodkinson JP. Az immunoglobulin adagolásának szempontjai elhízott betegeknél. Clin Exp Immunol. 2017; 188 (3): 353–62.
Rocchio MA, Hussey AP, Southard RA, Szumita miniszterelnök. Az ideális testtömeg-adagolás hatása az összes fekvőbeteg számára i.v. immun globulin indikációk. Am J Health Syst Pharm. 2013; 70 (9): 751–2.
Empson M, Sinclair J, O’Donnell J, Ameratunga R, Fitzharris P, Steele R. A primer antitesthiány értékelése és kezelése. NZ Med J. 2004; 117 (1195): U914.
Ameratunga R, Woon ST, Gillis D, Koopmans W, Steele R. Új diagnosztikai kritériumok a közös változó immunhiányhoz (CVID), amelyek segíthetnek az intravénás vagy szubkután immunglobulin kezelésében. Clin Exp Immunol. 2013; 174 (2): 203–11.
Ameratunga R, Brewerton M, Slade C, Jordan A, Gillis D, Steele R és mtsai. A gyakori változó immunhiányos rendellenesség diagnosztikai kritériumainak összehasonlítása. Front Immunol. 2014; 5: 415.
Ameratunga R, Storey P, Barker R, Jordan A, Koopmans W, Woon ST. Diagnosztikai és kezelési kritériumok alkalmazása gyakori változó immunhiányos rendellenesség esetén. Rev Clin Immunol szakértő. 2015; 12 (3): 257–66.
Ameratunga R, Lehnert K, Woon ST, Gillis D, Bryant VL, Slade CA és mtsai. Áttekintés: a gyakori változó immunhiányos rendellenesség diagnosztizálása a genomszekvenálás korában. Clin Rev Allergy Immunol. 2017; (a sajtóban).
Ameratunga R, Koopmans W, Woon ST, Leung E, Lehnert K, Slade C és mtsai. A TACI (TNFRS13B) és a TCF3 mutációi közötti episztatikus kölcsönhatások súlyos primer immunhiányos rendellenességet és szisztémás lupus erythematosust eredményeznek. Clin Trans Immunol. 2017; (a sajtóban).
Khan S, Grimbacher B, Boecking C, Chee R, Allgar V, Holding S és mtsai. A szérum minimális IgG-szintje és az éves intravénás immunglobulin-dózis nem függ össze a rendszeres helyettesítő terápiában részesülő betegek testméretével. Drog Metab Lett. 2011; 5 (2): 132–6.
Ameratunga R, Steele R, Jordan A, Preece K, Barker R, Brewerton M és mtsai. Az elsődleges immunhiányos rendellenességekkel foglalkozó nemzeti szolgálat esete Új-Zélandon. NZ Med J. 2016; 129 (1436): 75–90.
Chow S, Salmasi G, Callum JL, Lin Y. A zsír levágása IVIG jóváhagyási eljárással. Transfus Apheresis Sci. 2012; 46 (3): 349–52.
Nguyen NT, Varela JE. Elhízás és anyagcserezavarok kezelésére szolgáló bariatrikus műtét: a technika állása. Nat Rev Gastroenterol Hepatol. 2017; 14 (3): 160–69. doi: 10.1038/nrgastro.2016.170.
Köszönetnyilvánítás
Köszönöm a páciensnek az engedélyt, hogy mások javára közzéteheti ezt az esetet. Köszönöm Dr. Michael Booth-nak a bariatrikus műtéttel kapcsolatos észrevételeit.
Versenyző érdekek
A szerző kijelenti, hogy nincs versengő érdeke.
Hozzájárulás a közzétételhez
A beteg hozzájárult a jelentés közzétételéhez. A közzétételnek nincsenek akadályai.
Nincsenek további adatok.
Etikai jóváhagyás és hozzájárulás a részvételhez
Ez a szokásos kezelés. A szokásos klinikai gyakorlattal kapcsolatban nincsenek etikai kérdések. Ez nem intervenciós vizsgálat.
Finanszírozás
Ezt a tanulmányt belsőleg finanszírozták.
Kiadói megjegyzés
A Springer Nature semleges marad a közzétett térképeken és az intézményi kapcsolatokban szereplő joghatósági igények tekintetében.
Szerzői információk
Hovatartozások
Klinikai Immunológiai Osztály, Aucklandi Kórház, Park Rd, Grafton 1010, Auckland, Új-Zéland
A PubMed Google Scholar alkalmazásban is kereshet erre a szerzőre
- A hormoninjekció elősegíti a fogyást elhízott betegeknél
- Laparoszkópos méheltávolítás és súlycsökkentő műtét elhízott, endometriumban szenvedő betegeknél
- Hipnózis, önhipnózis és fogyás elhízott betegeknél - teljes szöveges nézet
- A hormoninjekció elősegíti a fogyást elhízott és cukorbetegeknél
- Képzeletbeli étkezés; csalja be a testet a fogyásba - Salk Institute for Biological Studies