A cöliákia prevalenciája, patogenezise és diagnosztikája
Míg a celiakia (CD) biopsziája továbbra is az Egyesült Államokban a szokásos szűrési gyakorlat, addig az európai gasztroenterológusok és laboratóriumok folyamatosan távolodnak ettől az invazív eljárástól, kivéve a különösen nehéz esetek tisztázását. A diagnosztikai megközelítés változásának egyik legfontosabb oka a laboratóriumok számára elérhető különféle szerológiai vizsgálati módszerek sokasága. Sok ilyen véralapú vizsgálatot minden eddiginél nagyobb specifitással és érzékenységgel fejlesztettek ki, lehetővé téve a standard diagnosztikai kritériumok alapját a CD-specifikus antitestek kimutatásán. Pontosabban a szöveti transzglutamináz (tTG-IgA) és a dezamidált (módosított) gliadin peptidek (DGP), az immunglobulin (Ig) A és az IgG ellen.
Coeliakia
A CD egy egész életen át tartó, gluténérzékeny autoimmun betegség, amely környezeti (glutén) és genetikai tényezőkből (emberi leukocita antigén [HLA] és nem HLA gének) ered. A CD egyre inkább elterjedt és elterjedt a világ fejlett régióiban, például az Egyesült Államokban és Európában, mivel a betegség fokozott ismerete és észlelése folyamatosan növekszik. A betegség gyomor-bélrendszeri tünetekkel, nem gasztrointesztinális tünetekkel vagy egyáltalán nem jelentkezik. Általában súlyos gyomor-bélrendszeri problémákkal, például hasmenéssel, hányással, hasi fájdalmakkal és görcsökkel jelentkezik. A CD-betegek körülbelül felének azonban nem gasztrointesztinális tünetei vannak, amelyek lehetnek vérszegénység, csontritkulás, bőrbetegségek és fogyás.
Eredetileg úgy gondolták, hogy a CD kizárólag az európai populációkat érinti, de jelenleg az egész világon elterjedt. Olyan területeket, mint Dél-Amerika, Ázsia, a Közel-Kelet és Afrika, amelyekről korábban úgy gondolták, hogy a CD nem befolyásolja őket, ma úgy vélik, hogy alul diagnosztizálták, hozzájárulva ahhoz, hogy a CD az egyik leggyakoribb autoimmun és genetikai betegség legyen.
Úgy gondolják, hogy a CD általában követte az emberek evolúciós vándorlási és étrendi áramlásait - az egyszer elsősorban hússal, gyümölcsökkel és zöldségekkel való táplálkozástól kezdve a gazdálkodás fejlődéséig és előtérbe kerüléséig, amikor a gluténtartalmú gabonafélék, például búza, árpa és rozs szerves részévé váltak egy diéta. Amint az emberi terjeszkedés folytatódott, a gazdálkodás inkább az alapvető életmód lett, és a mezőgazdasági gyakorlatok, valamint az őslakosok fokozatos helyettesítése genetikai rendellenességeket vezetett be a populációban, ami fokozott gluténérzékenységhez vezet.
Betegség patogenezise
A CD-t általában környezeti és genetikai okok kombinációja aktiválja. A fő genetikai tényező a HLA-DQ génekből, a DQ2 és DQ8 származik. Genetikailag előre beállított egyéneknél a bélrendszer betegségét (enteropathia) az immunrendszer túlzott reakciója váltja ki a gluténban lévő prolaminokra, különösen a gliadinra. A Gliadin peptidek nem emészthetőek meg teljesen a vékonybélben, ami lehetővé teszi a gliadin maradványok felvételét a bélfalba és a környező bél kötőszövetébe. Ezen a ponton a tTG enzim deamidálja (módosítja) a gliadint azáltal, hogy a glutamin aminosavat glutamáttá alakítja. A DGP befolyásolja a bélpermeabilitást, és immunreakciót okoz CD betegeknél, mivel ellenállnak a gyomor-bélrendszeri enzimeknek. Ez a folyamat a DGP és a testek saját tTG elleni antitestek termelődését és a gyulladásos citokinek szekrécióját eredményezi. A vékonybél-hám gyulladása a bélbolyhok sorvadásához vezet. Ez a kaszkád a vékonybél duzzadását és a fent említett emésztőrendszeri tünetek sokféleségét eredményezi.
CD-specifikus antitestek és diagnózis
A cöliákia patogenezise. A HLA genetikai hajlam mellett a tTG autoantigének döntő szerepet játszanak a CD patogenezisében. A tTG elleni autoantitestek nagyon érzékeny és specifikus markerek a CD-re. Kimutathatók monospecifikus immunvizsgálatokkal, például antigénnel bevont ELISA-val vagy immunblottal, vagy közvetett immunfluoreszcencia tesztekkel (IIFT). A tTG közvetíti a gliadinek deamidálását, létrehozva egy epitópot, amely hatékonyan kötődik a DQ2-hez, és amelyet a bélből származó T-sejtek felismernek. A gliadin fragmensek ezen deamidált epitópjaival szembeni antitestek specifikusak a CD-re. A natív gliadin elleni antitestek azonban kevésbé specifikusak, és már nem meghatározó tényezők, mivel gyakran egészséges egyénekben is megtalálhatók. Az anti-DGP antitestek meghatározhatók ELISA, immunoblot vagy monospecifikus IIFT vizsgálatokkal.
A prolamin kiváltó tényező
A glutén egy olyan gabonafélékben található fehérje, mint a búza, az árpa, a rozs és a zab, összevonva a fehérjéket, a prolamint és a glutelint. Az élelmiszerekben található fehérjék többsége, amelyek felelősek a CD immunreakcióiért, a prolaminok. Magas glutamin tartalmuk és bizonyos specifikus szekvencia minták miatt a prolaminok rezisztensek a gyomor-bél enzimjeivel szemben, amelyek megvédik a vékonybelet az autoimmun reakciótól. A glutén hiányos emésztőrendszeri emésztése glutén eredetű gliadin peptidek jelenlétéhez vezet. A gabonafélékből származó prolaminok bevitele megváltoztatja a lisztérzékenységben szenvedő betegek vékonybél nyálkahártyáját, ami gyenge felszívódási szindrómához vezet, autoimmun reakciót okozva a glutén bevitele után. A CD szűrésénél kötelező, hogy az egyének rendszeresen gluténtartalmú étrendet folytassanak, mivel a CD-specifikus antitestek eltűnnek gluténmentes étrenden.
Új ESPGHAN diagnosztikai irányelvek
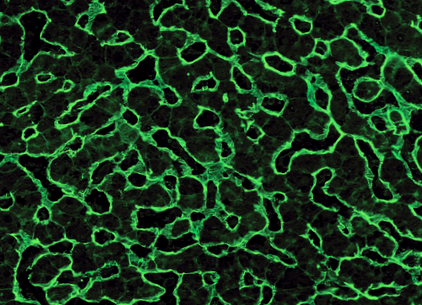
EmA kimutatása IFA-val a májszöveten. 2019 szeptemberében az Európai Gyermekgasztroenterológiai, Hepatológiai és Táplálkozási Társaság (ESPGHAN) frissített irányelveket tett közzé a CD diagnózisához. Amióta utoljára 2012-ben adták ki az irányelveket, érzékenyebb és specifikusabb módszereket fejlesztettek ki az antitestek kimutatására, ami a CD diagnosztikai tesztelésében való gondolkodás finomodásához vezetett. Az új irányelvek között szerepelnek olyan ajánlások, amelyek a kezdeti teszteléshez a teljes IgA és IgA osztályú transzglutamináz 2 (TGA-IgA) elleni antitestek kombinációját tartják pontosabbnak, mint más tesztkombinációk. Ha a teszt pozitív, akkor javasolt egy megerősítő teszt; ha mindkét teszt pozitív, akkor biopszia már nem ajánlott.
Az EmA kimutatása IFA segítségével a vékonybél szövetén. A gyermekgyógyászat tekintetében a CD-diagnózis biopszia nélküli megközelítése biztonságos a magas TGA-IgA-értékű (a normál felső határának ≥10-szerese) gyermekeknél, megfelelő tesztekkel és pozitív endomysialis antitestekkel (EMA-IgA) egy második szérummintában. Ha a TGA-IgA ≥10-szerese a normál felső határának (10xULN), és a család egyetért ezzel, biopszia nélküli diagnózist kell alkalmazni, feltéve, hogy az endomysialis antitestek (EMA-IgA) pozitív eredményt mutatnak egy második vérmintában. Pozitív TGA-IgA-val rendelkező, de alacsonyabb titerű gyermekek (rák
- Melyek azok a vörös zászlók, amelyeken gyermekem celiaciát szenvedhet; Egészségügyi alapanyagok Clevelandből
- Májbetegség kezelése Orvosi és táplálkozási szempontok (a Nestle Purina támogatása) DVM 360
- Tippek az egészséges testsúly megőrzésére a lisztérzékenységgel Modius Health
- Az α tumor nekrózis faktor meghatározó tényezője a patogenezisnek és a betegség progressziójának a mycobacteriumokban
- Fogyás - Anthony Medical; Kiropraktika Központ