A metabolikus kapcsolódás funkcionális kölcsönhatást tár fel a glükózfüggő inzulininotróp polipeptid és a ghrelin között emberben
A Potsdami Német Humán Táplálkozási Intézet Klinikai Táplálkozási Osztálya;
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Újranyomtatási kérelmek és egyéb levelezés címe: N. N. Rudovich, Potsdami Német Emberi Táplálkozási Intézet, Arthur-Scheunert-Street 114-116, 14558 Nuthetal, Németország (e-mail: [email protected]).
Molekuláris élettani tanszék, Max Planck Molekuláris növény-élettani Intézet, Potsdam-Golm;
II. Belgyógyászati Klinika, Klinikum Innenstadt, Ludwigs-Maximilians-Müncheni Egyetem;
A Potsdami Német Humán Táplálkozási Intézet Klinikai Táplálkozási Osztálya;
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Klinikai Táplálkozási Osztály, Potsdami Német Emberi Táplálkozási Intézet;
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Alkalmazott metabolomelemzés tanszék, Max Planck Molekuláris Növényélettani Intézet, Potsdam-Golm;
A Potsdami Német Humán Táplálkozási Intézet Klinikai Táplálkozási Osztálya;
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Klinikai Táplálkozási Osztály, Potsdami Német Emberi Táplálkozási Intézet;
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Coventryi egyetemi kórházak és Warwickshire NHS Trust, Coventry és Clincial Sciences Kutatóintézet, Warwicki Egyetem, Warwick, Egyesült Királyság; és
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Orvosi Osztály, Metabolikus Betegségek Intézete, Cincinnati Egyetem, Cincinnati, Ohio
Molekuláris élettani tanszék, Max Planck Molekuláris növény-élettani Intézet, Potsdam-Golm;
Alkalmazott metabolomelemzés tanszék, Max Planck Molekuláris Növényélettani Intézet, Potsdam-Golm;
Diabetes Center Bad Lauterberg, Bad Lauterberg, Németország;
Klinikai Táplálkozási Osztály, Potsdami Német Emberi Táplálkozási Intézet;
Endokrinológiai, Cukorbetegség és Táplálkozási Osztály, Campus Benjamin Franklin, Charité Egyetem Orvostudomány, Berlin;
Absztrakt
A legfrissebb adatok azt mutatják, hogy a ghrelin orexigén hatását befolyásolhatják más gyomor-bélrendszeri peptidek is, mint például a kolecisztokin (CCK), a bombezin, az YY3–36 (PYY3–36) peptid és a glukagon-szerű peptid-1 (GLP-1), ami arra utal, hogy releváns keresztbeszélgetés a perifériás orexigén és anorexigén jelek között az étvágy és a testsúly szabályozásában (49).
Az inkretin glükózfüggő inzulinotróp polipeptid (GIP), amely egy másik tápanyagfüggő tényező, amelyet a bél enteroendokrin sejtjei szekretálnak, a közelmúltban jelentős figyelmet kapott potenciális gyógyszercélként és az energia-anyagcsere endogén szabályozójaként (15, 21, 50). A GIP és a ghrelin közötti potenciálisan fontos kölcsönhatást javasolták az izolált patkány gyomrával végzett kezdeti kísérletekből, amelyek a GIP lehetséges közvetlen hatását sugallták a ghrelin szekréciójára (27). Ezenkívül a leíró asszociációs vizsgálatok azt mutatják, hogy az étkezés utáni ghrelin koncentrációk fordítottan korrelálnak az étkezés utáni GIP koncentrációkkal egészséges alanyokban (6). Ezek és más adatok azt sugallják, hogy a GIP érdekes jelölt az étkezés utáni ghrelin szekréciót szabályozó molekuláris intermedier számára: 1) A GIP a bél K-sejtjeitől a gyomortól távoli úton választódik ki a tápanyagok bevitelére reagálva, és fokozza a hasnyálmirigy inzulinszekrécióját (15); 2) az inzulinszekréció stimulálása GIP-vel csak megemelkedett glükózszint jelenlétében történik (15); és 3) A GIP-receptorok a gyomor nyálkahártyájában vannak (39, 45), a központi elhízásban pedig alacsonyan vannak szabályozva (39).
Korábban beszámolt kísérletünkben egészséges, nem elhízott egyéneknél (38) nem tudtuk bizonyítani a ghrelin szekréciójának GIP által történő csökkentett szabályozását, ami valószínűleg a rövid ideig tartó GIP infúzióval és mind a glükóz, mind az inzulin szintjének farmakológiai koncentrációival magyarázható a hiperglikémiás bilincs alatt. Ezenkívül ez a tanulmányterv nem volt képes boncolni a GIP és az inzulin potenciálisan független hatásait a ghrelin szekréciójára. Így a GIP-ghrelin kölcsönhatások egy átvilágított, de potenciálisan fontos kutatási területet jelentenek (1, 8, 27, 38).
Tekintettel arra, hogy a GIP, az inzulinhoz hasonlóan, részt vesz a szénhidrát- és zsíranyagcsere szabályozásában (15, 21, 50), a GIP és/vagy az inzulin közvetett szinergetikus és/vagy kombinatorikus hatása a plazma metabolomjának változásain keresztül befolyásolhatja a ghrelin szekrécióját. Ezenkívül a glükóz és/vagy inzulin adagolásának különböző technikáival ellentmondásos eredmények, amelyek a köztes metabolitok befolyásolásához vezetnek, és végső soron a ghrelin szekrécióra gyakorolt hatásuk (17, 18) tükrözhetik hatásuk alábecsült sokaságát. A hormon-hormon kölcsönhatások gyakran mutatják a kombinatorikus vagy/és szinergikus hatások összetett mintázatát a molekuláris információcsere sűrű hálózatában (5). Ezért metabolomikus rendszerek elemzését alkalmaztuk a ghrelin szabályozását befolyásoló új endokrin és metabolit szignál minták felkutatására.
A vizsgálat célja a GIP és a ghrelin funkcionális kapcsolatának vizsgálata volt, függetlenül a keringő vércukorszinttől és az inzulin koncentrációtól, függetlenül attól. Ennek a kérdésnek a kezelésére GIP infúziós tesztet, valamint euglikémiás és hiperglikémiás glükózbilincs-kísérleteket alkalmaztunk, kombinálva GIP vagy placebo keresztirányú infúzióval közepesen túlsúlyos férfi alanyokban. Ezenkívül a metabolikus profilok hálózati korrelációs elemzését alkalmaztuk a GIP-ghrelin kölcsönhatásokat tükröző molekuláris kapcsolatok generált adatainak tanulmányozására.
Tárgyak
Ezt a tanulmányt a németországi Brandenburgi Etikai Bizottság hagyta jóvá. AS 2 (a)/2005]. A vizsgálat előtt minden egyén írásos beleegyezését adta. Ezt a tanulmányt előzetesen regisztrálták a www.cliniccaltrials.gov webhelyen (NCT00774488).
Tizennégy túlsúlyos férfi önkéntest vizsgáltak (életkor 47,4 ± 8,4 év, BMI 32,5 ± 2,2 kg/m 2, derék-csípő arány 1,0 ± 0,1, zsírtömeg 31,6 ± 5,4 kg, sovány súly 67,5 ± 3,2 kg, éhomi vércukorszint 4,9 ± 0,4 mmol/l). Azokat az alanyokat kizártuk, akiknél a májenzimszintek meghaladták a normál felső határérték kétszeresét vagy a szérum kreatinin koncentrációja megemelkedett (> 1,3 mg/dl). Az önkéntesek egyike sem mutatott anyagcsere-betegség vagy glükóz-intolerancia bizonyítékát 75 g-os orális glükózterhelés esetén (11), és mindegyikük legalább 12 hónap alatt stabil testtömegről számolt be. A résztvevők egyike sem vett részt semmilyen releváns edzésprogramban. Az összes résztvevő, egy tantárgy kivételével, nemdohányzó volt. Az alanyokat arra utasították, hogy tartsák fenn normális fizikai aktivitásukat és fogyasszanak ~ 200 g szénhidrátot tartalmazó normál étrendet a vizsgálat előtt 3 napig és 14 napig a vizsgálat alatt.
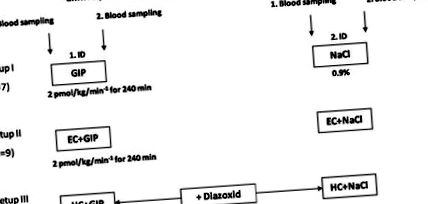
Dizájnt tanulni
1. ábra.A tanulmány megtervezése. Tizennégy mérsékelten elhízott alanyot négy alkalommal vizsgáltak, és minden alkalommal 6 különböző állapot közül 1-nek tették ki őket: glükagon-szerű peptid-1-vel (GIP, 2,0 pmol · kg –1 · min –1) vagy placebóval infundálva, éhomi állapotban, euglikémiás hiperinzulinémiás bilincsek (EC; vércukor-koncentráció 4,4 mmol/l) vagy hiperglikémiás hiperinsulinulin-bilincsek (HC; vércukor-koncentráció 7,8 mmol/l) alatt.
Peptidek
A szintetikus GIP-t a PolyPeptide Laboratories-tól (Wolfenbüttel, Németország) vásároltuk, és intravénás infúzióhoz dolgoztuk fel a leírtak szerint (30). Valamennyi alanynál ugyanabból a tételből (F-0818X2) származó GIP-t alkalmaztunk.
Kísérleti eljárások
Minden vizsgálatot reggel végeztek egyéjszakás éhgyomorra (> 10 órával az utolsó étkezés után). Két alkarvénát kanülökkel átszúrtak, és 0,9% -os fiziológiás sóoldattal (a vérmintavételhez, illetve a glükóz-, inzulin- és peptidadagoláshoz) szabadalmat tartottak. Mindkét füllebenyt hiperémiássá tettük a Finalgon (Nonivamid 4 mg/g, Nicoboxil 25 mg/g) alkalmazásával. Valamennyi bilincshez humán inzulint (Actrapid; Novo Nordisk, Bagsværd, Dánia) és glükózt (Serag Wiessner, Naila, Németország) használtunk. A kísérletek során placebót (0,9% NaCl, Fresenius, Németország) vagy GIP-t adtak 2,0 pmol · kg –1 · min –1 infúziós sebességgel folyamatos intravénás infúzióként 240 percig. Az összes tesztet 240 percig végeztük. Valamennyi vizsgálatban a vénás vérmintákat −70, 0, 60, 120, 180, 210, 220, 230 és 240 percnél vettük az infúzió kezdetéhez viszonyítva.
Az euglikémiás hiperinsulinémiás szorító kísérletekben (16) a teszt 0 percében folyamatos intravénás infúziós infúziót indítottak sóoldattal vagy GIP infúzióval kombinálva. A bilincs egyensúlyi állapotában a kapilláris vércukorszintet 4,4 mmol/l-re állítottuk be legalább 80 percig. A bilincs alatt 5 percenként monitoroztuk a plazma glükózkoncentrációkat, és a plazma glükózszabályozására használtuk a változó glükózinfúzió beállításával. Az egyetlen kapilláris glükózkoncentráció 10% -ot meghaladó eltérését feltételezett egyensúlyi állapotban nem stabil állapotnak határoztuk meg.
A 7,8 mmol/l egyensúlyi állapotú kapilláris plazma glükózkoncentrációt célzó hiperinzulinémiás hiperglikémiás clamp kísérleteket 20% glükóz bolus injekcióval [bolus glükóz = testtömeg (kg) × 0,3 g glükóz] 0 perc múlva injektálva kezdtük el, és fenntartottuk. az 5 percenként elvégzett glükóz-meghatározások alapján, adott esetben glükóz (20% vízben) beadásával. Az exogén hiperinzulinémiát 40 mU · m – 2 · min –1 humán inzulin folyamatos infúziójával 240 percig elértük, hogy összehasonlítható keringő inzulin koncentrációkat kapjunk, mind a placebo, mind a GIP infúzióval. Az endogén inzulinszekréció elnyomásához a kísérletek során kétszer (-60 perc és 120 perc) 150 mg diazoxidot (Proglycem, Schering, Németország) adtak. A diazoxid egy KATP csatornanyitó, amely a β-sejtek hiperpolarizálásával elnyomja az inzulin szekrécióját (13). A szomatosztatin, amelyet általában az endogén inzulintermelés elnyomására használnak, önmagában gátolja a ghrelin szekrécióját (18), és beavatkozott volna kísérleteinkbe.
Analitikai eljárások
Az összes vénás vérmintát azonnal centrifugáltuk és -70 ° C-on lefagyasztottuk, amíg elemzésre nem került. A kapilláris vércukor-koncentrációkat glükóz-oxidáz módszerrel határoztuk meg Dr. Müller glükózanalizátoron (Freital, Németország). A szérum inzulint és a C-peptidet kereskedelmi enzimmel kapcsolt immunszorbens vizsgálattal (Insulin ELISA, C-Peptide ELISA, Mercodia, Uppsala, Svédország) mértük. Az emberi plazma grelint egy kereskedelmi célú radioimmun vizsgálattal (Phoenix Pharmaceuticals, Belmont, CA) mértük, amely 125 I-vel jelölt bioaktív grelint használ nyomjelző molekulaként, és nyulakban tenyésztett poliklonális antitestet a teljes hosszúságú oktanoilezett humán ghrelin ellen [vizsgálaton belüli variációs koefficiens (CV) 4%]. Nem jelentettek keresztreaktivitást emberi szekretinnel, emberi vazoaktív bélpeptiddel, humán galaninnal, humán GHRH-val, NPY-vel vagy más releváns molekulákkal (34). A teljes GIP koncentrációját aprotinint tartalmazó plazmamintákban (Trasylol, Bayer-Germany, a proteázok gátlásához) határoztuk meg humán GIP (Total) ELISA Kit (Linco Research) alkalmazásával. Az érzékenység 8,2 pg/ml, a vizsgálaton belüli CV 3,0–8,8%, és a vizsgálatok közötti CV 1,8–6,1%.
Számítások, statisztikai és hálózati elemzések
Az összes statisztikai elemzést az SPSS for Windows 16.0 (SPSS, Chicago, IL) alkalmazásával végeztük. Az adatokat átlag ± SE értékként adjuk meg. A két egymást követő kiindulási minta átlagát kiszámítottuk (−70 és 0 perc) az alapszint egyéni variációjának csökkentése érdekében. A stabil állapotú hormonkoncentrációkat a 210-, a 220-, a 230- és a 240-perces értékek átlagaként számoltuk. A vizsgált hormonparaméterek ferde eloszlása miatt nem paraméteres teszteket alkalmaztunk. A csoportok közötti összehasonlításokat a Mann-Whitney alkalmazásával végeztük U-teszt és a csoportokon belül összehasonlítás Wilcoxon aláírt rangtesztjével. A különbségeket statisztikailag szignifikánsnak tekintették P
2. ábra.A szérum összes ghrelin-koncentrációjának változása (az átlagérték 210–240 perc)% -ban az egyes kísérletek alapszintjére: GIP infúzió (GIP-inf), NaCl infúzió (NaCl-inf), hiperinzulinémiás euglikémiás bilincsek NaCl-val (EC + NaCl) és GIP infúzió (EC + GIP); hiperinzulinémiás hiperglikémiás bilincsek NaCl-val (HC + NaCl) és GIP infúzióval (HC + GIP). Szürke oszlopok, kísérletek NaCl infúzióval; kikelt oszlopok, kísérletek GIP infúzióval (2,0 pmol · kg -1 -1 perc -1 infúziós sebességgel). Az adatokat box-and-whiskers-grafikonok mutatják. A doboz a 25–75% ile-ig terjed, a mediánban egy vonal 50% ile-t jelöl. A bajusz olyan tartományokat képvisel, amelyek a legalacsonyabbtól a legnagyobb értékig terjednek. *P
Hiperinzulinémiás euglikémiás clamp tesztek.
Ezekben a kísérletekben az egyensúlyi állapotú glükózkoncentráció és a szérum inzulinkoncentráció nem különbözött a GIP és a NaCl infúzióval végzett tesztek között (szérum inzulin: 398,4 ± 88,2 vs. 379,8 ± 75,0 pmol/l, ill., P = 0,26). Az infúzió során a GIP plazmakoncentráció 123,13 ± 12,48 pmol/ml volt, és szignifikánsan magasabb, mint a sóoldat infúziója (5,07 ± 1,02 pmol/l, P
1. táblázat: A plazma metabolitok korreláltak a ghrelinnel az egyes kísérlettípusok során
A Pearson-korrelációs együtthatók árnyékolva vannak a korrelációs együtthatók 2 szignifikancia szintjére P
3. ábra.A ghrelin bevonása a GIP-függő hormon-metabolit hálózatba 3 kísérlet adatainak ötvözésével: GIP infúziós teszt, hiperinsulinémiás euglikémiás bilincsek GIP-vel és hiperinsulinémiás hiperglikémiás bilincsek GIP-vel. A ghrelintől való hierarchikus távolság színkódja: a közvetlen csatlakozók zöldek voltak, a következő rendelések csatlakozói sárgaek, majd pirosak. Az összehangolt változásokat folytonos vonallal mutatjuk be; a kontraordinált változások törött vonallal jelennek meg.
4. ábra.A különböző kísérleti hálózatokban a hormonokkal és metabolitokkal való ghrelin-kapcsolatok teljes száma. Az összefüggések számát a korrelációs együtthatók 2 szignifikancia szintjére adjuk meg: P
Itt mutatunk be új adatokat, amelyek azt mutatják, hogy a GIP elnyomta a keringő ghrelint az inzulinhatásoktól függetlenül a hiperglikémiás bilincsben. Ezt alátámasztotta a ghrelin megfigyelt kifejezett szerepe a hormon-metabolit hálózatban a hosszú láncú zsírsavak együttesének koordinált változásain keresztül. Hiperinzulinémiás euglikémiában a GIP hatása a keringő ghrelinre csekély, de statisztikailag szignifikáns volt, ami arra utal, hogy a ghrelin szekréciójának szuppressziója a GIP inzulininotrop hatásához hasonlóan hiperglikémiás állapotokat igényel. Ezzel szemben a GIP nem volt hatással a ghrelin szint keringésére éhomi körülmények között.
A GIP képessége a ghrelin szekréciójának elnyomására meglepő volt, mivel ez a GIP közvetett szuppresszív hatását jelzi az étvágyra és az étkezési viselkedésre. 13 évvel ezelőtt feltételezték, hogy a GIP részt vehet az étvágyszabályozásban (25). A GIP, de nem a GLP-1, gyorsan növekedett az intraduodenális glükóz infúzió után, és az éhség, az energiafogyasztás és a teljesség növekedését figyelték meg. Érdekes módon az oktreotid koinfúziója elnyomta az inkretinek szekrécióját és az éhségérzet megfordulásához vezetett (25). Későbbi vizsgálatok hasonló tervezéssel (9, 36) kimutatták a ghrelin dózisfüggő szuppresszióját intraduodenális glükóz alkalmazásakor. Ez a hatás nem függött össze az inzulin vagy a glükóz koncentrációjának emelkedésével. A közvetlen intravénás GIP alkalmazással végzett vizsgálatok azonban ellentmondásos eredményeket mutattak az étvágyszabályozással kapcsolatban (4, 10, 46).
Fontos megjegyezni, hogy a metabolitok kimutatását ebben a vizsgálatban szemikvantitatív módszerrel végeztük, és hogy a zsírsavkészletekben megfigyelt változások eredményei kvantitatív módszerrel további replikációt igényelnek.
Jelen tanulmányban a ghrelin legnagyobb mértékű csökkenését a GIP infúzió alatt figyelték meg hiperglikémiás hiperinsulinémiás bilincs alatt. Az inzulinszint tehát valamivel magasabb volt GIP jelenlétében, bár ez statisztikailag nem volt szignifikáns. Mivel azonban a jelentősen megemelkedett inzulinszint csak kis mértékben csökkentette a ghrelin mennyiségét euglikémiás körülmények között, valószínűtlen, hogy az inzulinszintbeli különbség a ghrelinszint különbségét okozza. Egészséges, nem elhízott egyéneken végzett korábbi kísérleti tanulmányunkban (38) nem tudtuk kimutatni a ghrelin szekréciójának GIP által történő csökkentett szabályozását. A korábban publikált tanulmányok és a jelen tanulmány között azonban módszertani különbségek lehetnek. Első vizsgálatunkban (38) a hiperglikémiás clamp során magasabb glükóz- és inzulinkoncentrációt értek el, és GIP infúziót adtak 1 órán át, majd arginin infúziót. Tekintettel a tipikus ghrelin szekréciós mintázatra, amely étkezés után 60 és 120 perccel csökken (44), az előző vizsgálatunk infúziós protokollja valószínűleg túl rövid volt ahhoz, hogy megfigyeljük a GIP hatását a ghrelinre.
Összefoglalva, a jelen tanulmány eredményei azt mutatják, hogy a GIP az inzulintól függetlenül elnyomja a keringő teljes ghrelin szintet. Ezt a feltételezést integratív hormon-metabolit hálózat elemzések támasztották alá, amelyek összehangolt változásokat mutattak ki a hosszú láncú zsírsavkészletben. A GIP és a ghrelin gasztrointesztinális hormonok kölcsönös interakciója befolyásolhatja a bélből az agyba jutó szaturációs jeleket, és az éhségérzet és az étvágy elnyomásához vezethet.
A tanulmányt a német szövetségi oktatási és kutatási minisztérium támogatásával (0313042C. Sz. Támogatás NN Rudovich és Ö. Gögebakan számára), valamint a Német Tudományos Alap támogatásával (DFG. 164/021002. Sz. Támogatás NN Rudovich, Ö. Gögebakan és AFH Pfeiffer). Az adatok egy részét bemutatták az Európai Endokrinológiai Kongresszus 2010-ben Prágában.
A szerző (k) nem jelentenek be pénzügyi vagy egyéb összeférhetetlenséget.
- A székrekedéshez szükséges olívaolaj funkcionális táplálkozási válaszok
- Omega-3 funkcionális ételek zsírsavak gabonafélékben és még sok másban
- Nicole Kidman felfedi az egészséges étrendet és a testmozgást, hogy megőrizze a hihetetlen alakot
- Nicole Scherzinger a mértékletességről szól, mivel furcsán normális étel- és edzéstervet tár fel -
- Nicole Richie vékonyabb keretet mutat be, miután állítólag „napraforgómag, zeller étrendjén éltek,