Atrófiás gyomorhurut
Az atrófiás gyomorhurut foltos elváltozás, és mintavételi hibával kimaradhat, ha nem elegendő szövetet kapunk több helyről.47,50,53 Ez különösen fontos kérdés azokban a populációkban, ahol magas a H. pylori fertőzés és a gyomorrák aránya.
Kapcsolódó kifejezések:
- B12-vitamin
- Neoplazma
- Bél Metaplasia
- Belső tényező
- Kobalamin
- Gyomorhurut
- Pernicious vérszegénység
- Gyomorrák
- Cianokobalamin-hiány
Letöltés PDF formátumban
Erről az oldalról
Atrófiás gyomorhurut
Diagnózis
Az atrófiás gyomorhurutot általában az endoszkópia során kapott gyomorbiopsziás minták mikroszkópos értékelésével diagnosztizálják. A biopsziás mintavétel nélküli endoszkópia nem elegendő az atrófiás gastritis diagnosztizálásához vagy kizárásához. A csökkent bazális és stimulált gyomorsavmennyiség bemutatása alátámaszthatja az atrófiás gyomorhurut diagnózisát, de ezt a tesztet rutinszerűen nem alkalmazzák. A szérum pepszinogén- és gasztrinszint szintén segíthet az atrófiás gasztritisz diagnosztizálásában, különösen a populáció szűrése céljából. A krónikus aktív gyomorhurut diagnózisa ezután általában a H. pylori pozitív szerológiáján alapul, az atrófiás gyomorhurut diagnózisa pedig a megnövekedett szérum gasztrinszint és csökkent szérum pepszinogén szint kombinációján, különösen a szérum pepszinogén I csökkenésén alapul./pepszinogén II arány.
Az epithelia szövettani meghatározása és diagnózisa a nyelőcsőben és a proximális gyomorban
Parakrama T. Chandrasoma, GERD-ben, 2018
6.4 Krónikus atrófiás gasztritisz versus szívhám bélmetapláziával és anélkül
A CAG gyakori rendellenesség, változó földrajzi eloszlással. Autoimmun gastritis vagy sokkal gyakrabban a H. pylori fertőzés következménye. A H. pylori fertőzés viszonylag ritka a nyugati világ tehetős kaukázusi populációiban. A krónikus atrófiás gastritis rendkívül gyakori azokban a populációkban, ahol a H. pylori fertőzés elterjedt, például Kelet-Ázsia országaiban.
Fordított összefüggés van a GERD és a H. pylori fertőzés prevalenciája között a különböző populációkban. Ez nagy eltérést jelent a nyelőcső Észak-Amerikában és Európában túlsúlyban lévő adenokarcinóma és az Ázsiában túlsúlyban lévő gyomor adenokarcinóma előfordulásában.
Az autoimmun gastritis által okozott CAG elsősorban a parietális sejtet tartalmazza, amely a gyomor hámját tartalmazza, vagyis az antrumhoz közeli. Ezzel szemben a H. pylori előnyösen megfertőzi az antrumot, és antral gastritist eredményez. A betegség súlyosságának növekedésével a proximális gyomorba is kiterjedhet, ami pangastritist eredményezhet (4.45. Ábra).
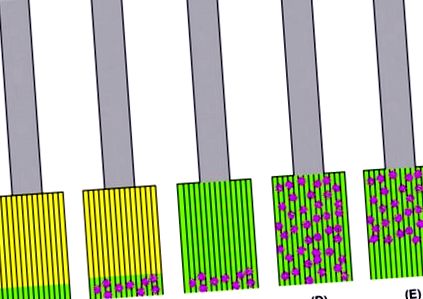
4.45. Ábra. A krónikus gyomorhurut különböző mintáinak vázlatos ábrázolása. (A) krónikus antrális gastritis (zöld) atrófia vagy bélmetaplázia nélkül; a test normális (sárga). (B) krónikus atrófiás antrális gastritis bélmetapláziával (lila pontok); a test normális. (C) Krónikus pangastritis atrófiával és bélmetapláziával, amely csak antrumot érint. (D) Krónikus atrófiás pangastritis az egész gyomrot érintő bélmetapláziával. (E) Krónikus pangastritis atrófiával és bélmetapláziával, amely megkíméli az antrumot. Az itt bemutatott összes esetben a nyelőcső nem érintett (szürke laphám epitélium metaplasztikus oszlopos hám nélkül).
Ha oszlopos metaplasztikus hám van jelen a disztális nyelőcsőben, a H. pylori kiterjedhet benne, ami megnöveli a krónikus gyulladás súlyosságát és az aktív gyulladás jelenlétét. 27 A H. pylori nem fertőzi a nyelőcső laphámját, és nem okozza a nyelőcső oszlopos metapláziáját.
A CAG-ban a mirigyek parietális sejtjeinek progresszív elvesztése krónikus gyulladással jár. A mirigyek rövidebbé válnak, a nyálkahártya vékonyabbá válik. Gyakran előfordul a foveolaris régió hiperpláziája. Az atrófiás mirigyek vagy eltűnnek, vagy metaplázián mennek keresztül a parietalis sejtek nyálkahártya-sejtekkel (pseudopyloric metaplasia; 4.46. Ábra) vagy serlegsejtekkel (IM; 4.47. Ábra) történő helyettesítésével. A mirigyek részleges atrófiájában a nyálkahártya-sejtek ritkán élhetnek együtt a maradék parietális sejtekkel egy egyedi foveoláris-mirigy komplexben.
4.46. Ábra. A gyomortest biopsziája krónikus gyomorhurutot mutat, atrófiával (parietális sejtek elvesztése) és pszeudopilorikus metapláziával. Nincs bélmetaplázia. Ez hasonlít a szív hámjára.
4.47. Ábra. A gyomor testének biopsziája krónikus gyomorhurutot mutat, atrófiával (parietális sejtek elvesztése) és bélmetapláziával. Ez hasonlít a szív hámjára és a bél metapláziájával.
Ennek eredményeként a GOE átalakul oszlopos hámrá, amely csak nyálkahártya-sejtekből áll (ami hasonlít a szív hámjához), nyálkahártya és parietális sejtek keverékéből (amely oxyntokardiális hámra hasonlít) vagy nyálkahártya és serleg sejtek keverékévé (amely a szív hámjához hasonlít az IM-mel). ).
Világosan meg kell érteni, hogy bár ezek az epitheliák hasonlíthatnak egymásra, teljesen különböznek egymástól. A CAG-ból eredő hám a GOE patológiás változásai, amelyek nem kapcsolódnak a GERD-hez. A szívhám IM-vel és anélkül, valamint az oxyntocardialis epithelium a nyelőcső pikkelyes epiteliumának GERD-indukálta oszlopos metapláziájának eredménye.
Amikor ezeket az epitheliákat az endoszkóposan látható CLE-ből vett biopsziákban találjuk, nincs nehézség (4.4. Táblázat). A megfigyelt hámtípusok a három olyan típusúak lesznek, amelyekről ismert, hogy tartalmazzák a CLE-t (szívhám IM-vel és anélkül, valamint oxyntocardialis hám).
4.4. Táblázat A bélmetaplazia jelenlétének differenciáldiagnosztikája a gasztroezofagealis csomópont régiójából vett biopsziában. A proximális és distalis intesztinális metaplazia alkalmazása a differenciáldiagnózisban
| LSBE | +; CLE> 3 cm | ± | - |
| SSBE | +; CLE 4.4. Táblázat). |
Az egyetlen problematikus és fontos helyzet az, amikor a betegeknél egyetlen biopsziát végeznek az SCJ-nél a CLE endoszkópos bizonyítékai nélkül. Ilyen esetben nehéz lehet megkülönböztetni a metaplasztikus nyelőcső oszlopos hámot, amelynek IM-je a DDE-re korlátozódik, az atrófiás pangastritistól, amelynek IM-je a GOE-ben a GEJ-ig terjed.
Ezt a problémát úgy lehet legegyszerűbben megoldani, hogy a DDE mellett a testből és az antrumból rutinszerűen veszünk biopsziákat (4.4. Táblázat). Ha a disztális gyomorbiopsziák normálisak, a szív hámjának megtalálása (parietális és/vagy serlegsejtekkel vagy anélkül) a GERD által kiváltott metaplasztikus nyelőcső oszlopos hámot jelzi. A CAG nem fordul elő elszigetelt jelenségként, amely a gyomor legközelebbi néhány centiméterére korlátozódik.
Amikor a szív hámját (parietális és/vagy serlegsejtekkel és anélkül) megtalálják a GEJ-től vett biopsziában egy endoszkóposan normális, CAG-ban szenvedő betegnél a disztális gyomorbiopsziákban, a diagnózis problémát jelent. A jellemzők átfedik egymást a CAG és a metaplasztikus nyelőcső oszlopos epitheliák között.
A metaplasztikus nyelőcső oszlopos epitheliában a következő differenciális jellemzők hasznosak a CAG megkülönböztetésében: (1) A felületi hám metaplasztikus nyelőcső oszlopos epitheliában gyakran villiform és CAG-ban lapos. (2) A többrétegű hám és a mirigycsatornák jelenléte metaplasztikus nyelőcső oszlopos hámokat jelez. Ezeket a gyomor oxyntikus nyálkahártyája nem látja. (3) A hasnyálmirigy metapláziáját gyakrabban észlelik a metaplasztikus nyelőcső oszlopos epitheliában, mint a CAG-ban. (4) A Paneth sejtek gyakoribbak a CAG-ban. (5) A neuroendokrin sejtek hiperpláziája kedvez a CAG-nak. Hasznos lehet a szinaptofizin festése. (6) A reaktív foveoláris hiperplázia, a muscularis mucosae izomrostjainak szabálytalan kiterjedésével a felületes epitheliumban, gyakoribb a metaplasztikus nyelőcső oszlopos epitheliában. (7) A neutrofilek ritkák a CLE-ben aktív H. pylori fertőzés vagy erózió nélkül. Ezen jellemzők egyike sem végleges.
Immunoperoxidáz festéssel megkísérelték megkülönböztetni a szív hámját és a CAG-t IM-vel. A DAS-1 monoklonális antitest pozitívnak bizonyult a szív epitheliumában előforduló IM-ben, a CAG-ban a gyomor IM-ben nem. 36 A beszámolók szerint a CK7 és 20 festési mintázata eltér. 37 A szívhám IM-vel a felületre korlátozott CK20-festést és a felszíni és mély mirigyekben egyaránt CK7-festést mutat. Ez ellentétben áll az IM-vel végzett CAG-mal, ahol teljes vastagságú festés történik CK20-mal és foltos festés CK7-vel. Ezek mind nem megbízhatóak, és általában elhagyták őket.
Ugyancsak elhagyták az IM teljes és hiányos differenciálását a magas vas-diamin foltos festési minták alapján, mint a szív hámjának az IM-vel történő megkülönböztetésének módszerét a CAG-tól. A látható CLE-ben lévő IM-vel rendelkező szívhám szinte mindig hiányos. A CAG gyomor-bél hámja lehet teljes vagy hiányos.
Kivéve azokat a ritka eseteket, amikor a nyelőcső elhelyezkedésének specifikus kritériumai vannak (lásd alább), nem próbálok krónikus atrófiás pangastritisben szenvedő betegnél a mikroszkópos CLE-t diagnosztizálni a junkcionális régióból származó biopsziában. Lehetséges, hogy hiányolunk egy ritka esetet, amikor a gasztritisz mellett egyidejűleg mikroszkópos CLE-t találunk. Ebben a helyzetben a diagnózis érzékenységét részesítjük előnyben.
Kiegészítés: Fejlett országok
Folsav
Az atrófiás gyomorhurut nagymértékben csökkenti az idős emberek folátfelszívó képességét. Ezt a problémát kijavíthatjuk folsav híg sósavval történő beadásával a gyomor savasságának növelése és ezáltal az abszorpció növelése érdekében. Aggodalomra ad okot azonban annak lehetősége, hogy a kiegészítő folsav elfedheti a B 12 -vitamin hiányának jeleit. A folsav orvosolhatja a vérszegénységet, amely a B12-vitamin hiányából következik be, a legfontosabb diagnosztikai jel. Nem tudja azonban kijavítani a tartós idegkárosodást, amely akkor lehetséges, ha a B12-vitamin hiányát nem kezelik. A kiegészítő folsav bevitele nem lehet nagyobb, mint 1000 μg naponta –1, hogy megakadályozza a B12-vitaminhiány jeleinek leplezését.
Emésztőrendszer (nyelőcső, gyomor, kis intesztin, vastagbél, végbél, végbél, epeutak)
Atrófiás gyomorhurut
A krónikus atrófiás gasztritisz a fundamentális nyálkahártya szekréciós elemeinek fokozatos megsemmisülésére utal a limfociták és a plazmasejtek behatolása révén. 111 Ennek eredményeként a normálnál vékonyabb nyálkahártya keletkezik, amelyet főleg nyálkaszekréciós sejtek foglalnak el. E pusztító változások következtében a sósav termelése jelentősen csökken. Sok betegnél keringő autoantitestek vannak, és feltételezhető, hogy egyes személyekben az atrófiás gyomorhurut autoimmun rendellenesség. Néhány beteg szintén káros vérszegénységben szenved. A bélmetaplázia mikroszkópos változásai gyakran kísérik az atrófiát és a gyulladást. Az endoszkópos megjelenés csak akkor jellemző, ha kifejezett nyálkahártya atrófia van. Ebben az esetben a normális rugalmas minta lapos lehet, és látható szubmukózális erekkel társulhat. Az atrófiás gyomorhurutban szenvedő betegek statisztikailag megnövekedett kockázattal járnak a gyomor adenokarcinóma kialakulásában. Úgy tűnik, hogy ez a folyamat a mirigy dysplasia révén fejlődik ki. 137
B12-vitamin és kognitív károsodás
Eileen M. Moore PhD. Alastair G. Mander MBBS, Dieta és táplálkozás a demenciában és a kognitív hanyatlásban, 2015
Összefoglaló pontok
Alacsony savasság, atrófiás gyomorhurut és káros anaemia a B12-vitamin hiányát okozza, és az időseknél gyakrabban fordul elő.
Kognitívan ép személyeknél és demens betegeknél végzett megfigyelési vizsgálatok bizonyítékot szolgáltatnak a kognitív károsodás és az alacsony B12-vitamin szint közötti összefüggésre.
Klinikai vizsgálatok során a B12-vitamin pótlása csak azoknál javítja a megismerést, akiknek hiányos a B12-vitamin.
A B12-vitamin pótlása nem javítja a kognitív funkciókat kognitívan intakt idősebb felnőtteknél vagy demenciában szenvedő betegeknél, akik megfelelő B12-vitamin-szinttel rendelkeznek.
A B12-vitamin szintjének középkorú javítása megakadályozhatja, csökkentheti a kognitív károsodás súlyosságát, vagy késleltetheti a kognitív károsodás kialakulását, de hosszú évekig követett, nagy kohorszú jövőbeni prospektív vizsgálatokra van szükség annak értékeléséhez, hogy az ilyen potenciális előnyök valósak-e.
Emésztőrendszeri és hasnyálmirigy-rendellenességek
Professzor Crispian Scully, CBE, PhD, MDS, MRCS, FDSRCS, FDSRCPS, FFDRCSI, FDSRCSE, FRCPath, FMedSci, FHEA, FUCL, FBS, DSc, DChD, DMed (HC), Dr (hc), Scully fogorvosi problémáiban (Hetedik kiadás), 2014
Diéta (füstölt ételek, sózott hal és hús, valamint savanyú zöldségek; a nitrátok és a nitritek általában a pácolt húsokban találhatók)
Genetikai hatások (a carcinoma gyakori a japánokban, és ahol az első fokú rokonok pozitív történettel rendelkeznek). Az E-kadherin/CDH1 gén felelős. Az örökletes, nem polipózisos vastagbélrák (HNPCC; Lynch-szindróma) és a családi adenomatózus polipózis (FAP) genetikai rendellenességek, amelyeknél a vastagbélrák kockázata jelentősen megnő, a gyomorrák pedig kissé megnő. A BRCA1 és a BRCA2 örökletes emlőrák génjeinek mutációi esetén a gyomorrák aránya is magasabb lehet
Ménétrier-betegség (hipertrófiás gasztropátia)
Foglalkozások - a szén-, fém- és gumiipar dolgozói
- Atherogén étrend - áttekintés a ScienceDirect témákról
- Akut gégegyulladás - áttekintés a ScienceDirect témákról
- Savasság - áttekintés a ScienceDirect témákról
- Testtömeg-index - áttekintés a ScienceDirect témákról
- Autoimmun pajzsmirigy-gyulladás - áttekintés a ScienceDirect témákról