Autoimmun pajzsmirigy-gyulladás
Az azonos fajú tiroglobulinnal végzett immunizálást követő autoimmun pajzsmirigy-gyulladást a csirke (26) és a patkány (11) újszülött timektómiája is megakadályozza.
Kapcsolódó kifejezések:
- Graves-kór
- Autoimmunitás
- T sejtek
- Pajzsmirigy-gyulladás
- Jód
- Monospecifikus antitest
- Autoimmun betegség
- Szisztémás lupus erythematosus
- Allele
Letöltés PDF formátumban
Erről az oldalról
Fiziológia és immunrendszeri diszfunkció
Absztrakt
Kötet II
Genetikai tényezők
Az öröklődés szerepét az autoimmun pajzsmirigy-betegségben számos tanulmány illusztrálta, amelyek autoimmun pajzsmirigy-betegség vagy pajzsmirigy-antitestek gyakoribb előfordulását mutatták autoimmun hypothyreosisban és Graves-kórban szenvedő betegek családtagjainál. 30 Az, hogy mindkét pajzsmirigybetegség együttesen csoportosul a családokban, további támogatást nyújt ahhoz az elképzeléshez, hogy ezek a kórképek ok-okozati és patogén tulajdonságokkal rendelkeznek. Számos öröklődési és génjelölt-mintát javasoltak, de a megállapítási artefaktumok és a genetikai asszociációs vizsgálatok hátrányai sok következetlenséget eredményeztek az eredményekben. Az aprólékos ikertanulmányok csak 22% -os konkordancia arányt mutattak ki Graves-kórra nézve - jóval alacsonyabb, mint azt korábban gondolták. 65
A legfontosabb érzékenységi tényező, amelyet eddig felismertek, az egyes HLA-DR allélekkel való kapcsolat; az ezen MHC II. osztályú gének szerepe az immunválaszban kiváló jelölté teszi őket. 66 A HLA-DR3 fehéreknél Graves-kórhoz és Hashimoto pajzsmirigy-gyulladásához kapcsolódik, és relatív kockázatot jelent 2 és 6 között, míg a HLA-DR4 és a HLA-DR5 egyes fehér populációkban golyva, de nem atrófiás pajzsmirigy-gyulladással társult. 67 A szülés utáni pajzsmirigy-gyulladás csak gyengén kapcsolódik a HLA-DR5-hez. Meg kell jegyezni, hogy a nem fehér populációk HLA asszociációi nagyon eltérőek. 68
Fertőzés és autoimmun pajzsmirigy betegségek
Sara Salehi Hammerstad,. Yaron Tomer, Fertőzés és autoimmunitás (második kiadás), 2015
1. Bemutatkozás
Az autoimmun pajzsmirigy betegségek (AITD) számos olyan állapotot foglalnak magukban, amelyek közös sejt- és humorális immunválaszokat mutatnak a pajzsmirigyre. Az AITD-k főként a Graves-kórt (GD) és a Hashimoto-féle pajzsmirigy-gyulladást (HT) tartalmazzák, amelyek mind a pajzsmirigy beszivárgását jelentik a pajzsmirigy antigénjeivel reagáló T- és B-sejtek által, amelyek pajzsmirigy autoantitesteket termelnek, ennek eredményeként a hyperthyreosis a GD-ben és a hypothyreosisban következik be. HT-ben (áttekintve az 1., 2. hivatkozásban). Míg a pajzsmirigyre adott immunválasz etiológiája továbbra sem ismert, a jelenlegi paradigma az, hogy az AITD komplex betegségek, amelyekben az érzékenységi gének és a környezeti kiváltó tényezők együttesen hatnak a pajzsmirigyre adott autoimmun válaszra. Ebben az áttekintésben egy környezeti tényező - a fertőzés - hozzájárulását vizsgáljuk az AITD-k patogenezisében. Megvizsgáljuk a fertőző organizmusok AITD-k kialakulásában betöltött szerepével kapcsolatos releváns adatokat, különös hangsúlyt fektetve azokra a mechanizmusokra, amelyekkel a fertőzés kiválthatja az AITD-ket.
NOD.H-2h4 egerek
Helen Braley-Mullen, Shiguang Yu, az immunológia fejlődésében, 2015
2.3 T-sejtek, mint effektor sejtek a SAT-ban
Pajzsmirigy rendellenességek
Az autoimmun pajzsmirigy betegség genetikai alapjai
Autoimmun pajzsmirigybetegség (AITD) érzékenységi géneket azonosítottak. Ezek immunmoduláló génekre és pajzsmirigy-specifikus génekre oszthatók.
Az autoimmun poliglanduláris szindrómák (APS) egy olyan betegségcsoport, amelyet több autoimmun rendellenesség kombinációjának jelenléte jellemez. Az AITD gyakran fordul elő ezeknél a betegeknél. Az APS-1 más néven autoimmun polyendocrinopathia candidiasis ectodermális dystrophia ritka monogén betegség, amelyet az autoimmun szabályozó gén mutációi okoznak. Az APS-2 a leggyakoribb APS, az Addison-kór kombinációja az AITD-vel (Hashimoto-féle pajzsmirigy-gyulladás vagy Grave-kór) vagy az 1-es típusú cukorbetegséggel, és öröklődése összetett, több lókusszal is érintett (Michels & Gottlieb, 2010).
Fertőzés és autoimmun pajzsmirigy betegségek
Yaron Tomer, Ronald Villanueva, Infekció és autoimmunitás, 2004
1. BEMUTATKOZÁS
Az autoimmun pajzsmirigybetegségek (AITD) számos olyan állapotot foglalnak magukban, amelyek közös sejt- és humorális immunválaszokkal rendelkeznek, amelyek a pajzsmirigyre irányulnak. Az AITD magában foglalja a Graves-kórt (GD) és a Hashimoto-féle pajzsmirigy-gyulladást (HT), amelyek mindegyike magában foglalja a pajzsmirigy beszivárgását a pajzsmirigy antigénjeivel reaktív T- és B-sejtek által, a pajzsmirigy autoantitestjeinek termelését, az ebből következő klinikai megnyilvánulásokkal (hyperthyreosis GD-ben és hypothyreosisban) HT-ben) (áttekintve [1, 2] -ben). Míg a pajzsmirigyre adott immunválasz etiológiája ismeretlen, a jelenlegi paradigma az, hogy az AITD összetett betegségek, amelyekben az érzékenységi gének és a környezeti kiváltó tényezők együttesen hatnak a pajzsmirigyre adott autoimmun válaszra. Ebben az áttekintésben egy környezeti tényező, nevezetesen a fertőzés hozzájárulására összpontosítunk az AITD patogenezisében. Megvizsgáljuk a fertőző organizmusok szerepét az autoimmun pajzsmirigybetegségek (AITD) kialakulásában, különös tekintettel azokra a mechanizmusokra, amelyekkel a fertőzés kiválthatja az AITD-t.
A prolaktin és az autoimmunitás mozaikja
Vânia Vieira Borba,. Yehuda Shoenfeld, az Autoimmunitás mozaikjában, 2019
Prolactin és autoimmun pajzsmirigy betegség
Az autoimmun pajzsmirigybetegségek főként két rendellenességet foglalnak magukba: Grave-kór és Hashimoto-pajzsmirigy-gyulladás. Az etiológia multifaktoriális, genetikai és környezeti tényezőket foglal magában, a nőknél nagy a túlsúly [129]. Az autoimmun pajzsmirigy betegségben szenvedő betegek 20% -ában magas prolaktinszintet találtak, és kétszer akkora volt, mint az autoimmun hypothyreosisban. Hashimoto pajzsmirigy-gyulladásában szenvedő betegek körülbelül 90% -a szignifikánsan magasabb prolaktinszintet mutatott a csökkent kortizol-titerrel együtt [130]. A dopamin-agonisták szerepét az autoimmun betegségek kezelésében még meg kell határozni.
A spontán autoimmun pajzsmirigy-gyulladással rendelkező csirkék elhízott törzse a Hashimoto-betegség modelljeként
VI Immunogenetika
A SAT egy multigén betegség. Amint azt a fentiekben tárgyaltuk, a funkcionális rendellenességek legalább négy csoportja vesz részt a fejlődésében (Kroemer és mtsai., 1989): (1) a célszerv érzékenysége az egyetlen, autoszomális, recesszív gén által kódolt autoaggresszív effektor sejtekre; (2) a T-sejtek általános hiperreaktivitása (megemelkedett proliferáció, IL-2 szekréció és IL-2R expresszió a Con A-val történő stimulálás után), amelyet egy domináns, autoszomális gén szabályoz; (3) csökkent glükokortikoid tónus a CBG megemelkedett plazmakoncentrációja miatt, amely autoszomális recesszív tulajdonságként öröklődik; (4) autoszomális domináns tulajdonság, ev22, amely együtt társul a plazma kortikoszteron hiányos növekedésével antigénre vagy GIF-injekcióra adott válaszként, például IL-1.
Kezdetben a B-lokusz haplotípust tárgyalták a SAT kimenetelét befolyásoló lehetséges lényeges tényezőként (Bacon et al., 1974, 1977, 1981). Később azonban világossá vált, hogy az MHC típus csak moduláló szerepet játszik (Bacon és Rose, 1979), mivel például magas válaszkészség (magas TgAAb titer és súlyos SAT) és alacsony válaszkészség (nincs TgAAb és alacsony SAT) alvonalak, mind a B15 homozigóta kifejleszthető (Hála, 1988).
II. Táblázat Az SAT fejlesztését befolyásoló tényezők az operációs rendszerben
| "Kőkorszak" | 1956–1970 | 7–12 hét | Szex | Kor |
| "Közép kor" | 1971–1983 | 5–10 hét | MHC | Nem MHC immunválasz gének |
| „A mai kor” | 1984– | 2–4 hét | T-sejt hiperreaktivitás, a célszerv érzékenysége (étkezési jód), környezeti hatás (vírus, baktériumok) | Glükokortikoid, tonus, IL-2 hiperprodukció, környezeti hatás (vírus, baktérium), MHC |
Pajzsmirigy
Limfocita (szülés utáni, fájdalommentes, csendes) pajzsmirigy-gyulladás
Járványtan
A limfocita pajzsmirigy-gyulladás leggyakrabban a szülés utáni nőknél fordul elő, a szülés vagy a felmondás után 2–12 hónappal a nők 6% -át érinti. Ritkán fordul elő ez az állapot nem szülés utáni nőknél vagy férfiaknál. A hajlamosító tényezők között szerepel a szülés utáni pajzsmirigy-gyulladás, az 1-es típusú diabetes mellitus és a keringő antithyroid autoantitestek korábbi története.
Pathobiology
Ez a pajzsmirigy fájdalommentes gyulladása átmeneti tirotoxikózist okozhat, amelyet átmeneti vagy tartós hypothyreosis követ. A pajzsmirigy diszfunkciójának ezen fázisai általában 2-8 hétig tartanak. Úgy gondolják, hogy ez az állapot átmeneti autoimmunitást tükröz.
Diagnózis
A lymphocytás pajzsmirigy-gyulladás diagnózisát gyakran figyelmen kívül hagyják, ha a tirotoxicosis nem specifikus tüneteit (pl. Fogyás, álmatlanság, szorongás) vagy hypothyreosisot (pl. Fáradtság, depresszió) tévesen értelmezik, mint gyakori szülés utáni panaszokat. A pajzsmirigy nem normális, vagy normál méretű, vagy szerényen megnagyobbodott. Ha megfontolják, a limfocita pajzsmirigy-gyulladás diagnózisa laboratóriumi vizsgálatokkal könnyen megerősíthető vagy kizárható, amely a tireotoxikózis fázisaiban elnyomott TSH-szintet és a hypothyreosis fázisaiban megemelkedett TSH-szintet tár fel. Ezt az állapotot meg kell különböztetni a Graves-kórtól, amely a szülés után is ugyanabban az időkeretben jelentkezhet. A T4 és T3 magasság relatív foka néha arra utalhat, hogy mely állapot fennáll; a lymphocytás pajzsmirigy-gyulladást jellemzően a T4 szint domináns növekedése jellemzi. A radiojód frakcionális felvétele vagy hiányzik, vagy nagyon alacsony a lymphocytás pajzsmirigy-gyulladásban, de fokozódik az aktív Graves-kórban, így hasznos diagnosztikai tesztet nyújt (lásd 233-6. Táblázat).
Kezelés
A limfocita pajzsmirigy-gyulladás gyakran egyedül megnyugtatással és megfigyeléssel kezelhető. A tüneti tirotoxikózis korlátozott β-blokkoló terápiával kezelhető. A túlzott hypothyreosis átmeneti tiroxin-pótlást igényelhet.
Prognózis
Míg a legtöbb érintett beteg végül visszatér euthyroid állapotba, addig 25% -ban tartós hypothyreosis alakul ki a klasszikus autoimmun thyreoiditis miatt .
Az autoimmun betegség előrejelzése
George S. Eisenbarth,. Roberto Gianani, The Autoimmun Diseases (Ötödik kiadás), 2014
Pajzsmirigy
A hipotireózis vagy hipertireózis formájában megnyilvánuló autoimmun pajzsmirigybetegség (AIT) nagyon általános az általános populációban. A populáció körülbelül 5% -a hipotireózis és 1,3% hyperthyroid (Hollowell et al., 2002). Az AIT fokozott gyakorisággal fordul elő T1D-ben szenvedő egyéneknél (28% (Umpierrez et al., 2003)), Addison-kórban (AD) (14–21%) (Betterle és mtsai, 2002; Kasperlik-Zaluska és mtsai, 1998; Zelissen és mtsai 1995; Lendrum és mtsai, 1975), a lisztérzékenység (CD) (legfeljebb 12% (Ansaldi és mtsai, 2003)) és más autoimmun betegségek. Ezért az előrejelzés első lépése megköveteli az egyén kórtörténetének ismeretét. A pajzsmirigybetegség rutinszűrése általában ajánlott ezeknél az egyéneknél, mivel a betegség előzetes valószínűsége nagy, és a vizsgálatok viszonylag nem invazívak.
Az AIT kockázata gyengén kapcsolódik a HLA genotípusokhoz, amelyek a lakosságtól függően változnak. Santamaria és mtsai. (1994) szerint a DRB1 * 0201 növelte az AIT kockázatát a T1D-ben. Kim és mtsai. (2003) szerint a DQB1 * 0401 növelte a kockázatot a koreai cukorbetegek körében. A DQB1 * 0302 az AIT-hez társult a cseh cukorbetegek körében (Sumnik et al., 2003). A DR3 és a DR5 összefüggést mutat a pajzsmirigy autoimmunitásával német véradóknál (Boehm et al., 1993).
Az AIT-t pajzsmirigy antigének, anti-pajzsmirigy-peroxidáz (TPO) és anti-tiroglobulin (TG) antitestek kísérik (Vakeva et al., 1992). Ezek az autoantitestek az általános populáció körülbelül 10% -ában (Hollowell et al., 2002) és a hypothyreos populáció körülbelül 90% -ában pozitívak (Vakeva et al., 1992). Vanderpump és munkatársai várható nyomon követése. (1995) a Whickham-tanulmányban kimutatta, hogy a pozitív TPO autoantitestekkel és normális TSH-val rendelkező nők évente 2,1% -os rizikót mutatnak a hypothyreosis kialakulásában, a hypothyreosis általános kockázata 20 év alatt 20 év alatt.
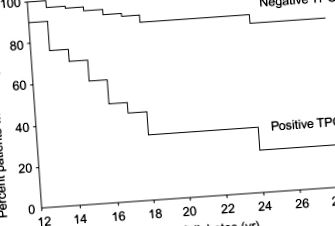
Nagy kockázatú populációkban, mint például a T1D, az AIT-re való progresszió a TPO és a TG antitestek jelenlétével függ össze, a TPO-antitestek T1D-pozitívjának körülbelül 80% -a halad AIT-re, szemben a TPO-negatív 15% -ával (Umpierrez et al., 2003) (78.6. Ábra). Megjegyzendő, hogy a negatív TPO autoantitesttel rendelkező személyek továbbra is az AIT-be fejlődtek, de sokkal alacsonyabb ütemben.
78.6. Ábra A hypothyreosis kialakulása a cukorbetegek körében a pajzsmirigy autoantitestek termelésétől függ. Azoknál a személyeknél, akik TPO-t expresszálnak, sokkal nagyobb a hypothyreosis kockázata, mint azoknál, akik nem (Umpierrez et al., 2003).
Hasonlóan a T1D-hez, amelyben a glükóz-anyagcsere rendellenességei azonosítják azokat az egyéneket, akiknél nagyobb a kockázata a klinikai cukorbetegségnek, a pajzsmirigy-anyagcsere rendellenességekkel küzdő egyéneknek fokozott a kockázata a nyilvánvaló hypothyreosis kialakulásának. Az emelkedett TSH-értékkel és normál pajzsmirigyhormonral rendelkezők 55% -a 20 évesen hypothyreosis volt, 4,3% -os éves előfordulással.
A pajzsmirigy autoimmunitásának szűrése olyan magas kockázatú populációkban, mint a T1D TPO-val és/vagy TG autoantitestekkel, szorosabb monitorozás céljából azonosíthatja az autoimmun pajzsmirigybetegség fokozott kockázatú egyéneket. A szűrés hatékonyságát nem értékelték teljes körűen.
- Atherogén étrend - áttekintés a ScienceDirect témákról
- Akut gégegyulladás - áttekintés a ScienceDirect témákról
- Savasság - áttekintés a ScienceDirect témákról
- Atrófiás gyomorhurut - áttekintés a ScienceDirect témákról
- Testtömeg-index - áttekintés a ScienceDirect témákról