A nem alkoholos zsírmáj cirrhosis: Epidemiológiájának, kockázati tényezőinek, klinikai bemutatásának, diagnózisának, kezelésének és prognózisának áttekintése
Bei Li
Gasztroenterológiai Osztály, Pekingi Tongren Kórház, Fővárosi Orvostudományi Egyetem, Peking 100730, Kína
Chuan Zhang
Gasztroenterológiai Osztály, Pekingi Tongren Kórház, Fővárosi Orvostudományi Egyetem, Peking 100730, Kína
Yu-Tao Zhan
Gasztroenterológiai Osztály, Pekingi Tongren Kórház, Fővárosi Orvostudományi Egyetem, Peking 100730, Kína
Absztrakt
A cirrhosis számos krónikus májbetegség végső stádiuma, valamint a morbiditás és a mortalitás jelentős oka. Az elhízás és a metabolikus szindróma növekvő járványával az alkoholmentes zsírmájbetegség (NAFLD) a krónikus májbetegségek leggyakoribb oka lett világszerte, és a cirrhosis egyik vezető okává válik. Elengedhetetlen a NAFLD cirrhosisának fokozott ismerete és megértése. A mai napig nem tettek közzé szisztematikus áttekintést a NAFLD cirrhosisáról. Így ez a cikk áttekinti a NAFLD cirrhosis epidemiológiájával, kockázati tényezőivel, klinikai megjelenésével, diagnózisával, kezelésével és prognózisával kapcsolatos legújabb tanulmányokat.
1. Bemutatkozás
2. Epidemiológia
Az elhízás és a metabolikus szindróma járványával a NAFLD vált a krónikus májbetegségek leggyakoribb okaivá világszerte [8]. Becslések szerint a NAFLD globális prevalenciája körülbelül 24% [9]. A cirrhosis fontos tényező a májkal kapcsolatos morbiditás és mortalitás szempontjából a NAFLD-ben szenvedő betegeknél [10]. Azonban még mindig nincs részletes megértésünk arról, hogy milyen gyakran fordul elő a NAFLD cirrhosis. A különféle vizsgálati objektumokkal, diagnosztikai módszerekkel és egyéb változó paraméterekkel meglévő vizsgálatok a NAFLD cirrhosis inkonzisztens epidemiológiai eredményeit mutatták.
2.1. Általános népességvizsgálat
Kabbany és mtsai. elemezte a Nemzeti Egészségügyi és Táplálkozási Vizsgálat (USA) 2009 és 2012 közötti adatait. A cirrhosist AST/trombocita arány index> 2> kóros májfunkciós tesztekkel diagnosztizálták. A NAFLD cirrhosist cirrhosisként határozták meg, amely az alábbiak legalább egyikével jár: elhízás, cukorbetegség, inzulinrezisztencia és metabolikus szindróma. Beszámoltak arról, hogy a NAFLD cirrhosis prevalenciája 0,178% volt [11]. Fung és mtsai. prospektív keresztmetszeti vizsgálatot végzett 2493 önkéntesből, akiket a lakosság és a Vöröskereszt transzfúziós központja toborzott Hongkongban (Kína). A cirrhost átmeneti elasztográfiával (TE) diagnosztizálták. Megállapították, hogy a NAFLD cirrhosis előfordulása 0,17% volt [12].
2.2. Betegségek vagy morbiditású betegek vizsgálata
Egy 1799, 2-es típusú cukorbetegségben (T2DM) szenvedő betegen végzett vizsgálat kimutatta, hogy a TE által diagnosztizált NAFLD cirrhosis prevalenciája 11,2% volt [13]. 29956 súlyos elhízásban szenvedő beteg 16 egyedi vizsgálatának áttekintése azt mutatta, hogy a betegek 5,8% -ának van NAFLD-cirrhózisa [8]. Ezek a tanulmányok azt sugallták, hogy a T2DM-ben vagy súlyos elhízásban szenvedő betegeknél magas a NAFLD cirrhosis előfordulási gyakorisága [14].
2.3. Cirrhosisos kórházi betegek vizsgálata
2.4. Májtranszplantált betegvizsgálatok
A skandináv májtranszplantáció egyik tanulmánya 2011 és 2015 között arról számolt be, hogy a NASH cirrhosis a májtranszplantációra felsorolt felnőtt betegek (91/1476) körülbelül 6,1% -a volt [19]. A United Network for Organ Sharing adatbázis egy másik tanulmánya azt mutatta, hogy a májtranszplantációra felsorolt összes amerikai fiatal beteg 5% -át a NASH cirrhosis okozza [20], és a NASH cirrhosis 2002-től 2016-ig 1% -ról 16% -ra nőtt. a szervbeszerzési és transzplantációs hálózat (OPTN) 2000 és 2014 közötti adatbázisa szintén támogatta a NASH cirrhosisának idővel növekvő tendenciáját, 2016 és 2030 között 55,4% -os növekedéssel [21].
3. Kockázati tényező
3.1. Szövettani altípus
A szövettani altípus a legnagyobb kockázati tényező a NAFLD cirrhosisra történő előrehaladásában. A NAFLD-t két fő szövettani altípusra osztották: az alkoholmentes zsírmájra (NAFL) és az alkoholmentes steatohepatitisre (NASH) [22]. A cirrhosis progressziójának gyakorisága magasabb a NASH-ban, mint a NAFL-ben. Egy longitudinális vizsgálat, átlagosan 15,6 éves követéssel, azt mutatta, hogy a NAFL-ben szenvedő betegek csak 1% -ában alakult ki cirrózis, míg a NASH-ban szenvedők 11% -ában cirrhosis alakult ki [23]. Sőt, a NASH gyorsabban fejlődött cirrhosisra. A NASH-ban szenvedő betegek éves fibrózis progressziós aránya 0,14 stádium volt, szemben a NAFL-ben szenvedő betegek 0,07 stádiumával [24].
3.2. Metabolikus tényezők
Számos tanulmány azt sugallta, hogy a cukorbetegség a NAFLD cirrhosisra való progressziójának legerősebb metabolikus tényezője [25]. Porepa és mtsai. Ontario (Kanada) (1994–2006) adminisztratív egészségügyi adatbázisait használta populációalapú, egyeztetett retrospektív kohorsz vizsgálat elvégzéséhez. 438 069 újonnan diagnosztizált cukorbetegségben szenvedő személyt 2 059 708 diabétesz nélküli egyénhez hasonlítottak. A medián 6,4 éves követési időtartam után 1119 (3,71%) cukorbeteg páciensnél alakult ki cirrózis, és 1896 (1,34%) cukorbetegségben szenvedő egyénnél cirrhosis [26]. Nderitu és mtsai. 509 436 résztvevőt vizsgált meg a svéd Apolipoprotein Mortality Risk (AMORIS) kohorszból 1985 és 1996 között, és megállapította, hogy 2775 résztvevőnél alakult ki cirrhosis; a cukorbetegség és a magas vércukorszint az elhízástól független cirrhosishoz kapcsolódott [27]. Egyéb metabolikus tényezők, beleértve a hiperlipidémiát, az elhízást és a magas vérnyomást, szintén fontos kockázati tényezők voltak a NAFLD cirrhosis szempontjából.
3.3. Genetikai polimorfizmusok
A genetikai tényezőkről úgy gondolják, hogy hozzájárulnak a magas prevalenciájú betegségek, például az elhízás, a T2DM, a szív- és érrendszeri betegségek (CVD) és a cirrhosis kockázatának 30–50% -ához [28]. A genom egészére kiterjedő asszociációs vizsgálatok (GWAS) és a jelölt gén vizsgálatok nagyban hozzájárultak ahhoz, hogy megértsük a genetikai hozzájárulást a NAFLD progressziójához. A GWAS-vizsgálatok azonosították a NAFLD progressziójához kapcsolódó genetikai variánsokat. Az azonosított lókuszok közül a PNPLA3-ban (rs738409 c.444 C4G, p.Ile148Met), a 3-at tartalmazó patatin-szerű foszfolipáz-doménben, a nem szinonimás egy nukleotid polimorfizmus (SNP) több páciens kohorszán is érvényesült. Nevezetesen, ennek az SNP-nek a jelenléte erőteljesen összefügg a NAFLD cirrhosis kialakulásával [29]. Egy, több mint 1000, biopsziával igazolt NAFLD-vel rendelkező személy vizsgálata kimutatta, hogy a transzmembrán 6 szupercsalád 2-es tagjának SNP-je (rs58542926 c.449 C> T, p.Glu167Lys) a nemtől, az életkortól a biopsziánál függetlenül megnövekedett kockázattal járt. BMI, T2DM és PNPLA3 rs738409 genotípus [30].
3.4. Kor
Az Egyesült Királyságból származó retrospektív kohorszvizsgálat során 351, biopsziával igazolt NAFLD-ben szenvedő beteget osztottak egy idősebb (≥60), középkorú (50-60) és egy fiatalabb (≤50) csoportba. A cirrhotikus betegek szignifikánsan idősebbek voltak, mint a nem cirrhotikus betegek. Az idősebb betegeknél lényegesen több kockázati tényező volt, beleértve a magas vérnyomást, az elhízást, a cukorbetegséget és a hiperlipidémiát [31]. Az Egyesült Államok keresztmetszeti multicentrikus vizsgálatában 796, biopsziával igazolt NAFLD-ben szenvedő beteget soroltak az idős betegek (≥65) és a nem idős betegek (18-65) csoportjába. A NAFLD-ben szenvedő idős betegeknél szignifikánsan magasabb volt az előrehaladott fibrózis aránya, mint a nem idős NAFLD-s betegeknél. Sőt, az idős betegeknél nem volt több olyan kockázati tényező, mint a cukorbetegség vagy az inzulinrezisztencia [32]. Az életkor és a cirrhosis közötti összefüggés azonban a NAFLD-ben inkább a betegség időtartamához köthető, mint magához az életkorhoz [33].
3.5. Egyéb tényezők
5.3. Pontrendszerek a fibrózishoz
A demográfiai tényezők és a vérvizsgálatok alapján a NAFLD fibrózisának vagy cirrhosisának értékelésére több pontozási rendszert javasoltak: NAFLD fibrosis score (NFS), fibrosis-4-score (FIB-4), BARD (BMI-AST/ALT- Diabetes), fokozott májfibrózis panel (ELF), Hepascore, Fibro Meter ™, Fibro Test ™ és így tovább [51]. Az NFS és a FIB-4 jobb, mint a pontrendszerek az NAFLD-ben szenvedő betegek előrehaladott fibrózisának előrejelzésében. Az Amerikai Májbetegségek Tanulmányi Szövetségének (AASLD) NAFLD gyakorlati útmutatójában az NFS és az FIB-4 ajánlott szűrővizsgálati eszközként az előrehaladott fibrózis és/vagy cirrhosis nagyobb valószínűséggel rendelkező NAFLD betegek azonosítására. Az NFS-t két határérték jellemzi: alacsonyabb és magasabb határérték. Az alacsonyabb határértéknek van a legnagyobb negatív prediktív értéke az előrehaladott fibrózis kizárására. A magasabb cut-off érték rendelkezik a legnagyobb pozitív prediktív értékkel az előrehaladott fibrózisban szenvedő betegek azonosítására. A két határérték közötti „szürke terület” a meghatározhatatlan tartomány [53]. A FIB-4 kettős határértéket is kínál, mint NFS: a 3,25-ös pontszámmal rendelkező betegek valószínűleg előrehaladott fibrózisban szenvednek.
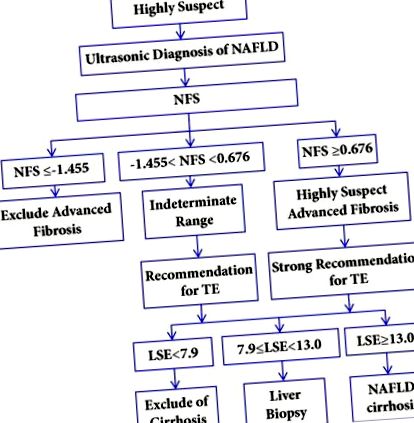
Figyelembe véve a cirrhosis diagnosztikai módszereinek különböző pontosságát, költségét és elérhetőségét, a következő módon javasolható a diagnosztikus megközelítés kiválasztása a gyanús NAFLD cirrhosisban szenvedő betegek számára: (1) Az NFS-t (vagy FIB-4) először diagnosztizált diagnosztizált betegeknél alkalmazzák NAFLD. (2) Az alsó küszöbérték alatti NFS-ben szenvedő betegek cirrhosisa kizárható. Azoknál a betegeknél, akiknek NFS-je meghaladja a meghatározhatatlan tartományt vagy magasabb határértéket, további diagnosztikai vizsgálatokra van szükség TE-vel. (3) A 13,0 kPa TE-vel rendelkező betegek cirrhosisát cirrhosisként diagnosztizálják. A diagnosztikai algoritmus javaslatát az 1. ábra szemlélteti (a [45, 53] szerint módosítva).
Javaslat diagnosztikai algoritmusra a NAFLD által érintett betegek osztályozására. NAFLD: nem alkoholos zsírmájbetegség; NFS: NAFLD fibrózis pontszám; TE: átmeneti elasztográfia; LSE: májmerevség mérése; kPa: kilopascal.
6. Menedzsment
Az elhízás nagy prognosztikai jelentőséggel bír a cirrhosisban szenvedő betegek számára, és a súlycsökkenés fontos a NAFLD cirrhosisban szenvedő betegeknél. A dekompenzált végstádiumú májbetegségben szenvedő betegeknél azonban a fehérjekalória-alultápláltság kockázata miatt nem ajánlott súlycsökkentés [54]. Az antifibrotikus terápia fontos stratégia a NAFLD cirrhosis megelőzésében és visszafordításában. A feltörekvő gyógyszerek, köztük a farnesoid X receptor aktivátora (obeticholsav), a CC kemokin receptorok 2 és 5 típusú antagonistája (Cenicriviroc) és az apoptózis szignál kináz-1 inhibitora (Selonsertib) megerősítették, hogy antifibrotikus hatásúak, és várhatóan a NAFLD cirrhosis potenciális terápiájaként fejlesztették ki [55]. Az alkohol a májkárosodás megerősített tényezője. Az alkoholt meg kell tiltani a NAFLD cirrhosisban szenvedő betegeknél. A NAFLD-ben szenvedő betegeknél a cirrhosis kialakulását fokozó egyéb állapotok közé tartozik a cukorbetegség, a hiperlipidémia és a magas vérnyomás, amelyeket át kell szűrni és kezelni kell. A CVD és a cirrhosis szövődményeinek megelőzése, szűrése és kezelése kritikus fontosságú a NAFLD cirrhosis prognózisa szempontjából. A májtranszplantáció hatékony kezelés a végstádiumú májbetegségben a NAFLD cirrhosisban szenvedő betegeknél.
6.1. A szív- és érrendszeri betegségek megfigyelése és megelőzése
A NAFLD cirrhosisban szenvedő betegeknél magas a CVD előfordulása. Gondos figyelmet kell fordítani a CVD megfigyelésére. Nem invazív funkcionális szívvizsgálat javasolt NASH-cirrhosisban szenvedő betegeknél, progresszióval invazív tesztekké, amikor a noninvazív teszt kóros vagy nem meggyőző [54]. A hiperlipidémia fontos tényező a CVD kialakulásában. A sztatinok, mint lipidcsökkentő gyógyszerek a CVD megelőzésére ajánlottak a NAFLD cirrhosisban szenvedő betegeknél, akik megfelelnek a jelenlegi ajánlások alapján felállított kritériumoknak, de dekompenzált cirrhosisban szenvedő betegeknél kerülni kell őket [52].
6.2. Gastroesophagealis varikumok szűrése és kezelése
A gastroesophagealis varicealis vérzés a cirrhosis súlyos végzetes szövődménye. A NAFLD cirrhosisban szenvedő betegeket az AASLD gyakorlati irányelveinek [56] megfelelően át kell vizsgálni és kezelni kell a gasztro -ophagealis varikációkat: (1) A kompenzált cirrhosisban (CC) szenvedő betegeknél az endoszkópiás szűrővizsgálatok során 2 évente meg kell ismételni az endoszkópiát; a CC-ben szenvedő betegeknél, akiknek az endoszkópos szűrővizsgálata során kis eltérések vannak, minden évben meg kell ismételni az endoszkópiát; a varicus nélküli CC-vel rendelkező vagy kis visszérrel rendelkező betegeknél, akiknél dekompenzáció alakul ki, meg kell ismételni az endoszkópiát, amikor ez bekövetkezik. (2) Hagyományos nem szelektív béta-blokkolók (NSBB-k) (propranolol, nadolol és karvedilol) vagy endoszkópos varicealis ligáció (EVL) ajánlottak közepes vagy nagy varicusos betegek első varicealis vérzésének megelőzésére; Az NSBB az ajánlott terápia magas kockázatú, kis nyelőcső-varikációkban szenvedő betegek számára; az NSBB és az EVL kombinációja az első vonalbeli terápia a vérzés megelőzésében.
6.3. A hepatocelluláris karcinóma felügyelete és kezelése
Jelentős bizonyíték van arra, hogy a cirrhosis a HCC kialakulásának gyakori oka [57]. A NAFLD cirrhosisban szenvedő betegeknél nagyobb a kockázata a HCC-nek [58]. A NAFLD cirrhosisból származó HCC kumulatív incidenciáját 2,4% -nak és 12,8% -nak jelezték a 3,2–7,2 éves medián követés során [59]. A nemzetközi társadalmak ajánlják a HCC megfigyelését a kiválasztott célpopulációkban, beleértve a bármilyen okból származó cirrhosisban szenvedő betegeket is [60]. Az AASLD javasolja, hogy a NAFLD cirrhosisban szenvedő betegeket 6 havonta vegyék figyelembe a HCC szűrés során ultrahangvizsgálattal és a vér alfa-fetoprotein (AFP) szintjének mérésével vagy anélkül [52, 61]. A NAFLD cirrhosisban szenvedő betegek HCC kezelésére hivatkozhatunk az AASLD gyakorlati irányelveire [61]. A T2DM jelentősen növeli a HCC kialakulásának kockázatát [62]. A metformin és a sztatinok jelentősen csökkentik a HCC kockázatát a cukorbetegek körében [63]. Statinokat és metformint javasoltak a HCC elsődleges megelőzésének lehetséges stratégiájaként NAFLD-ben és cukorbetegségben szenvedő betegeknél [60, 62].
6.4. Májtranszplantáció
7. Előrejelzés
8. Következtetések
A NAFLD a cirrhosis egyik vezető okává válik. A NAFLD-ben szenvedő betegeknél a cirrhosis progressziójának kockázati tényezői közé tartozik a NASH, az anyagcsere-tényezők, a genetikai polimorfizmusok és az idősebb kor. A NAFLD cirrhosis klinikai megjelenése hasonló az egyéb etiológia által okozott cirrhosishoz. A dekompenzált cirrhosis diagnosztizálása viszonylag könnyű a NAFLD-ben szenvedő betegek számára. A májbiopszia, a képalkotás és a fibrózis pontozási rendszerei fontos módszerek a kompenzált cirrhosis diagnosztizálására a NAFLD-ben szenvedő betegeknél. A súlycsökkentés, az ivás megtiltása, a cirrhosis előrehaladásának egyéb kockázati tényezőinek kezelése és az antifibrosis alapvető kezelés. A cirrhosis szövődményeinek és a CVD szűrése, kezelése és megelőzése kulcsfontosságú a NAFLD cirrhosis kezelésében. A májtranszplantáció a NAFLD cirrhosisban szenvedő betegek végső stádiumú májbetegségének hatékony kezelése. A NAFLD cirrhosis prognózisa gyenge. Hangsúlyozni kell a NAFLD cirrhosisának megelőzését és kezelését.
Köszönetnyilvánítás
Ezt a kutatást a Kínai Nemzeti Természettudományi Alapítvány támogatta (támogatás száma: 8157040055).
- NEM ALKOHOLOS ZSÍROS MÁJBETEGSÉGEK KEZELÉSE RAIKHELSON Kísérleti és klinikai
- Mikroelemek az alkoholmentes zsírmáj betegség patogenezisében - ScienceDirect
- Elhízás és alkoholmentes zsírmájbetegség - méltó fogyás
- Az étrend és az életmódváltások szerepe alkoholmentes zsírmájbetegségben
- Az alkoholmentes zsíros hasnyálmirigy-betegség (NAFPD) és rizikófaktorainak elterjedtsége a felnőtt orvosok körében