Betegségek áttekintése Myelodysplastic Syndromes (MDS) HCP
Ez a webhely az Egyesült Államok egészségügyi szakembereinek szól.
Ez a webhely az Egyesült Államok egészségügyi szakembereinek szól.
- Betegségek áttekintése
- MDS
- Mi az MDS?
- Ring Sideroblasts
- IPSS-R
- Hatástalan vörösvértest
- β-thalassemia
- Járványtan
- Hatástalan vörösvértest
- MDS
- MOA
- Hatékonyság
- MDS-RS
- MEDALISTA Trial Design
- Alapjellemzők
- Hatékonysági eredmények
- β-thalassemia
- HIGYEK Próbatervezés
- Alapjellemzők
- Hatékonysági eredmények
- MDS-RS
- Biztonság
- MDS-RS
- Figyelmeztetések és óvintézkedések
- Mellékhatások és biztonsági profil
- β-thalassemia
- Figyelmeztetések és óvintézkedések
- Mellékhatások és biztonsági profil
- MDS-RS
- Adagolás és adminisztráció
- MDS-RS
- Adagolás
- Megszakítások és dózismódosítások
- Adminisztráció
- β-thalassemia
- Adagolás
- Megszakítások és dózismódosítások
- Adminisztráció
- Feloldás
- Tárolás
- MDS-RS
- Hozzáférés és támogatás
- Celgene betegtámogatás ®
- Hozzáférés és visszatérítés
- Erőforrások
- β-thalassemia
- Erőforrások
- Videók
- Beteg- és gondozói források
- MDS-RS
- Erőforrások
- Videók
- Beteg- és gondozói források
- β-thalassemia
- Betegségek áttekintése
- MDS
- Mi az MDS?
- Ring Sideroblasts
- IPSS-R
- Hatástalan vörösvértest
- β-thalassemia
- Járványtan
- Hatástalan vörösvértest
- MDS
- MOA
- Hatékonyság
- MDS-RS
- MEDALISTA Trial Design
- Alapjellemzők
- Hatékonysági eredmények
- β-thalassemia
- HIGYEK Próbatervezés
- Alapjellemzők
- Hatékonysági eredmények
- MDS-RS
- Biztonság
- MDS-RS
- Figyelmeztetések és óvintézkedések
- Mellékhatások és biztonsági profil
- β-thalassemia
- Figyelmeztetések és óvintézkedések
- Mellékhatások és biztonsági profil
- MDS-RS
- Adagolás és adminisztráció
- MDS-RS
- Adagolás
- Megszakítások és dózismódosítások
- Adminisztráció
- β-thalassemia
- Adagolás
- Megszakítások és dózismódosítások
- Adminisztráció
- Feloldás
- Tárolás
- MDS-RS
- Hozzáférés és támogatás
- Celgene betegtámogatás ®
- Hozzáférés és visszatérítés
- Erőforrások
- β-thalassemia
- Erőforrások
- Videók
- Beteg- és gondozói források
- MDS-RS
- Erőforrások
- Videók
- Beteg- és gondozói források
- β-thalassemia
A mielodiszpláziás szindrómák (MDS) a myeloid malignus betegségek heterogén csoportja, amelyeket többsoros citopéniák jellemeznek, beleértve az anémiát is. 1
Az Egészségügyi Világszervezet (WHO) az MDS-t neoplasztikussá és ezért rákként osztályozza 2
- Az MDS-t a következők jellemzik:
- A csontvelő diszfunkciója 2,3
- Dysplasia 2,3
- Genomikai instabilitás 2
- Perifériás vér citopéniái 2,3
- Nem hatékony vérképzés 3
Az anaemia az MDS 1-ben szenvedő betegek többségénél jelentkezik
- A diagnózis felállításakor az anaemia a leggyakoribb citopenia az MDS 1-ben szenvedő betegeknél *
- Az MDS-ben szenvedő betegek 94% -a részesült vörösvértesttranszfúzióban a SEER-Sound regiszterben 783 betegből 2001 és 2007 között 4
- A vörösvérsejt-transzfúziót igénylő MDS-ben szenvedő betegek 13% -ának gyűrűs szideroblasztja volt 4
* Egy 11 országból származó, 7012 kezeletlen MDS-ben szenvedő beteg adatbázis-elemzésében meghatározták az MDS prognózisával foglalkozó nemzetközi munkacsoport (IWG-PM) projekt számára. 1
Az NCCN onkológiai klinikai gyakorlati útmutatói (NCCN Guidelines ®) alapján az MDS kezelési megközelítései az MDS altípustól és a betegség súlyosságától függően különböznek 5
IPSS-R, Felülvizsgált Nemzetközi Prognosztikai Pontozási Rendszer.
* Az IPSS-R kockázati pontszámok megoszlását a diagnózis idején értékelték a nemrégiben diagnosztizált betegcsoportban; (N = 7012) az IPSS-R elemzésbe bevont betegpopulációra.
A gyűrűs sztereoblasztok jelenléte MDS betegeknél korrelál az alacsonyabb kockázatú MDS-kel
Az Egészségügyi Világszervezet (WHO) az MDS két altípusát ismeri el gyűrűs sima lapokkal (MDS-RS)
- MDS-RS és egyvonalas dysplasia
- MDS-RS és többsoros dysplasia
- A gyűrűs szideroblasztokat egy patológus által kiértékelt vasfoltos csontvelő-aspirátum alapján lehet azonosítani
- A szideroblasztok az MDS-ben szenvedő betegek legfeljebb 45% -ában vannak jelen
- Ismert változékonyság a csontvelői jelentésben
Az MDS-re vonatkozó NCCN-irányelvek a luspatercept-aamt (REBLOZYL) alkalmazását javasolják a tüneti vérszegénység kezelésére nagyon alacsony vagy közepes kockázatú MDS-ben gyűrűs sideroblastokkal (2A kategória):
- Szérum EPO-ban szenvedő betegek 3 hónapos ESA-kezelés nélküli válasza után
- Kezdeti kezelésként azoknál a betegeknél, akiknél a szérum EPO> 500 E/L
Az MDS-ben szenvedő betegeknél gyűrűs sideroblasztok is lehetnek 6
A gyűrűs simaoblasztok a WHO 2016 osztályozásának részét képezik
- A WHO 2016 két MDS altípust ismer el, amelyek a gyűrűs sideroblastok 7-re jellemzőek:
- MDS-RS egyvonalas dysplasiaval (MDS-RS-SLD)
- MDS-RS többsoros diszpláziával (MDS-RS-MLD)
- Az MDS-RS altípust a 7 azonosítja:
- ≥15% gyűrűs szideroblaszt a csontvelőben
- ≥5% gyűrűs szideroblaszt a csontvelőben és SF3B1 mutáció jelenléte (molekuláris teszteléssel azonosítva)
- Az MDS-RS az ICD-10-CM kódolórendszer 8 részeként ismerhető fel
- A gyűrűs szideroblasztok bármely szinten jelen lehetnek az MDS 9 más altípusaiban is
- Az MDS/MPN-RS-T egy ritka altípus, amelyet a WHO 2016 elismert. Ez hasonlóságot mutat az MDS-RS-vel, de sajátos klinikai jellemzők jellemzik 7,10
- Ezek közé tartozik a vérszegénység, a csontvelő diszplázia gyűrűs sideroblasztokkal és a tartós thrombocytosis ≥450 x 10 9/L a nagy és morfológiailag atipikus megakariociták proliferációjával 7
ICD-10-CM, Betegségek Nemzetközi Osztályozása, tizedik felülvizsgálat, klinikai módosítás.
A gyűrűs szideroblasztok vörösvérsejtek, amelyek vérszegénységgel járó, vassal terhelt mitokondriumokkal rendelkeznek 9
Csak szemléltető célokra.
- A gyűrűs szideroblasztokat vasfestéssel azonosítják, és az eredmények a patológiai jelentésekben találhatók 9
- Változó lehet, hogy a patológusok hogyan írják le a gyűrűs szideroblasztok jelenlétét a patológiai jelentésekben 11
Konzultáljon a patológusával arról, hogy az MDS-ben szenvedő betegeknél hogyan jelennek meg a gyűrűs sztereoblasztok
Az IPSS-R kategorizálás az NCCN irányelvek 5 előnyben részesített * prognosztikai rendszere
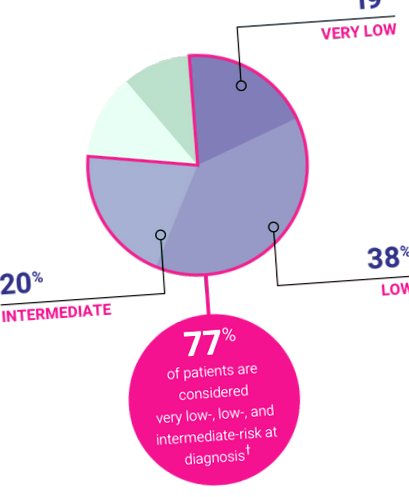
Az MDS-ben szenvedő betegek többségének az 1. diagnózisnál az IPSS ‑ R nagyon alacsony vagy közepes kockázatú betegségben szenved
Az MDS-ben szenvedő betegek megoszlása az IPSS-R kockázati státus szerint (N = 7012) †
* Az NCCN MDS-irányelvei szintén megjegyzik, hogy más kockázati rétegződési rendszerek jó értékkel bírnak. 5.
† Az IPSS-R kockázati pontszámok megoszlása a diagnózis időpontjában a közelmúltban diagnosztizált betegcsoportban értékelve; (N = 7012) az IPSS-R elemzésbe bevont betegpopulációra. 1
IPSS-R, Felülvizsgált Nemzetközi Prognosztikai Pontozási Rendszer.
Az IPSS-R a csontvelő citogenetikáján, a velőrobbanás százalékán, valamint a citopéniák jelenlétén és mélységén alapul 1
| Prognosztikai pontszámok 1 | ||||||||
| Prognosztikai változó | BM robbantások,% | Citogenetika | Hgb, g/dL | Trombociták, x 10 9 sejt/l | ANC, x 109 sejt/l | |||
| 0 | ≤2 | Nagyon jó | ≥10 | ≥100 | ≥0,8 | |||
| 0.5 | - | - | - | 50–2–10 | Szegény | - | - | - |
| 4 | - | Nagyon rossz | - | - | - | |||
ANC, abszolút neutrofilszám; BM, csontvelő; Hgb, hemoglobin.
Az IPSS-R pontszám kiszámítása a prognosztikai tényezők értékeinek összeadásával történik
Példa az IPSS-R alacsony kockázatú pontszámára:
- 2% robbanásszám = 0
- Jó citogenetika = 1
- 8 g/dl Hgb = 1
- Vérlemezkék 75 x 109 sejt/L = 0,5
- ANC 0,9 x 109 sejt/L = 0
Összeadva az összes érték = 2,5
A diagnózis felállításakor az MDS-ben szenvedő betegek több mint 90% -a vérszegénységben szenved (
Az anaemia rossz prognózissal jár együtt az MDS-ben
- Azok a betegek, akik havonta mindössze 2 egység vért kapnak, szignifikánsan csökkent túlélést mutattak azokhoz képest, akik nem igényelnek transzfúziót
- Az MDS-ben szenvedő betegek alacsonyabb hemoglobin (Hgb) szintje a csökkent túléléshez és a rosszabb kardiovaszkuláris eredményekhez kapcsolódik
Segíteni kell a vörösvérsejt-transzfúziót igénylő MDS-ben szenvedő betegek hatástalan eritropoéziséből eredő vérszegénység kezelésében
Az MDS 12 vérszegénységének oka az ineffektív eritropoezis
Az MDS vérszegénysége a csontvelő diszfunkciójához kapcsolódik, amelyet hatástalan vörösvértestként jellemeznek 13
- Az MDS-ben az őssejtek nem képesek differenciálódni és érlelődni, ami csontvelő-diszfunkcióhoz és rossz vérsejt-termeléshez vezet, különösen a vörösvértesteknél
Az MDS-ben bekövetkező hatástalan eritropoézis vérszegénységhez vezethet, amely vörösvérsejt-transzfúziót igényel, és 12,14 jellemzi:
Az eritroid progenitorok fokozott szaporodása
Az eritroid prekurzorok fokozott halála
Károsodott erythroid érés
Az anaemia jelenléte a progenitor sejtek fokozott szaporodása ellenére az MDS-ben bekövetkező hatástalan eritropoézist jelzi
Segíteni kell a vörösvérsejt-transzfúziót igénylő MDS-ben szenvedő betegek hatástalan eritropoéziséből eredő vérszegénység kezelésében
Jelzés
A REBLOZYL vérszegénység kezelésére javallt béta-thalassémiában szenvedő felnőtt betegeknél, akiknek rendszeres vörösvértest-transzfúzióra van szükségük.
A REBLOZYL olyan vérszegénység kezelésére javallt, amely sikertelen eritropoézist stimuláló szerrel rendelkezik, és 8 hét alatt 2 vagy több vörösvértest-egységre van szüksége, nagyon alacsony vagy közepes kockázatú, gyűrűs sztereoblasztokkal (MDS-RS) vagy mielodiszplasztikus/myeloproliferatív neoplazma gyűrűs szideroblasztokkal és thrombocytosis (MDS/MPN-RS-T).
A REBLOZYL nem javallt a vörösvérsejt-transzfúzió helyettesítésére olyan betegeknél, akiknek vérszegénység azonnali korrekciójára van szükség.
FONTOS BIZTONSÁGI INFORMÁCIÓK
FIGYELMEZTETÉSEK ÉS ÓVINTÉZKEDÉSEK
Trombózis/tromboembólia
Béta thalassémiában szenvedő felnőtt betegeknél 8/223 (3,6%) REBLOZYL-kezelt betegnél jelentettek thromboemboliás eseményeket (TEE). A TEE-k között szerepelt a mélyvénás trombózis, a tüdőembólia, a portális vénák trombózisa és az ischaemiás stroke. Azok a betegek, akiknél a tromboembólia kockázati tényezői ismertek (splenectomia vagy a hormonpótló kezelés egyidejű alkalmazása), a tromboembóliás állapotok további kockázata lehet. Fontolja meg a tromboprofilaxist azoknál a betegeknél, akiknél fokozott a TEE kockázata. Figyelje a betegeket a tromboembóliás események jeleire és tüneteire, és haladéktalanul kezdje meg a kezelést.
Magas vérnyomás
A magas vérnyomást a REBLOZYL-nal kezelt betegek 10,7% -ánál (61/571) jelentették. A klinikai vizsgálatok során a 3–4 fokozatú hipertónia előfordulása 1,8% és 8,6% között mozgott. Normál kiindulási vérnyomással rendelkező béta-thalassémiában szenvedő betegeknél 13 (6,2%) betegnél szisztolés vérnyomás (SBP) ≥130 Hgmm, 33 (16,6%) betegnél diasztolés vérnyomás (DBP) ≥80 Hgmm volt. Normális kiindulási vérnyomással rendelkező MDS-ben szenvedő felnőtt betegeknél 26 (29,9%) betegnél SBP ≥130 Hgmm, 23 (16,4%) betegnél DBP ≥80 Hgmm alakult ki. Minden beadás előtt ellenőrizze a vérnyomást. Kezelje a már fennálló magas vérnyomás új vagy súlyosbodásait magas vérnyomáscsökkentő szerekkel.
Embrió-magzati toxicitás
A REBLOZYL magzati károsodást okozhat, ha terhes nőnek adják be. A REBLOZYL a vemhes patkányokkal és nyulakkal kapcsolatos vizsgálatokban fokozta az implantáció utáni veszteséget, az alom méretének csökkenését és a csontváz variációk fokozott előfordulását. Tájékoztassa a terhes nőket a magzat potenciális kockázatáról. Tanácsot adjon a reproduktív képességű nőknek, hogy hatékony fogamzásgátlást alkalmazzanak a kezelés alatt és az utolsó adag után legalább 3 hónapig.
MELLÉKHATÁSOK
Béta-thalassemia
- A REBLOZYL-kezelés alatt álló betegek 3,6% -ánál súlyos mellékhatások jelentkeztek. A betegek 1% -ánál jelentkező súlyos mellékhatások között volt agyi érrendszeri baleset és mélyvénás trombózis. Végzetes mellékhatás jelentkezett 1 REBLOZYL-lel kezelt betegnél, aki egy meg nem erősített akut myeloid leukémia (AML) meg nem erősített esete miatt halt meg
- A leggyakoribb mellékhatások (a REBLOZYL esetében legalább 10%, a placebónál 1% -kal több) a fejfájás (26% vs 24%), csontfájdalom (20% vs 8%), arthralgia (19% vs 12%), fáradtság (14). % vs 13%), köhögés (14% vs 11%), hasi fájdalom (14% vs 12%), hasmenés (12% vs 10%) és szédülés (11% vs 5%)
Myelodysplasticus szindrómák
- ≥3 (≥2%) fokozatú mellékhatások a fáradtság, a magas vérnyomás, az ájulás és a mozgásszervi fájdalom voltak. 5 (2,1%) betegnél végzetes mellékhatás fordult elő
- A leggyakoribb (≥10%) mellékhatások a fáradtság, mozgásszervi fájdalom, szédülés, hasmenés, émelygés, túlérzékenységi reakciók, magas vérnyomás, fejfájás, felső légúti fertőzés, hörghurut és húgyúti fertőzés
SZOPTATÁS
Nem ismert, hogy a REBLOZYL kiválasztódik-e az anyatejbe, vagy szoptatikusan felszívódik-e az ápoló csecsemő lenyelése után. A REBLOZYL-t laktáló patkányok tejében detektáltuk. Ha egy gyógyszer van jelen az állati tejben, akkor valószínű, hogy a gyógyszer jelen lesz az emberi tejben. Mivel sok gyógyszer kiválasztódik az anyatejbe, és mivel a REBLOZYL csecsemőknél ismeretlen hatásai vannak, döntést kell hozni az ápolás vagy a kezelés abbahagyásáról. A szoptatott gyermek súlyos mellékhatásai miatt a szoptatás nem ajánlott a kezelés alatt és az utolsó adag után 3 hónapig.
- Gasztrointesztinális betegség - áttekintés a ScienceDirect témákról
- Cushing; s Betegség- Gyors áttekintés Az Őszinte Konyha Blog
- A lisztérzékenység - a MedlinePlus Medical Encyclopedia kiadványa
- Celiac betegség és gluténérzékenységi szójegyzék
- A lisztérzékenység enyhíti a gyomor-bélrendszeri tüneteket