Élelmiszerallergiák és öregedés
Massimo De Martinis
1 L’Aquila Egyetem Élet-, Egészség- és Környezettudományi Tanszéke, 67100 L’Aquila, Olaszország; [email protected] (M.M.S.); [email protected] (L.G.)
2 Allergia és Klinikai Immunológiai Osztály, AUSL 04 Teramo, Olaszország
Maria Maddalena Sirufo
1 L’Aquila Egyetem Élet-, Egészség- és Környezettudományi Tanszéke, 67100 L’Aquila, Olaszország; [email protected] (M.M.S.); [email protected] (L.G.)
2 Allergia és Klinikai Immunológiai Osztály, AUSL 04 Teramo, Olaszország
Angelo Viscido
3 Gasztroenterológiai osztály, L’Aquila Egyetem, Élet-, Egészség- és Környezettudományi Tanszék, 67100 L’Aquila, Olaszország; [email protected]
Lia Ginaldi
1 L’Aquila Egyetem Élet-, Egészség- és Környezettudományi Tanszéke, 67100 L’Aquila, Olaszország; [email protected] (M.M.S.); [email protected] (L.G.)
2 Allergia és Klinikai Immunológiai Osztály, AUSL 04 Teramo, Olaszország
Absztrakt
1. Bemutatkozás
Az ételallergiák a közegészségügy szempontjából releváns problémává válnak, világszerte több mint 200 millió embert érintenek, és gyakorisága növekszik, elsősorban a fejlett országokban [1]. Az FA-ket a számos szervet érintő megnyilvánulások széles spektruma jellemzi, az enyhe és a súlyos, valamint az életet veszélyeztető reakciók között [2,3]. Az ételallergia diagnózisa összetett, mivel a különböző immunológiai mechanizmusok (IgE-közvetített, sejt-közvetített vagy kevert) szerepet játszhatnak. Mint a legtöbb immunmediált betegségben, a klinikai expresszió változékonyságát, valamint növekvő prevalenciáját a genotípusos, epigenetikus és környezeti tényezők határozzák meg [4,5,6].
Az FA-k sokkal gyakoribbak gyermekeknél, mint felnőtteknél. A legtöbb FA korai gyermekkorban kezdődik, és általában felnőttkorban eltűnik. Emiatt az FA-kat gyakran szinte kizárólag gyermekbetegségnek tekintik. Noha annak előfordulása a kisgyermekeknél a legnagyobb, az FA-reakciók gyakoriak az időseknél [7,8]. A legtöbb epidemiológiával, immunopatogenezissel és a FA-k klinikai megnyilvánulásával foglalkozó vizsgálatokat gyermekeknél és serdülőknél végezték, nem pedig idős embereknél. A világ népességének demográfiai megoszlása azonban gyorsan változik, növekszik az idősebb emberek aránya, és jelentős százalékuk haveallergiás betegségekkel küzd [9,10]. Ezekkel a demográfiai változásokkal párhuzamosan tehát arra számíthatunk, hogy az általános népességben már növekvő FA-k az időseknél is növekedni fognak [11].
Becslések szerint az idősek allergiás megbetegedéseinek jelenlegi előfordulása eléri a 10% -ot, de ezeket az adatokat alábecsülik, és növekedni is szánják [12]. Az FA-ban szenvedő gyermekek egyre nagyobb hányada éri el felnőttkorát és öregségét, és némelyikben az allergiás probléma tartósan fennáll. Továbbá az FA-k felnőttkorban is kialakulhatnak, és az első tünetek még időseknél is jelentkezhetnek [13]. A mai napig azonban még mindig nem fordítanak nagy figyelmet az FA-kre időskorú embereknél, és az FA-kkal kapcsolatos tünetek, mint például hányás, dyspepsia, hasmenés, viszketés, valamint a bőr és a légzőszervi megnyilvánulások, időseknél gyakran nem diagnosztizáltak [14].
Az epidemiológiai adatok hiánya mellett nagyon keveset tudunk az idős emberek immunopatogenetikai sajátosságairól és klinikai megjelenéséről [15].
Jelen áttekintés célja az élelmiszer-allergia hátterében álló patofiziológiai mechanizmusok elemzése az időseknél, kiemelve a népesség ezen szegmensének legsajátosabb szempontjait, amelyek a lehetséges intervenciós intézkedések alapját képezik.
2. Idősek immunrendszerének átalakítása
A genetikai háttér ellenőrzi az immunitást és a gyulladást, és befolyásolja mind az öregedési folyamatot, mind az allergia kialakulását. Az FA-k több alapmechanizmusát felismerték időseknél, amelyek közül az első az immunszenzencia, vagyis az immunrendszer sajátos, életkorral összefüggő átalakítása. Az öregedés során a veleszületett és az adaptív immunreakciók egyaránt mélyen megváltoznak, elősegítve az FA-k kialakulását [16].
A fokozott gyulladásos citokinek és az antigént bemutató sejtek diszfunkciója hozzájárul az allergiás szenzibilizációhoz és az öregedés gyulladásához. A dendritikus sejtek, amelyek az adaptív válaszok fő lépcsője, megváltozott kostimulációs molekulák expresszióját mutatják gyenge idős egyéneknél, kondicionálva a diszfunkcionális antigénfeldolgozást és megjelenítést, ami allergiás reakciókat válthat ki [22].
Az allergiás reakciók effektorsejtjeivel kapcsolatban a legtöbb tanulmány az eozinofil degranuláció csökkenéséről számol be az IL-5 stimulációra reagálva és a hízósejtek funkciójának csökkenéséről, a szövetekben lévő hízósejtek normál száma ellenére [23].
Az időskorúaknál a T helper funkciójának megsértését és az izotípusváltás hibáit figyelték meg, amelyek az immunológiai memória károsodásához és az oltásokra adott alacsonyabb válaszhoz vezetnek [24]. Ezzel szemben az IgE izotípust kevésbé veszélyezteti az öregedés [25]. Különösen az immunoszenesencia nem befolyásolja az atópiában szenvedő idős betegek IgE-szintjét, ami arra utal, hogy az allergia hajlandósága fennmarad magas életkorban [14,26].
3. A nyálkahártya immunrendszere az öregedésben
A gyulladás, a krónikus gyulladás állapota, amely az öregedést vezérli [32], növeli a szoros kereszteződés áteresztőképességét a gyulladáscsökkentő citokinek hatásán keresztül [33]. A gyomor-bél traktus hámsejtjei maguk felelősek mind a nagy mennyiségű citokinek termeléséért, mind a szűk kereszteződések és az occludens zonula fehérjéjének csökkentéséért, ami fokozott bélpermeabilitást eredményez [34]. Ez a csökkent gátló hatás a tolerancia mechanizmusának megrepedését eredményezi, ami hajlamosítja a betegeket az FA-ra. A gyulladásos citokinek, például az IFN-γ, az IL-6 és az IL-1β jelenléte a bél nyálkahártyájában fontos tényező ebben a folyamatban [35].
4. Hámgát és emésztési funkció károsodása
Az ételallergének többnyire szerkezetileg stabil fehérjék, amelyek általában nagyobb kockázatot jelentenek a szisztémás reakciók kiváltására. Az emésztés sérülése esetén a labilis ételfehérjék részben emésztetlenül is fennmaradhatnak a gyomor-bél traktusban, és ételallergénekké válhatnak [46]. A gyomorproteáz propepszin csak 3,0 alatti pH-érték esetén aktiválódik. Továbbá csak a duodenumba bejutó savas chymus indukálhatja a hasnyálmirigy-enzimek felszabadulását. Így az idős lakosság gyomorsavcsökkenése miatt a fehérje emésztése veszélybe kerül, és az ártalmatlan fehérjék potenciálisan veszélyes allergénekké alakulnak [47]. Az idősek protonpumpa-gátlókkal történő terápiája ezen mechanizmusok révén megkönnyítheti az élelmiszer-allergének iránti érzékenységet, vagy csökkentheti az allergiás reakció kiváltó küszöbét, ha FA már jelen van [48].
Emellett a béltől eltérő szervek és rendszerek életkorral kapcsolatos változásai fontos szerepet játszhatnak az idősek FA-k kialakulásában. A bőr az ételekkel szembeni allergiás reakció egyik fő célpontja, valamint az elsődleges szenzibilizáció fontos helyszíne. A kronológiai és környezeti tényezők eredményeként az idős bőrt atrófia és kiszáradás jellemzi [49]. A strukturális integritás fokozatos elvesztése az immunválasz és a bőrsorompó funkció károsodásához, a reaktív oxigén és az extracelluláris mátrix komponensek növekedéséhez, valamint az érrendszeri károsodáshoz vezet [50]. Bár a T-sejtek által közvetített immunitás csökkentnek tűnik, az idős betegeknél kialakulhat kontakt dermatitis, valamint a bőrön keresztül érzékenyíthetik magukat az ételallergénekre [3].
5. Korhoz kapcsolódó mikrobiális diszbiózis
A helyi immunitás károsodása és a gyomor-bélrendszer nyálkahártya permeabilitásának megnövekedése mellett a bél mikrobiotájának életkorral összefüggő változásai is elősegíthetik az FA fejlődését idősekben.
A bélmikrobiota egy összetett ökológiai rendszer, amely több fiziológiai funkcióban központi szerepet tölt be, és összetétele a gazdaszervezet egész életében változik. Érzékeny a környezeti hatásokra és a fogadó étrendjére, és függ a gazda genetikájától, nemétől és önmagában az öregedési folyamattól [51].
A szekréciós IgA rendszere kritikus szerepet játszik nemcsak a fertőzések elleni védekezésben, hanem a helyi immunválasz modulációjában is a bél mikrobiota fenntartása révén. A gyulladásos folyamatok a bél mikrobiota és az öregedő gazda közötti homeosztatikus kölcsönhatások diszregulációjával társulnak [52].
A bél mikrobiota jelentős életkorral összefüggő változásokat mutat az összetételben és a sokféleségben, valamint a funkcionális jellemzőkben, elsősorban az immunrendszer átalakulása és az alacsony fokú krónikus gyulladás okozta, amelyek az immunoszenesenciát és a gyulladásokat jellemzik [22].
Az immunszenszcencia kulcsfontosságú szerepet játszik a gazdaszervezet mikrobiotára adott válaszának módosításával, a gyulladás kiváltásával és a Th1 és a Th2 válaszok elmozdításával, ezáltal elősegítve a tolerancia zavarát és az allergiás reakció kialakulását [52].
Az antibiotikumok az időseknél a leggyakrabban használt gyógyszerek közé tartoznak, és gyakran helytelenül használják őket. Befolyásolják a mikrobiom összetételét és működését, zavarva az immun homeosztázist. Idős korban az antibiotikumok tovább zavarhatják a mikrobiota összetételét [53,54]. Azonban még időseknél is a bélflóra helyreállítható probiotikumokkal, de egyelőre nem tudni, hogy ez hogyan akadályozhatja meg a FA-k kialakulását [55].
6. Táplálkozási hiány miatt bekövetkező immunműködési zavarok
Az immunrendszer öregedéskori sajátos átalakításával, az epitheliális akadályok sérült integritásával és az időseknél gyakran megfigyelt szubklinikai krónikus gyulladásos állapotokkal együtt az élelmiszerallergének iránti szenzibilizálásban központi szerepet játszik a mikroelemek és vitaminok hiánya is. [12].
A mikroelemek és az antioxidánsok modulálják az immunválaszokat, és azt javasolják, hogy hiányuk elősegítse a Th2 típusú válaszok kialakulását. Például az időseknél nagyon gyakori vas-, cink- és D-vitamin-hiány további kockázati tényezőket jelenthet az allergiás reakciók kialakulásának öregedése során [10].
A cink elengedhetetlen nyomelem, amely központi szerepet játszik az immunhatékonyság szempontjából. A cink intracelluláris homeosztázisa, amelyet metallotioneinok és specifikus transzporterfehérjék szabályoznak, megváltozik az öregedés során, ami az immunfunkciókhoz való hozzáférhetőség csökkenéséhez vezet. Az időseknél gyakran megfigyelhető csökkent cinkszint felelős lehet a Th1 citokinek termelésének csökkenéséért, míg ez nem befolyásolja a Th2 citokinek termelését, így citokin egyensúlyhiányt idéz elő, amely elősegíti az allergiás betegségek kialakulását [56].
A cinkhiány hozzájárul a thymás atrófiához; éretlen B-sejtek felhalmozódása; és csökkent IgM, Ig-G2a és IgA alosztályok. A stresszhelyzetek pro-gyulladásos citokintermelés révén, beleértve az IL-6-ot és a TNF-α-t is, gyakran cinkhiánnyal járnak. A geriátriai populációban tartósan megnövekedett gyulladásos citokinek megkötik a cinkionokat, ennek következtében csökken a cink biohasznosulása és megváltozott az immunfunkció. Különösen a csökkent cinkszint a Th1 citokinek, például IFN-y, IL-2 és TNF-a redukcióját indukálja, míg a Th2 citokinek, különösen az IL-4 fokozódnak. Ezen mechanizmus révén a cinkhiány elősegítheti a FA-k kialakulását az időseknél [57].
Az időseknél is gyakori a vashiány [20]. A csökkent vasszint csökkent humorális válaszokat vált ki, és különösen csökkenti az IgG4 alosztály termelését, amely fiziológiailag elkapja az allergéneket, mielőtt azok az IgE-hez kötődnének, megakadályozva ezzel az effektor sejtek, például mastocyták és bazofilek aktiválódását [58].
Számos tanulmány azt sugallja, hogy a D-vitamin hiány az időseknél is nagyon gyakori, támogatva az FA fejlődését. Az immunrendszernek a megnövekedett mellékpajzsmirigyhormon-szint és a csontok egészségének romlása mellett, amely fokozza a törések kockázatát, az idősek D-vitamin-hiányának súlyos következménye [59,60]. A D-vitamin aktív metabolitja, a kalcitriol, befolyásolja a T-limfocitákat és az antigént bemutató sejteket, hogy a gyulladásos válaszok gátlásával és a szabályozó T-sejtek elősegítésével perifériás toleranciát indukáljon [61]. A D-vitamin-hiány tehát az autoimmun és atópiás betegségek fokozott kockázatával jár, bár az IgE-szintekkel való összefüggés nem egyértelmű [62].
7. Az idősek FA-k klinikai jellemzői
A változó természettörténet és a lehetséges patogenetikai mechanizmusok összetettsége, valamint számos, az életkorral összefüggő tényező megnehezíti az idősek FA-k diagnosztizálását és kezelését. Táplálkozási rendellenességek és vitaminhiány, valamint hormonális egyensúlyhiány és gyulladás, kölcsönhatásba lépve a genetikával, megváltoztathatja az immunválaszokat, ami FA-fejlődéshez vezethet. A fiziológiai funkciók életkorral összefüggő csökkenése, az öregedést jellemző immunrendszer-átalakítás mellett, hozzájárul az FA furcsa klinikai megállapításainak időseknél [23,63].
Ezen túlmenően, annak ellenére, hogy az allergiás és a specifikus allergénekkel végzett szúrópróbákra elegendő pozitív válasz adott idő alatt az allergiás bőrön lévő hízósejtek száma normális vagy megnövekedett, az idősek gyengébb bőrreakciókat mutatnak, és kevésbé intenzív pomfoid reakciókat mutatnak a hisztamin-kontrollra [64]. Ezért, mivel az allergiára adott bőrteszt pozitív reakciói részben csökkenthetők az időseknél, ami a hamis negatív bőrteszt kockázatát eredményezheti, idősebb betegeknél általában specifikus IgE-keresést alkalmaznak az FA diagnosztizálására [65].
A daganatellenes gyógyszerek bevitele időseknél gyakori a gyomorhurut, a gyomor-nyelőcső refluxjának, a gyomorfekélynek a kezelésére, vagy kortikoszteroidokkal és nem szteroid fájdalomcsillapítókkal együtt a gasztroenzív hatásuk minimalizálása érdekében. A gyomor hipo-savasság és a felső gyomor-bél traktus fokozott permeabilitása a savszuppresszív gyógyszerekkel végzett terápia eredményeként is előfordul, megkönnyítve az FA kialakulását, valamint az eozinofil nyelőcsőgyulladást. A protonpumpa-gátlókkal vagy a H2-receptor blokkolókkal kezelt idős betegeknél nagyobb a szenzibilizáció kockázata, mivel az étkezési fehérjék nem teljesen emésztettek maradnak, és a megnövekedett permeabilitás miatt könnyebben átléphetik a nyálkahártya gátját, így allergénekké válnak [8,49].
8. Következtetések
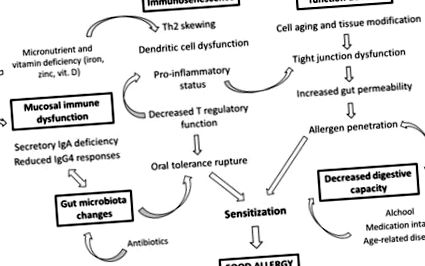
A káros ételreakciók az idősek sajátos jellemzőit mutatják, amelyek mind a patogenezist, mind a klinikát érintik. Az időskorúak FA-ját az immunszenszcencia, valamint a sejtek öregedése és az időskort jellemző szöveti módosítások vezérlik. Az idősek gyomor-bélrendszerének nyálkahártyája központi szerepet játszik az idősek FA-k kialakulásában az emésztési tulajdonságainak és a szerkezeti változásoknak, valamint az immunfunkciók és az életkorral összefüggő mikrobiota átalakítással összefüggő immunfunkcióinak megváltoztatásán keresztül. Az ételallergének szenzibilizációjának rizikófaktorai között az időseknél az öregedési folyamat következtében bekövetkező krónikus károsodás és a bélhám gyulladása mellett krónikus alkoholfogyasztás, krónikus fertőzések, multimorbilitás, polimedikáció és gyógyszeres mellékhatások találhatók (1. ábra). ).
Élelmiszerallergia időseknél. Az ábra az ételallergia kialakulásának fő kockázati tényezőit mutatja időseknél. Az immunszenszcencia és a gyomor-bél traktus nyálkahártya immunműködési zavarai mozgatórugók az ételallergia kialakulásában az időseknél. A bélgát funkciójának csökkenése és a károsodott emésztési tulajdonságok, valamint az életkorral összefüggő mikrobiota átalakulása szintén központi tényező mind az allergén behatolásában, mind az érzékenységben.
Szerző közreműködései
Minden szerző egyformán járult hozzá a munkához.
Finanszírozás
A tanulmány nem kapott támogatást.
Összeférhetetlenség
A szerzők nem jelentenek összeférhetetlenséget.
- Francia bulldog ételallergiák tünetei; Általános allergiás ételek
- Az étkezés elfogyasztása megölhet, ha a szakácsok nem veszik komolyan az ételallergiákat
- Az ekcéma és a BF felszámolási étrend - Élelmiszerallergia fórumok Mire számíthatunk
- Kedves Kara ételallergia (Hill támogatása; Pet Nutrition) DVM 360
- Az ételallergiák kezelése vegánként (a vegán munka megteremtése…