Endoszkópos gyomorhurut, szérum pepszinogén teszt és Helicobacter pylori fertőzés
Absztrakt
BEVEZETÉS
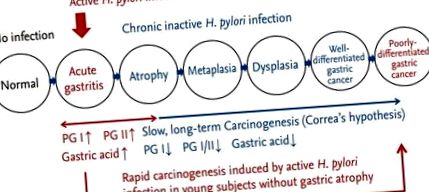
A felső gasztrointesztinális (UGI) endoszkópia lehetővé teszi az orvosok számára, hogy megbecsüljék a gyomornyálkahártya szekréciós képességét és a gyomorrák kockázatát a háttér gyomornyálkahártya eredményei alapján (1. ábra). A gyomornyálkahártya-sejtek szekréciós képességének mérésére nem invazív szerológiai teszteket részesítenek előnyben az invazív csővizsgálatokkal szemben [1]. A noninvazív tesztek a szérum pepszinogén (PG) tesztből, a kalcium-karbonát lélegzetvizsgálatból és a hidrogén lélegeztetésből állnak, míg az invazív tesztek aspirációs tesztekből (pentagasztrin és tetragasztrin tesztek), endoszkópos gasztrin tesztből és intragasztrikus pH mérésekből állnak [2]. A közelmúltban a szérum PG-teszt a szérum-gasztrin-vizsgálathoz képest előnyösebbé vált a gyomornyálkahártya állapotának mérésében, mivel a gasztrint elsősorban az antrum endokrin G-sejtjei termelik [3,4]. A negatív PG assay az egészséges gyomornyálkahártyát jelzi, negatív prediktív értéke> 99% volt a szérum PG I/II alkalmazásával [5].
A háttér gyomornyálkahártya endoszkópos megállapításai a gyomor karcinogenezisének útja szerint. Helicobacter pylori fertőzéskor a gyomornyálkahártya olyan változásokat mutat, amelyek aktív fertőzésre utalnak, például többszörös vérzéses foltok, csomók és a gyomor rugae megvastagodása. Ebben a szakaszban megnő a diffúz típusú gyomorrák kockázata, az intragasztrikus környezet hipersavvá válik, és megnő a szérum pepszinogén (PG) szintje. Amikor az aktív gyulladás alábbhagy, és a fertőzés krónikus stádiumba kerül, a háttér gyomornyálkahártya atrófiát és metapláziát mutat. Ez a hosszú távú, lassú folyamat növeli a bél típusú gyomorrák kockázatát, az intragasztrikus környezet hipoakká válik, és csökken a szérum PG szintje.
Az UGI endoszkópiát Koreában kétévente végzik, mint nemzeti szűrőrendszert a gyomorrák másodlagos megelőzésére minden 40 évnél idősebb felnőttnél. Ennek ellenére nincs standardizált jelentési formátum, amely leírná a gyomor hátterének hátterében található megállapításokat, és az endoszkópos gyomorhurutot a szűrési folyamat során gyakran alábecsülik. Ez az áttekintő cikk a háttér gyomornyálkahártya endoszkópos megállapításaira koncentrálódik az intragasztrikus állapotokkal összefüggésben, amint azt a szérum PG assay eredményei tükrözik.
ÉRINTETT LÉPÉS FERTŐZÉS NÉLKÜL
A gyomorsav és más gyomormormonok kiválasztásának képessége sértetlen H. pylori fertőzés nélküli személyeknél. A háttér gyomornyálkahártya rendszeresen elrendezi a gyűjtő vénákat, amikor az alany soha nem volt fertőzött H. pylori-val (2. ábra). Hipersavállapotban többszörös hiperémiás erózió vagy lineáris csík fordulhat elő az antrumon, ami eróziós gastritishez (EG) vagy krónikus felületes gastritishez (CSG) vezethet.
(A) Endoszkópos leletek Helicobacter pylori fertőzés nélküli egyéneknél. A pepszinogént (PG) I kizárólag főfenék és nyaki nyaki sejtek termelik a funduson. A PG II a gyomorban és a nyombél izzójának Brunner-mirigyéből is kiválasztódik. (B) A szög normál endoszkópos megállapítása nem fertőzött alanynál. A gyűjtő vénák rendszeres elrendezése a szögben normális gyomornyálkahártyát jelez. (C) A korpusz normál megállapítása ugyanabban az alanyban. A gyűjtő vénák rendszeres elrendezése egészen a kardiáig és a fundusig terjed. (D) Krónikus felületes gasztritisz. Számos hiperémiás csíkot észlelnek az antrum nagyobb görbületén. (E) Eróziós gasztritisz. Többszörös emelt, hiperémiás erózió látható az antrumon.
Krónikus felületes gasztritisz
A CSG-t az lineáris csíkok jellemzik az antrum nagyobb görbületén. A CSG a leggyakoribb endoszkópos gyomorhurut Koreában, ezt követi az EG, a krónikus atrófiás gyomorhurut (CAG) és a metaplasztikus gyomorhurut (MG) [6]. A CSG-ben talált hiperémiás csíkok nem igényelnek későbbi biopsziát, mivel ezek nem járnak a gyomorrák kockázatának növekedésével. A CSG hiperacid állapotokat foglal magában. A gyomornyálkahártya sejtek szekréciós képessége érintetlen marad.
Eróziós gastritis
Az EG többszörös megemelkedett erózióval jár, hiperémiás változásokkal az antrumon. Az eróziókat nem fertőzött és aktív H. pylori fertőzésben szenvedő betegeknél egyaránt megtalálhatjuk (1. táblázat). H. pylori fertőzés hiányában a gyomorrák előfordulása alacsony [7]. EG-ben az intragasztrikus állapotok túl savasak, és a gyomornyálkahártya-sejtek szekréciós képessége érintetlen marad.
Asztal 1.
Gyakori endoszkópos leletek a Helicobacter pylori fertőzés endémiás területén
| Nincs fertőzés | Krónikus felületes gasztritisz | Több hiperémiás csík | Antrum, nagyobb görbületű oldal | Ép | Normosav | Normál |
| Nincs összefüggés a fertőzéssel | Eróziós gastritis | Számos hiperémiás, emelt elváltozás | Antrum | Ép | Hipersav | Normál |
| Aktív fertőzés | Nodularis gastritis | Több apró és szabályos submucosalis emelkedett elváltozás színváltozás nélkül | A korpusz felé nyúló antrum | Ép | Hipersav | Megnövekedett szérum PG II szint |
| Vérzéses foltok | Több apró és szabályos vöröses folt | Corpus (szemfenék és magas test) | Ép | Hipersav | Megnövekedett szérum PG II szint | |
| Hipertrófiás gyomor rugae | Több megvastagodott rúga ödémás elváltozással és fehéres, ragacsos váladékkal | Corpus | Ép | Hipersav | Megnövekedett szérum PG II szint | |
| Krónikus inaktív fertőzés | Krónikus atrófiás gastritis | Látható átlátszó edények | Antrum, kisebb görbületű oldal a korpusz felé, nagyobb görbületű oldal | Károsodott | Hipoacid | Csökkent szérum PG I szint |
| Metaplasztikus gastritis | Több nagy és szabálytalan fehéres emelkedés | A korpusz felé nyúló antrum | Károsodott | Hipoacid | Csökkent szérum PG I szint |
A H. pylori fertőzéssel nem összefüggő egyéb gyomorhurut
A nem fertőzött egyének endoszkópos gyomorhurutja ritka, endémiás H. pylori fertőzésben. Az A típusú autoimmun gastritis eredetileg tünetmentes betegség, amely károsító adenomával (B12-hiány) vagy vashiányos vérszegénységgel járó korpusz atrófiává fejlődik [8]. A granulomatózus gyomorhurut összefügg a Crohn-betegséggel, a tuberkulózissal, a szifilissel, a szarkoidózissal, az anisakiasissal vagy az idegen testre adott reakcióval. Az eozinofil gastroenteritis nem specifikus gyomor-bélrendszeri tünetekkel jár, és előfordulhat a nyelőcső vagy a vastagbél [9]. A gasztritisz egyéb típusai közé tartozik a kollagén gasztritisz, a besugárzás utáni gasztritisz és a gyógyszerekkel kapcsolatos gasztritisz.
LAKÁS AKTÍV H. PYLORI FERTŐZÉSSEL
Aktív vagy akut H. pylori fertőzés diagnosztizálható gyomornyálkahártya biopsziával. A patológiai eredmények a mononukleáris sejtek és a polimorfonukleáris neutrofilek behatolását mutatják. A H. pylori fertőzésre utaló egyetlen endoszkópos lelet hiánya miatt gyakran alkalmaznak szerológiai vizsgálatokat a gyomornyálkahártya állapotának ellenőrzésére.
Vérzéses foltok, nodularitás és megvastagodott gyomor redők
Az akut H. pylori-fertőzés tipikus endoszkópos megállapításai közé tartoznak a szemfenéken és/vagy a magas testben lévő vérzéses foltok, a noduláris gyomorhurut és a hipertrófiás gyomor-ruga (3. ábra). A noduláris gasztritisz endoszkópos leletei kicsi, kerek, sárgásfehér csomók, amelyek szövettani lymphoid tüszőket képviselnek [10]. Az endoszkópos noduláris gastritis gyakoribb az antrumnál, mint a korpusz H. pylori fertőzésben.
(A) Endoszkópos leletek aktív Helicobacter pylori fertőzésben szenvedő betegeknél. (B) Noduláris gastritis a proximális antrum elülső-nagyobb oldalán. Az antrumon több apró csomó látható, amelyek a korpusz nagyobb görbületű oldaláig terjednek. A csomók submucosalis emelkedett elváltozásokból állnak, és így a nodularis gastritisben nincs színváltozás. (C) A proximális antrum és az alacsony test közötti megnagyobbodott csomók nyomon követési eredményei ugyanabban a betegben. A korábban megjegyzett apró, szabályos csomók megnövekedtek. A csomók szabálytalanok voltak, és 12 hónappal azelőtt nőttek. (D) A hemorrhagiás foltok megtalálása a funduson noduláris gastritisben szenvedő betegeknél a kezdeti endoszkópián (B). Több apró vöröses folt, úgynevezett diffúz vörösség látható a funduson és a korpusz nagyobb görbületén. (E) Hipertrófiás gyomorredők. A megvastagodott gyomor ruga fehéres, ragacsos váladékokkal jelzi az aktív H. pylori fertőzést. PG, pepszinogén.
A gyomor nyálkahártya sejtjeinek fokozott szekréciós képessége
A gyomor nyálkahártya sejtjeinek szekréciós képessége továbbra is érintetlen az aktív H. pylori fertőzés során. Ezért stimuláció vagy gyulladás esetén fokozott PG- vagy savszekréció léphet fel. Az intragasztrikus pH-szintek jól korrelálnak a H. pylori sűrűségével és a gastritis súlyosságával [11]. A H. pylori által kiváltott gyomorhurut a szérum PG szintjeivel azonosítható, mivel a PG II szint emelkedik és a PG I/II arány csökken a H. pylori fertőzésben szenvedő betegeknél a fertőzés nélküli betegekhez képest [12,13]. A szérum PG II koncentrációja hasznosabb az aktív H. pylori fertőzés előrejelzésében, mint a PG I koncentráció.
A diffúz típusú gyomorrák megnövekedett kockázata
Élettől függetlenül a noduláris gastritis növeli a gyomorrák kockázatát [14]. Noha a szérum PG-vizsgálat ismeretesebb a bél típusú gyomorrák szűrésére, mint a diffúz típusú gyomorrák, a magas PG II szint a diffúz típusú gyomorrák megnövekedett kockázatát jelzi [15-17]. Ezért a H. pylori felszámolása nagyon ajánlott az aktív fertőzés ezen szakaszában; a sejtszintű változások reverzibilisnek tűnnek, mielőtt a gyomor nyálkahártya sejtjei túljutnak a vissza nem térés pontján [18,19].
LETÖLTÉS KRÓNIKUS TÉNYLEN H. PYLORI FERTŐZÉSSEL
A krónikus fertőzés inaktív H. pylori fertőzésre utal, amely atrófiás változásokat produkál bélmetapláziával (IM) vagy anélkül. Az MG észrevehető, amikor a mirigyek elvesztése a CAG-ban IM-re fejlődik, és a nyitott típusú CAG szorosan összefügg a Cdx2 expresszióval és az MG-vel [20]. Ennek ellenére vannak korlátai a gyomorbiopsziával végzett patológiás értékelésnek MG esetén, mert nehéz meghatározni az optimális biopsziás helyet, amely lehetővé tenné a teljes gyomor értékelését [21,22].
A gyomor nyálkahártya sejtjeinek csökkent szekréciós képessége
A szérum PG I szintjének csökkenése, a nyílt típusú CAG és az időskor előrejelzi a hypoacid állapotot a H. pylori fertőzés során [23]. Miután a normál gyomormirigyeket irreverzibilis fibrózis és IM váltja fel, a gyomorkörnyezet hipo-savassá válik. Emiatt a gastrooesophagealis reflux (GERD) ritkán fordul elő CAG és/vagy MG esetén [24]. Az atrófiás gasztritisz fejlett endoszkópos osztályozása fordítottan összefügg a GERD-vel.
A gyomor korpusz atrófiája a szérum PG assay tükrében
A gyomor korpusz atrófiáját a 4. ábra szérum PG I/II arányaként határozzuk meg. Az endoszkópia megbízható, nagy reprodukálhatóságú módszer, amelyről kimutatták, hogy egy multinacionális vizsgálat megjósolja a szövettani atrófiát [28]. A gyomorhurut-stádium, az úgynevezett operatív kapcsolat a gasztritisz-felmérés (OLGA) stádiumában, információt nyújt a gyomornyálkahártyáról az atrófia-pontszám és a topográfia integrálásával [29]. Nemrégiben a kiotói globális konszenzus ülésen globális konszenzus alakult ki a krónikus gyomorhurut osztályozásáról [30]. Fontos megkülönböztetni az endoszkópos eredményeket jellemzőik alapján (5. ábra).
A fertőzések reverzibilis szakaszban felszámolódtak
Hosszú távú nyomonkövetési tanulmány kimutatta, hogy az enyhe CAG és CSG által kiváltott változások mind a szövettani, mind a szerológiai megállapításokban reverzibilisek [42]. A gyulladás és aktivitás mértéke, valamint a lymphoid tüsző beszivárgása csökken a H. pylori felszámolása után [43]. A PG II szérum jól jelzi az intragasztrikus környezeti változásokat a H. pylori felszámolása előtt és után [44].
Nevezetesen még a súlyos gyomor atrófia és az IM is reverzibilis egyes betegeknél [45]. Beszámoltak arról, hogy az alacsony szérum PG I/II arányú MG és corpus-domináns gastritis reverzibilis volt [46,47]. Éppen ellenkezőleg, a karcinogenezissel kapcsolatos molekuláris változásokban még H. pylori felszámolása után sem találtak jelentős változást [48].
A fertőzéseket visszafordíthatatlan szakaszban irtották ki
A felszámolás utáni rákkockázat a felszámolás előtti CAG mértékétől függ, és szoros összefüggésben áll a korpusz atrófia súlyosságával [49,50]. A gyomornyálkahártya visszafordíthatatlan károsodása esetén a szérum PG I szintje és a PG I/II arány tovább csökken. Ezért periodikus endoszkópos szűrés szükséges [51]. Ennek ellenére a súlyos CAG-ban szenvedő betegek csak 5% -ában alakul ki bél típusú gyomorrák [52]. Koreában nincs konszenzus a felszámolás szerepéről a gyomorrák megelőzésében [53-55], de ezeknek az alanyoknak ajánlott az endoszkópos szűrés, csakúgy, mint azoknak a koreai amerikaiaknak, akiknek ismert CAG, IM vagy családi gyomor-kórja van rák [56].
A H. pylori spontán regressziója
A spontán regresszió a gyomor atrófia és/vagy IM legsúlyosabb, késői szakaszában következik be, amikor a gyomor környezete nem vendégszerető a H. pylori növekedésére [57]. Ilyen előrehaladott körülmények között a szérum anti-H. a pylori immunglobulin G (IgG) teszt negatív eredményre tér vissza [58]. Ez jelzi a gyomor hipoatsavasságát, és indokolttá teszi a szérum PG szintjének mérését, mint a gyomorrák szűrésének másodlagos eszközét [59]. A gyomor korpusz atrófiájában és alacsony H. pylori koncentrációban szenvedő alanyok mutatják a leginkább a savas szekréció károsodását és a bél típusú gyomorrák legnagyobb kockázatát. Összességében elmondható, hogy a bél típusú gyomorrák legnagyobb kockázata a korábban fertőzött és alacsony PG I/II arányú szeronegatív alanyoknál jelentkezik [60-62].
KÖVETKEZTETÉSEK
Köszönetnyilvánítás
Ezt a munkát a Konkuk Egyetem támogatta 2016-ban.
- Gastritis kezelése Gastroesophagealis reflux betegség kezelése Helicobacter Pylori kezelés Haddon
- Az erjesztett rozskorpa termékek hatása a Helicobacter Pylori (HP) fertőzésre és az anyagcsere kockázatára
- A Helicobacter Pylori táplálkozási terve - egészséges étrend a H számára
- A dohányzás elősegíti az atrófiás gyomorhurutot a Helicobacter pylori-pozitív alanyokban SpringerLink
- Lehet, hogy a Helicobacter Pylori lehet a gyökér kiváltó oka; s nyűgös evés