Fanconi-szindróma
Mersedyes D. Boatman, BSc, PharmD jelölt
Ivan Juarez, a PharmD jelöltje
Megtestesült Szó Egyeteme
Feik Gyógyszerészeti Iskola
San Antonio, Texas
Eugene Talatala, BSc, gyógyszerészjelölt
Hawaii-Hilo Egyetem
Gyógyszerészeti Főiskola
Hilo, Hawaii
Monica Litzinger BSc, BSc Pharm, RPh
Ambuláns gyógyszerész
Suwanee, Georgia
A Fanconi-szindróma olyan betegség, amely a vese proximális tubulájának diszfunkciójával jár. A foszfát, az aminosavak, a glükóz és a hidrogén-karbonát különböző mértékű pazarlása jellemzi. 1 A klinikai megnyilvánulások a tubulus rendszer közvetlen vagy közvetett zavaraiból erednek. 2 A Fanconi gyermekeknél és felnőtteknél gyakran a csontbetegségeket mutatja be a szindróma következményeként.
Emil Abderhalden először 1903-ban vizsgálta a Fanconi-szindrómát. Egy csecsemőnél megtalálva a cisztein kristályait, „családi cisztin-diathesisnek” nevezte. 3 Guido Fanconi svájci gyermekorvos később hozzájárult a betegség megértéséhez, amikor észrevette a hasonlóságokat az általa tapasztalt esetekben. Az alanyok ezekben az esetekben törpével, hipofoszfatémiával és szerves savval ürültek a vizelettel. 3
A betegségért felelős mechanizmusok feltárásának előrehaladása továbbra is elkerüli a nyomozókat. Az intézményi körülmények között működő gyógyszerészek mélyreható hatást gyakorolhatnak, ha megismerik a Fanconi-szindrómában szenvedő betegek számára rendelkezésre álló kezelési lehetőségeket.
Epidemiológia és kórélettan
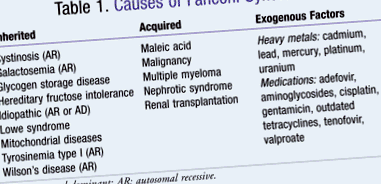
A Fanconi-szindróma ritka betegség, szórványos előfordulással és az újonnan diagnosztizált esetek jelentésével. 4 A Fanconi-szindrómát öröklött, szerzett vagy exogén tényezők okozhatják (ASZTAL 1). 5 Morbiditása másodlagos az általa generált anyagcserezavaroktól. 3 Például a foszfaturia, a glikozuria és a vese tubuláris acidózis olyan rendellenességek, amelyek a betegség következtében kialakulhatnak. Ezek befolyásolhatják a csontnövekedés kialakulását, ami serkentheti a csontbetegség megnyilvánulásait. Áttekintett tanulmányokban a veszélyeztetett személyek leggyakrabban kaukázusi fiatal gyermekek. 3 A Fanconi-szindróma egyéb, mind megszerzett, mind exogén formái esetében nincs jelentős, kedvezőtlenül érintett populáció. Az érintettek életkora változó, mivel az etiológia sokféle. Ha a betegség gyógyszeres kezeléssel, fémtoxicitással vagy más káros szerekkel való érintkezésből származik, akkor bármely életkorban jelentkezhet. Ha azonban a Fanconi-szindrómát autoszomális recesszív mintában örökölték, akkor a megjelenése általában a korai fejlődésben nyilvánvaló. 3
A fehérjéket és az oldott anyagokat a proximális tubulusok abszorbeálják speciális transzporterek és csatornák segítségével (1.ÁBRA). Ezek a csőszerű sejtmembránokban helyezkednek el, amelyek a luminális vagy bazolaterális membránon helyezkednek el. 5 A tubulusok felelősek a sav-bázis egyensúly, az ásványi homeosztázis és a gyógyszer eliminációjának szabályozásáért is. Fanconi-szindrómában az oldott anyagokat megakadályozzák, hogy áthaladjanak a proximális vese tubulus sejt apikális hálózatán. 5 A betegeknél jelentős biokémiai és transzport hordozó rendellenességek vannak, amelyek jelentős fehérjék, elektrolitok és más oldott anyagok pazarlását eredményezik. Az aminosavakat, a glükózt, a foszfátot és a hidrogén-karbonátot ezek a hordozók szállítják. Jelenleg nincs olyan jól meghatározott modell vagy mechanizmus, amely kiemelné a patofiziológia megértését. A legújabb bizonyítékok azonban alátámasztják a népszerű elméletet, miszerint a hibás transzporterek sokasága okozza az oldott anyagok pazarlását. Sokkal hihetőbb, hogy a metabolikus rendellenességek összege csökkenti az adenozin-trifoszfát (ATP) hozzáférhetőségét a Na/K ATPáz enzim számára. 6 Ez csökkenti az oldott anyag szállításának gradiensét, ami súlyos oldott anyag diszfunkcióhoz vezet.
A cystinosis a Fanconi-szindróma leggyakoribb genetikai oka a CTNS gén mutációjából eredő cisztinosin hibás funkciója miatt, amely intralysosomális cystin-felhalmozódáshoz vezet. 7 Ez a cisztinosis csecsemőtípusának korai megjelenéséhez vezet, amelyet a vese proximális tubuláris diszfunkciója jellemez a fejlődés első évében. A cisztinosin proton-vezérelt transzporterként funkcionál, amely felelős a cisztin lizoszómákból történő kiviteléért. Megfelelő bizonyíték hiányzik az intralysosomális cisztin akkumuláció és a Fanconi-szindróma közötti kapcsolatról. 7 Az örökletes Fanconi-szindróma általában cystinosisszal jár, bár az állapot kísérheti az egyéb átvitt örökletes anyagcsere-betegségeket is, mint például a Wilson-kór és a Lowe-szindróma. 8.
A mitokondriális diszfunkciót kiváltó gyógyszerek potenciálisan Fanconi-szindrómát okozhatnak. 9,10 A leggyakoribb gyógyszerek az elavult tetraciklin antibiotikumok, kemoterápiás szerek, vírusellenes szerek, aminoglikozidok és görcsoldók. Ezek a gyógyszerek különböző mechanizmusok révén indukálhatják a Fanconi-szindrómát. A tetraciklin metabolitjai vese tubulus betegségeket okozhatnak elektrolit egyensúlyhiányban, és tubuláris károsodást okozhatnak a kezelés megkezdését követő 2–8 napon belül. A Fanconi-szindróma visszafordítása akár egy évig is eltarthat. Legutóbbi állatokkal végzett kísérletek arra utaltak, hogy az ifoszfamid, a ciszplatin és a karboplatin csökkenti a vaszkuláris rezisztencia okozta véráramlást. A ciszplatin a proximális tubuláris sejtek közvetlen toxinja, ami a b2-mikroglobulin és/vagy az aminoaciduria és/vagy a proteinuria növekedését eredményezi. 9.
A tenofovir és az adefovir Fanconi-szindrómát indukál AIDS/HIV betegeknél. 10-12 AIDS/HIV nem vezet közvetlenül Fanconi-szindrómához; inkább a vírusellenes gyógyszer-metabolitok felelősek a gyógyszer által kiváltott Fanconi-szindrómáért. Szövettanilag a HIV által kiváltott nephropathiát a tubuláris sejtek apoptózisa jellemzi. Klinikai és kísérleti bizonyítékok szerint a vesekárosodás oka lehet a vírusfertőzés, mivel a proximális tubuláris sejtek HIV-specifikus receptorokat és coreceptorokat expresszálnak. 9 A mitokondriális toxicitás megállapításra került; a tenofovirot használó betegek száma azonban kifejezetten alacsony. 14
A nefrotoxicitás az aminoglikozid kórházi betegeknél történő alkalmazásának következménye. 15 Bár az amino-glikozidok által kiváltott Fanconi-szindróma ritka, az egészségügyi szakembereknek gondosan ellenőrizniük kell ezen antibiotikumok alkalmazását kritikus állapotú betegeknél; a monitorozás különösen fontos a folyadékok, az elektrolitok és a táplálkozás kezelésében. Az aminoglikozidok újra felszívódnak a proximális tubulusban, ami csökkent glomeruláris szűrési sebességet okoz. A patofiziológia bizonytalan, de úgy gondolják, hogy az aminoglikozidok visszafordíthatatlanul kötődnek a sejtmembránokhoz, és lizoszomális duzzanatot okoznak. 15,16
A Fanconi-szindróma a valproinsav-indukálta vesekárosodás spektrumának szélső végét jelenti. Korábbi tanulmányok kimutatták, hogy a vesekárosodás magából az epilepsziából ered, nem pedig a gyógyszerből. Ezenkívül a valproinsav által kiváltott Fanconi-szindróma a gyermekek számára kizárólagosnak tűnik, és általában enyhíti a gyógyszer abbahagyását. 17.
Klinikai előadás
A Fanconi-szindróma klinikai bemutatása a proximális tubuláris transzport különböző hibáinak köszönhető. Ide tartozik a glükóz, foszfát, aminosavak, hidrogén-karbonát, húgysav, víz, kálium és nátrium visszaszívódása. 18 Az örökletes Fanconi-szindróma a proximális tubuláris vese acidózist, hipofoszfatémiás rachitát, hipokalémiát, polyuriát és polydipsiát (általában csecsemőkorban) jellemzi. 18 A Fanconi a cystinosis, a növekedés retardációja, a retina depigmentációja, az interstitialis nephritis és a progresszív veseelégtelenség eredménye. A megszerzett Fanconi-szindróma kissé eltérő rendellenességekkel jár, például vese tubuláris acidózissal, hipofoszfatémiával, hipokalémiával, osteomalaciával és izomgyengeséggel (2. TÁBLÁZAT). 18.
Kezelés
A Fanconi-szindróma elsődleges terápiája a kiváltó okok kezelése és a vizelettel pazarolt anyagok pótlása. A folyadékokat és az elektrolitokat orális vagy parenterális úton adják be a polyuria következtében kialakuló kiszáradás miatt, amely cystinosisos betegeknél meghaladhatja a napi 2-6 liter híg vizeletet. Akut állapotban a betegnek nagy bolusmennyiségre lehet szüksége a test teljes vizének helyreállításához, ezért gyakran ellenőrizni kell. A szájon át történő vagy a szülői rehidratációra vonatkozó döntés attól függ, hogy a beteg képes-e szájon át folyadékot fogyasztani, a veszteségek helyreállításához szükséges teljes becsült mennyiségtől és a kiszáradás észlelt súlyosságától.
A metabolikus acidózist a vese károsodott képessége okozza, hogy felszívja a normál bikarbonát-szintet. Akut körülmények között kis mennyiségű intravénás nátrium-hidrogén-karbonát bolus felhasználható a vér pH-értékének emelésére. 20 Krónikus terápiában a hidrogén-karbonátot orálisan adagolják, 3-15 mEq/kg/nap tartományban; keserű íze van, és emésztőrendszeri (GI) zavart okozhat. 20-24 citrát sókat adagolunk az általuk generált hidrogén-karbonát-ekvivalensek mennyisége alapján. Például a Cytra-K, amely kálium-citrátot és citromsavat tartalmaz, 2 mEq káliumot és 2 mEq bikarbonátot hoz létre ml-enként. 25 Bikarbonát hozzáadása a vérhez növelheti a sejtek káliumfelvételét; ezért a szérum elektrolitok monitorozása elengedhetetlen azoknál a betegeknél, akik már hajlamosak a hypokalemiára a Fanconi-szindróma miatt. A térfogat-tágulás és a hidrogén-karbonát kiválasztásának minimalizálása érdekében gyenge vizelethajtót, például hidroklorotiazidot alkalmazunk 1-3 mg/kg/nap dózisban. Ez a vízhajtó azonban nem kímél káliumot; ezért kálium-kiegészítést kell előírni.
A metabolikus acidózist a bikarbonátpótló folyadékkal kell korrigálni, de ez önmagában nem fogja korrigálni a csontbetegség patogenezisét. A jelentős foszfátveszteség miatt pótlása a D-vitaminnal együtt is szükséges. Az optimális foszfátszint a szérumban 1-3 g/nap kiegészítő foszfáttal érhető el. A beteget a legalacsonyabb dózissal kell elkezdeni, majd az optimális tartományba kell titrálni a GI irritációjának elkerülése érdekében. A hipokalémia elleni profilaxishoz napi 20 mEq orálisan adható be, majd szükség szerint titrálható 100 mEq-ig, felnőtteknek naponta ötször adva. 26,27 gyermek napi 3-8 mEq/kg/nap dózisban, osztott adagokban, napi egy-ötször. A D-vitamin pótlását aktív formájában kell beadni a májfunkció lehetséges károsodása miatt.
A mögöttes genetikai okok általában a tápanyagok metabolizmusában hibás enzimet jelentenek, ami a proximális tubulus károsodását eredményezi. Örökletes galaktozémiában, fruktóz intoleranciában és tirozinémiában szenvedő betegek számára előnyös lenne, ha étrendjükből korlátoznák a galaktóz, a fruktóz és a tirozin, illetve a fenilalanin mennyiségét. 21 A Wilson-kórban szenvedő betegeket arra kell ösztönözni, hogy alacsony réztartalmú étrendet fogyasszanak (például korlátozzák a szervi húsok, kagylók és teljes kiőrlésű állatok fogyasztását), és vegyenek be D-penicillamint a kedvező eredményekre utaló tanulmányok miatt. 4,28 A testmozgást is korlátozni kell, mivel a szervi elégtelenség vagy az izomerő jelentős csökkenése származhat a genetikai állapotokból.
A ciszteamin (Cystagon) egy FDA által jóváhagyott gyógyszer, amelyet a cystinosis kezelésére használnak. 27,28 Úgy működik, hogy reagál a lizoszómákba befogott cisztinnel, majd exportálja, így csökkenti a sejtkárosodás kiváltására rendelkezésre álló terhelést. A kezdeti adagok a fenntartó adag egynegyede – hatod része, és 4–6 héten át a kezdeti fenntartó adagig kell titrálni. Gyermekgyógyászati betegeknél a kezdeti fenntartó adag 1,3 g/m 2/nap, elosztva naponta négyszer. 12 évesnél idősebb és 110 fontnál nagyobb betegeknél a kezdeti fenntartó adag napi négyszer 500 mg. A terápia célja, hogy a leukocita cisztin szintjét 1 nmol fél-cisztin/mg fehérje alatt tartsa, ha a gyógyszer beadása után 5-6 órával mérjük. E cél elérése érdekében mindkét korcsoport dózisa legfeljebb 1,95 g/m2/nap maximális dózisra titrálható. A mellékhatások közé tartozik a letargia, hasmenés, görcsrohamok, GI toxicitás, vérszegénység és remegés. Nincs ismert gyógyszerkölcsönhatás a ciszteaminnal. A penicillaminra allergiás betegeket gondosan ellenőrizni kell a nemkívánatos események előfordulása szempontjából, amikor ciszteamint adnak. 27.
Monitoring
A Fanconi-szindrómában szenvedő betegek monitorozása a terápia döntő része, függetlenül a betegség patogenezisétől vagy etiológiájától (3. TÁBLÁZAT). A Fanconi-szindrómát befolyásoló belső és külső tényezők a beteglátogatások gyakorisága, a súlyosság mértéke, a folyadék- és elektrolitegyensúly, valamint a gyógyszerek hatékonysága és mellékhatásai. 5 A megszerzett Fanconi-szindrómában szenvedő betegek kezelhetők a toxinoknak (pl. Ólom, elavult tetraciklinek, aminoglikozidok) való kitettség megelőzésével és a tünetek enyhítésével az étrendi módosításokkal rendelkező gyermekeknél. A beteg prognózisa függ a szindróma okától, valamint a vese- és extrarenalis megnyilvánulások súlyosságától. A genetikai formákat nehéz kezelni, általában a növekedés zavaraival társulnak, és más szerveket is érintenek. 5.
A kisgyermek szüleinek tanácsot kell adniuk a betegség tüneteinek megelőzésére vagy csökkentésére irányuló stratégiákról. A szülőknek történő tanácsadás, hogy megakadályozzák gyermekeik ólomnak való kitettségét, és az elavult antibiotikumok kerülése, a gyermekgondozás fontos része. A galaktozémiától vagy tirozinémiától másodlagos Fanconi-szindrómás gyermekeknek speciális étrendi utasításokat kell adni az elviselhetetlen tápanyagok étrendjükből való kiküszöbölésére. 5.
Következtetés
A Fanconi-szindróma kiterjedt klinikai bemutatása számos nehézséget okoz az egészségügyi szakemberek számára. A betegek hatékony diagnosztizálása és kezelése aggodalomra ad okot a betegség patofiziológiájáról rendelkezésre álló korlátozott információk miatt. Bár az alapul szolgáló szövődmények és az elektrolit-egyensúlyhiány kezelésére elegendő lehetőség áll rendelkezésre, a terápiás előrelépéseket még mindig el kell érni. A ritka betegséggel kapcsolatos további kutatások szükségesek a jelenlegi gyakorlat kialakításához. Létfontosságú, hogy a gyógyszerészek ismerjék a gyógyszerek által a Fanconi-szindróma kiváltásában és kezelésében betöltött szerepet. A rendelkezésre álló farmakológiai kezelések megértése segíthet a betegek tüneteinek és általános eredményeinek javításában.
- Testmozgás, diétázás javította a termékenységet a policisztás petefészek szindrómában szenvedő nőknél
- Alveoláris hipoventilációval járó rendkívüli elhízás - egy pickwicki szindróma - ScienceDirect
- A metabolikus szindróma jellemzői kórosan elhízott alanyokban - PubMed
- Diéta irritábilis bél szindrómában
- Crigler Najjar-szindróma 2-es típusú (CNS-2-es típusú) sárgaság nem kívánt oka felnőtteknél