Fekete kömény
Kapcsolódó kifejezések:
- Kurkuma
- Nitrogén-oxid
- Oxidatív stressz
- Fokhagyma
- Görögszéna
- Gyömbér
- Paeonia
- Ranunculaceae
- Leporidae
Letöltés PDF formátumban
Erről az oldalról
Az afrikai gyógynövények szubkrónikus és krónikus toxicitása
6.7.11 Nigella sativa Linn. (Ranunculaceae)
Az afrikai gyógyfűszerek és zöldségek gyulladáscsökkentő és anti-nociceptív tevékenységei
3.5 Nigella sativa
Diétás fűszerek a reumás ízületi gyulladás megelőzésében
5.2.4 Fekete kömény
A Nigella sativa növényt, amely eredetileg Dél-Európában, Észak-Afrikában és Délnyugat-Ázsiában őshonos, ma a világ számos országában termesztik, beleértve a Földközi-tenger közép-keleti régióját, Dél-Európát, Indiát, Pakisztánt, Szíriát, Törökországot és Szaúd-Arábiát [ 25]. A magok a legfontosabb növényi részek, és ezeket az idők óta használják az orvostudomány különféle hagyományos rendszereiben, például Unani-Tibb, Ayurveda és Siddha, különféle betegségek kezelésére [25]. A magok és az olaj hosszú múltra tekint vissza a folklórhasználatban, széles körben használják vérnyomáscsökkentőként; májtónusként, vízhajtóként, emésztési, hasmenés elleni, étvágygerjesztõ és antibakteriális szerekként; bőrbetegségek esetén; és fájdalomcsillapítóként [25]. A közelmúltban elvégzett tudományos vizsgálatok igazolták az etnomedicinális felhasználást, és a jelentések szerint antidiabetikus, rákellenes, immunmoduláló, fájdalomcsillapító, antimikrobiális, gyulladáscsökkentő, spasmolyticus, bronchodilatator, hepatoprotective, vesét védő, gastroprotective, antioxidáns és rákellenes tulajdonságok [25,26]. Tanulmányok azt is kimutatták, hogy a thymoquinon, amely a mag illóolajának fő bioaktív összetevője, számtalan előnnyel rendelkezik, és működésében pleiotróp [25–29] .
Antiarthritikus hatásaival kapcsolatban a vizsgálatok kimutatták, hogy a thymoquinone hatékonyan csökkentette a patkányokban a hiányos Freund-adjuváns (IFA) által kiváltott ízületi gyulladás által kiváltott gyulladást és ízületi gyulladást, a klinikai és radiológiai osztályozással értékelve [30]. Részletes vizsgálatok kimutatták, hogy a placebóval kezelt kohorszokhoz képest a thymoquinone beadása a TNF-α és az IL-1β szintjének csökkenését okozta [30]. Későbbi vizsgálatok kimutatták, hogy a thymoquinone orális beadása ízületi gyulladású patkányoknak az ízületi gyulladás pontszámának és a csontreszorpciónak, valamint a csontforgalom markereknek, például az alkalikus foszfatáznak és a tartarát-rezisztens savas foszfatáznak a csökkenését okozta [31]. .
Emellett humán RA fibroblaszt-szerű szinoviocitákkal végzett sejttenyésztési vizsgálatok azt is kimutatták, hogy a thymoquinone gátolta a szinoviociták lipopoliszacharid (LPS) által kiváltott proliferációját, a H2O2 által indukált 4-hidroxinonenal képződését és az IL-1β, TNF-α, metalloproteinase szintjét. -13, ciklooxigenáz-2 és prosztaglandin E2 [31]. A thymoquinone időfüggő módon blokkolta a p38, MAPK, ERK1/2 és NF-KB p65 LPS-indukálta foszforilációját [31]. Ezenkívül tanulmányok kimutatták, hogy a thymoquinone orális beadása ízületi gyulladású patkányoknak csökkenti a HNE, az IL-1β és a TNF-α szérumszintjét [31] .
Klinikai vizsgálatok azt is kimutatták, hogy a napi kétszer 500 mg-os Nigella sativa olaj kapszula fogyasztása szignifikánsan csökkentette a betegség aktivitási pontszámát (DAS-28) RA-ban szenvedő betegeknél a placebó előtt és után. [32] Hasonlóképpen javult a duzzadt ízületek száma és a reggeli merevség időtartama. A betegség aktivitásának jelentős javulását mutatta mind az ACR20, mind az EULAR válaszkritérium a betegek 42,5% -ánál, illetve 30% -ánál Nigella bevétele után [32]. Ezek a megfigyelések együttesen egyértelműen jelzik, hogy a Nigella sativa-val történő kiegészítés RA-ban a DMARD-terápia során megfizethető potenciális adjuváns biológiai terápiának tekinthető [32]. .
Biztonságos afrikai gyógynövények a klinikai vizsgálatokhoz
Theophine Chinwuba Okoye,. K. Okereke Emeka, az afrikai gyógynövények toxikológiai felmérésében, 2014
18.2.24. Nigella sativa L. (Ranunculaceae)
A Nigella sativa magjait (közismert nevén fekete mag vagy fekete kömény) a népi gyógyászatban számos olyan betegség kezelésére és megelőzésére használják, amelyek közé tartozik az asztma, a hasmenés és a dyslipidaemia. Kimutatták, hogy a magok biológiai aktivitásának nagy része a thymoquinonnak köszönhető. A thymoquinonról beszámoltak arról, hogy görcsoldó és rákellenes hatásokkal rendelkezik [77]. A magok és néhány aktív alkotóelemének jelentett farmakológiai hatása magában foglalja a nephrotoxicitás és a hepatotoxicitás elleni védelmet, valamint a gyulladáscsökkentő, fájdalomcsillapító, lázcsillapító, antimikrobiális, daganatellenes, immunológiai, vérnyomáscsökkentő, légzést stimuláló, hematinikus és tripanocid aktivitást [78,79]. A magkivonat alacsony fokú toxicitást mutatott, és bebizonyosodott, hogy nem okoz jelentős káros hatást a máj vagy a vese működésére. Úgy tűnik, hogy a magok és a thymoquinone alkalmazásának jótékony hatása összefüggésben állhat citoprotektív és antioxidáns hatásukkal, valamint a gyulladás egyes közvetítőire gyakorolt hatásukkal [78]. .
Álmatlanság
Fekete kömény
Khanna és mtsai (1993) azt találták, hogy a fekete kömény (Nigella sativa) illóolaj nyugtató hatása erősebb volt, mint a klórpromazin (Largactil) gyógyszer, és fájdalomcsillapító. A tanulmány szerint a fekete kömény opioidszerű komponenst tartalmazott. Újabb állatkísérletek egereken az anksiolitikus hatásokra (Gilhotra & Dhingra 2011) és a görcsgátló hatásokra (Hosseinzadeh & Parvardeh 2004) összpontosítottak. Érdekes lenne a belélegzett fekete köményt tanulmányozni az emberi álmatlanságról. Mivel a fekete kömény erős, csípős aromával rendelkezik, valószínűleg „lágyítani” kellene egy másik nyugtató aromával, például levendulával, klarisszával vagy római kamillával.
Alkaloid kémia
2.9.3.3 Vetőmagszín módszer
Azt az egyszerű megfigyelést, miszerint a fehér magvak édesebbek, a fekete magokat alkalmazták a csillagfürtmagok minőségi megítélésének gyakorlati módszerének felépítésében. Ez a módszer nem alkalmazható magabiztosan, mert különösen a fehér csillagfürtnél még a nagyon fehér magvak is magas alkaloidtartalommal bírnak. Másrészt az azonos fajba tartozó növények „édesek”. Egyes fajokban, például a L. angustifolius vagy az L. luteus esetében a fehér magvak hajlamosabbak „édesre” válni, de nem teljesen biztos.
Thymoquinone
Bhanushree Gupta,. Ramesh C. Gupta, Nutraceuticals, 2016
Absztrakt
A thymoquinone (TQ) a fekete magolaj (Nigella sativa) fő bioaktív alkotóeleme. A TQ ígéretes farmakológiai tulajdonságokkal rendelkezik számos betegség ellen. Kiemelkedő antioxidáns, gyulladáscsökkentő, rákellenes és más fontos biológiai aktivitást mutat. A TQ hatékonyan átalakítja a rák progressziójának szignál útjait. Nem csak javítja a kemoterápiás gyógyszerek rákellenes aktivitását, hanem csillapítja mellékhatásukat is. Figyelembe véve a TQ rendkívüli aktivitását, ez a fejezet a TQ eredetét és farmakológiai jellemzőit számolja fel. Nemrégiben tárgyaltak a közelmúltban elért eredmények kémiai módosítások formájában, és a TQ-analógok kialakításának semmilyen formulájáról. Végül összefoglaljuk a TQ adjuváns hatékonyságának jelenlegi állapotát és in vivo toxicitását.
A thymoquinone terápiás potenciálja a reumás ízületi gyulladás és a kapcsolódó autoimmun betegségek kezelésében
2 Thymoquinone a reumás és autoimmun betegségek ellen
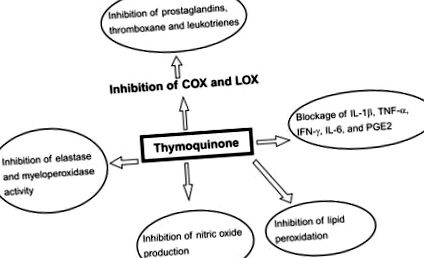
33.3. Ábra A thymoquinon mechanizmusa.
A gyulladásos folyamat közvetítését még mindig nem értik, mivel a citokinek komplex folyamatából áll. Manapság a mitogén-aktivált protein kináz (MAPKs) p38 potenciális terápiás célpontként vonzotta a kutatók figyelmét, mivel képes elnyomni a legfontosabb gyulladásos mediátorok termelését. Az oxidatív stressz, a kalcium túlterhelés és a gyulladásos citokinek, mint például a tumor nekrózis faktor α (TNF-α) aktiválják az apoptózis szignált szabályozó kináz 1-et (ASK1, a MAP3K család tagja), amely tovább aktiválja mind a JNK, mind a p38 MAPK utakat. Ezért az ASK1 ígéretes terápiás célpontként szolgálhat RA-ban, mivel szabályozza a gyulladásos citokin felszabadulást, és aktivitását foszforilezés és más fehérjékkel való kölcsönhatások szabályozzák. A ROS az egyik tényező, amely aktiválja az ASK1-et azáltal, hogy az ASK1 defoszforilezését indukálja a Ser967-nél, valamint a Thr845 foszforilezését az ASK1 aktivációs hurokban.
Egy másik tényező, a TNF-a szintén fokozza az ASK1 foszforilációját a Thr845-nél és aktiválja. A thymoquinonról kiderül, hogy hatékonyan gátolja az ASK foszforilációját, ezáltal lassítva a downstream jelátviteli utat. Aktiválás után a MAP kinázok az ingert az mRNS transzlációjában bekövetkező patofiziológiai válaszokká is átalakítják azáltal, hogy foszforilálják a downstream szubsztrátumokat, beleértve a transzkripciós faktorokat és a citoszkeletális fehérjéket. A thymoquinonról kiderül, hogy erős kis molekula ezen stimulációs folyamatok gátlásában. 22.
A lupusról jelentett fitokémiai anyagok ugyanazon filozófián keresztül hatnak az RA gyulladásos mediátorainak gátlására. A lupuszban a fitokémiai anyagok gátolják a gyulladásos mediátor (PGE2, IL-17a, Th sejtek, IFN-γ és IL-6 stb.), A LOX enzim és a COX enzim szintjét. Egyes fitokemikáliák csökkentik az autoantitestek termelését és gátolják az immun komplex (autoantitestek és autoantigén komplex) képződését, ami a szövetkárosodás gátlását eredményezi (33.2. Táblázat).
33.2. Táblázat Jelentett fitokémiai hatás a lupus 23–25
| Aconitin | Csökkent PGE2, IL-17a és IL-6 szint |
| Kurkumin | Csökkent PGE2, IL-17a és IL-6 szint |
| Dehyroepiandrosterone | Csökkent PGE2, IL-17a és IL-6 szint |
| Docosahexaenoic | A lipoxigenáz gátlása, gátolja az NF-κB-t |
| Eikozapentaénsav | A lipoxigenáz gátlása |
| Izofl avonok | Az autoantitestek termelésének gátlása |
| l -Canavanine | A T-sejtek szuppresszor-induktora |
| N-acetil-cisztein | Csökkent PGE2, IL-17a és IL-6 szint |
| Omega 3 zsírsavak | Csökkent PGE2, IL-17a és IL-6 szint |
| A-vitamin | A Th-sejtek aktivitásának hibái |
| B-vitamin | A homocisztein szint csökkentésének elősegítése |
| C vitamin | Csökkenti az IgG-t |
| D-vitamin | Gátolja a Th proliferációját, csökkenti az IL-2 és az IFN-y szekrécióját |
| E-vitamin | A PGE2, a leukotrién B4 és a tromboxán B redukciója |
| Ω-3 PUFA | Elnyomja a makrofágok aktivitását és a ciklooxigenáz termelését |
Ezek mellett számos felfedezetlen és be nem jelentett fitokémiai anyag is található, amelyeket alaposan meg kell vizsgálni. Az RA és a lupus patofiziológiájában számos célpont van, amelyek egy új fitokémiai anyag tanulmányozása során megcélozhatók. Mivel ezek a gyógyszerek csak a gyulladás tüneteit gyógyítják, például fájdalmat és duzzanatot RA-ban és lupusban, nem pótolják az okozott kárt. Széles megközelítésre van szükségünk az autoimmun betegségek (RA és lupus) területén, és olyan új fitokémiai molekulákat kell felfedeznünk, amelyek helyreállítják a sérült szöveti integritást.
Öt- és hattagú kondenzált rendszerek hídfő (gyűrűs csomópont) heteroatomokkal: 6-6 biciklus egy vagy két N vagy más heteroatomgal; Policiklusos; Spirociklusos
12.10.15.1 Természetes termékek
Alkaloidok nigellicin 257 és nigellidin 672 a Nigella sativa magjaiból izoláltakat a CHEC-II (1996) említi. A Chemical Abstracts referencia alapján mindkét alkaloid teljes szintézisét megemlítették a CHEC-II (1996). A három természetes termék: Nigellicine, Nigellidine és Chilenone-A (Guneratne, R. D., Cornell University, 1988) tézise címe azonban félrevezető, mivel a tézis nem írja le az említett alkaloidok szintézisét. Nemrégiben egy új alkaloid nigeglanin izolálása 673 a Nigella glandulifera magjairól számoltak be. Beszámoltak a nigellicin és a nigeglanin-hidrobromid első köztes közbenső szintéziseiről .
A reproduktív rendszer
Robert Tisserand, Rodney Young PhD, Essential Oil Safety (Második kiadás), 2014
Szülés
Számos illóolaj csökkenti a méhösszehúzódásokat elszigetelt macska vagy patkány méhekben. Ide tartoznak a fekete magok, kömény, édeskömény (édes), gyömbér, kanuka, levendula, manuka, pennyroyal, rue, savin, tansy, teafa, tökviasz (Bupleurum fruticosum), kakukkfű, Zataria multiflora (41,4% carvacrol, 21,2%) timol) és terpentin, a petrezselyem-apiol, (+) - δ-3-carene, 1,8-cineole, citral, ligustilide, piperitone, (1R) - (+) - β-pulegone és α-terpineol összetevõin kívül. (Macht 1913; Lorente és mtsai 1989; Ocete és mtsai 1989; Aqel és Shaheen 1996; Lis-Balchin és Hart 1999; Lis-Balchin és mtsai 2000; Ostad és mtsai 2001; Sadraei 2003; Soares PM és mtsai 2005; Du és mtsai 2006a; Buddhakala és mtsai 2008; Ponce-Monter és mtsai 2008).
Néhány konkrétumot megadva, egy ex vivo patkányvizsgálat során az édes édeskömény olaj dózisfüggő csökkenést mutatott az oxitocin vagy a prosztaglandin E2 (PGE2) által kiváltott méhösszehúzódások intenzitásában. Némi hatást észleltek az oxitocin esetében 25 μg/ml és a PGE2 esetében 10 μg/ml értéket; szignifikánsabb hatásokat észleltek az oxitocin esetében 50 μg/ml, a PGE2 esetében pedig 20 μg/ml-t (Ostad et al 2001). A fekete magolaj koncentrációjától függően gátolta a patkány és a tengerimalac méh simaizomzatának spontán mozgását, valamint az oxitocin stimuláció által kiváltott összehúzódásokat (Aqel és Shaheen 1996). Hasonlóképpen, a Bupleurum gibraltaricum illóolaja (33,0% δ-3-karén) és a δ-3-karén antagonizált oxitocin által kiváltott összehúzódásokat patkány méhében (Ocete és mtsai 1989).
Bár ezeknek az olajoknak némelyike hasznos alkalmazási lehetőségekkel bírhat, például dysmenorrhoában, azt lehetne állítani, hogy nem szabad használni a nem jól haladó vajúdás alatt. Azonban semmit sem tudunk ezen eredmények klinikai jelentőségéről az emberi szülés szempontjából. Az illóolajok fent felsorolt változatos összetevői miatt valószínűnek tűnik, hogy sok más hasonló aktivitást tud felmutatni. Mivel nincs olyan illóolaj, amelyről kiderült, hogy stimulálja a méh összehúzódását, a görcsoldó hatás szinte minden illóolaj nem specifikus hatása lehet ex vivo teszteléskor.
Az aromaterápia alkalmazása a szülés során egyre népszerűbb gondozási lehetőség volt az anyák és a szülésznők körében egy nyolc éves megfigyelési tanulmány során, az angliai John Radcliffe Kórházban, Oxfordban. Összesen 8058 anya leendő adatait elemezték, akik 1990 és 1998 között születtek, és az egységvizsgálat egyidejű adatai 15 799 olyan anya összehasonlító csoportját szolgáltatták, akik nem alkalmazták az aromaterápiát. A nőknek illóolajokat kínáltak a szorongás, a fájdalom, az émelygés és/vagy a hányás enyhítésére vagy az összehúzódások erősítésére. Az illóolajok a következők voltak: kamilla (marokkói), clary zsálya, eukaliptusz, tömjén, jázmin abszolút, levendula, citrom, mandarin, borsmenta és rózsa abszolút.
Az aromaterápia minden nő számára elérhető volt, aki a szülőcsomagban jelent meg, a kockázati tényezőktől függetlenül. Az egyetlen kizárás a beleegyezés hiánya és a többszörös allergiás nők voltak. A minta 60 százaléka (4834) volt először terhes, és összességében 32% -ának (2578) volt a munkája. Úgy tűnt, hogy az aromaterápia szüléskor csökkenti az anyák egy részének további fájdalomcsillapítás szükségességét. Az első terhesek több mint 8% -a (387), és a nem 18 évesnél 18% (580) nem alkalmazott hagyományos fájdalomcsillapítást az illóolajok használata után a vajúdás során. A vizsgálat évei alatt a petidin használata a tanulmányi központban a nők 6% -áról 0,2% -ára csökkent. Az eredmények azt sugallják, hogy az aromaterápia fokozhatja a diszfunkcionális vajúdásban szenvedő nők összehúzódásait. Az aromaterápiát alkalmazóknál a nők 1,0% -a (100) számolt be káros hatásokról, amelyek között hányinger, kiütés, fejfájás és gyors vajúdás szerepelt, bár nem ismert, hogy ezek valamelyikét illóolajok okozták-e, és nincs információ a káros eseményekről az összehasonlító csoportba gyűjtöttük (Burns et al 2000).
Egy kísérleti RCT-ben 251 nő részesült aromaterápiában a vajúdás során, 262 kontroll mellett. Az öt illóolaj egyikét alkalmazták az aromaterápiás csoport minden résztvevőjére: római kamilla, levendula, tömjén, mandarin vagy klary zsálya. Az alkalmazási módok közé tartozott az akupresszúra, a masszázs, a kúp (egy csepp illóolaj a ruházatra erősített nedvszívó papírcsíkon), a borogatás, a lábfürdő vagy a szülőmedence. Nem voltak szignifikáns különbségek a következő eredmények tekintetében: császármetszés, ventouse, Kristeller-manőver, spontán hüvelyi szülés, első és második szakaszos augmentáció. Lényegesen több csecsemőt, akiket a kontroll résztvevők születtek, áthelyeztek egy újszülött intenzív osztályra, 0 szemben 6 (2%), és a nullaparae aromaterápiás csoportjában csökkent a fájdalomérzékelés (Burns et al 2007).
Állítólag a vajúdó nők belélegzése a vajúdó nőknél minimálisra csökkenti a fájdalmat és a szorongást, nincs káros hatása az anyára vagy a magzatra (Huntose et al 1999). Ezek a tanulmányok azt sugallják, hogy az aromaterápia előnyei a vajúdás alatt meghaladják a kockázatot, legalábbis szakképzett egészségügyi szakember felügyelete mellett.
- Atkins Diet - áttekintés a ScienceDirect témákról
- Blue Whiting - áttekintés a ScienceDirect témákról
- Auriculoterápia - áttekintés a ScienceDirect témákról
- Atrófiás gyomorhurut - áttekintés a ScienceDirect témákról
- Hajdina - áttekintés a ScienceDirect témákról