Hidrogén-szulfid
A hidrogén-szulfid (H2S) egy metabolit és jelző molekula a biológiai szövetekben, amely számos fiziológiai folyamatot szabályoz.
Kapcsolódó kifejezések:
- Metabolikus út
- Cisztein
- Szulfát
- Nitrogén-oxid
- Szulfid
- Alfa-oxidáció
- Baktérium
Letöltés PDF formátumban
Erről az oldalról
Hidrogén-szulfid
Környezeti expozíció (Levegő, víz, üledék, talaj és bióta monitoring adatai)
A hidrogén-szulfid koncentrációja a környezeti levegőben 0,11–0,33 ppb és a városi területeken általában
Hidrogén-szulfid
Leonard G. Forgan, John Alexander Donald, a Hormonok kézikönyvében, 2016
Felfedezés
A hidrogén-szulfid (H 2S) egy természetben előforduló vegyület, amely számos fizikai és biológiai rendszerben gazdag. Magas koncentrációban akutan mérgező, a toxicitás a mitokondriális citokróm c-oxidáz (CCO), karboanhidráz (CA), monoamin-oxidáz, Na +/K + -ATPáz és kolinészterázok gátlásának tulajdonítható [1]. A H2S fiziológiai jelátviteli tulajdonságait csak 1996-ban ismerték fel. Eredetileg neuromodulátorként azonosították [2], azóta rengeteg tanulmány jelent meg, amelyek bizonyítják a H2S szerepét a szív- és érrendszerben, és szinte az összes többi, eddig megvizsgált szervrendszert [3]. .
Hidrogén-szulfid
C Hatásmechanizmusok
Kimutatták, hogy a hidrogén-szulfid nagyszámú enzimrendszerrel lép kölcsönhatásba (pl. Lúgos foszfatáz, adenozin-foszfatáz és a fehérjeszintézisben részt vevők), de a citokróm-oxidázt a toxicitás kritikus célpontjaként azonosították. Ez hasonló a cianid hatásához, de valamivel erősebb. A citokróm-oxidáz részt vesz az elektrontranszport rendszerében az oxidatív foszforilációban, amely sejtenergiát generál. Az enzimgátlás tehát csökkent oxigénellátást és celluláris anoxiát eredményezne. A funkcionális hisztotoxikus (szöveti toxicitás) hipoxiát javasolták a toxicitás elsődleges mechanizmusaként a magas O 2 igényű szövetekben. A H2S nem rontja az O2 hemoglobin általi transzportját, és nem okozza a szulfhemoglobin képződését sem, amint azt a korábbi vizsgálatok kimutatták. Alacsony koncentráció esetén a H2S gátolhatja a hem szintézisét is, és esetleg megzavarhatja a vas anyagcseréjét. A biokémiai hatások mellett a nyálkahártyákra gyakorolt közvetlen irritáló hatások és az ingerlõ szövetek stabilizálása (azaz érzéstelenítése) is szerepet játszhatnak az általános toxikus reakciókban.
Hidrogén-szulfid a redoxbiológiában, B. rész
Burcu Gemici, John L. Wallace, in Methods in Enzymology, 2015
Absztrakt
Hidrogén-szulfid a Redox Biology-ban, A. rész
Vivian S. Lin,. Christopher J. Chang, in Methods in Enzymology, 2015
Absztrakt
A hidrogén-szulfid egy redox aktív kénfaj, amely az emlős rendszerekben endogén módon képződik antioxidáns és jelátviteli molekulaként a sejtszint működésének támogatására. A hidrogén-szulfid alapvető és mindenütt jelenlévő műveletei érzékeny és specifikus módszereket követelnek meg ennek a biomolekulának a nyomon követésére, mivel időbeli és térbeli szabályozással az élő szervezeteken belül termelődik. Ebben az összefüggésben az azid hidrogén-szulfiddal közvetített aminokká történő redukciója hasznos módszer a szerves szintézishez, és ezt a reakciót sikeresen kihasználták biokompatibilis fluoreszcens próbák előállítására a hidrogén-szulfid detektálására in vitro és sejtekben. Ez a fejezet protokollokat és útmutatásokat tartalmaz az azid alapú fluoreszcencia szondák alkalmazásához a kén-szulfid kimutatására élő rendszerekben, beleértve egy protokollt, amelyet az endogén kén-szulfid kimutatására használtak élő egyetlen sejtekben konfokális mikroszkóppal.
Környezeti mérgek és a szív
Sahand Rahnama-Moghadam,. Richard A. Lange, a Heart and Toxins-ban, 2015
3.20.7 Hidrogén-szulfid
A hidrogén-szulfid egy vízben oldódó, színtelen gáz, amelynek rothadt tojások szaga kifejezett. A 100–150 ppm feletti koncentrációjú hidrogén-szulfidnak kitett emberek 2–15 perc folyamatos expozíció után a szaglási fáradtság miatt elveszíthetik a hidrogén-szulfid szagát. 310 311 Szénhidrogént szennyvíziszapból, folyékony trágyából, kénes forrásokból és földgázból állítanak elő. Ez különféle ipari folyamatok mellékterméke, például kőolaj-finomítás, fatermék-feldolgozás, műselyemgyártás, trágya-feldolgozás, cukorrépa-feldolgozás, halfeldolgozás és forró aszfaltburkolat. Toxikusságának mechanizmusa a mitokondriális sejtlégzés megszakításával történik a citokróm-oxidáz inaktiválása révén. 310,311
Hidrogén-szulfiddal mérgezett betegeknél nyálkahártya károsodás, hemoptysis, tachycardia, cyanosis, tejsavas acidózis és eszméletvesztés léphet fel. A miokardiális infarktust, a szívizomgyulladást és a dilatált kardiomiopátiát mind leírták a hidrogén-szulfid expozíciót követően. 310 A hidrogén-szulfid kimutatása az expozíció gyanúja esetén a tioszulfát szintjének mérésével végezhető a vér vagy a szövet kromatográfiájával. 311,312
A hidrogén-szulfid-mérgezés áldozatait el kell távolítani az expozíció helyéről, és oxigént kell beadni. A hiperbarikus oxigén felhasználható, bár hatékonyságának bizonyítéka anekdotikus. 310,313 Az inhalált amil-nitritet és az intravénás nátrium-nitritet antidotumokként alkalmazták, és hatásosak, ha a hidrogén-szulfid expozíciótól számított néhány percen belül beadják. A nitritek methemoglobint indukálnak, amely versenyképesen megköti a szulfidiont, felszabadítva ezzel a citokróm-oxidázt. A kapott vegyület, a szulfmethemoglobin metabolizálható és kiválasztódhat. 312 Óvatosan kell eljárni, mert a nitritek hipotenziót válthatnak ki, a methemoglobin pedig csökkentheti az oxigén szállítását.
Hidrogén-szulfid a Redox Biology-ban, A. rész
Xinggui Shen,. Christopher G. Kevil, in Methods in Enzymology, 2015
1.2 Hidrogén-szulfid medencék
A hidrogén-szulfidot számos forrásból állítják elő, ideértve a kémiai reakciókat (például hidrogéngáz és elemi kén, vas-szulfid és HCl, alumínium-szulfid és víz), a szulfát-redukáló baktériumokat és az emlősök szöveteiben. Az emlős szövetekben a hidrogén-szulfid termelés során három szövetspecifikus enzim vesz részt, nevezetesen a cisztationin-β-szintáz, a cisztationin-γ-liáz és a 3-merkaptoszulfurtranszferáz (Moore, Bhatia és Moochhala, 2003).
A savval labilis szulfid és a kötött szulfán-kén az emlős sejtekben tárolt hidrogén-szulfid két fő formája. Savas és redukáló körülmények között képesek hidrogén-szulfidot felszabadítani (Shen, Peter, Bir, Wang és Kevil, 2012). A megkötött szulfán-kén példái közé tartozik a tioszulfát, a perszulfid, a tioszulfonát, a poliszulfidok, a politionátok és az elemi kén. Összességében ezek a különböző biokémiai formák fontosak a biológiailag hozzáférhető kén-szulfid mennyiségének szabályozásához (Ishigami et al., 2009; Wintner et al., 2010).
Idegrendszeri és viselkedési toxikológia
13.15.5.4 hidrogén-szulfid
A hidrogén-szulfid egy gyakori és erős mérgező anyag, amely az elsődleges kémiai veszély a savanyú gáz (azaz kéntartalmú) előállításakor. Hidrogén-szulfid toxicitással a sertések elszigetelő létesítményei, valamint a trágya és szennyvíz kezelésével foglalkozó iparágak is találkoznak. A legtöbb ember könnyen érzékeli ezt a gázt, mivel a hidrogén-szulfid szaglási detektálási határa ≥5 ppb (Hoshika et al. 1993). A hidrogén-szulfid toxikus hatásai jellemzően a dózistól függenek, és leginkább az idegrendszert, a szív- és érrendszert, valamint a légzőrendszert érintik. A ~ 100 ppm hidrogén-szulfiddal akutan kitett emberek általában könnyezést, fotofóbiát, szaruhártya fedettségét, tachypnoát, nehézlégzést, tracheobronchitist, hányingert, hányást, hasmenést és szívritmuszavarokat tapasztalnak. Ezek a változások általában a friss levegőre történő kiürítéssel oldódnak meg. A hidrogén-szulfid expozícióból kilábaló embereknek azonban köhögésük, hyposmiauk, dysosmiaik és phantosmiaik lehetnek néhány naptól hétig (Glass 1990). Emberekben a 100–250 ppm hidrogén-szulfid csupán néhány percen át történő belégzése koordinációs zavarokat, memória- és motoros diszfunkciókat, valamint anosmiát (úgynevezett szaglásos bénulás) eredményezhet (Glass 1990).
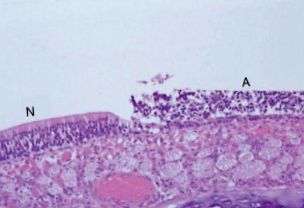
Brenneman és mtsai. (2002) 10 hetes Sprague – Dawley patkányok csoportjait legfeljebb 400 ppm hidrogén-szulfidnak tették ki naponta 3 órán át, 1 vagy 5 egymást követő napon. A legkifejezettebb orrelváltozás a szagló nyálkahártya nekrózis volt ( 3. ábra ). Ezt az elváltozást az expozíciót követő körülbelül 30 napon belül sikerült helyrehozni (Brenneman és mtsai 2002). Az első és ötnapos expozíció közötti hatásokban megfigyelt elsődleges különbségek az voltak, hogy az elváltozások előfordulási gyakorisága 100% volt a három legmagasabb dózisszintnél, és az orrelváltozások régiósabban kiterjedtek az orrüregben. A multifokális, bilaterálisan szimmetrikus szagló idegsejtek veszteségét és a szagló nyálkahártyára korlátozódó bazális sejtek hiperpláziáját figyelték meg patkányokban, amelyeket szinkronban tettek ki 30 vagy 80 ppm kénhidrogénnek. Léziókat figyeltünk meg a dorzális medialis meatusban, valamint az ethmoid mélyedés dorsalis és medialis területein. 10 ppm-nél nem figyeltek meg a kezeléssel összefüggő hatásokat, ami a szaglónyálkahártya elváltozásainak a nem észlelt káros hatásszintje (NOAEL) volt (Brenneman et al. 2000a).
3. ábra Szagló nyálkahártya nekrózis, bazális sejtek hipertrófiájával, patkány orrának háti septumja mentén, 200 ppm kén-hidrogén-szulfidnak 3 órán át (N) való kitettségét követően. Az érintett hámszagú szérum (A) szomszédos a normálisabban megjelenő hámmal, ami rágcsálókban mutatja az elváltozás helyspecifikus jellegét.
Csökkent citokróm-oxidáz aktivitást figyeltek meg a patkány szaglóhámban, egyszeri 3 órás ≥30 ppm hidrogén-szulfid expozíciót követően (Dorman és mtsai 2002). A hidrogén-szulfid orrban történő extrakcióját hím Sprague – Dawley patkányok izolált felső légúti traktáiban mértük, és 32% -ot tett ki 10 ppm-es expozíció esetén 75 ml/perc –1 és 7% között 200 ppm-es expozíció esetén 300 ml/perc –1 (Schroeter és mtsai 2006). A hidrogén-szulfid előre jelzett regionális fluxusa korrelál az orrszaglási elváltozások eloszlásával patkányokban (Schroeter et al. 2006).
Akut válaszok a mérgező expozícióra
Hidrogén-szulfid
A hidrogén-szulfid a kőolaj-kitermelés és -finomítás gyakori mellékterméke, valamint a szerves anyagok lebontásának potenciális veszélye (ezért közönséges neve, „szennyvízgáz”); a túlzott expozíció zárt terekben végzett munkából, trágyagödrökbe merülésből, 306 vagy a geotermikus és vulkanikus források közelségéből származhat. 307 A hidrogén-szulfid légúti irritáló hatású, de még erőteljesebb citotoxikus fulladást okozó, károsítja a citokróm-oxidázt és a sejtlégzést. Ezért súlyos kén-szulfid-expozíció esetén a gyors kardiovaszkuláris összeomlás és halál gyakran beárnyékolja a tüdőszerv bármely hatását, bár akut tüdősérülési mintázat jelen lehet azoknál, akik túl sokáig élnek túl intenzív támogató kezelésben; Az ingerlő tünetek mint domináns jellemzők nagyobb jelentőségűek lehetnek alacsonyabb intenzitású expozíciók esetén. 306,308-311
Foglalkozási neurológia
Tulajdonságok
A hidrogén-szulfid (H 2S, molekulatömeg 34,08) gyúlékony, színtelen gáz, amely offenzív szagú (rothadt tojás vagy káposzta szaga), lipidben oldódik és vízben rosszul oldódik (vízben a gőznyomás 18,75 10 2 kPa), és nehezebb, mint a levegő (1,19 sűrűség). Vizes közegben könnyen disszociál hidroszulfiddá, de nem szulfiddá az alábbiak szerint. A disszociálatlan hidrogén-szulfid és a hidroszulfid-ion 1: 2 arányban dominál pH = 7,4 mellett (Reiffenstein et al., 1992; Toxikus Anyagok és Betegségek Nyilvántartásának Ügynöksége, 2006):
A hidrogén-szulfid biológiai forrásai általában szakaszos csúcsokat vagy impulzusokat bocsátanak ki a gázból, általában metánnal együtt (ami minden gyakorlati szempontból nem mérgező). Kiszabadulása után a sűrű gáz addig maradhat, amíg szél vagy szellőzés kiszorítja azt alacsonyan fekvő talajon, mélyedésekben, mint például árkok vagy gödrök, vagy zárt helyiségekben. A vízben lévő hidrogén-szulfid, például a szennyvízben, a mocsarakban és a mély óceánban hajlamos telítettségre halmozódni, majd spontán vagy zavartan, például hevítéssel vagy fizikai zavarban szabadul fel. Ennek eredményeként a gáz „felpattan” és egy bolus effektus alakul ki, amely aztán zárt terekben vagy gödrökben csapdába eshet (Nogue et al., 2011).
A tartós kibocsátás általában gyakoribb geológiai forrásokból, mint az „olajfoltban”. A vulkáni aktivitás, a csapolt gázzsebek, valamint az olaj- és gázkitermelés szeszélyei még ott is változó expozíciós profilt eredményezhetnek rövid ideig.
- Folyékony parafin - áttekintés a ScienceDirect témákról
- Fokozott étvágy - áttekintés a ScienceDirect témákról
- Iszap súlya - áttekintés a ScienceDirect témákról
- Lipid diéta - áttekintés a ScienceDirect témákról
- Hidrogén-szulfid - Toxikológia - Merck Veterinary Manual