Nem alkoholos zsírmájbetegség és metabolikus szindróma
Absztrakt
Az alkoholmentes zsírmájbetegség (NAFLD) egy klinikopatológiai egység, amelyet a fejlett országokban egyre nagyobb mértékben elismernek fő egészségügyi terhet. Ez magában foglalja a májkárosodás spektrumát, az egyszerű steatosistól az alkoholmentes steatohepatitisig (NASH), az előrehaladott fibrózisig és ritkán a cirrhosissá válásig. A legújabb tanulmányok hangsúlyozzák az inzulinrezisztencia, az oxidatív stressz és az azt követő lipidperoxidáció, a proinflammatorikus citokinek, az adipokinek és a mitokondriális diszfunkció szerepét a NAFLD kialakulásában és progressziójában. Ezenkívül a bizonyítékok felhalmozása alátámasztja a NAFLD és a metabolikus szindróma közötti kapcsolatot. Bár az adatok főként epidemiológiai adatok, a NAFLD és a metabolikus szindróma patogenezise közös patofiziológiai mechanizmusoknak tűnik, kiemelt fontosságú tényező az inzulinrezisztencia. Ez az áttekintés összefoglalja a NAFLD és a metabolikus szindróma epidemiológiájáról, patofiziológiájáról és diagnózisáról szóló jelenlegi ismereteket, valamint azokat az eredményeket, amelyek erősen támogatják az alkoholmentes zsírmájbetegség társulását, mint a metabolikus szindróma klaszterének lehetséges összetevőjét.
A nem alkoholos zsírmájbetegség (NAFLD) a leggyakoribb májbetegség, mivel előfordulása a becslések szerint 20-30% a nyugati országok általános populációjában1. A NAFLD a betegség szövettani spektrumaként fordul elő, és magában foglalja az egyszerű steatosis és az alkoholmentes steatohepatitis (NASH) altípusait. Úgy gondolták, hogy ez jóindulatú állapot, de ma már egyre inkább felismerik a májkal kapcsolatos morbiditás és mortalitás fő okaként. Tanulmányok bevezették, hogy a NAFLD cirrhosissá, májelégtelenséggé és hepatocelluláris carcinomává alakulhat át 2. Kimutatták, hogy a NAFLD szorosan kapcsolódik a metabolikus szindróma jellemzőihez. Az inzulinrezisztencia kulcsfontosságú patogén tényező mind a NAFLD, mind a metabolikus szindróma szempontjából. A klinikai, kísérleti és epidemiológiai vizsgálatokból származó rendelkezésre álló adatok azt mutatják, hogy a NAFLD lehet a metabolikus szindróma májmegnyilvánulása 3 .
Metabolikus szindróma
Definíció - diagnózis
A metabolikus szindróma a kockázati tényezők csoportosulása, amely nagymértékben növeli az egyén valószínűségét az érelmeszesedéses szív- és érrendszeri betegségek (ASCVD), a 2-es típusú diabetes mellitus és a krónikus vesebetegségek kialakulásában. Úgy tűnik, hogy a legfontosabb kockázati tényezők a hasi elhízás, az aterogén dyslipidaemia, a magas vérnyomás, az emelkedett plazma glükózszint, a protrombotikus állapot és a gyulladáscsökkentő állapot 4 - 7 .
Számos szervezet megkísérelte megfogalmazni a metabolikus szindróma definícióját, és egyszerű kritériumokat alkalmazott diagnózisának felállításához, de a közzétett definíciók körvonalazása meghaladja a jelen áttekintés kereteit. 2001-ben a Nemzeti Koleszterin Oktatási Program (NCEP) Felnőtt Kezelő Testülete (ATP III) egyszerű klinikai kritériumokat vezetett be, amelyeket széles körben elfogadottak, mivel ezeket egyszerűen lehet használni a klinikai gyakorlatban, és mivel számos tanulmány értékelte megbízhatóságukat 13. 2005-ben az Amerikai Szív Szövetség (AHA) és az Országos Szív Lung and Blood Institute (NHLBI) kisebb módosításokkal frissítette az ATP III kritériumokat 5. Így a metabolikus szindrómát a következő összetevők közül három vagy több jelenléte azonosítja: hasi elhízás (derék kerülete> 102 cm férfiaknál,> 88 cm nőknél), emelkedett trigliceridszint (> 150 mg/dl vagy gyógyszeres kezelés esetén). emelkedett trigliceridszintek), csökkent HDL-C szint (130 Hgmm vagy diasztolés vérnyomás> 85 Hgmm vagy antihipertenzív gyógyszeres kezelés esetén) és csökkent éhgyomri glükóz (100 - 125 mg/dl vagy antidiabetikus gyógyszeres kezelés esetén) 5 .
A szabványos definíció hiánya megnehezíti a vizsgálatok összehasonlítását. Az alkalmazott definíciótól függően a metabolikus szindróma prevalenciájának becslései eltérnek. A definíciókat összehasonlító tanulmányok azonban arról számoltak be, hogy minden meghatározás azonosítja azokat a személyeket, akiknél fokozott a cukorbetegség, a szív- és érrendszeri betegségek és az összes okból fakadó halálozás kockázata 7, 10. Az adatok azt mutatják, hogy a metabolikus szindróma prevalenciája népességenként nagyon eltérő. A Nemzeti Egészségügyi és Vizsgálati Felmérés (NHANES) III (1988-1994) és az NHANES 1999-2000 adatai szerint az MSZ életkor szerint korrigált prevalenciája 24,1%, illetve 27% volt 14. Görögországban 2003 folyamán a MetS-Greece tanulmányt hajtották végre, és a metabolikus szindróma életkor szerint módosított prevalenciája az általános populációban 23,6% volt. Ez hasonló volt a férfiaknál (24,2%) és a nőknél (22,8%), de a prevalencia az életkor előrehaladtával mindkét nemnél nőtt. Ez a metabolikus szindróma egyes komponenseinek hasonló, az életkorral összefüggő trendjének tulajdonítható. Az SM-ben szenvedő egyének többségének a szindróma három összetevője volt (61%), 29% -uknak négy, 10% -ának pedig mind az öt komponense volt.
A leggyakoribb rendellenességek a hasi elhízás (72%) és az artériás hipertónia (66%) voltak. Az emelkedett glükóz előfordulása (beleértve a diabetes mellitusban szenvedőket is) váratlanul magas volt (53%). Az SM-ben szenvedő alanyok között az emelkedett trigliceridszint prevalenciája 62%, az alacsony HDL-C szinté pedig 54% volt 15 .
Kórélettan
Az inzulinrezisztencia és a kompenzáló hiperinszulinémia központi etiológiai szerepet játszik az SM kialakulásában. Állatmodellekből, valamint humán vizsgálatokból származó bizonyítékok a máj nagyon alacsony sűrűségű lipoprotein (VLDL) túltermelését azonosították a hipertrigliceridémia kialakulásának kritikus mögöttes tényezőként, az SM egyik fő jellemzője. A HDL-koleszterinszint csökkenése a HDL összetételében és anyagcseréjében bekövetkező változások következménye 17. Az elhízást a SM kialakulásának központi okozó komponenseként is leírják. Az elhízott egyének izomsejtjeiben és zsírsejtjeiben egyaránt csökken az inzulin receptorához való kötődése, a receptor foszforilációja, a tirozin-kináz aktivitása és az IRS-ek foszforilációja. Az elhízásban megnövekedett zsírenergia-tárolás fokozza az egyéb szövetekbe irányuló FFA-fluxust és fokozott triglicerid-tárolást ezekben a szövetekben, ami elősegíti az inzulinrezisztenciát és más káros hatásokat 18 .
A felhalmozódott zsigeri zsírszövet számos adipocitokint termel és szekretál, például TNF-a és IL-6, amelyek a magas vérnyomás kialakulását idézik elő 19. Az SM-ben szenvedő betegeknél a proximális tubuláris szinten a nátrium és a víz újrafelszívódása jelentősen magasabb. Az inzulin elősegíti az endothelin-1 (ET-1) termelését az endothel sejtekből, valamint az ET-1 működését a vaszkuláris simaizomsejtekben, érszűkületet és fokozott simaizomsejtek proliferációt okozva 21, 22. Az inzulin a szimpatikus idegrendszer aktivitását is növeli 23 .
A krónikus gyulladás gyakran társul az SM-hez, és a fő gyulladásos mediátorok az adipocitokinek és az FFA-k. Az MS-hez társított gyulladásos citokinek közé tartozik a CRP, a TNF-a, az IL-6 és mások, és ezek több inzulinrezisztenciát és a zsírszövet triglicerid raktárainak lipolízisét eredményezik, fokozott máj glükóz és VLDL termelésben. A citokinek és az FFA emelik a májban a fibrinogén és a plazminogén aktivátor inhibitor-1 (PAI-1) termelését is, amely kiegészíti a PAI-1 zsírtermeléssel történő túltermelését, így előidézve a pro-trombotikus állapotot 24 .
Nem alkoholos zsírmájbetegség
Meghatározás
A NAFLD egy széles szövettani spektrumú klinikopatológiai egység, amely magában foglalja az egyszerű steatosist és a steatohepatitist (NASH). A steatosis meghatározása a zsírcseppeket tartalmazó hepatociták arányának becslésével történik. A javasolt alsó küszöb a hepatociták 5% -a. A steatohepatitis jellemzői a hepatocelluláris sérülések (ballonozás, apoptózis/nekrózis, Mallory-hialin, óriás mitokondrium), gyulladás és fibrózis (perisinusoidalis, pericelluláris) 25, 26. Különböző javaslatok vannak az alkoholfogyasztás szintjéről, amelyek megbízhatóan megkülönböztethetik az alkoholos zsírmájat és a NAFLD-t. Sok központ elfogadja, hogy a NAFLD meghatározásához az alkoholfogyasztás maximálisan megengedett szintje a férfiaknál napi 2 szokásos ital (140 g etanol/hét), a nőknél pedig napi egy szokásos ital (70 g etanol/hét) 27 .
A NAFLD a mögöttes patogenezistől függően elsődleges vagy másodlagos kategóriába sorolható. Az elsődleges NAFLD az inzulinrezisztenciával és a metabolikus szindrómával jár. A NAFLD-hez kapcsolódó egyéb állapotok a teljes parenterális táplálás, az akut éhezés, a hasi műtétek (pl. Kiterjedt vékonybél-reszekció, biliopancreaticus eltérítés és a jejunális bypass), számos gyógyszer (pl. Amiodaron, tamoxifen, glükokortikoidok, szintetikus ösztrogének, diltiazem, aszpirin, metotrexát) használata, nagyon aktív antiretrovirális terápia). Hepatitis C-vel, HIV-vel és anyagcserezavarokkal, azaz hipobetalipoproteinémiával, lipodystrophiával, hypopituitarismussal, hipotalamusz elhízással, Weber-Christian szindrómával, terhesség akut zsírmájával, Reyes-szindrómával és Mauriac-szindrómával 28, 29 is társul. Tanulmányok azt mutatják, hogy a szerves oldószerek munkahelyi expozíciója szerepet játszhat a NAFLD 30 kialakulásában, és hogy a policisztás petefészek-szindrómában szenvedő nőknél gyakoribb lehet az alkoholmentes zsírmájbetegség 31 .
Epidemiológia - természettudomány
Annak ellenére, hogy gyakori és potenciálisan súlyos, a NAFLD természettörténete továbbra sem elég tisztázott. A halandóság jelentősen megnő a NAFLD-ben szenvedő betegek körében az azonos korú és nemű általános populáció várható halálozásához képest. A máj okozta halálozás a halálozás vezető oka, bár az abszolút kockázat alacsony 2. Az egyszerű steatosisban szenvedő betegek viszonylag jóindulatú májjal kapcsolatos prognózisa 1,5% -kal alakul ki cirrhosisban, 1% -uk pedig májjal kapcsolatos okok miatt hal meg egy-két évtized alatt 44. Ezzel szemben a steatohepatitisben szenvedő egyének 30-50% -ában alakul ki fibrózis, 15% -ában cirrhosis és 3% -ukban végleges májelégtelenség alakul ki 3, 38. A tanulmányok szerint az idősebb kor, az elhízás és a diabetes mellitus jelenléte független előrejelzője a súlyos májfibrózisnak az alkoholmentes steatohepatitisben (NASH) szenvedő betegeknél 45, 46. Fontos megfigyelés, hogy sok kriptogén cirrhosisban szenvedő betegnél hibásan diagnosztizálták a NAFLD-t. Ennek oka a máj steatosis szövettani bizonyítékainak csökkenése, mivel a betegség cirrhosis 2-re fejlődik. Végül a NAFLD a hepatocelluláris karcinóma (HCC) eseteinek jelentős hányadát jelentheti. Egy tanulmány szerint a NAFLD a HCC 47 eseteinek legalább 13% -át teszi ki .
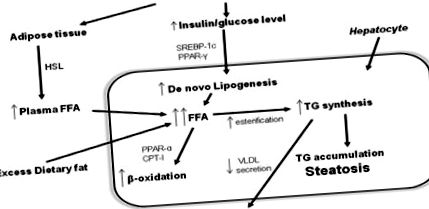
Kórélettan (1. ábra)
A legszélesebb körben elfogadott modell a NAFLD fejlődésének és az egyszerű steatosisból a NASH-nak való előrehaladás magyarázatára a "két találat hipotézise". Az "első találat" a lipidek felhalmozódása a hepatocitákban, az inzulinrezisztencia pedig a legfontosabb kórokozó tényező a máj steatosisának kialakulásában. A "második találat" hepatocita sérüléshez, gyulladáshoz és fibrózishoz vezet. A második találatot kiváltó tényezők: oxidatív stressz és az azt követő lipidperoxidáció, proinflammatorikus citokinek, adipokinek és mitokondriális diszfunkció 52 .
Az állati modellek legújabb eredményei arra utalnak, hogy a triglicerid májban történő felhalmozódása inkább májvédő lehet, mintsem hepatotoxikus, mivel csökkenti a hepatocitákban lévő szabad zsírsavak felhalmozódását, azok peroxidációját és oxidatív stresszét 56. A "kétütemű hipotézis" szerint azonban a steatosis növeli a máj sebezhetőségét a "második találat", az oxidatív stressz iránt. A prooxidáns/antioxidáns egyensúly megzavarása oxidatív stresszt jelent. Az oxidatív stressz következményei a lipidperoxidáció, a sejtek degenerációja és nekrózisa, apoptózis, gyulladásgátló citokin expresszió, a máj stellát sejtjeinek aktiválása és fibrogenezise. Az oxidatív stressz több lehetséges forrását azonosították, ezek közé tartozik a mitokondriális diszfunkció, a máj citokróm CYP2E1, a peroxiszómák által végzett β-oxidáció a mitokondriumokban és a toborzott gyulladásos sejtek 57 - 59 .
Kezdetben úgy gondolták, hogy a májvas meghatározó tényező a NASH kialakulásában. A legutóbbi tanulmányok szerint azonban a NAFLD-ben szenvedő betegek többségében a vasterhelés és a HFE-mutációk nem járulnak hozzá jelentősen a májfibrózishoz 69 .
A máj steatosisának és gyulladásának további potenciális hozzájárulója a baktériumok elszaporodása. Felvetődött, hogy a baktériumok elszaporodása fokozza a toxinok, például az etanol vagy a bakteriális lipopoliszacharid endogén termelését, amelyek elősegítik a reaktív oxigénfajták termelését a hepatociták és a máj makrofágjai által. Ezt a javasolt mechanizmust állatkísérletek is alátámasztják, de a 70-es, 71-es betegeknél még nem tesztelték .
Az a tény, hogy a NAFLD prevalenciája a különböző fajcsoportok szerint változó, a májbetegség súlyosságának jelentős eltéréseinek közös megfigyelése a NAFLD és hasonló kockázati tényezőkkel rendelkező egyének körében, valamint az a megfigyelés, hogy számos nagyon ritka emberi monogén rendellenesség társul a zsírmáj kialakulásához betegség arra utal, hogy genetikai tényezők befolyásolják a NAFLD fejlődését. Jelenleg csak néhány kicsi tanulmány vizsgálja azokat a potenciális géneket, amelyek összefüggenek a NAFLD patogenetikai mechanizmusaival. Az adatok azt mutatják, hogy a génexpresszió többszörös változása jellemzi az egyszerű steatózist. Mindezek a tanulmányok érdekesek és provokatívak, de további validálást igényelnek nagyobb populációkban, mielőtt valódi jelentőségük megismerhető 91 .
Tünetek, laboratóriumi rendellenességek, diagnózis
A legtöbb NAFLD-ben szenvedő beteg tünetmentes. A betegséget véletlenül fedezik fel a hypolipidaemiás gyógyszerekkel kezelt betegek rutin laboratóriumi vizsgálata során, valamint az epekő gyanújának feltételezett szonográfiai vizsgálata során. Jelenleg a klinikai tünetek nem specifikusak és megbízhatatlanok a betegség súlyosságának megítélésében. A leggyakoribb tünetek a fáradtság és a jobb felső negyed kellemetlenségei. A fizikális vizsgálat során nincsenek patognómikus tünetek, és a leggyakoribb rendellenességek az elhízás és a hepatomegalia, amelyekről az alanyok legfeljebb 50% -ánál számoltak be. A betegek kisebb hányadánál olyan súlyosabb májbetegségre utaló tünetek jelentkeznek, mint az ascites, a sárgaság és a máj encephalopathia 58, 92 - 94 .
A CT-leképezéssel pontosan kimutatható és számszerűsíthető a betegek steatosisának mennyisége. 30% feletti steatosis esetén az érzékenység 82% és 93%, illetve a specificitás 100%. A CT-vizsgálat azonban nem képes megkülönböztetni az egyszerű steatózist a steatohepatitistől. A nem kontrasztos CT és a kontrasztot fokozó 108, 110, 111 diagnosztikai értéke között nincs különbség .
A mágneses rezonancia képalkotás (MRI) a legpontosabb rendelkezésre álló technika a máj steatosisának diagnosztizálásában és számszerűsítésében. A zsír és a víz közötti jelkülönbségeken alapul. Az MRI jó összefüggést mutat a szövettani vizsgálattal, és az érzékenység és a specificitás 100%, illetve 92,3%, illetve 111, 112. A módszer korlátai között szerepel a ráfordítás, az alkalmazhatatlanság implantálható eszközökkel vagy klausztrofóbiában szenvedő betegeknél, valamint a megváltozott értékek a vashaladó betegeknél 93 .
A mágneses rezonancia spektroszkópia (MRS) egy alternatív, nem invazív módszer a máj trigliceridtartalmának (HTGC) mérésére, de csak kis kutatási tanulmányokban alkalmazták. Az MRS elve a protonok rezonancia frekvenciáinak különbségein alapszik. Szczepaniak és munkatársai arról számoltak be, hogy az MRS elég érzékeny a kis mennyiségű triglicerid kimutatására, és az étkezés nem befolyásolja. További előny a többi általánosan alkalmazott képalkotó módszerrel szemben, hogy ez inkább kvantitatív, mint minőségi vagy félig kvantitatív módszer. Az MRS pontossága és biztonsága ideális módszertanná teszi a máj steatosis 113 értékelését és nyomon követését .
A tranziens elasztográfia (TE) egy nemrégiben kifejlesztett, nem invazív módszer, amelyet a májfibrózis előrejelzésére terveztek, a rezgés által generált mechanikai hullám alapján. A máj parenchima hullámsebességének mérése becslést ad a máj rugalmasságáról, ami viszont a májfibrózis markere. Pontosan diagnosztizálhatja az előrehaladott májfibrózist, de a korai májfibrózisban nyújtott teljesítménye kevésbé kielégítő. Steatosisban és megnövekedett BMI-ben szenvedő betegeknél reprodukálhatósága jelentősen csökken. A májfibrózist a TE is túlbecsüli, ha az ALT szintje megemelkedik 114, 115 .
A máj apoptózisának jelentős szerepe van a NAFLD előrehaladásában, és a máj apoptózisának biomarkereit potenciális diagnosztikai eszközként feltárták. A kaszpáz által generált citokeratin-18 (CK-18) az apoptózisban szerepet játszó fehérje, és magasabbnak találták NASH-ban szenvedő betegeknél. Wieckoska és mtsai. számoltak be arról, hogy a plazma CK-18 fragmensek feltűnően emelkedtek a NAFLD-ben szenvedő betegeknél a kontrollokhoz képest, és a plazma szintek korreláltak a máj expressziós szintjével. Ezek az eredmények azt sugallják, hogy a CK-18 a NASH független prediktora, és hasznos és megbízható eszközzé válhat a szövettani betegség súlyosságának meghatározásában a NAFLD-ben szenvedő betegeknél. Egy nagy multicentrikus prospektív validációs vizsgálat folyamatban van, 93, 94, 121 .
Metabolikus szindróma és alkoholmentes zsírmáj
Egy 4401 látszólag egészséges egyén prospektív megfigyelési tanulmányában Hamagushi és mtsai azt találták, hogy az SM erős kockázati tényező a nem alkoholos zsírmájbetegség szempontjából. Az SM-ben szenvedő résztvevőknek 4–11-szer nagyobb a kockázata a jövőbeli alkoholmentes zsírmájbetegség szempontjából. Ezenkívül, ha nem alkoholos zsírmájbetegség és MS áll fenn, a betegség regressziója kevésbé valószínű 105. Hsiao és mtsai bebizonyították, hogy a súlyos zsírmáj jelenléte szignifikánsan korrelált a magas vérnyomás prevalenciájával és mértékével, a kóros glükóz- és triglicerid-anyagcserével. .
Következtetés
Az alkoholmentes zsírmáj jelentős tudományos és klinikai érdeklődés tárgyát képezi, amely a következő években növekszik. Epidemiológiai vizsgálatok azt mutatják, hogy a NAFLD és a tagállamok a közegészségügy egyik fő problémájaként jelennek meg. A jövőbeli vizsgálatok célja a patogenezis tisztázása és a hatékony kezelés megteremtése mind a NAFLD-ben, mind a tagállamokban. Számos tanulmány folyamatban van, és közülük néhány biztató eredményt hozott.
- Metabolikus szindróma és alkoholmentes zsírmáj betegség Annals of Hepatology
- A tartós, magas zsírtartalmú étrendi táplálás elősegíti az alkoholmentes zsírmáj betegségeket és megváltoztatja a beleket
- Metabolikus szindróma; a stresszhez kapcsolódó betegség modern változata; Revista Española de Cardiología
- A táplálkozás szerepe az alkoholmentes zsírmájbetegség patogenezisében és megelőzésében Legutóbbi
- Az étrend és az életmódváltások szerepe alkoholmentes zsírmájbetegségben