Perforált peptikus fekély - frissítés
Levelezés: Vishalkumar G Shelat, FRCS, FICS, Hesperis Diploma in Organ Transplantation (ECOT), Hepatobiliary Consultant Surgeon, General Surgery Department, Tan Tock Seng Hospital, 4. szint, 1. melléklet, 11., Jalan Tan Tock Seng, Szingapúr 308433, Szingapúr. moc.liamffider@talehsgv
Telefon: + 65-63577807 Fax: + 65-63577809
Absztrakt
Alap tipp: A hasi fájdalom, tachycardia és hasi merevség hirtelen megjelenésének klasszikus triádja a perforált peptikus fekély jellemzője. A korai diagnózis, a gyors újraélesztés és a sürgős műtéti beavatkozás elengedhetetlen az eredmények javításához. A feltáró laparotómia és az omentális tapasz javítása továbbra is arany színvonalú, és a laparoszkópos műtétet fontolóra kell venni, ha szakértelem áll rendelkezésre. Gasztrektómia ajánlott nagy vagy rosszindulatú fekélyben szenvedő betegeknél az eredmények fokozása érdekében; a gyomor reszekcióval kezelt betegek kimenetele azonban továbbra is alacsonyabb.
BEVEZETÉS
A peptikus fekélybetegség (PUD) a gyomorsav-pepszin és a nyálkahártya védekezési akadályainak egyensúlyhiányából ered. Évente világszerte 4 millió embert érint [1]. Becslések szerint a PUD előfordulása körülbelül 1,5-3% [2]. A fejlett országokból származó hét tanulmány szisztematikus áttekintése szerint a PUD éves előfordulási aránya 0,10% -0,19% volt az orvos által diagnosztizált PUD esetében és 0,03% -0,17% volt, ha kórházi adatok alapján számoltak be [3]. Bár a PUD-ban szenvedő betegek 10% -20% -ánál fog szövődményeket tapasztalni, a fekélyek csak 2% -14% -a perforálódik, ami heveny megbetegedést okoz [4,5]. A perforáció a PUD súlyos szövődménye, és a perforált peptikus fekélyben (PPU) szenvedő betegeknél gyakran akut has jelentkezik, amely magas kockázatot jelent a morbiditás és a mortalitás szempontjából [6]. A perforáció előfordulási gyakorisága PUD-ben szenvedő betegeknél körülbelül 5% [7]. A PPU mortalitása 1,3% és 20% között mozog [8-10]. Harminc napos halálozási arány elérte a 20% -ot és a 90-d halálozási arány akár 30% -ot is jelentettek [11,12]. Ebben az áttekintésben összefoglaltuk a PPU-val kapcsolatos jelenlegi bizonyítékokat, és reméljük, hogy felülvizsgálatunk segítséget nyújt majd a sebészeknek, akiket a bizonyítékokon alapuló gyakorlat frissít.
AETIOLÓGIA
Bár korábbi tanulmányok azt mutatták, hogy a szezonális eltérések befolyásolták a PPU előfordulását, más vizsgálatok nem bizonyították ezt a mintát [13-16]. A fejlődő világban a betegek általában fiatal férfi dohányosok, míg a fejlett országokban; a betegek általában idősek, többszörös társbetegséggel és a nem szteroid gyulladáscsökkentők (NSAID-ok) vagy a szteroidok ezzel összefüggő alkalmazásával [17,18]. Az NSAID-k, a Helicobacter pylori (H. pylori), a fiziológiai stressz, a dohányzás, a kortikoszteroidok és a PUD korábbi kórtörténete a PPU kockázati tényezője [1,19-27]. Kockázati tényezők jelenlétében a kezdeti sikeres kezelés ellenére a fekély kiújulása gyakori. A 93 vizsgálat szisztematikus áttekintése azt mutatta, hogy a perforáció átlagos hosszú távú kiújulása 12,2% volt (95% CI: 2,5-21,9) [5].
NSAID-ok
Az NSAID-okat fájdalomcsillapító, gyulladáscsökkentő és lázcsillapító hatása miatt széles körben használják. Az NSAID használata ismert módon növeli a PPU kockázatát [28,29]. A krónikus nem szteroid gyulladáscsökkentők kb. Negyede PUD-t fog kialakítani, és 2–4% -a vérzik vagy perforálódik [30–33]. A szteroidokkal és a szelektív szerotonin újrafelvétel-gátlókkal való gyógyszerkölcsönhatás szintén növeli a PUD kockázatát. A szelektív ciklo-oxigenáz-2 inhibitorok kevésbé társulnak a PUD-hoz. Egy nyugat-dániai tanulmány kimutatta, hogy a PPU standardizált kórházi elhelyezkedési aránya az 1996-os 100 000 lakosról számított 17-ről 2004-re 12/100 000 lakosra csökkent (HR 0,71; 95% CI: 0,57-0,88) a szelektív ciklo-oxigenáz-2 bevezetése után inhibitorok a klinikai gyakorlatba [34].
H. pylori
A H. pylori továbbra is az egyik leggyakoribb fertőzés az egész világon. A H. pylori előfordulása a fejlett országokban csökkent a higiénia és a korai gyermekkorban bekövetkezett csökkent fertőzés következtében. A H. pylori átlagos prevalenciája PPU-ban szenvedő betegeknél a különböző diagnosztikai módszerek és földrajzi eltérések miatt a vizsgálatok között változik. A H. pylori kimutatásának hisztopatológiai módszereivel végzett legújabb vizsgálatok kimutatták, hogy a perforált nyombélfekélyben szenvedő betegeknél a H. pylori prevalencia 50% -80% között mozog [22,35]. Egy randomizált, kontrollált vizsgálat 2008-ban, 65 olyan beteg bevonásával, akiken a perforált nyombélfekély egyszerű lezárása történt, a H. pylori-val kezelt betegeknél 6,1% -os egyéves fekélyismétlődési arány mutatkozott, szemben a kontrollcsoport 29,6% -ával [36]. A visszatérő PUD főként a H. pylori fertőzésben szenvedő betegeknél fordul elő, ami arra utal, hogy a H. pylori fontos szerepet játszik a PUD és szövődményeinek kialakulásában [22,37]. A visszatérő H. pylori fertőzés kockázata jelentősen csökken a protonpumpa-gátló terápiával, de a protonpumpa-gátlóknak csak mérsékelt hatékonyságuk van az NSAID-ot használó fekélyek csökkentésére.
Dohányzó
Úgy gondolják, hogy a dohány gátolja a hasnyálmirigy-hidrogén-karbonát szekrécióját, ami fokozott savasságot eredményez a duodenumban [38,39]. Gátolja a nyombélfekély gyógyulását is. Egy metaanalízis azt mutatta, hogy a PUD 23% -a összefüggésbe hozható a dohányzással [40]. Egyes vizsgálatokban azonban nem volt különbség a dohányzás terén a nem H-ban szenvedő betegek között. pylori, nem NSAID duodenum fekélyek és H. pylori rokon fekélyekkel rendelkezők, ami a dohányzás korlátozott szerepét jelzi [41]. Ez összhangban van a korábbi tanulmányokkal, amelyek azt mutatták, hogy a dohányzás nem növelte a fekély kiújulásának kockázatát, miután a H. pylori felszámolásra került [42,43].
Mások
KLINIKAI SZOLGÁLTATÁSOK
1843-ban Edward Crisp kijelentette, hogy „a tünetek annyira tipikusak, alig hiszem, hogy lehetséges, hogy bárki megbukhatna a diagnózis felállításában” [48].
A PUD tünetei közé tartozik a hasi fájdalom, a felső hasi kényelmetlenség, a puffadás és a teltségérzet. Amikor a PUD súlyosbodik és végül perforálódik, a gyomornedv és a gáz belép a hasüregbe, ami kémiai peritonitishez vezet. A PPU-ra tipikusan hirtelen jelentkező hasi fájdalom vagy a folyamatos hasi fájdalom heveny romlása jellemző. Jellemzően a fájdalom a szokásos premedikális gyógymódok ellenére sem szűnik meg teljesen, és arra kényszeríti a beteget, hogy orvoshoz forduljon. A gasztroduodenális tartalom kiáramlása és a súlyos fájdalom miatt fellépő kémiai peritonitis tachycardiához vezet. A hirtelen fellépő hasi fájdalom, tachycardia és hasi merevség klasszikus triádja a PPU jellemzője.
A klinikai megnyilvánulás három fázisra osztható [49]. A kezdeti fázisban a megjelenéstől számított 2 órán belül epigasztrikus fájdalom, tachycardia és hűvös végtagok jellemzőek. A második fázisban (2–12 órán belül) a fájdalom általánosodik, és mozgáskor rosszabb. Jellemző jelek láthatók, mint például a hasi merevség és a jobb alsó negyed gyengédsége (a jobb paracolus csatorna mentén folyó folyadékkövetés eredményeként). A harmadik fázisban (több mint 12 óra) nyilvánvaló lehet a hasi feszülés, a pyrexia és az alacsony vérnyomás akut keringési összeomlással.
Egy tanulmány, amelyben 84 PPU-ban szenvedő beteg vett részt, arról számolt be, hogy a leggyakoribb tünetek a súlyos epigasztrikus fájdalom (97,6%), a hasi duzzanat (76,2%) és a hányás (36,9%) hirtelen fellépése [50]. A hasi érzékenység és a peritonitis klasszikus jelei kiválthatók ebben a vizsgálatban a PPU-ban szenvedő betegek 88,1% -ánál és 66,7% -ánál. Egyéb tünetek közé tartoztak az émelygés (35,7%), a súlyos dyspepsia (33,3%), a székrekedés (29,8%) és a láz (21,4%) [50]. 332 PPU-beteg kezelésének tapasztalata alapján a leggyakoribb tünet a hasi fájdalom akut megjelenése volt (61,7%) [51]. Egy nemrégiben végzett tajvani tanulmány kimutatta, hogy a PPU-ban szenvedő betegek nagyobb valószínűséggel érkeztek hétvégén az ügyeletre, és ezt érvényesíteni kell [52].
A tachycardia és a merevséggel járó hasi érzékenység gyakori klinikai tünetek. Súlyos fájdalom, a kémiai peritonitis okozta szisztémás gyulladásos válasz és a folyadékhiány a rossz bevitel, hányás vagy pyrexia miatt kompenzációs tachycardiához vezet. Azoknál a betegeknél, akik késik az orvoshoz fordulást, a teljes test vízhiánya miatt hipotenzió következik be. Ha megszakítás nélkül; ez mentális obtundációvá és akut vesekárosodássá válik. Ez ahhoz az állapothoz vezet, amikor a beteg fiziológiailag alkalmatlanná válik a feltétlenül szükséges operatív beavatkozásra. Ezért fontos a gyors megerősítő diagnózis felállítása.
DIAGNÓZIS
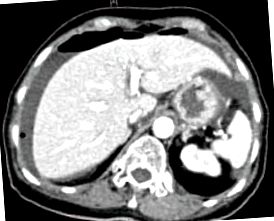
A számítógépes tomográfia a szabad levegőt mutatja a rekeszizom alatt peri-máj szabad folyadékkal.
Ugyanazon páciens mellkasröntgen képének felállítása kétségtelen szabad levegővel a jobb hemidiaphragma alatt.
A laboratóriumi vizsgálatokat a PPU-ban nem a diagnózis felállítása, hanem a differenciáldiagnózis kizárása, valamint a különféle szervrendszerek sértésének megértése érdekében végzik. Nem specifikusak [56]. A szérum amilázt az indexnek a sürgősségi osztályon történő bemutatásakor vagy normál mellkasröntgen után kell elvégezni. A megemelkedett szérum amiláz összefüggésbe hozható a PPU-val, és általában a normális szintjének kevesebb, mint négyszerese emelkedik [57]. Az olyan vizsgálatok, mint a fehérvérsejtek száma és a C-reaktív fehérje, elvégezhetők a PPU-ban végzett vizsgálat részeként. A leukocytosis és a megnövekedett C-reaktív fehérje felemelkedhet gyulladás vagy fertőzés következtében [57]. Az emelkedett kreatinin-, karbamid- és metabolikus acidózis a szisztémás gyulladásos válasz szindrómát (SIRS) és a prerenalis sérülést tükrözi [58]. A szérum gasztrinszint olyan betegeknél javallt, akiknek kórtörténetében visszatérő fekélyek vagy újrakezdő PUD voltak, és ez segíthet a Zollinger Ellison-szindróma diagnózisának felállításában. A mellékpajzsmirigy-rendellenesség gyanúja esetén a szérum kalciumszintje javallt.
VEZETÉS
A PPU egy sebészeti szükséghelyzet, amely magas halálozással jár, ha nem kezelik. Általánosságban elmondható, hogy minden PPU-ban szenvedő betegnek gyors újraélesztésre, intravénás antibiotikumokra, fájdalomcsillapításra, protonpumpa-gátló gyógyszerekre, nasogastricus csőre, vizeletkatéterre és műtéti forráskontrollra van szüksége.
Gyógyszeres kezelés PPU-ban
Az omeprazol és a H. pylori felszámolásának hármas terápiája hasznos kiegészítő a PPU kezelésében. Bizonyítékok azt mutatják, hogy az omeprazol és a hármas terápiás kezelés jelentősen csökkenti a kiújulás arányát. Az endoszkópiával végzett 8 hetes követés után kimutatott fekélygyógyulás szignifikánsan magasabb volt a hármas terápia felszámolási csoportjában [36]. A fekélyek 85 pont három százaléka gyógyult meg a hármas terápiás csoportban, szemben az egyedül omeprazol csoport 48,4% -ával. Számos más, különböző országokból származó tanulmány is bizonyította a hármas terápia felszámolását, miután a PPU egyszerű lezárása csökkentette a visszatérő fekély előfordulását [37,59,60]. Gyakorlatunk, hogy intravénás protonpumpa gátlót írunk fel 72-96 órán át, és azonnal utána kezdjük az orális hármas terápiát. Karbamid lélegeztető tesztet hajtunk végre a H. pylori felszámolásának megállapítására az orvosi kezelés befejezése után.
Nem operatív irányítás
Operatív irányítás
VAGOTÓMIA
A vagus ideg fontos szerepet játszik a gasztrin felszabadulásának és a gyomorsav szekréciójának szabályozásában, mivel a parietális sejteket kolinerg receptorokon keresztül stimulálja [70]. A vagális stimuláció a hisztamint és a gasztrint is felszabadítja az enterokromaffinhoz hasonló sejtekből és a G-sejtekből, amelyek viszont a parietális sejteket savas szekréció előállítására serkentik. A vagotómia a vagális törzseket (truncalis vagotomia) vagy a disztális idegrostokat (erősen szelektív vagotomia) transzfektáló eljárás. A truncalis vagotomia célja a gyomorsav-szekréció csökkentése, ezáltal csökkentve a visszatérő PUD kockázatát. A szelektív vagotomia, amely megkíméli a vagális törzsek máj- és celiakia-osztódását, magasabb hosszú távú kiújulási arányokkal jár [71]. Ezért a szelektív vagotomiát már nem hajtják végre. Tanulmányok kimutatták, hogy a fekély kiújulási aránya 42% volt a perforált nyombélfekélyben szenvedő betegeknél, akiknél egyszerű omentális tapasz-javítás történt [72,73]. Kevés prospektív randomizált vizsgálat számolt be lényegesen kevesebb fekély megismétlődésről azoknál a betegeknél, akiknél az omentális tapasz javításán túl vagotomiát végeztek [37,74]. Mindazonáltal a vagotomiát ritkán hajtják végre a PPU-nál, mivel olyan gyógyszerek állnak rendelkezésre, mint a hisztamin receptor antagonisták, a protonpumpa inhibitorok és a H. pylori felszámolása.
GASTRECTOMY
LAPAROSZKÓPOS JAVÍTÁS
„Az oldattal történő hígítás a szennyezés megoldása”. A műtét vége felé néhány sebész szívesen öntözi a hasüreget 6-10 literrel, sőt akár 30 liter meleg sóoldattal is, bár az irodalomban nem találtak bizonyítékot arra, hogy az öntözés csökkenthetné a szepszis kockázatát [98,99 ]. Másrészt a laparoszkópos műtét során kiváltott pneumoperitonuem növelheti a baktériumok terjesztésének kockázatát [100]. Úgy tűnik, hogy a sebész is preferálja, hogy a műtét végén hagy-e lefolyót vagy sem [101]. Nincs olyan bizonyíték, amely alátámasztaná, hogy a beömlés elhagyása csökkentheti az intraabdominális gyűjtemények előfordulását [101, 102]. Ellenkezőleg, a lefolyó fertőzéséhez és a bélelzáródás fokozott kockázatához vezethet [102]. A Schein által készített kérdőív azt mutatta, hogy a sebészek nyolcvan százaléka a fentebb ismertetett okok miatt nem hagyott csatornát műtét után [63]. Manapság ritkán alkalmazzák a gumiabroncs tesztet (figyelje meg a buborékokat, miután a tapasz víz alá merült), és a festék tesztet (a festék befecskendezésére a nasogastricus csövön keresztül) a szivárgás keresésére a PPU lezárása után (ábra (3. ábra)).
Laparoszkópos omentális tapasz javítását mutatja. V: Elülső nyombél perforáció; B: Laparoszkópos varrás; C: Omental tapasz; D: A hasüreg elhelyezése.
ÖN BŐVÍTHETŐ FÉM STENTEK
Az elsődleges sztentelés és a vízelvezetés új kezelési lehetőségként használható a PPU számára [103]. Nyolc PPU-ban szenvedő beteget önterjeszthető fém stentekkel kezeltek [103]. Két beteget posztoperatív szivárgás miatt sztenteléssel kezeltek a kezdeti műtéti zárás után, hat beteget primer stenteléssel kezeltek. Nyolc betegből hét szövődmények nélkül gyógyult meg, stentelés után 9-36 nap múlva bocsátották ki őket. Egy másik, 10 stenteléssel kezelt PPU-s beteg bevonásával végzett tanulmány szintén jó klinikai eredményeket mutatott [104]. Ez a tanulmány a stentkezelést minimális invazív alternatívaként jelezte, kevesebb komplikációval, mint a műtéti kezelés. Ezek a tanulmányok azt mutatják, hogy a PPU-ban szenvedő betegek elsődleges sztenteléssel és vízelvezetéssel kezelhetők, ahol képzés és szakértelem áll rendelkezésre. További adatokra van szükség a módszer hatékonyságának bizonyításához.
MARGINÁLIS ULCER PERFORÁCIÓ
MŰKÖDÉS utáni komplikációk
A PPU-kezelés jelentős posztoperatív morbiditással és mortalitással jár, függetlenül attól, hogy laparoszkópos vagy nyitott javítást végeznek-e [113]. Becslések szerint a műtét utáni mortalitás a PPU esetében 6% -10% [114]. 60 évesnél idősebb életkor, késleltetett kezelés 24 óránál hosszabb, a bemutatáskor bekövetkező sokk 100 Hgmm alatti szisztolés vérnyomással és az ezzel járó betegségek a fő kockázati tényezők, amelyek befolyásolják az eredményt [2 115]. A műtét utáni halálozás idősekben 3-5-ször magasabb [116]. Ennek oka lehet orvosi kísérő betegségek, késleltetett megjelenés, atipikus megjelenés vagy 24 órás késés a diagnózisban [116].
Helyi vizsgálatunkban 332 beteg vett részt, akiken PPU-műtétet végeztek, a posztoperatív szövődmények közé tartozott az intraabdominális gyűjtés (8,1%), a szivárgás (2,1%) és az újbóli műtét (1,2%) [51]. Az intraabdominális tályog továbbra is súlyos posztoperatív szövődmény a PPU műtét után. Ezért ennek a szövődménynek a megelőzése érdekében jó műtéti technikát kell alkalmazni. Alacsony szivárgási arányunk (2,1%) a korai bemutatással, azonnali diagnózissal, a korai újraélesztéssel és a megfelelő műtéttel magyarázható. A 30 d. Halálozásra vonatkozó adataink 7,2% -ot tettek ki, ami összehasonlítható egy friss dél-koreai tanulmányval [120]. Helyi vizsgálatunkban az alacsonyabb mortalitás oka lehet fiatalabb életkor (54,7), kevesebb társmorbiditás (16,2%) és kevesebb preoperatív sokkban szenvedő beteg (7,2%).
Egy nemrégiben készült tanulmány megvizsgálta a halálozás összefüggését a PPU-ban szenvedő betegek órákon kívüli felvételével [121]. Összesen 726 beteget vontak be ebbe a vizsgálatba, akiket műtéti úton kezeltek PPU-val. Ez a vizsgálat nem mutatott statisztikailag szignifikáns jelentőséget a 90-d mortalitás és az órákon kívüli felvétel között azoknál a betegeknél, akiket műtéti úton kezeltek PPU-val.
Az erőforrások megfelelő elosztása és az optimális ellátás biztosítása érdekében fontos, hogy a betegeket alacsony és magas halálozási kockázatra rétegezzük. Számos pontozási rendszer áll rendelkezésre a halálozás előrejelzésére.
PONTOSÍTÁSI RENDSZEREK A KIMUTATÁSOK ELŐREJELZÉSÉHEZ a PPU-ban
Mintegy 11 különböző pontozási rendszer, amelyet a PPU kimenetelének előrejelzésére használnak, azonosítható az irodalmon keresztül: a Boey-pontszám, az Amerikai Aneszteziológusok Társaságának (ASA) pontszáma, a Szepszis-pontszám, a Charlson-féle komorbiditási index, a Mannheim-peritonitis index (MPI) Akut fiziológia és krónikus egészségi állapotértékelés II (APACHE II), egyszerűsített akut élettani pontszám II (SAPS II), fiziológiai és operatív súlyossági pontszám a mortalitás és a megbetegedés fizikai részpontszámának felszámolásához (POSSUM-phys score, a mortalitás valószínűségi modelljei II (MPM II), Peptikus fekélyperforáció (PULP) pontszám, Hacettepe pontszám és Jabalpur pontszám [121]. E 11 pontozási rendszer közül a Boey és az ASA pontszám a leggyakrabban validált rendszerek [8,80,122-124] . Más pontozási rendszereket nem alkalmaznak széles körben a validálás hiánya vagy a klinikai alkalmazás komplexitása miatt. Hitelesítettük az ASA pontszámot, Boey-féle pontszámot, MPI és PULP pontszámot, és megállapítottuk, hogy mind a négy rendszer mérsékelt pontosságú a mortalitást 72% -77,2% -os vevő-operátor görbe alatti területtel határozza meg [51]. Egy nemrégiben végzett tanulmányban 148 beteg vett részt két szingapúri egyetemi kapcsolt kórházból, Lee és mtsai [125] beszámoltak arról, hogy a kiválasztott betegeknél 48 órán belüli prezentáció és fekélyméret 21.
Egy nemrégiben készült tanulmány 62 beteget vizsgált, akiket sürgősségi műtéten estek át a PPU-nál [126]. Ez a tanulmány a peritonealis folyadék mennyisége és a klinikai paraméterek közötti összefüggést vizsgálta PPU-ban szenvedő betegeknél. Ishiguro és mtsai [126] által leírt módszerek alkalmazásával CT-felvétel segítségével meg lehetett jósolni a felhalmozódott intraperitoneális folyadék mennyiségét. Ez a tanulmány kimutatta, hogy Ishiguro és mtsai [126] módszere hasznos volt az intraperitoneális folyadék mennyiségének előrejelzésére PPU-ban szenvedő betegeknél. Úgy gondolják, hogy hasznos lesz a posztoperatív szövődmények súlyosságának előrejelzésében, és hasznos a kezeléssel kapcsolatos döntéshozatalban is (ábra (4. ábra).
- Peptikus fekély (gyomorfekély) étrend és receptek
- Gyomorfekély Peptikus fekély tünetei, okai; Kezelés @DocOnline
- Peptikus fekély gyermekeknél
- Peptikus fekélybetegség - Emésztőrendszeri betegségek - Merck Manuals Professional Edition
- Peptikus fekély mini áttekintés az eset tekintetében - MedCrave online