Randomizált, kontrollált vizsgálat: az inulin hatása a testsúly-szabályozásra és a méhen kívüli zsírra prediabéteszben szenvedő betegeknél
Nicola D. Találd meg
Táplálkozási és dietetikai kutatócsoport, Imperial College, London, Hammersmith Hospital, London, W12 0NN UK
Cukorbetegség, endokrinológia és anyagcsere osztály, 6. emeleti Nemzetközösség épülete, Orvostudományi Kar, Imperial College Hammersmith Campus, Du Cane Road, London, W12 ONN, Egyesült Királyság
Anne Dornhorst
Diabetes, endokrinológia és anyagcsere osztály, Imperial College NHS Trust, London, Egyesült Királyság
Nick Oliver
Diabetes, endokrinológia és anyagcsere osztály, Imperial College NHS Trust, London, Egyesült Királyság
Jimmy D. Bell
Élettudományi Tanszék, Természettudományi és Technológiai Kar, University of Westminster, London, W1W 6UW UK
E. Louise Thomas
Élettudományi Tanszék, Természettudományi és Technológiai Kar, University of Westminster, London, W1W 6UW UK
Gary S. Frost
Táplálkozási és dietetikai kutatócsoport, Imperial College, London, Hammersmith Hospital, London, W12 0NN UK
Társított adatok
Absztrakt
Háttér
A máj, az izom és a hasnyálmirigy zsírszivárgása összefügg az inzulinrezisztenciával és a cukorbetegség kockázatával. A fogyás csökkenti a méhen kívüli zsírlerakódást és a cukorbetegség kockázatát, de az étvágy kompenzációs növekedése miatt nehéz fenntartani. A fermentálható szénhidrátok kimutatták, hogy csökkentik az étvágyat és az ételt, valamint elősegítik a testsúlycsökkenést a túlsúlyos személyeknél. Állatkísérletek során a fermentálható szénhidrátok csökkentik a méhen kívüli zsírt, függetlenül a fogyástól. Megvizsgáltuk a fermentálható szénhidrát inulin hatását a testsúly fenntartására, az étvágyra és a méhen kívüli zsírra prediabéteszes betegeknél.
Mód
Negyvennégy prediabéteszes alanyot randomizáltak 18 hetes inulin- vagy cellulóz-kiegészítésre. Az 1–9. Héten (súlycsökkenési szakasz) minden alanynak négy látogatása volt dietetikussal, hogy az 5% -os fogyás felé irányítsa őket. A 10–18. Héten (testsúly-fenntartó fázis) az alanyok folytatták a hozzárendelt kiegészítéseket, és felkérték őket, hogy tartsák fenn az elvesztett súlyukat, de további támogatást nem kaptak. Valamennyi alany részt vett a kezdeti, 9. és 18. heti tanulmányokon a súly mérése céljából; a zsírszövet és a méhen kívüli zsírtartalom értékelése mágneses rezonancia képalkotással és mágneses rezonancia spektroszkópiával; glükóz, inzulin és GLP-1 szintek étkezési tolerancia tesztet követően; étvágyat ad libitum étkezési teszttel és vizuális analóg mérleggel.
Eredmények
Elektronikus kiegészítő anyag
A cikk online verziója (doi: 10.1186/s12986-015-0033-2) kiegészítő anyagot tartalmaz, amely az engedélyezett felhasználók számára elérhető.
Háttér
Az életmódbeli beavatkozások jelentősen csökkenthetik a 2-es típusú cukorbetegség (T2DM) kialakulásának kockázatát [1], a fogyás az elsődleges közvetítője a kockázat csökkentésének [2]. A munkaigényes klinikai vizsgálatokon kívül azonban a hosszú távú fogyást köztudottan nehéz elérni [3, 4].
Az egyik magyarázat a sikeres fogyás fenntartásának ritkaságára az, hogy az energiahiány és a testzsír csökkenése mind az étvágy növekedésével, mind az étkezés mennyiségével együtt jár [5, 6]. Ezért az olyan beavatkozások, mint a glukagon-szerű peptid-1 (GLP-1) agonisták, amelyek célja az étvágy ilyen változásainak csökkentése vagy enyhítése, elősegítik a fogyás hosszú távú fenntartását [7]. Az emészthetetlen szénhidrátokat (élelmi rostokat) régóta összekapcsolják a csökkent táplálékfogyasztással [8], és az erjedhető szénhidrátok (FCHO) különösen hatékonyak lehetnek [8]. Ez a szénhidrátosztály emésztetlenül és felszívatlanul jut át a felső gyomor-bél traktusból a vastagbélbe, ahol a bakteriális fermentáció rövid láncú zsírsavakat (SCFA) eredményez, amelyek stimulálhatják a GLP-1-et és szabályozhatják az egyéb étvágyhormonokat [9]. Ezenkívül az FCHO-k természetes étrendi vegyületekként széles körben alkalmazható közegészségügyi beavatkozást jelenthetnek. Az étvágy természetes csökkenésének elősegítésével ritkább klinikai támogatásra lehet szükség. Egy túlsúlyos serdülőkön végzett egyéves vizsgálat során az inulin csoportban a testtömeg-index (BMI) szignifikánsan alacsonyabb emelkedést mutatott, anélkül, hogy egészségügyi szakemberektől kapott volna hozzájárulást [10].
A fogyás inzulinérzékenységre gyakorolt jótékony hatásának kulcsfontosságú közvetítője a méhen kívüli zsírvesztés [11], amely szoros összefüggésben áll az inzulinrezisztenciával és a T2DM-mel [11–13]. Érdekes módon az FCHO-ról kimutatták, hogy a fogyástól független állatkísérletek csökkentik a méhen kívüli zsírokat [14]. Ez felveti annak lehetőségét, hogy ez a természetes étrendi szénhidrát nemcsak fokozza a fogyást, hanem elősegítheti ennek az anyagcserére káros zsírnak az emberekben való elvesztését, még a fogyás elszámolása után is. Egészséges és inzulinrezisztens alanyokban az FCHO kimutatta, hogy javítja az inzulinérzékenységet [15, 16], de nem világos, hogy az ektópiás zsír csökkentése játszik-e szerepet. Egyetlen korábbi tanulmány sem vizsgálta az étrendi beavatkozás hatását a méhen kívüli zsírra prediabéteszes betegeknél.
Itt beszámolunk a 30 g/nap (4 hetes dózisemelési periódust követően) inulinpótlás hatásáról, amelyet egy 9 hetes súlycsökkentő program és egy 9 hetes testsúly-fenntartó periódus mellett végeztek. Feltételezzük, hogy az inulin nagyobb súlycsökkenés-fenntartást eredményez a prediabéteszes betegeknél a 18 hetes követés során, és elősegíti a méhen kívüli zsír- és inzulinrezisztencia csökkenését a súlyvesztéstől függetlenül, amelyet az arany-standard mágneses rezonancia képalkotás ( MRI) és mágneses rezonancia spektroszkópia (MRS) technikák.
Önkéntesek
A helyi háziorvosok nyilvántartásaiból ismert prediabétessel rendelkező vagy magas prediabétesz kockázati tényezőkkel rendelkező alanyokat azonosítottak. A vizsgálat előtt tájékozott beleegyezést kaptunk. A protokollokat az North West 1 Kutatási Etikai Bizottság hagyta jóvá (nyilvántartási szám: 10/H0717/32) (Klinikai vizsgálat száma:> NCT01841073), és megfelelt a Helsinki Nyilatkozatnak. Orális glükóz tolerancia tesztet (OGTT) végeztek a glikémiás állapot tisztázására [17]. A felvételi kritériumok az életkor ≥ 18 év volt, a BMI 25–35 kg/m 2, a prediabetes (az éhomi éhgyomri glükóz (IFG) és/vagy a csökkent a glükóz tolerancia (IGT)) az American Diabetes Association kritériumainak alkalmazásával [17] és a stabil testtömeg. 3 hónapig a vizsgálat előtt. Kizárási kritériumok voltak a normál glükóz tolerancia, a T2DM, a gyomor-bélrendszeri rendellenességek, a terhesség vagy a szoptatás, az étvágyat vagy a glükóz homeosztázisát befolyásoló gyógyszerek felírása, valamint a prebiotikus termékek fogyasztása vagy az antibiotikumok használata a vizsgálat kezdetétől számított 3 hónapon belül. Az önkénteseket BMI és nem alapján randomizálták egy véletlenszám-táblázat segítségével, 1: 1 elosztási arány mellett.
Kísérleti terv
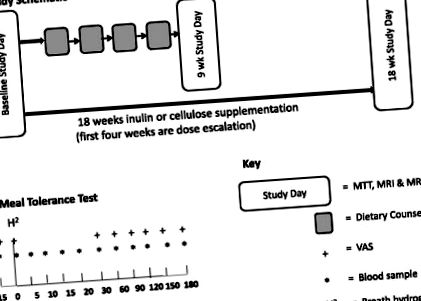
A vizsgálat kettős-vak, randomizált, párhuzamos kontroll vizsgálat volt, amelyben a 30 g/nap inulin (Synergy1, Orafti, Tienen, Belgium) és a kontroll cellulóz (Vitacel® Powdered Cellulose L 600–20, J. Rettenmaier & Söhne GmbH +) hatását vizsgálták. Co.) egy 9 hetes fogyás és 9 hetes testsúly-fenntartó program mellett (1. ábra). A cellulózrostot választottuk összehasonlítónak, mivel a (β4-1) kötésekkel összekötött glükózmolekulák elágazatlan polimerje minimális vastagbél fermentáción megy keresztül. A 30 g-os dózist csoportunk korábbi vizsgálatai alapján választottuk ki [18, 19]. Mindkét étrend-kiegészítőt 10 g tasakként adták naponta háromszor étellel vagy itallal. A gyomor-bélrendszeri mellékhatások csökkentése érdekében a kiegészítőket 2 hetente 10 g/nap-kal növelték, hogy elérjék a napi 30 g-os dózist. Ezért a kilenc hetes súlycsökkenési szakasz ötödik hetére minden alany a maximális 30 g/nap dózist kapta. Az inulin- és cellulóz tasakok A vagy B betűvel voltak ellátva, és egyébként azonosak voltak.
A tanulmány vázlatát bemutató vázlat, beleértve a vérminták időzítését, a VAS-t és a légzés-hidrogén mérését az MTT alatt. H 2: levegő hidrogén mérése; MTT: étkezési tolerancia teszt; MRS: mágneses rezonancia képalkotás; MRS: mágneses rezonancia spektroszkópia; VAS: vizuális analóg mérleg
A 9 hetes súlycsökkentő program során minden alany standardizált étrendi beavatkozáson esett át, amely négy, 2-3 hetes időtartamú étrendet tartalmaz, regisztrált dietetikussal együtt (1. ábra). A dietetikus elvakult a kiegészítők elosztása miatt. A keményítők, a fehérje, a tej és a tejtermékek, a zsírok és a cukrok, valamint a gyümölcsök és zöldségek energiaigényét és a hozzárendelt adagméretet a Hammersmith Kórházban kifejlesztett kész számlálóval határozták meg. A 9 hetes látogatást követően az alanyok nem kaptak további segítséget vagy támogatást a vizsgálati csoporttól. Csak arra kérték őket, hogy próbálják fenntartani az elvesztett súlyt.
Valamennyi alany részt vett egy kiindulási napon, 9 héten (a fogyás fázisának vége) és 18 héten (a testsúly fenntartó fázis vége) étkezési tolerancia teszten (MTT) (Ensure Plus ™ (220 ml), Teljes energia: 1380 kJ, 44,4 g szénhidrát, 10,8 g zsír, 13,8 g fehérje). A vérmintákat –15, 0, 5, 10, 15, 20, 30, 45, 60, 90, 120, 150, 180 percnél vettük a glükóz, az inzulin és a GLP-1 mérésére (1. ábra).
Az étvágyat az MTT során értékelték validált [20] vizuális analóg mérleg (VAS) alkalmazásával, gyakori időközönként, majd ad libitum étkezési tesztet [20]. A felhasznált étvágykérdések a következők voltak: „Mennyire éhes vagy most?” (általános éhség): "Szerinted mennyit ehetne most?" (várható élelmiszer-fogyasztás), "Mennyire lenne kellemes enni?" (enni vágy) és „Mennyire érzed jól magad jelenleg?” (teltségérzet a gyomorban) (1. kiegészítő fájl).
A testösszetételt egy 9 elektródás bioelektromos impedancia (BIA) eszközzel (Tanita BC-418 MA szegmentális testösszetétel-analizátor) értékeltük (Tanita Corporation, Tokió, Japán). A BIA eszköz becsléseket ad a testzsír% -áról (± 0,1%), a zsírtömegről (± 0,1 kg) és a szabad zsírtömegről (± 0,1 kg). Ezenkívül az alanyok egy része, akik alkalmasak voltak rá (nincs in situ fém vagy jelentett klaustrofóbia) (n = 20), MRI-n és MRS-en estek át a teljes és a regionális zsírmennyiség kiértékeléséhez a kiindulási, a 9. és a 18. héten. Gyors T1-súlyozott mágneses rezonancia a képeket 1,5 T-os Phillips Achiva szkennerrel (Phillips, Best, Hollandia) [21] készítettük, intrahepatocelluláris lipiddel (IHCL), valamint a soleus és a tibilalis izmokban lévő intramyocelluláris lipiddel (IMCL-S, ill. IMCL-T). MRS a korábban leírtak szerint [22].
A megfelelőséget úgy értékeltük, hogy megkérdeztük az alanyokat a fel nem használt tasakok visszaszolgáltatásáról, és a lehelet hidrogént a vastagbél fermentációjának helyettesítőjeként mértük egy légzés hidrogénmonitor segítségével (Gastrolyzer, Bedfont Scientific Ltd. Kent, Egyesült Királyság).
Laboratóriumi elemzés
A glükózt fluorid-oxalát csövekbe gyűjtöttük, és egy Architect ci8200 analizátorral (Abbott Diagnostics, Maidenhead, Egyesült Királyság) mértük, 0,3 mmol/l vizsgálati kimutatási határértékkel és 1% vizsgálaton belüli variációs koefficienssel (CV). A plazma inzulinmintákat a Vacutte® gél alvadási aktivátort tartalmazó szérum gélszeparátor csövekbe gyűjtöttük, és kereskedelmi radioimmun vizsgálati készlettel (Millipore; Watford, Egyesült Királyság) mértük. Az inzulin érzékenysége és a vizsgálaton belüli CV értéke 7,1 pmol, illetve 3,0% volt. A GLP-1 mintákat lítium-heparin csövekbe gyűjtöttük, aprotinint (Trasylol, Bayer, Newbury, Egyesült Királyság) (200 μl/7,5 ml vér) adtunk hozzá. A vérmintákat 4000 g-nál 4 ° C-on 10 percig centrifugáltuk, plazmába választottuk és -20 ° C-on tároltuk, amíg házon belüli radioimmunassay-vel meg nem analizáltuk [23]. A GLP-1 assay érzékenysége és a vizsgálaton belüli CV értéke 7,5 pmol/l, illetve 3,3% volt.
Számítások és statisztikai elemzés
Parnell és mtsai tanulmánya alapján. [24] várható súlycsökkenéssel 2,0 kg-mal és 2,0 kg-os szórással, 0,8 teljesítmény alapján a szignifikáns különbség kimutatására (P 1. Az inulin- és a cellulózcsoportok között az alapjellemzők egyikében sem volt különbség. Összesen 44 alanyból toboroztak és randomizáltak, közülük öt kilépett a vizsgálatból a 9. hét előtt, köztük egy inulint és egy cellulózot szed, akik mellékhatások miatt kiesnek. Egy másik alany kilépett a kilenc heti látogatást követően. Lásd a CONSORT diagramot (További Továbbá, a lemorzsolódás (n = 1) ütemezési nehézségei (n = 2), az MRI-vel kapcsolatos hozzájárulás visszavonása (n = 1) miatt, és már nem jogosultak MRI-re (n = 1), öt alany a kiindulási alapon és a kilencedik héten végzett MRI-vizsgálatok 18 hetesen nem voltak szkenneltek, ezért 19 alany 9 héten keresztül végzett MRI utóvizsgálatot (inulin csoport: három nő és hét férfi; cellulóz csoport: négy nő és öt férfi), és 14 alany teljesítette az utánkövetési MRI-t a 18. héten s inzulincsoport: három nő, hat férfi; cellulózcsoport: három nő és két férfi).
Asztal 1
Tárgyi jellemzők a vizsgálat egyes karjainál
| Nem (M: F) | 13: 8 | 11: 9 | 0,66 |
| Életkor (év) | 58,2 ± 12,0 | 59,7 ± 8,9 | 0,53 |
| Súly (kg) b | 88,2 ± 14,0 | 83,4 ± 19,7 | 0,28 |
| BMI (kg/m 2) | 30,8 ± 4,1 | 30,0 ± 2,3 | 0,41 |
| FPG (mmol/L) | 5,7 ± 0,5 | 5,9 ± 0,6 | 0,20 |
| 2hPG (mmol/L) | 7,3 ± 2,3 | 7,3 ± 2,0 | 0,99 |
| HbA1c (%) és (mmol/mol a) | 5,9 ± 0,1 (41,3 ± 1,4) | 5,7 ± 0,1 (38,8 ± 0,9) | 0,78 |
| Éhomi inzulin (pmol/L) | 95,4 (116,8) b | 114,1 (132,9) b | 0,17 |
Az értékek eszközök és SD. A nemet a férfiak és a nők arányában fejezik ki. A kiindulási változók egyikében sem volt szignifikáns különbség a csoportok között. FPG éhomi plazma glükóz; 2hPG 2 órás plazma glükóz
a zárójelben látható SI-egységek a HbA1c-hez
b Az éhomi inzulin nem volt normálisan elosztva, ezért a megadott értékek a mediánra vonatkoznak (interkvartilis tartomány)
- Cikkek Ingyenes próba Rendkívüli fogyókúrás étrendek Természetes - HazMat Management
- Félelmetes a legfrissebb fogyókúrás edzésterv bolt - HazMat Management
- Ajurvédikus tippek a testsúly kezeléséhez - Veda Wellness - Siker stressz nélkül Veda Wellness -
- BodyStart Keto Chia mag egészséges fogyás - HazMat Management
- Félelmetes fogyás 1 napos boltban pénzvisszafizetési garancia - HazMat Management