5.8: Élelmiszerek és üzemanyagok
- A termokémia és a táplálkozás kapcsolatának megértése.
A termokémiai mennyiségek, amelyekkel valószínűleg a leggyakrabban találkozik, az ételek kalóriaértékei. Az élelmiszer biztosítja azokat a nyersanyagokat, amelyekre a testednek szüksége van a sejtek pótlásához, valamint az energiát, amely biztosítja a sejtek működését. Ennek az energiának körülbelül 80% -a szabadul fel hő formájában, hogy fenntartsa a testhőmérsékletet, hogy életben maradjon. A táplálékkalória (nagybetűvel C), amelyet az élelmiszer-címkéken lát, 1 kcal (kilokalória). Az élelmiszerek kalóriatartalmát az égésentalpia (Δ Hcomb)/gramm alapján határozzuk meg, bombakaloriméterben mérve, az általános reakció felhasználásával.
\ [étel + felesleg \; O_ (g) \ jobbra CO_ (g) + H_O (l) + N_ (g) \ label \]
Két fontos különbség van azonban az élelmiszerek esetében jelentett kalóriaértékek és ugyanazon ételek kaloriméterben elégetett Δ Hcomb között. Először is, a joulában (vagy kilojoule-ban) leírt Δ Hcomb negatív minden éghető anyagra. Ezzel szemben az élelmiszer kalóriatartalmát mindig pozitív számként fejezzük ki, mert az energiatárolt. Ezért,
\ [kalória \; tartalom = - \ Delta H_ \ label \]
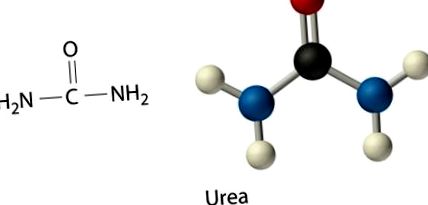
Másodszor, ha az ételeket kaloriméterben égetik el, az azokban lévő nitrogén (főként nitrogénben gazdag fehérjékből származik) N2-vé alakul. A testben azonban az élelmiszerekből származó nitrogén az ürítés előtt karbamiddá [(H2N) 2C = O] alakul át, nem pedig N2-vé. A bomba kalorimetriával mért karbamid Δ Hcomb-értéke -632,0 kJ/mol. Következésképpen a kalorimetriával mért entalpia-változás bármely nitrogéntartalmú ételnél nagyobb, mint amennyi energiát a test nyerne belőle. Az értékek különbsége megegyezik a karbamid Δ Hcomb-jával, szorozva az élelmiszer lebontásakor keletkező karbamid-molok számával. Ezt a pontot vázlatosan szemléltetik a következő egyenletek:
\ [étel + felesleg \; O_ \ left (g \ right) \ xrightarrow [] H értékek negatívak, és Hess törvénye szerint Δ H3 = Δ H1 + Δ H2. A Δ H1 nagyságának kisebbnek kell lennie, mint Δ H3, az étel kalorimetrikusan mért Δ Hcomb. Ezért az karbamid termelésével az N2 helyett az emberek kiválasztják az ételükben tárolt energia egy részét.
Különböző kémiai összetételük miatt az élelmiszerek kalóriatartalma nagyon eltérő. Mint korábban láthattuk, egy zsírsav, például a palmitinsav égés közben körülbelül 39 kJ/g, míg a cukor, például a glükóz 15,6 kJ/g. A zsírsavak és a cukrok a zsírok és a szénhidrátok építőkövei, amelyek az étrend két fő energiaforrása. A táplálkozási szakemberek általában a zsírok és a szénhidrátok esetében átlagosan 38 kJ/g (kb. 9 Cal/g) és 17 kJ/g (kb. 4 Cal/g) értéket rendelnek, bár az egyes élelmiszerek tényleges értékei eltérnek az összetételbeli különbségek miatt. A fehérjék, az étrend harmadik fő kalóriaforrása, szintén változnak. A fehérjék aminosavakból állnak, amelyek általános szerkezete a következő:
Egy aminosav általános szerkezete. Egy aminosav tartalmaz egy aminocsoportot (−NH2) és egy karbonsavcsoportot (−CO2H).
Az aminosavak amin- és karbonsavkomponenseik mellett számos más funkciós csoportot is tartalmazhatnak: R lehet hidrogén (–H); alkilcsoport (például -CH3); arilcsoport (például –CH2C6H5); vagy szubsztituált alkilcsoport, amely amint, alkoholt vagy karbonsavat tartalmaz (\ (\ PageIndex \) ábra). A 20 természetesen előforduló aminosav közül 10 szükséges az emberi étrendben; ezt a 10-et esszenciális aminosavaknak nevezzük, mert testünk nem képes szintetizálni őket más vegyületekből. Mivel R különböző csoportok bármelyike lehet, mindegyik aminosavnak eltérő értéke van a Hcomb-nak. A fehérjék átlagos Δ Hcomb-értéke általában 17 kJ/g (kb. 4 Cal/g).
\ (\ PageIndex \) ábra: 10 aminosav szerkezete. Ebben a csoportban az esszenciális aminosavak csillaggal vannak jelölve.
Számítsa ki a rendelkezésre álló energia mennyiségét, amelyet 1000 g alanin (aminosav) biológiai oxidációjával nyertek. Ne feledje, hogy a nitrogéntartalmú termék karbamid, nem N2, így az alanin biológiai oxidációja kevesebb energiát eredményez, mint az égés. Az Δ Hcomb értéke alaninra –1577 kJ/mol.
Adott: aminosav és Δ Hcomb/mol
Kérte: kalóriatartalom/gramm
- Írjon kiegyensúlyozott kémiai egyenleteket az alanin CO2, H2O és karbamid oxidációjához; karbamid elégetése; és az alanin elégetése. Szorozza meg az egyenletek mindkét oldalát a megfelelő tényezőkkel, majd rendezze át őket, hogy az egyenletek hozzáadásakor mindkét oldalról töröljék a karbamidot.
- Használja Hess törvényét arra, hogy az alanin karbamiddá történő oxidációjára vonatkozó ΔH kifejezést kapjuk az alanin és a karbamid Δ Hcomb-jában. Helyettesítse az Δ Hcomb megfelelő értékeit az egyenletbe, és oldja meg a Δ H-t az alanin CO2 -vá, H2O-val és karbamiddá történő oxidációjára.
- Számítsa ki a felszabadult energia mennyiségét grammonként úgy, hogy elosztja a H értékét az alanin moláris tömegével.
Az alaninból biológiailag rendelkezésre álló tényleges energia kevesebb, mint Δ Hcomb-ja, inkább Nea-karbamid-termelés miatt. Ismerjük az alanin és a karbamid Δ Hcomb értékeit, így Hess törvénye alapján kiszámíthatjuk az Δ H értékét az alanin CO2, H2O és karbamid oxidációjához.
A Kiegyensúlyozott kémiai egyenleteket írunk ki az (1) alanin CO2, H2O és karbamiddá történő oxidációjára; (2) karbamid elégetése; és (3) alanin elégetése. Mivel az alanin csak egyetlen nitrogénatomot tartalmaz, míg a karbamid és az N2 két nitrogénatomot tartalmaz, könnyebb egyensúlyba hozni az 1. és a 3. egyenletet, ha 2 mol alanin oxidációjára írjuk őket:
\ [\ balra (1 \ jobbra) \; \; 2C_H_NO_ \ left (s \ right) + 6O_ \ left (g \ right) \ rightarrow 5CO_ \ left (g \ right) + 5H_O \ left (l \ right) + \ left (H_N \ right) _C = O \ left ( s \ jobb) \]
\ [\ balra (2 \ jobbra) \; \; \ balra (H_N \ jobbra) _C = O \ balra (s \ jobbra) + \ dfracO_ \ balra (g \ jobbra) \ jobbra CO_ \ balra (g \ jobbra) + 2H_O \ balra (l \ jobbra) + N_ \ balra (g \ jobb) \]
\ [\ balra (3 \ jobbra) \; \; \ bal (1 \ jobb) \; \; 2C_H_NO_ \ left (s \ right) + \ dfracO_ \ left (g \ right) \ rightarrow 6CO_ \ left (g \ right) + 7H_O \ left (l \ right) + N_ \ left (g \ right) \]
Az 1. és 2. egyenlet hozzáadásával és a karbamid mindkét oldalról történő törlésével közvetlenül a teljes kémiai egyenletet kapjuk:
\ [\ balra (1 \ jobbra) \; \; 2C_H_NO_ \ left (s \ right) + 6O_ \ left (g \ right) \ rightarrow 5CO_ \ left (g \ right) + 5H_O \ left (l \ right) + \ cancelN \ right) _C = O \ left (s \) jobbra)> \]
\[ \megszünteti< \left ( 2 \right ) \; \; \left( H_N \right )_C=O\left ( s \right )> + \ dfracO_ \ left (g \ right) \ rightarrow CO_ \ left (g \ right) + 2H_O \ left (l \ right) + N_ \ left (g \ right) \]
\ [\ balra (3 \ jobbra) \; \; \ bal (1 \ jobb) \; \; 2C_H_NO_ \ left (s \ right) + \ dfracO_ \ left (g \ right) \ rightarrow 6CO_ \ left (g \ right) + 7H_O \ left (l \ right) + N_ \ left (g \ right) \]
B Hess törvénye szerint Δ H3 = Δ H1 + Δ H2. Tudjuk, hogy Δ H3 = 2Δ Hcomb (alanin), Δ H2 = Δ Hcomb (karbamid) és Δ H1 = 2Δ H (alanin → karbamid). A megfelelő értékek átrendezése és helyettesítése megadja
\ [= 2 \ bal (-1577 \; kJ/mol \ jobb) - \ bal (-632.0 \; kJ/mol \ jobb) \] = -2522 \; kJ/\ bal (2 \; mol \; analin \ jobb) \]
Így ΔH (alanin → karbamid) = -2522 kJ/(2 mol alanin) = -1261 kJ/mol alanin. Az alanin oxidációja karbamid, nem pedig nitrogénné következtében a felszabaduló energia mennyiségének körülbelül 20% -os csökkenését eredményezi (−1261 kJ/mol versus −1577 kJ/mol).
C Az alanin biológiai oxidációjával grammonként felszabaduló energia
Ez egyenlő -3,382 Cal/g.
Számítsa ki a valin (egy aminosav) CO2-dá, H2O-val és karbamiddá történő oxidációja során felszabaduló energiát grammonként. Jelentse válaszát három jelentős számra. A valin esetében a Δ Hcomb értéke −2922 kJ/mol.
−22,2 kJ/g (−5,31 Cal/g)
Az élelmiszerek bejelentett kalóriatartalma nem tartalmazza a H Hombot azokra az összetevőkre, amelyek nem emészthetők, például rostokra. Sőt, a húsok és gyümölcsök 50% -70% víz, amelyet O2 nem képes oxidálni, hogy energiát nyerjen. Tehát a víz nem tartalmaz kalóriát. Egyes ételek nagy mennyiségű rostot tartalmaznak, amely elsősorban cukrokból áll. Annak ellenére, hogy a rostot úgy lehet égetni egy kaloriméterben, mint a glükózt, hogy széndioxidot, vizet és hőt nyújtson, az embereknek hiányoznak az enzimek, amelyek ahhoz szükségesek, hogy a rostot apróbb, oxidálható molekulákra bontsák. Ezért a rost szintén nem járul hozzá az élelmiszerek kalóriatartalmához.
\ (\ PageIndex \) táblázat: 8 oz szelet sült marhahús hozzávetőleges összetétele és üzemanyag-értéke FogalmazásKalóriák
| 97,5 g vizet | × 0 Cal/g = 0 |
| 58,7 g fehérje | × 4 Cal/g = 235 |
| 69,3 g zsír | × 9 Cal/g = 624 |
| 0 g szénhidrát | × 4 Cal/g = 0 |
| 1,5 g ásványi anyagot | × 0 Cal/g = 0 |
| Össztömeg: 227,0 g | Összes kalória: kb. 900 Cal |
Az ételek kalóriatartalmát kétféleképpen határozhatjuk meg. A legpontosabb módszer egy gondosan lemért minta szárítása és égési reakció végrehajtása bomba kaloriméterben. A tipikusabb megközelítés azonban az, hogy elemezzük az élelmiszer fehérjét, szénhidrátot, zsírt, vizet és „ásványi anyagokat” (mindent, ami nem ég), majd kiszámoljuk a kalóriatartalmat az egyes energiát termelő komponensek átlagértékeinek felhasználásával ( 9 Cal/g zsírok, 4 Cal/g szénhidrátok és fehérjék, valamint 0 Cal/g víz és ásványi anyagok esetében). Erre a megközelítésre mutat példát a \ (\ PageIndex \) táblázat a sült marhahús szeletére. Néhány általános étel összetételét és kalóriatartalmát a \ (\ PageIndex \) táblázat tartalmazza.
Mivel a Kalória ilyen nagy mennyiségű energiát képvisel, néhány közülük hosszú utat tesz meg. Átlagosan 73 kg (160 font) embernek 67 kal/órára (1600 kal/nap) van szüksége az alapvető biokémiai folyamatok táplálásához, amelyek életben tartják az illetőt. Erre az energiára van szükség a testhőmérséklet fenntartásához, a szívverés fenntartásához, a légzéshez használt izmok meghajtásához, kémiai reakciók végrehajtásához a sejtekben és az idegimpulzusok küldéséhez, amelyek vezérlik ezeket az automatikus funkciókat. A fizikai aktivitás megnöveli a szükséges energia mennyiségét, de nem annyival, amennyit sokan remélünk (táblázat \ (\ PageIndex \) táblázat). Egy közepesen aktív egyénnek kb. 2500–3000 kal/napra van szüksége; a sportolók vagy mások, akik erõs tevékenységet folytatnak, naponta 4000 Cal-t égethetnek el. A felesleges kalóriabevitelt a szervezet tárolja későbbi felhasználás céljából, általában zsír formájában, ami a legkompaktabb módja az energiatárolásnak. Ha több energiára van szükség, mint az étrend-ellátás, a tárolt üzemanyagok mobilizálódnak és oxidálódnak. Általában kimerítjük a tárolt szénhidrátkészletet, mielőtt a zsírok felé fordulnánk, ami részben az alacsony szénhidráttartalmú diéták népszerűségét is jelenti.
Táblázat \ (\ PageIndex \): A különféle tevékenységeket végző 160 fontos személy hozzávetőleges energiafelhasználása TevékenységCal/h
| alvás | 80 |
| autót vezet | 120 |
| álló | 140 |
| enni | 150 |
| gyaloglás 2,5 mph | 210 |
| füvet nyírni | 250 |
| úszás 0,25 mph | 300 |
| görkorcsolyázás | 350 |
| tenisz | 420 |
| kerékpározás 13 mph | 660 |
| futás 10 mph | 900 |
Mennyi az a kalóriaszám, amelyet egy 30 emeletes épületre felmászó 72,6 kg-os személy használ fel? (Tegyük fel, hogy minden lépcsősor 14 láb magas.) Hány gramm glükóz szükséges ahhoz, hogy ezt az energiamennyiséget ellátja? (A glükóz elégetése során felszabaduló energiát az 5.5.4. Példa számította ki.).
Adott: a glükóz elégetésével felszabaduló tömeg, magasság és energia
Kérte: elfogyasztott kalóriák és a szükséges glükóz tömege
- Konvertálja a tömeget és a magasságot SI egységekre, majd cserélje ki ezeket az értékeket az 5.6. Egyenletbe a potenciális energia változásának kiszámításához (kilojoule-ban). Ossza el a kiszámított energiát 4,184 Cal/kJ-vel, hogy a potenciális energiaváltozást kalóriává alakítsa.
- Használja az 5.5.4. Példában kapott értéket a glükóz elégetéséhez az energiamennyiség biztosításához szükséges glükóz tömegének kiszámításához.
A lépcső megmászásához szükséges energia megegyezik a személy potenciális energiájának (PE) különbségével az épület tetején és a talaj szintjén.
A Emlékezzünk vissza, hogy PE = mgh. Mivel m és h nem SI egységekben vannak megadva, ezeket kilogrammra, illetve méterre kell átalakítanunk
\ [PE = \ bal (72,6 \; kg \ jobb) \ bal (9,81 \; m/s ^ \ jobb) \ bal (128 m \ jobb) = 8,55 × 10 ^ \ bal (kg \ cdot m ^/s ^ \ jobbra) = 91,2 kJ \]
A kalóriákká való átalakításhoz 4,184 kJ/kcal-val osztjuk fel:
\ [PE = \ left (91.2 \; \ cancel \ right) \ left (\ dfrac> \ right) = 21.8 \; kcal = 21.8 \; Cal \]
B Mivel a glükóz elégetése 15,6 kJ/g-ot eredményez (5. példa), a 85,5 kJ energiaellátáshoz szükséges glükóz tömege
\ [PE = \ left (91.2 \; \ cancel \ right) \ left (\ dfrac> \ right) = 5,85 \; g \; glükóz \]
Ez a tömeg csak körülbelül egy teáskanál cukornak felel meg! Mivel a test csak körülbelül 30% -ban hatékonyan használja fel a glükózban lévő energiát, a tényleges szükséges glükózmennyiség nagyobb lenne: (100%/30%) × 5,85 g = 19,5 g. Mindazonáltal ez a számítás azt mutatja be, hogy sok embernek nehézségei vannak abban, hogy egyedül testmozgással próbáljon lefogyni.
Számolja ki, hogy egy 160 fontos embernek hányszor kellene megmásznia az Egyesült Államok legmagasabb épületét, a chicagói 110 emeletes Willis-tornyot, hogy leégjen 1,0 font tárolt zsírt. Tegyük fel, hogy az épület minden szintje 14 láb magas, és 9,0 kcal/g zsírtartalmat használjon.
Az 5.8.2. Példa számításai figyelmen kívül hagynak különféle tényezőket, például azt, hogy az ember milyen gyorsan mászik. Bár a sebesség nem releváns a potenciális energia változásának kiszámításakor, nagyon fontos a lépcsőn való feljutáshoz ténylegesen szükséges energiamennyiség szempontjából. A számítások figyelmen kívül hagyják azt a tényt is, hogy a test kémiai energiájának átalakítása mechanikai munkává lényegesen kevesebb, mint 100% -ban hatékony. Az 5.8.3. Táblázatban felsorolt különféle tevékenységekhez elfogyasztott átlagos energia szerint az embernek 4,5 óránál többet kell futnia 10 km/h sebességgel, vagy 6 órán át 13 km/h sebességgel kerékpárral 1 lb zsír elégetéséhez. × 9,0 Cal/g = 4100 Cal). De ha az ember napi 6 óránként 13 km/h sebességgel közlekedik a hét 6 napján, akkor ez a személy 50 kg zsírból éget el egy év leforgása alatt (természetesen feltételezve, hogy a kerékpáros nem növeli kalória bevitele a gyakorlat ellensúlyozására).
Összegzés
A termokémiai koncepciók alkalmazhatók az élelmiszerekben rendelkezésre álló tényleges energia meghatározására. A táplálkozási kalória 1 kcal-nak (4,184 kJ) felel meg. Az élelmiszerek kalóriatartalma a grammban Δ Hcomb. A nitrogéntartalmú anyagok elégetésével N2 (g) keletkezik, de az ilyen anyagok biológiai oxidációja karbamidot eredményez. Ezért a nitrogéntartalmú anyagokból, például fehérjékből rendelkezésre álló tényleges energia kevesebb, mint a karbamid Δ Hcomb-értéke, szorozva az előállított karbamid molok számával. Az ételek tipikus kalóriatartalma 9 Cal/g zsírok esetében, 4 Cal/g szénhidrátok és fehérjék esetében, és 0 Cal/g víz és ásványi anyagok esetében.
- Egészségtelen; olyan ételek, mint a kávé, a tészta, a vaj, amelyek jók az Ön számára - Business Insider
- Union City CA pszichiáter orvosai - IBS-D tünetek, étrend, elkerülendő ételek, kezelések és okok
- A mosatlan kés és reszelő baktériumokat terjeszthet az ételek között - NDTV Food
- A Foods amerikaiak egykor szerették a művészetet enni; Culture Smithsonian magazin
- Az ételek, amelyekből többet kell enni télen - a bemelegítés