A diéta által kiváltott ateroszklerózis és az endothel diszfunkció gátlása az Apolipoprotein E/Angiotenzin II 1A típusú receptor kettős kiütéses egerekben
A Klinik für Innere Medizin III-ból (S.W., T.C., M.B., G.N.), Universitätsklinikum des Saarlandes, Homburg/Saar, Németország; Aventis Pharma Deutschland (M.v.E.), Cardiovascular Disease Group, Frankfurt/Main, Németország; és Institut für Kardiovaskuläre Physiologie (I. F.), Johann W. Goethe-Egyetem, Frankfurt am Main, Németország.
A Klinik für Innere Medizin III-ból (S.W., T.C., M.B., G.N.), Universitätsklinikum des Saarlandes, Homburg/Saar, Németország; Aventis Pharma Deutschland (M.v.E.), Cardiovascular Disease Group, Frankfurt/Main, Németország; és Institut für Kardiovaskuläre Physiologie (I. F.), Johann W. Goethe-Egyetem, Frankfurt am Main, Németország.
A Klinik für Innere Medizin III-ból (S.W., T.C., M.B., G.N.), Universitätsklinikum des Saarlandes, Homburg/Saar, Németország; Aventis Pharma Deutschland (M.v.E.), Cardiovascular Disease Group, Frankfurt/Main, Németország; és Institut für Kardiovaskuläre Physiologie (I. F.), Johann W. Goethe-Egyetem, Frankfurt am Main, Németország.
A Klinik für Innere Medizin III-ból (S.W., T.C., M.B., G.N.), Universitätsklinikum des Saarlandes, Homburg/Saar, Németország; Aventis Pharma Deutschland (M.v.E.), Cardiovascular Disease Group, Frankfurt/Main, Németország; és Institut für Kardiovaskuläre Physiologie (I. F.), Johann W. Goethe-Egyetem, Frankfurt am Main, Németország.
A Klinik für Innere Medizin III-ból (S.W., T.C., M.B., G.N.), Universitätsklinikum des Saarlandes, Homburg/Saar, Németország; Aventis Pharma Deutschland (M.v.E.), Cardiovascular Disease Group, Frankfurt/Main, Németország; és Institut für Kardiovaskuläre Physiologie (I. F.), Johann W. Goethe-Egyetem, Frankfurt am Main, Németország.
A Klinik für Innere Medizin III-ból (S.W., T.C., M.B., G.N.), Universitätsklinikum des Saarlandes, Homburg/Saar, Németország; Aventis Pharma Deutschland (M.v.E.), Cardiovascular Disease Group, Frankfurt/Main, Németország; és Institut für Kardiovaskuläre Physiologie (I. F.), Johann W. Goethe-Egyetem, Frankfurt am Main, Németország.
Ön a cikk legfrissebb verzióját nézi. Előző verziók:
Absztrakt
Háttér- Az 1-es típusú angiotenzin II (AT1) receptor aktiválása potenciálisan részt vesz az ateroszklerózis multifaktoriális patogenezisében.
Következtetések - Az AT1A receptor genetikai megzavarása a vaszkuláris oxidatív stressz, az endothel diszfunkció és az ateroszklerotikus elváltozás kialakulásának gátlásához vezet ApoE -/- egerekben, a vérnyomástól és a plazma koleszterinszintjétől függetlenül. Ezek az eredmények jelzik az AT1 receptor aktiváció alapvető szerepét az aterogenezisben.
Az érelmeszesedés patogenezise magában foglalja a kockázati tényezők elhúzódó expozícióját és a rosszul ismert genetikai hajlamot. 1 Az oxidatív stressz és a gyulladás döntően részt vesz az érelmeszesedés megindulásában és előrehaladásában, ami a makrofágok és limfociták fokozott vonzódásához, tapadásához és inváziójához, lipidek lerakódásához az érfalban, plakkképződéshez és az előre kialakult érelmeszesedés elváltozásainak destabilizálásához vezet. 2,3
Ezt a felfogást azonban eddig csak mechanisztikus és farmakológiai vizsgálatok bizonyították. Az AT1 receptor aktivációjának ateroszklerózisban betöltött szerepének tesztelésére egy másik, specifikusabb modellben genetikai megközelítést alkalmaztunk. Az Apolipoprotein E– hiányos (ApoE -/-) egerek korai érelmeszesedésben szenvednek, amelynek alapja egy súlyos lipid rendellenesség, amelyet koleszterinben gazdag étrend is kiegészít. 14 Dupla-knockout állatokat generáltunk, akiknek hiányos volt az ApoE és az AT1A receptor, és megvizsgáltuk a koleszterinben gazdag étrend hatását a vaszkuláris oxidatív stressz, az endotheliális diszfunkció és az ateroszklerotikus elváltozások kialakulására ebben a lipidek által kiváltott ateroszklerózis modellben.
Mód
Olajvörös O oldatot, sókat és egyéb vegyszereket a Sigma Chemicaltól vásároltak. Az L-012-et a Wako Chemicals-tól szereztük be.
Állatok és eljárások
A vaszkuláris reaktív oxigénfajták mérése
A szuperoxid felszabadulást az intakt aorta szegmensekben L-012 kemilumineszcenciával határoztuk meg. Az L-012 egy szuperoxid gyökök iránti nagy érzékenységű luminol-származék, amely önmagában nem gyakorolja a redox-ciklust. 15 Aortát gondosan kivágtunk és hűtött, módosított Krebs-HEPES pufferbe helyeztünk (pH 7,4; mmol/l-ben: NaCl 99,01, KCl 4,69, CaCl2 1,87, MgSO4 1,20, Na HEPES 20,0, K2HPO4 1,03, NaHCO3 25,0, D (+) glükóz 11,1). A kötőszövetet eltávolítottuk, és az aortákat 2 mm-es szegmensekre vágtuk. Az aorta szegmenseket szcintillációs fiolákba helyeztük, amelyek Krebs-HEPES puffert tartalmaztak 100 μmol/L L-012-vel, és 5 percig inkubáltuk. A kemilumineszcenciát ezután 15 perc alatt értékeltük egy szcintillációs számlálóban (Lumat LB 9501, Berthold), 1 perces időközönként. Az edényszegmenseket ezután megszárítottuk, és meghatároztuk a száraz tömeget. A szuperoxid felszabadulást relatív kemilumineszcenciában fejezzük ki az aorta szövet milligrammjára számítva.
Az aorta gyűrű előkészítése és a feszültség rögzítése
A leszálló aorta kivágása után az edényt hűtött pufferba merítettük, amely mmol/l NaCl 118,0, CaCl2 2,5, KCl 4,73, MgCl2 1,2, KH2PO4 1,2, NaHCO3 25,0, Na EDTA 0,026, D (+) glükóz 5,5, mmol/l koncentrációban tartalmazta. pH 7,4. Az adventi szövetet gondosan eltávolítottuk. Három milliméteres gyűrűket a fent leírt pufferrel (37 ° C; folyamatosan levegőztetve 95% O2 és 5% CO2-val) töltött szervfürdőkbe szereltünk, erőátalakítóhoz rögzítettük, és izometrikus feszültséget rögzítettünk. Az érszakaszokat fokozatosan 60 perc alatt nyújtjuk 10 mN nyugalmi feszültségig, amely a kísérlet során fennmaradt, és további 30 percig hagytuk egyensúlyba lépni. A kumulatív koncentráció-válasz görbék eléréséhez növekvő koncentrációban adtak hozzá gyógyszereket: KCl 20 és 40 mmol/L, fenilefrin 1 nmol/L - 10 μmol/L, karbachol 10 nmol/L - 100 μmol/L és nitroglicerin 1 nmol/L 10 μmol/l-ig. A gyógyszer koncentrációja megnőtt, amikor az érszűkület vagy az érelaxáció befejeződött. A gyógyszereket a következő anyag hozzáadása előtt kimosták.
Ateroszklerotikus elváltozások festése és morfometriai elemzés
Statisztikai analízis
Az adatokat átlag ± SEM formában mutatjuk be. A statisztikai elemzést ANOVA teszttel, majd Neuman-Keuls post hoc analízissel végeztük. P A -/-, az ApoE -/- és az ApoE -/- -AT1 -/- egereknek 7 héten át 1,25% koleszterint tartalmazó magas zsírtartalmú étrendet adtak. Az 1. táblázat a vér lipidjeinek plazmakoncentrációit mutatja. A vad típusú és az AT1 -/- egerekkel ellentétben az összkoleszterin, a HDL-koleszterin és az LDL-koleszterin plazmakoncentrációja szignifikánsan magasabb volt az ApoE -/- és az ApoE -/- -AT1 -/- állatokban. Nem voltak szignifikáns különbségek az ApoE -/- és az ApoE -/- - AT1 -/- egerek között.
1. TÁBLÁZAT Vérzsírok, vérnyomás és renin aktivitás
SBP, pulzus és plazma renin aktivitás
Az SBP-t és a pulzusszámot minden állatcsoportban farok-mandzsetta méréssel mértük. Az 1. táblázat mutatja az SBP szintjét és a pulzusszámot 7 hét magas koleszterinszintű diétás kezelés után. Az SBP szignifikánsan alacsonyabb volt az AT1 -/- és az ApoE -/- -AT1 -/- egerekben, mint a vad típusú és az ApoE -/- állatokban. Az állatcsoportok között nem volt szignifikáns különbség a pulzusszámban. Ezenkívül a koleszterinben gazdag étrend után minden csoportban meghatároztuk a plazma renin aktivitását. Nem észleltünk szignifikáns különbséget a vad típusú, AT1 -/-, ApoE -/- és ApoE -/- -AT1 -/- egerek között (1. táblázat).
Ateroszklerotikus elváltozás kialakulása
Az ateroszklerotikus elváltozások kialakulását 7 hét koleszterinben gazdag étrend után kvantifikáltuk vad típusú, AT1 -/-, ApoE -/- és ApoE -/- -AT1 -/- állatokban olajvörös O festésekkel, majd makroszkópos a leszálló mellkasi aorta elemzése, valamint az aorta sinus és a felemelkedő aorta szövettani elemzése. Az 1. ábra a négy állatcsoport reprezentatív aorta készítményeit és aorta keresztmetszeteit mutatja. A vad típusú és az AT1 -/- egerek az aorta egyik vizsgált részén sem mutattak ateroszklerózis jeleit. Ezzel szemben az ApoE -/- egerek súlyos ateroszklerózist mutattak ki az aorta sinusban és az emelkedő aortában, kisebb mértékben a leszálló mellkasi aortában. Az életkornak megfelelő ApoE -/- -AT1 -/- egereknél az aorta összes vizsgált részén szinte hiányzott az érelmeszesedés kialakulása. ApoE -/- és ApoE -/- -AT1 -/- egerekben az érelmeszesedés kialakulásának kvantitatív elemzését a 2. táblázat mutatja. 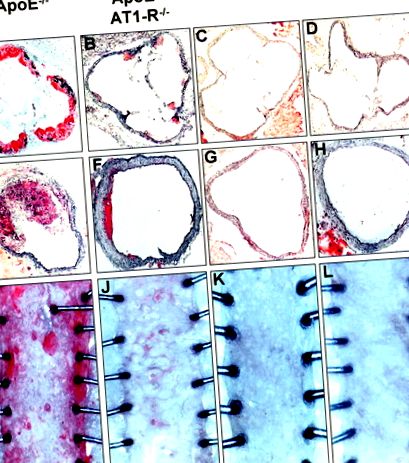
1.ábra. Ateroszklerotikus elváltozás kialakulása. Az ateroszklerotikus elváltozás kialakulását 7 hetes koleszterinben gazdag étrenddel végzett kezelés után határoztuk meg aorta sinusban (A bár D) és emelkedő aortában (E-H; szövettani elemzés) és csökkenő mellkasi aortában (I-L; makroszkopikus elemzés) olajvörössel O festés. A vad típusú (WT), AT1 -/-, ApoE -/- és ApoE -/- -AT1 -/- kettős knockout egerek reprezentatív szakaszai. Az AT1-R -/- az AT1 -/- egereket jelzi.
2. TÁBLÁZAT Ateroszklerotikus elváltozás mérete
Érrendszeri funkció
Koleszterinnel dúsított étrenddel történő kezelés után az érrendszer működését izolált aorta gyűrűs készítményekben értékeltük. A vad típusú és az AT1 -/- egerekkel ellentétben az endothelium-függő értágulat szignifikánsan károsodott az ApoE -/- egerekben, karbachollal történő stimulációval értékelve (2A. Ábra). Az ApoE -/- -AT1 -/- egereknél nem alakult ki endothel diszfunkció, és az endothelium-függő értágulat hasonló volt a vad típusú és az AT1 -/- állatokhoz (2A. Ábra). A nitroglicerin által kiváltott endothel-független vazorelaxáció minden csoportban hasonló volt (2B. Ábra). Ezenkívül a fenilefrin vagy a KCl által kiváltott érszűkület hasonló volt minden csoportban (az adatokat nem közöljük).
2. ábra. Érrendszeri működés. 7 hetes, koleszterinben gazdag étrenddel történő kezelés után a WT, AT1 -/-, ApoE -/- és ApoE -/- - AT1 -/- egerek aorta szegmenseit izoláltuk, és funkcionális teljesítményüket szervkamrás kísérletekben értékeltük. . A karbachol (A) által indukált endothelium-függő értágulat és a nitroglicerin (B) által kiváltott endothelium-független vazorelaxáció látható, mindkettő a maximális fenilefrin által kiváltott érszűkület százalékában kifejezve. Átlag ± SEM, n = 6 csoportonként. *P -/-. A WT a vad típust jelzi.
Vaszkuláris oxidatív stressz
A szuperoxid gyökök felszabadulását L-012 kemilumineszcencia vizsgálatokkal mértük vad típusú, AT1 -/-, ApoE -/- és ApoE -/- -AT1 -/- egerek intakt aorta szegmenseiben. A 3. ábra azt mutatja, hogy a vaszkuláris szuperoxid felszabadulás kétszeresen növekedett ApoE -/- egerekben a vad típusú állatokhoz képest (a vad típus 195 ± 44% -a; P -/- -AT1 -/- egerek (a vad típus 96 ± 27% -a; P -/-).
3. ábra. Érrendszeri szuperoxid termelés. 7 hetes, koleszterinben gazdag étrenddel történő kezelés után vad típusú (WT), AT1 -/-, ApoE -/- és ApoE -/- - - AT1 -/- egerek aortáit kivágtuk, és az érrendszeri szuperoxid termelését érintetlenül az aorta szegmenseket L-012 kemilumineszcencia vizsgálatokkal számszerűsítettük. A szuperoxid felszabadulást relatív kemilumineszcenciában fejezzük ki az aorta szövet milligrammjára számítva. Átlag ± SEM, n = 8 csoportonként. *P -/- .
A hidralazinnal vagy irbezartánnal végzett kezelés hatása az ateroszklerotikus elváltozások kialakulására és az érrendszer működésére
A vérnyomáscsökkenés ateroszklerotikus elváltozások kialakulására és érrendszeri működésére gyakorolt hatásának tisztázása érdekében a hím 12 hetes ApoE -/- egereket vagy vazodilatátor hidralazinnal, vagy AT1 receptor antagonistával irbezartánnal, a magas zsírtartalmú, koleszterinszinttel párosítva kezelték. gazdag étrend 7 hétig. Mindkét kezelés jelentős SBP-csökkenést eredményezett ugyanarra a szintre, mint a kettős kiütéses egereknél (ApoE -/- -AT1 -/-, 83 ± 2 Hgmm; ApoE -/- plusz hidralazin, 87 ± 2 Hgmm; ApoE -/- plusz irbezartán, 86 ± 3 Hgmm; mind P -/-). A jelentős SBP-csökkenés ellenére a hidralazinnal kezelt ApoE -/- egerekben semmilyen hatást nem figyeltünk meg az ateroszklerotikus elváltozások képződésében a hordozóval kezelt ApoE -/- állatokkal összehasonlítva (4A. És 4C. Ábra; 2. táblázat). Ezzel szemben az irbezartán-kezelés az ateroszklerotikus elváltozás képződésének jelentős gátlását eredményezte az ApoE -/- egerekben (4B. És 4D. Ábra; 2. táblázat). Ezenkívül az AT1 receptor antagonistával végzett kezelés az endothelium-függő vazodilatáció jelentős javulásához vezetett az aorta gyűrűs készítményekben, míg a hidralazinnal kezelt ApoE -/- egerekben az endothelium funkció károsodott, azonosak a hordozóval kezelt ApoE -/- állatokkal (ábra 4E). Végül, a hidralazin-kezelés nem volt hatással a vaszkuláris szuperoxid termelésére az ApoE -/- egerekben (a vad típus 200 ± 38% -a; P -/-).
4. ábra. Ateroszklerotikus elváltozás kialakulása és vaszkuláris működés hidroazinnal vagy irbezartánnal kezelt ApoE -/- egerekben. Az ApoE -/- egereket 7 hétig koleszterinben gazdag táplálékkal kezeltük, vagy vivőanyaggal, hidralazinnal vagy irbezartánnal. A-tól D-ig, ateroszklerotikus elváltozás képződése az aorta sinusban (A, B) és felmenő aortában (C, D), olajvörös O festéssel meghatározva (szövettani elemzés). A hidralazinnal kezelt és az irbezartánnal kezelt ApoE -/- egerek reprezentatív szakaszai. E, a karbachol által indukált aorta gyűrűs készítmények endothelium-függő vazodilatációja, a fenilefrin által kiváltott maximális vazokonstrikció százalékában kifejezve. Átlag ± SEM, n = 8 csoportonként. *P -/-. Irb irbezartánt jelöl; Hy, hidralazin.
Vita
A felgyorsult érelmeszesedéssel járó hiperkoleszterinémia az érrendszerben az AT1-receptorok túlzott mértékű expressziójához vezet, amint azt sejttenyésztési kísérletek, állatmodellek és emberek is bizonyítják. 10–12. Fontos megjegyezni, hogy a hiperkoleszterinémiás nyulak, az ApoE -/- egerek és a nem emberi főemlősök AT1 receptor antagonistákkal történő kezelése csökkentette a vaszkuláris oxidatív stresszt és gyulladást, javította az endotheliális funkciót és csökkentette az ateroszklerózis progresszióját, annak ellenére, hogy a vérnyomás és a plazma lipidszintje változatlan maradt . 13,16–18 Az endothel működésének javulását AT1 receptor antagonistákkal hiperkoleszterinémiás embereknél is igazolták. 19.
A várakozásoknak megfelelően a vérnyomás szignifikánsan alacsonyabb volt az ApoE -/- -AT1 -/- egerekben, mint az ApoE -/- egerekben, míg a pulzusszám mindkét csoportban hasonló volt. A csökkent vérnyomásszintnek az ateroszklerózis kialakulására gyakorolt jelentős hatásának kizárása érdekében az ApoE -/- egereket értágító hidralazinnal kezelték. Bár a vérnyomást ugyanarra a szintre csökkentették, mint a kettős kiütéses egereknél, az érelmeszesedéses elváltozások kialakulása és az endotheliális funkció megegyezett a hordozóval kezelt ApoE -/- egerekével, ami azt jelzi, hogy a megfigyelt vérnyomáscsökkenés nincs hatással az érelmeszesedésre. folyamat a jelen tanulmányban használt modellben. Ezzel szemben az ApoE -/- állatok irbezartán-kezelése hasonló vérnyomáscsökkenést eredményezett, de jelentősen gátolta az érelmeszesedést és az endotheliális diszfunkciót. Ezek az eredmények igazolják az AT1 receptor blokkolásnak a vérnyomáscsökkentéstől független jelentőségét.
A bemutatott tanulmány megállapításai szerint az AT1 receptor lényegében részt vesz egerekben a hiperkoleszterinémiával társult ateroszklerózisban. A csökkent AT1 receptor aktiváció ezért mélységes érvédelmet fejt ki. További vizsgálatokra van szükség az AT1 receptorok szerepének vizsgálatához az ateroszklerózisban, amelyet más kockázati tényezők, például cukorbetegség vagy ösztrogénhiány okoz. Végül, ha emberben beigazolódnak, a jelen eredmények arra utalnak, hogy az AT1 receptor antagonisták nagyon ígéretes atheroprotective kezelési lehetőséget jelenthetnek.
Ezt a tanulmányt a Deutsche Forschungsgemeinschaft (DFG), a Boehringer Ingelheim korlátlan kutatási támogatásával és az Európai Vascular Genomics Network, az Európai Bizottság által nyújtott kiválósági hálózat (LSHM-CT-2003-503254 szerződésszám) támogatta. . Nagyra értékeljük Sybille Richter kiváló technikai segítségét.
- Az IJMS szabad teljes szövegű eritropoietin-utánzó peptid (pHBSP) korrigálja az endothel diszfunkciót
- Kölcsönös függőségek az endothel diszfunkció kiválasztott gyulladásgátló markerei, a C-peptid között,
- A hasi elhízás különböző fokozatainak jelentősége a tesztoszteron szintjén, merevedési zavarok,
- Az endoteliális nitrogén-oxid-szintáz (NOS3) genetikai variánsainak és metabolikus anyagainak elemzése
- A hasi elhízás különböző fokozatainak jelentősége a tesztoszteron szintjén, merevedési zavarok,