Az endotheliális nitrogén-oxid-szintáz (NOS3) genetikai variánsainak és metabolikus szindrómájának haplotípusanalízise egészséges egyénekben és skizofrénia-betegeknél
Tárgyak
Absztrakt
Háttér/célok
A metabolikus szindróma (MetS) gyakorisága szignifikánsan magasabb a skizofrénia (SCH) betegeknél, összehasonlítva az általános populatiotinnal. A vizsgálat célja annak értékelése volt, hogy az endoteliális nitrogén-oxid (NOS3) génben és/vagy azok haplotípusaiban a T-786C (rs2070744), a G894T (rs1799983) és a C774T (rs1549758) genetikai variánsok összefüggésben lehetnek-e a MetS kockázatával Az orosz lakosságból származó SCH betegek vagy egészséges alanyok.
Tantárgyak/módszerek
Két eset-kontroll összehasonlítást hajtottunk végre. A NOS3 polimorfizmusokat 70, MetS-ben szenvedő SCH-ben, 190 normál testsúlyú SCH-ben, 155 MetS-ben szenvedő betegben és 100 egészséges kontrollban genotipizáltuk. A MetS-t a Nemzetközi Diabetes Szövetség (IDF) által javasolt kritériumok szerint határozták meg. Minden mintában antropometriai, klinikai, biokémiai paramétereket és szérum nitrit koncentrációt mértünk. A Haploview 4.2 gyakoriságával becsültük meg a haplotípus gyakoriságának becslését és a kötés egyensúlyhiányát.
Eredmények
A magasabb C allél (P = 0,009) és az alacsonyabb TT genotípus (P = 0,008) a T-786C polimorfizmus gyakoriságát találták MetS-ben szenvedő SCH-betegeknél, összehasonlítva a normál testsúlyú SCH-betegeknél. A MetS-ben szenvedő SCH betegeknél, akik a T-786C TT genotípus hordozói voltak, a szérum összes koleszterinszintje alacsonyabb volt, mint a CC genotípusé (P = 0,016). Továbbá, a 774T/894T haplotípus gyakoribb volt a nem SCH-ben szenvedő, MetS-t szenvedő egyéneknél az egészséges kontrollokhoz képest (P = 0,0004, esélyhányados = 2,18, 95% -os megbízhatósági intervallum 1,4–3,37). Ezzel szemben a leggyakoribb haplotípus 774C/894G ritkábban fordult elő MetS-ben szenvedő betegeknél, mint egészséges kontrollokban (P = 0,013, esélyhányados = 0,61, 95% -os megbízhatósági intervallum 0,41–0,9).
Következtetések
Ezek az eredmények azt mutatják, hogy a NOS3 T-786C promóter polimorfizmusa szorosan összefügg a MetS kockázatával az SCH betegeknél. Ezenkívül a G894T és C774T polimorfizmusokból álló haplotípusok összefüggenek az orosz populáció MetS érzékenységével.
Bevezetés
Az endotheliális nitrogén-oxid-szintáz (eNOS) enzim által termelt nitrogén-monoxid (NO) szabályozza az alapvető kardiovaszkuláris és metabolikus funkciókat [10]. A NO termelése káros a MetS jellemzőkkel rendelkező betegeknél. Ez a károsodás összefüggésbe hozható az eNOS enzimatikus aktivitásának és expressziójának csökkenésével, az eNOS foszforilációjának változásával és az eNOS szétkapcsolódásával [11]. Egerek, amelyekből hiányzott a NOS3 Az eNOS-t kódoló génnek bizonyos kardiovaszkuláris kockázati tényezői voltak, amelyek úgy tűnik, hogy utánozzák az emberi MetS-t, beleértve a magas vérnyomást, a metabolikus inzulinrezisztenciát és a hiperlipidémiát [12, 13]. Ezen túlmenően a. Részleges és teljes törlése NOS3 gén jelentős hiányt eredményez a koszorúér-értágító képességben, még több bizonyítékot szolgáltatva arra vonatkozóan, hogy ez a gén elszámolható a MetS és a kardiovaszkuláris morbiditás közötti kapcsolatért [14].
A mai napig egyetlen tanulmány sem vizsgálta az NOS3 haplotípusok és a MetS közötti összefüggést az orosz populációban. Továbbá, amennyire tudjuk, még egyetlen tanulmány sem vizsgálta a NOS3 SNP-k hozzájárulását az SCH betegek MetS kockázatához. A közelmúltban azonban végeztek egy olyan tanulmányt, amely értékeli a NOS3 G894T és a T-786C SNP-k és az endoteliális funkció közötti kapcsolatot az SCH alanyok egy csoportjában, akik antipszichotikumokat szednek [26]. A NOS3 T-786C SNP rosszabb endotheliális funkcióval való kapcsolatát csak azoknál a SCH-betegeknél találták meg, akik nem rendelkeztek MetS-sel. Ezért vizsgálatunk célja a NOS3 T-786C, G894T és C774T SNP-k potenciális asszociációinak vagy azok Metl-kockázattal járó haplotípusainak vizsgálata volt az orosz populációban és az SCH-ben. Ezenkívül megvizsgáltuk ezen SNP-k asszociációját a szérum nitritkoncentrációval SCH és nem SCH alanyoknál MetS-szel.
Anyagok és metódusok
Tárgyak
A második eset-kontroll összehasonlításhoz 155 orosz MetS-beteget (60 férfit, 95 nőt) vettünk fel a kalinyingrádi körzet regionális klinikai kórházából, és 100 egészséges kontrollt (48 férfit, 52 nőt) vettünk fel ugyanazon földrajzi régióból. A MetS előfordulását az IDF kritériumainak megfelelően állapították meg. Az általános populáció összes kontrollja normál súlyú volt, fertőző, krónikus és endokrin betegségektől mentes. Az Immanuel Kant Balti Szövetségi Egyetem (Kalinyingrád, Oroszország) Helyi Etikai Bizottsága jóváhagyta ezt a tanulmányt.
Mindkét tanulmány a Helsinki Nyilatkozatot követően készült. Tájékozott beleegyezést szereztek minden alanytól. A minták homogenitásának elősegítése érdekében az összes érintett SCH és nem SCH alany az orosz kaukázusi populációhoz tartozott. Az etnikai hovatartozást mind az egyes alanyok önazonossága, mind a szülő és négy nagyszülő etnikai hovatartozásának megértése alapján határozták meg. Valamennyi kohorsz esetében minden résztvevőt kérdőív segítségével kérdeztek meg cigaretta dohányzási állapotának megállapítására (nem dohányzó vagy jelenlegi dohányos).
Antropometriai és biokémiai értékelések
Az antropometriai mérések magukban foglalták a derék kerületét, a csípő kerületét, a derék és a csípő arányát és a BMI-t. A derék kerületét a legkisebb szélességként határozták meg a part menti peremek és a csípő címerek között, ha minimális légzéssel vették őket. A csípő kerületét a fenék maximális kinyúlásánál értük el, miközben a résztvevő álló helyzetben volt. A derék-csípő arányt úgy találtuk, hogy a derekát elosztottuk a csípőértékeivel. A BMI az alany súlya (kg) osztva az alany magasságával (m 2).
Valamennyi résztvevő számára egy éjszakán át tartó éhomi vénás vérmintát vettünk ugyanazon a napon, mint az áramlásméréseket. Az éhomi vércukorszint és a szérum lipidparaméterek (trigliceridek, összes koleszterin alacsony sűrűségű lipoprotein (LDL) koleszterin és HDL-koleszterin) biokémiai vizsgálatait egy biokémiai autoanalizátorral CA-180 (Furuno Electric Co., Ltd., Hyogo, Japán) végeztük. ) DiaSys reagenskészletek (DiaSys Diagnostic Systems, Holzheim, Németország) felhasználásával. A nitrit szintjét spektrofotometriásan határoztuk meg, a Griess reakció alapján, Moshage és mtsai. [27]. Röviden: 100 μl szérummintát négyszeresére hígítottunk ionmentes vízzel, és 20 μl cink-szulfát (1,85 M) hozzáadásával deproteinizáltuk. Centrifugálás után (10 000 × g, 5 perc), a felülúszókat két-két példányban vittük át a mikrotiterlemezek mélyedéseibe, majd 100 μl Griess-reagenst adtunk hozzá. Az abszorbanciát 540 nm-en 10 perc múlva leolvassuk. Az egyes minták nitritkoncentrációját extrapolálással számszerűsítettük a nátrium-nitrit standard görbéjéből.
Genotipizálás
Valamennyi alany genotipizálva volt a T-786C, G894T és C774T SNP-khez a NOS3 gén allél-specifikus valós idejű PCR-t használ. A T-786C és C774T SNP-k ciklusos körülményei 95 ° C-on voltak 3 percig, 50 ciklus 15 másodpercig 95 ° C-on, 40 másodpercig 65 ° C-on. A G894T SNP PCR-protokollja magában foglalta a reakcióelegy melegítését 3 percig 95 ° C-on és 50 amplifikációs ciklust az alábbiak szerint: 95 ° C 15 másodpercig, 63 ° C 40 másodpercig. Minden mintához két PCR-amplifikációs reakciót állítottunk fel. Valamennyi PCR-t a LightCycler 480 valós idejű PCR rendszeren futtattuk (Roche Diagnostics, Bécs, Ausztria). Mindhárom SNP-t az SNP genotipizáló vizsgálataival (Syntol JSC, Moszkva, Oroszország) genotipizáltuk. Az alapozókat és a szondákat a Syntol JSC tervezte és gyártotta (Moszkva, Oroszország).
Statisztikai analízis
A statisztikai adatok elemzését a Statistica 10.0 verziójával hajtottuk végre (StatSoft, Tulsa, OK, USA). A Levene tesztjét alkalmazták az egyenlő eltérések feltételezésének megerősítésére. A Kolmogorov – Smirnov tesztet alkalmaztuk annak felismerésére, hogy az adatok követik-e a normális eloszlást, és a folyamatos változókban a csoportok közötti különbségek jelentőségét a független t teszt. A nemi változókat Chi-négyzet teszt alkalmazásával értékeltük.
A genotípus frekvenciák Hardy – Weinberg arányoktól való eltéréseit Chi-négyzet teszt alkalmazásával értékeltük. Az SNP-k allél-, genotípus- és haplotípus-gyakoriságát összehasonlítottuk a csoportok között, vagy Chi-négyzet, vagy Fisher pontos tesztjének felhasználásával, amikor ezt helyénvalónak ítéltük. Egyirányú ANOVA-t, majd Fisher LSD post hoc tesztjét végeztük a szérum biokémiai profilok differenciálására a genotípustól függően az SCH és a nem SCH MetS betegek között.
A haplotípus gyakoriságának becslését és az LD méréseket a Haploview 4.2-es verziójával (Broad Institute, Cambridge, MA, USA) végeztük. Az LD módszer szilárd gerincét alkalmaztuk a haplotípus blokk páronkénti becsléséhez D′ Értéke nagyobb, mint 0,7 az SNP-k között. Az esélyhányadok és annak 95% -os megbízhatósági intervallumainak (CI) kiszámítását a VassarStats honlapjának statisztikai számológépével (http://vassarstats.net/) végeztük. A P érték
Eredmények
A klinikai és biokémiai változók összehasonlítását az esetminták és a kontrollminták között az 1. táblázat mutatja be. A MetS-ben szenvedő SCH betegeknél a BMI, a derék kerülete, a derék és a csípő aránya, a vérnyomás magasabb volt a normál testsúlyú SCH alanyokhoz képest. Az egészséges kontrollokhoz képest a MetS-betegek magasabb pontszámot értek el mind a négy antropometriai paraméter, vérnyomás, éhgyomri glükóz, trigliceridek és alacsonyabb HDL-koleszterin szint mellett. A MetS-ben szenvedő SCH-betegek szérum-nitrit-tartalma háromszor nagyobb volt, mint a normál testsúlyú SCH-betegeké, míg a MetS-es betegek szérum-nitrit-tartalma összehasonlítható volt az egészséges kontrollokkal. Nem volt különbség a dohányzás gyakoriságában a MetS-ben szenvedő SCH-betegek között a normál testsúlyú SCH-alanyokhoz képest. Emellett a jelenlegi dohányosok arányában nem mutatkozott szignifikáns eltérés a MetS-betegek és az egészséges kontrollok között. Amikor antidiabetikus, vérnyomáscsökkentő és koleszterinszint-csökkentő gyógyszereket hasonlítottak össze a MetS és MetS betegekben szenvedő SCH betegek között, csak az orális antidiabetikumot szedő betegek arányában találtunk szignifikáns különbséget (2. táblázat).
A 3. táblázat az NOS3 variánsok allél és genotípus gyakoriságát mutatja minden esetben és kontrollon. Az összes mintában a genotípus gyakorisága nem tért el a Hardy – Weinberg arányoktól (mind P > 0,05). Megállapítottuk, hogy a T allél (P = 0,009) és a TT genotípus (P = 0,008) a T-786C SNP szignifikánsan ritkábban fordult elő MetS-ben szenvedő SCH-betegek között, mint normál testsúlyú SCH-alanyokban. A C774T és a G894T SNP-k nem társultak MetS-hez SCH-betegeknél. A G894T T alléljának elterjedtsége azonbanP = 0,002) és a C774T T allélje (P = 0,003) magasabb volt MetS-betegeknél az egészséges kontrollokhoz képest. A GT (P = 0,011) és TT genotípusok (P = 0,0004) G894T, valamint a C774T heterozigóta genotípusa (P = 0,035) gyakoribbak voltak MetS-ben az egészséges kontrollokhoz képest. Továbbá a GG genotípus frekvenciái (P = 0,002) és a CC genotípus (P = 0,002) viszont kevesebb volt MetS-ben az egészséges kontrollokhoz képest.
Annak feltárása, hogy a polimorfizmusok a NOS3 génnek patofiziológiai jelentősége lehet, ha figyelembe vesszük a MetS kockázatát SCH és nem SCH alanyokban, a NOS3 polimorfizmusokat értékeltük a MetS biokémiai tulajdonságokkal való összefüggésekre ezekben a csoportokban (4. táblázat). A T-786C SNP TT genotípusú MetS-ben szenvedő SCH-betegek alacsonyabb összkoleszterinszintet mutattak, mint a CC genotípus hordozói (P = 0,016). Ezekben a csoportokban a genotípus szignifikáns hatását a szérum nitrit szintjéhez viszonyítva nem fedezték fel.
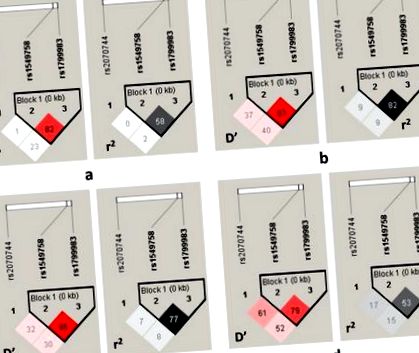
Az LD diagram az LD pontszámokkal (D′ És r A vizsgált SNP-k páros összehasonlításával létrehozott 2. ábra az 1. ábrán látható. A C774T és G894T SNP-k minden mintában erős LD-ben voltak (D′> 0,7, r 2> 0,5). Az 5. táblázat a két NOS3 SNP által alkotott haplotípusok frekvenciáit tükrözi. A haplotípus-elemzés azt mutatta, hogy a mindkét mutáns allélt tartalmazó 774T/894T haplotípus gyakorisága magasabb volt MetS-betegeknél az egészséges kontrollokhoz képest, és ez a haplotípus a MetS fokozott előfordulásával volt összefüggésben (P = 0,0004, esélyhányados = 2,18, 95% CI 1,4–3,37). Viszont a leggyakoribb 774C/894G haplotípus a MetS kockázat csökkenésével járt (P = 0,013, esélyhányados = 0,61, 95% CI 0,41–0,9). A haplotípus frekvenciák megoszlása a MetS-ben szenvedő SCH-betegek és a normál testsúlyú SCH-betegek között nem volt szignifikáns különbség.
LD diagram, amely a három helyzetét mutatja NOS3 génpolimorfizmusok MetS-ben szenvedő SCH-betegeknél (a), normál testsúlyú SCH betegek (b), MetS-betegek (c) és az egészséges kontrollok (d). A négyzetes értékek az LD együttható páronkénti kiszámítását jelentik D′ És a korrelációs együttható r 2 százalékban kifejezve. A színkód D′ Parcellák követik a standard színt D′/Logaritmus (10. alap) az esélyek (LOD) sémája a Haploview esetében: fehér, |D′ | 2 ábra, különböző színek jelzik az LD mértékét: a r 2 LD parcella fehér (r 2 = 0), szürke árnyalatok (0 2 2 = 1)
Vita
A legtöbb tanulmány, amely a NOS3 a MetS szempontú génvariánsok egyedül a NOS3 SNP-ket használták a genetikai architektúra leírására. Például a G894T SNP egyénileg társult a MetS jellemzőivel a brazil, az olasz, a tunéziai, a tajvani és az indiai populációkban [22, 44,45,46,47,48]. Továbbá kiderült, hogy a -786C/894G haplotípus összefügg a MetS-érzékenységgel hipertóniás alanyokban a spanyol populációban [34]. Hasonlóképpen kiderült, hogy az LD-ben lévő G894T SNP más SNP-kkel összefügg a MetS-érzékenységgel az arab és tajvani populációkban [20, 21]. Nem találtunk összefüggést a G894T vagy C774T SNP-kkel a lipid- és szénhidrát-metabolizmus biokémiai paramétereivel az SCH-ben szenvedő vagy anélkül szenvedő MetS-betegeknél. Néhány más tanulmány azonban kimutatta a G894T SNP és a plazma trigliceridek közötti összefüggéseket elhízott kaukázusi betegek és T2DM között [49, 50]. Ezenkívül a NOS3 G894T polimorfizmus valószínűleg megjósolja a tartós hiperglikémiát azoknál az egyéneknél, akiknél az ázsiai populációkban kompromittált glükóz tolerancia és atherogén lipid profil van [30, 46, 51].
Ez a tanulmány az első, amely értékeli és összehasonlítja a MetS-ben és normális BMI-ben szenvedő SCH-betegek szérum-nitritszintjét. Úgy gondolják, hogy a nitritek a NO-medence keringésének fő tárolási területei. A plazma-nitritek változásai érzékenyen tükrözik az eNOS-aktivitás akut változását az emberi alkar keringésében [52]. Munkánk során a MetS-ben szenvedő SCH-ben szenvedő betegeknél a normál testsúlyú SCH-betegeknél megfigyelt nagymértékben megnövelt plazmatikus nitritek szintézise kompenzáló és védő szerepet játszhat az endothelium-károsító molekuláris anyagok semlegesítésében. Ellentétben a keringő nitritszintek összehasonlításával az SCH mintákban, a MetS betegek és az egészséges kontrollok között nem figyeltek meg szignifikáns változást a szérum nitritekben. Eredményeink összhangban vannak két korábbi munkával, amelyek arra a következtetésre jutottak, hogy a MetS és a T2DM úgy tűnik, hogy nem befolyásolják a plazma nitritszintjét [53, 54]. Egy másik tanulmányban a hipertóniás, elhízott gyermekek és serdülők teljes vérének nitritkoncentrációja nem különbözött a kontrolltól [55].
Nem találtunk mindhárom NOS3 SNP-nek a nitritkoncentrációra gyakorolt hatását a MetS-re SCH vagy nem SCH alanyokban. Egészséges egyéneken végzett más vizsgálatokban szintén beszámoltak a T-786C és a G894T SNP-k hozzájárulását a cirkuláló nitrit/nitrát szintjének hiányáról [56, 57]. Érdekes módon, míg Metzger és munkatársai tanulmányában a NOS3 genotípusoknak nem volt szignifikáns összefüggésük a plazma nitritkoncentrációival, a NOS3 haplotípus, beleértve a −786C allélt és a G894 allélt, alacsonyabb plazma nitritekkel volt összefüggésben, összehasonlítva más haplotípusokban csoportok egészséges alanyokban [58]. Ugyanez a haplotípus azonban nem mutatott összefüggést a magas vérnyomású vagy normotenzív, elhízott gyermekek és serdülők nitritkoncentrációival [59]. A nitritkoncentrációkról szóló tanulmányunkban vizsgált mindhárom NOS3 SNP hatásának hiánya azt sugallja, hogy ezek az SNP-k más mechanizmusokkal is elősegíthetik a MetS-t, eddig még nem határoztak meg.
Az adatok elérhetősége
Az adatok az NCBI ClinVar adatbázisában (http://www.ncbi.nlm.nih.gov/clinvar/) állnak rendelkezésre SUB3605688: SCV000680062 és SUB3729182: SCV000692592 csatlakozási szám alatt.
Hivatkozások
Kolovou GD, Anagnostopoulou KK, Salpea KD, Mikhailidis DP. A metabolikus szindróma előfordulása különböző populációkban. Am J Med Sci. 2007; 333: 362–71.
- Az étrendi energiatartalom és a genetikai szelekció által kiváltott máj és izom anyagcsere-változások
- Az emberi elhízás genetikai változatokhoz kapcsolódik a receptor koaktivátorban
- Az elhízás hatása a török ország egész területén a 2-es típusú cukorbetegség metabolikus kontrolljára
- Az étrend-kiegészítők, az étrend hatása az anyagcsere-egészségre a Nutritional Outlook áttekintésében
- Az utcai élelmiszer-higiénia és választási tényező fontosság-elégedettség elemzése Koreában és Tajvanon