A GABA, γ-amino-vajsav, véd a súlyos májkárosodás ellen
Dr. Toshiyuki Hata
Máj- és hasnyálmirigy-hasnyálmirigy- és transzplantációs sebészet, Kiotói Egyetem Orvostudományi Kar, Kiotó, Japán
Dr. Fatima Rehman
Biológiai Tanszék, University of North Florida, Jacksonville, Florida
Dr. Tomohide Hori
Máj- és hasnyálmirigy-hasnyálmirigy- és transzplantációs sebészet, Kiotói Egyetem Orvostudományi Kar, Kiotó, Japán
Dr. Justin H. Nguyen
Transzplantációs Sebészeti Osztály, Mayo Clinic, Jacksonville, Florida
T. Hata megtervezte a vizsgálatot, elvégezte a kísérleteket és megírta a kézirat tervezetét; F.R. vizsgálatokkal segítette, elvégezte a szukcinát-dehidrogenáz-vizsgálatokat és áttekintette a kéziratot; T. Hori reagenseket biztosított és áttekintette a kéziratot; J.H.N. megalkotta a koncepciót, áttekintette a tervet és az adatelemzést, átdolgozta és kiegészítette a kéziratot. Minden szerző áttekintette és jóváhagyta a kézirat végleges változatát.
Absztrakt
Háttér:
A súlyos akut májkárosodásból eredő akut májelégtelenség (ALF) a magas halálozással járó kritikus állapot. Ennek a vizsgálatnak a célja az volt, hogy megvizsgálja a γ-aminovajsav (GABA) megelőző alkalmazásának hatását a májkárosodásra és a túlélési eredményekre egerekben, kísérletileg indukált ALF-fel.
Anyagok és metódusok:
Az ALF kiváltására a C57BL/6NHsd egereknek 7 napig GABA-t, fiziológiás sóoldatot vagy semmit sem adtak, majd 500 μg tumor nekrózis α és 20 mg D-galactosamine intraperitoneálisan adták be. A vizsgálati egereket 4–5 órával humán úton eutanizálták az ALF kiváltása vagy a túlélés megfigyelése után. Az eutanizált egerek vérmintáiban és májszövetében található fehérjéket Western blot, valamint immunhisztokémiai és hisztopatológiai elemzésekkel elemeztük. Gátlási vizsgálatokhoz a STAT3-specifikus inhibitort, az NSC74859-et adtuk be, 90 perccel az ALF indukciója előtt.
Eredmények:
Megállapítottuk, hogy a GABA-val kezelt egerek jelentősen gyengítették a TUNEL-pozitív hepatocitákat és a hepatocelluláris nekrózist, csökkentek a kaszpáz-3, H2AX és p38 MAPK fehérje szintek; és megnövekedett Jak2, STAT3, Bcl-2 és Mn-SOD expresszió, javított mitokondriális integritással. A redukált apoptotikus fehérjék jelentősen meghosszabbított túlélést eredményeztek az ALF indukciója után a GABA-val kezelt egerekben. Az NSC74859 STAT3-specifikus inhibitor kiküszöbölte a túlélési előnyöket a GABA-val kezelt ALF-es egerekben, jelezve a STAT3-út szerepét a GABA-indukálta apoptózis-csökkenésben.
Következtetések:
Eredményeink azt mutatták, hogy a GABA-val végzett megelőző kezelés egerekben a GABA-közvetített STAT3 jelátvitel révén megvédte a súlyos akut májkárosodást. A GABA megelőző beadása hasznos megközelítés lehet a marginális donormáj optimalizálására a transzplantáció előtt.
Grafikai absztrakt
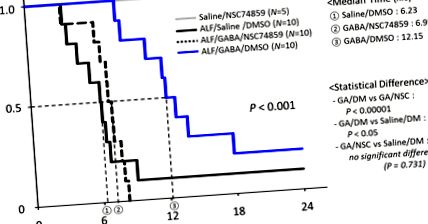
A GABA (ƴ-aminovajsav) a Stat-3 jel segítségével véd a májkárosodás ellen. A tumor nekrózis faktorral (TNF) és a D-galaktozaminnal (Gal) kiváltott súlyos májkárosodásnak ebben a modelljében a GABA-val végzett előkezelés jelentősen meghosszabbítja a TNF/Gal által indukált egereket 12,15 órás mediánnal, összehasonlítva a sóoldattal előkezelt TNF/Gal-indukálta állatok, 6,23 óra. Amikor a specifikus Stat-3 inhibitor NSC74859-et 90 percen keresztül adják be a GABA-val kezelt TNF/Gal-indukált egerekben, a GABA-közvetített túlélési előny megszűnik.
Bevezetés
A közelmúltban kimutatták, hogy a jól ismert gátló neurotranszmitter, a γ-amino-vajsav (GABA) regeneratív hatást fejt ki, és szerepet játszik az öregedő majmok vizuális kérgi funkciójában és a felnőttek neurogenezisében (1–3). A perifériás szövetekben a GABA kimutatták, hogy csökkenti a béta-sejtek gyulladását (4), regenerálja a hasnyálmirigy béta-sejtjeit és megfordítja a kísérleti diabetes mellitust (5–7); A GABA αglucagon termelő sejteket is indukálhat inzulintermelő béta sejtekbe, ami potenciális terápiához vezethet az 1-es típusú diabetes mellitusban (8). A GABA szerepe azonban más perifériás szervekben kevésbé érthető. A GABA hidrofil, ha beadják, a perifériás szervekben marad, és nem lépi át a vér-agy gátat (9); így alkalmas a máj és más perifériás szervek bevonásával végzett regenerációs kísérletekhez. Ezzel szemben a hidrofób muszimol, egy GABA-specifikus agonista, könnyen behatol a vér-agy gátba (10), és ezért nem alkalmas ilyen kísérletekhez. Hasonlóképpen, a bicucullin, egy GABA-specifikus antagonista, könnyen átjárható a vér-agy gáton; rohamot (11) és sejtburjánzást (10) indukál, és szintén nem alkalmas céljainkra.
A GABA-t régóta a májbetegség melléktermékének tekintik, és hozzájárul a máj encephalopathiájához cirrhosisban szenvedő betegeknél (12). A GABA-t azonban egyre inkább felismerték a perifériás szervek hatására is. A GABA kötődik a hepatocita GABA-A béta3 receptorhoz (Gabrb3) (13), hiperpolarizálja a hepatocitákat és a májat (14), aktiválja a sejtciklust, a sejtciklus 2-es (G2) szakaszában megállítja a hepatocitákat és csökkenti a kromoszóma rendellenességeket ( 13), és csökkenti a rosszindulatú daganatok potenciálját (13, 14). A GABA-t azonban nem szabad részleges hepatectomia után beadni, mivel a benne rejlő tulajdonság miatt megállítja a máj regenerálódását (15, 16). Ha nanorészecskékben kitozánnal párosul, a GABA-ról kimutatták, hogy stimulálja a patkányok májának regenerálásához szükséges DNS-szintézist (17, 18), és kicsi epevezeték-képződésben indukálja a kolangiociták proliferációját és differenciálódását (19). A legutóbbi munka megmutatta a GABA jelzésének védő szerepét az akut májkárosodás ellen (20, 21). Korábbi tanulmányokban a GABA előnyös hatását figyeltük meg a teljes totális májeltávolítás egérmodelljében és a részleges májtranszplantáció patkánymodelljében (22, 23). A GABA hatása a nem sebészeti, súlyos májkárosodásra azonban nem ismert.
Ebben a tanulmányban arra törekedtünk, hogy felmérjük a megelőző GABA alkalmazásának hatását súlyos akut májkárosodásra. A halálos akut májelégtelenség egér modelljét alkalmaztuk, amelyet α (TNF-α) és D (+) - galaktozamin (D-gal) tumor nekrózis faktorral indukáltunk, hogy megvizsgáljuk a GABA súlyos májkárosodásra gyakorolt lehetséges hatását. Feltételezték, hogy a GABA megelőző beadása az akut májkárosodás előtt védőhatású.
Anyagok és metódusok
Állatok
A beltenyésztett hím C57BL/6NHsd egereket (életkor, 7–11 hét; súly, 21–28 g) (Harlan Laboratories, Indianapolis, Indiana) specifikus, kórokozóktól mentes körülmények között, 12 órás fény/sötét ciklusokkal, táplálékkal és víz. Az összes kísérleti protokollt a Mayo Klinika Intézményi Állattenyésztési és Felhasználási Bizottsága hagyta jóvá (Protokollszám> A40711), és az intézményi irányelvek szerint történt.
Antitestek és reagensek
GABA adminisztrációs protokoll
Az egereknek napi 7 napon keresztül intraperitoneálisan adták a GABA-t (500 μmol [50 mg]) 0,5 ml sóoldatban vagy 0,5 ml sóoldatban. A normál kontroll egerek nem kaptak sóoldatot vagy GABA-t (1A. Ábra). Az egerek testtömegét az első (−7. Nap) és az utolsó (−5 perc) beadás előtt kaptuk meg.
A tanulmány megtervezése és az alapjellemzők. A, Átfogó tanulmányterv, beleértve az előkezelést GABA-val, sóoldattal vagy semmivel, valamint akut májelégtelenség (ALF) kiváltását TNF-α-val és D-gal-szal. B-E, a vizsgált állatok kiindulási jellemzői indukált ALF nélkül. B, súly (n = 10/vizsgálati csoport), az ALF-indukció előtt és közvetlenül előtte 7 nappal mérve. Az egerek súlygyarapodása szignifikáns és hasonló tendenciákat mutat (P 1A ábra). Az ALF-indukció után 4-5 órával az állatokat pentobarbitális túladagolással humán módon eutanizálták. A vért szívpunkcióval vették; a májat ezután 3 ml sóoldattal perfundálták a kapu vénáján keresztül 1,5 ml/perc sebességgel, majd megszerezték. A bal oldali lebenyt 10% pufferolt formalinban rögzítettük; más lebenyeket folyékony nitrogénben azonnal lefagyasztottak. A túlélési vizsgálatokhoz az egerek körülményeit értékelték, neurológiai eredményekkel, az általunk korábban közölt egérkómás skálán (0. stádium, normális; 1. stádium felkeltette; 2. stádium, ataxiás; 3. stádium, álmos, érintetlen reflexekkel; stádium 4, tönkrement és kómás) (25, 26).
A STAT3 Pathway gátlása
A STAT3 útvonalat szelektív inhibitor, NSC74859 (27) alkalmazásával teszteltük. Röviden, 5 mg/kg NSC74859-et 5% DMSO-ban vagy 5% DMSO-t önmagában (vivőanyag) intraperitoneálisan adtunk 90 perccel a TNF-a és a D-gal előtt.
Máj biokémiai vizsgálatok
A vérmintákat 1000 × g-vel 10 percig centrifugáltuk, hogy szérummintákat kapjunk. Alanin-aminotranszferáz (ALT) reagens készletet (37490, Biotron Diagnostics, Hemet, Kalifornia), teljes bilirubin reagens készletet (0070, Biotron Diagnostics) és QuantiChrom karbamid vizsgálati készletet (DIUR-500, BioAssay Systems, Hayward, Kalifornia) használtunk. elemezze a szérumkoncentrációkat a gyártó utasításai szerint. A mintákat mikrolemezolvasóval értékeltük (SpectraMax M5, Molecular Devices, Sunnyvale, Kalifornia).
Spektrofotometrikus kapcsolt vizsgálat szukcinát-dehidrogenázhoz
A szukcinát-dehidrogenázt (SDH) BioVision glutamát-dehidrogenáz-aktivitás kolometriai vizsgálati készlet (Cat. K729–100) segítségével határoztuk meg, a gyártó utasításai szerint. Szérummintákat nyertünk a fent leírtak szerint; Minden állatból 100 μg szérumfehérjét vizsgáltunk.
Western Blot elemzések
Szövettani elemzések
A 10% -os pufferelt formalinban rögzített májmintákat paraffinba ágyazottuk, és 5 μm vastag metszeteket festettünk hematoxilin-eozinnal, TUNEL-rel (terminális dezoxinukleotidil-transzferáz dUTP nick end jelöléssel) és foszfo-STAT3-mal. A TUNEL festést a gyártó utasításai szerint, ApopTag Peroxidase In situ apoptózis detektáló készlet (S7100, Millipore) és DAB (3,3’-diaminobenzidin) Quanto (TA-060-QHDX, Millipore) felhasználásával végeztük. Minden mintából tíz véletlenszerű nézetet kaptunk nagy teljesítményű mezőben, és a TUNEL-pozitív sejteket külön megszámoltuk mikroszkóppal (BX50; Olympus, Center Valley, Pennsylvania) és képszoftverrel (DP Controller, Olympus). A foszfo-STAT3 elleni antitestekkel végzett immunhisztokémiai festést (Cell Signaling, 9145) Vectastain Universal Elite ABC készlet (PK-6200; Vector Laboratories, Burlingame, Kalifornia), Avidin/Biotin blokkoló készlet (SP-2001, Vector Laboratories), és a DAB Quanto, a gyártó utasításainak megfelelően.
Statisztikai elemzések
A következő statisztikai elemzéseket végeztük a túlélésre a SigmaPlot 11.0 (Systat Software, San Jose, Kalifornia) alkalmazásával: párosítatlan t teszt, Mann-Whitney U teszt, varianciaanalízis és log-rank teszt. Az adatokat az átlag ± standard hiba (SEM) formájában mutatjuk be, a P értéke 1A ábra), és nem mutattak ki a GABA káros hatásait a mozgásra, az étrendre és a társadalmi viselkedésre. Továbbá az átlagos testtömegben nem figyeltek meg szignifikáns különbségeket a GABA beadása előtt vagy után, bár a testtömeg szignifikánsan növekedett az egyes csoportokban a vizsgálati intervallum alatt (1B ábra; P = 0,001). A szérumelemzések nem mutattak szignifikáns különbséget az ALT-szintben (1C. Ábra) és a teljes bilirubin-szintben (1D. Ábra) a 3 vizsgálati csoport között, ami arra utal, hogy a GABA nem gyakorolt káros hatást a máj működésére. Ugyanakkor a GABA-val kezelt csoport szignifikánsan magasabb szérum karbamidszinttel rendelkezett, mint a kizárólag sóoldatot kapó csoport (P 1E ábra). A máj minden csoportban makroszkóposan normálisnak mutatkozott, és nem mutattak nyilvánvaló szín- és méretbeli különbségeket. Ezenkívül nem észleltek nyilvánvaló különbségeket a hematoxilin-eozin festés során (1F. Ábra).
A GABA véd a súlyos májkárosodás ellen
Ezután a GABA előkezelés hatását vizsgáltuk az egér akut májkárosodásra adott válaszára. A D-gal és a TNF-α által kiváltott akut májelégtelenség kísérleti modellje laboratóriumunkban jól megalapozott (25). A kísérleti állatok TNF-α-t (1,0 μg/egér) és D-gal (20 mg/egér) -et kaptak - ez a kombináció, amely az ALF kiváltása után mindig 18 órán belül végzetes. A kontroll és a fiziológiás só csoportba tartozó egerek májja sötétnek és zsúfoltnak tűnt, ami súlyos májkárosodásra utal, míg a GABA csoportból származó állatok szinte normálisnak tűntek (2A. Ábra). A hematoxilin-eozin festés diffúz vérzést és nekrózist mutatott a kontroll és a fiziológiás só egerek májában, míg a máj szerkezete jól megmaradt a GABA-val kezelt egerek májjában. TUNEL-pozitív sejteket láttunk a kontroll és sóoldatok májaiban (2A. Ábra). A TUNEL-pozitív sejtek mezőnkénti száma szignifikánsan csökkent a GABA-val kezelt egerek májában, ami az apoptotikus károsodás jelentős gyengülését jelzi (2A. És 2B. Ábra). A szérum ALT szintje szintén jelentősen csökkent a GABA csoportban (2C. Ábra). Ezenkívül a májkivonatok Western blot-analízise a hasított kaszpáz-3 és a foszfo-hiszton H2AX alacsonyabb expresszióját mutatta a GABA csoportban, ami az apoptotikus sejtpusztulás gyengülését jelzi (2D., 2E. És 2F. Ábra).
- Gamma-aminosavsav (Gaba) felhasználás, mellékhatások, kölcsönhatások, adagolás és figyelmeztetés
- Zöld tea kivonat és a gyógyszer okozta májkárosodás kockázata Szakértői vélemény a kábítószer-anyagcseréről és
- Konjugált linolsav (CLA)
- Konjugált linolsav (CLA) kapszulák - csökkentik a zsírt; Építsd az izmokat - az evolúció karcsúsító
- Jó hír a zsírmájbetegségben szenvedők számára Az ellenállóképzés segíthet - ScienceDaily