A metoklopramid, az ondansetron és a maropitant összehasonlító hatékonysága a parvovirális enteritis által kiváltott hányás megelőzésében kutyákban
Belgyógyászati Klinika, Állatorvos-tudományi Kar, Uludag Egyetem, Bursa, Törökország
Levelezés
Ebru Yalcin, Belgyógyászati Klinika, Állattanító Kórház, Állatorvostudományi Kar, Uludag Egyetem, Bursa, Törökország.
Belgyógyászati Klinika, Állatorvos-tudományi Kar, Uludag Egyetem, Bursa, Törökország
Belgyógyászati Klinika, Állatorvos-tudományi Kar, Uludag Egyetem, Bursa, Törökország
Levelezés
Ebru Yalcin, Belgyógyászati Klinika, Állattanító Kórház, Állatorvostudományi Kar, Uludag Egyetem, Bursa, Törökország.
Belgyógyászati Klinika, Állatorvos-tudományi Kar, Uludag Egyetem, Bursa, Törökország
Absztrakt
A vizsgálat célja a kiválasztott hányáscsökkentő gyógyszerek (metoklopramid, ondansetron és maropitant) hatékonyságának értékelése volt a hányás megelőzésében a kutya parvovirális enteritis kezelésében. Randomizált, prospektív klinikai vizsgálatot terveztünk. 4–12 hónapos PVE gyors ELISA teszt pozitív kutyákat vontak be a vizsgálatba. A metoklopramid, az ondansetron, a maropitant és a kontroll csoport mindegyikében 8 kutya volt. A metoklopramidot és az ondansetront naponta háromszor, 0,5 mg/kg dózisban, intravénás úton, a maropitantot pedig 1 mg/kg dózisban adták be naponta egyszer szubkután. Feljegyeztük a napi hányások számát és súlyosságát. Az összes kutyát öt napig kezeltük és ellenőriztük; a kezeléseket addig folytattuk, amíg az összes állat meg nem gyógyult. A metoklopramid, az ondansetron és a maropitant csökkentette a hányás súlyosságát az első naptól és a hányás számát a harmadik naptól a PVE-kezelés során. A kapott eredmények azt mutatták, hogy a maropitant sikeresen alkalmazható, mint például a metoklopramid és az ondansetron, amelyeket gyakran használnak PVE kezelésére. Ugyanakkor kiderült, hogy a metoklopramid, az ondansetron és a maropitant egyaránt hatékonyan csökkentette a hányás gyakoriságát és súlyosságát.
1. Bemutatkozás
A parvovirális enteritis (PVE) a parvovirus ‐ 2 (CPV ‐ 2) által okozott betegség kutyákban, amely egyláncú, köpeny nélküli DNS vírus (Crawford & Sellon, 2010). A PVE egy vírusos betegség, amely leggyakrabban fiatal, be nem oltott, 6 hónapnál fiatalabb kutyákat érint (Macintire és Smith-Carr, 1997). A klasszikus PVE-kért a kutya parvovirus ‐ 2 (CPV ‐ 2) felelős, és most már legalább három azonosított törzs van (CPV ‐ 2a, CPV ‐ 2b, CPV 2c) (Willard, 2009). Rottweiler, Doberman pincher, amerikai bullterrier, Labrador retriever és németjuhász kutyák érzékenyebbek (Crawford & Sellon, 2010). A PVE-vel rendelkező kutyák tünetmentesek lehetnek, vagy hamarosan súlyos klinikai tünetekkel el is pusztulhatnak. A vírus gyorsan osztódó sejteket (különösen) a GI traktust és a csontvelőt támadja meg. A klinikai tünetek gyakran anorexiával, letargiával, lázzal kezdődnek és 1-2 napon belül haladnak hányássá és hasmenéssé, amelyek sárgák, nyálkahártyák vagy vérzésesek lehetnek (Crawford & Sellon, 2010). A hányás általában kiemelkedő, és elég súlyos lehet ahhoz, hogy utánozza az idegen test elzáródását és/vagy nyelőcsőgyulladást idézzen elő (Willard, 2009). A hányás és hasmenés okozta nagy folyadék- és fehérjeveszteség súlyos kiszáradást és hipovolémiás sokkot okozhat (Crawford & Sellon, 2010).
A neurokinin ‐ 1 (NK1) receptorok a nucleus tractus solitarius-ban, a területi postrema és a dorzális motoros vagális mag jelentős szerepet játszanak a hányásban (Gardner et al., 1996), és megállapítást nyert, hogy a P neuropeptid anyag, amely erős az NK1 receptor agonistája alapvető neurotranszmitter a hányás patofiziológiájában (Gardner et al., 1995, 1996). A maropitant egy erős és szelektív neurokinin-1 receptor antagonista, amely dózisfüggő módon hányáscsökkentőként hat a P anyag kötődésének gátlásával; ezért hatékony a hányás idegi és humorális (központi és perifériás) okai ellen.
Kutyáknál a maropitant orálisan és szubkután egyaránt gyorsan felszívódik, a plazmakoncentráció-csúcsok (Tmax) 1 és 2 óra között vannak (Food & Drug Administration, 2007). A maropitant ajánlott parenterális adagja 1 mg/kg kutyáknál hányáshoz.
Sedlacek és mtsai. (2008) összehasonlította a maropitant, a metoklopramid, a klórpromazin és az ondansetron hatásait apomorfin- és ipecac-szirup által kiváltott hányásban szenvedő betegeknél. Beszámoltak arról, hogy a maropitant, a metoklopramid és a klórpromazin szignifikánsan jobb volt az ondansetronnál az apomorfinnal összefüggő központi hányásnál, míg a maropitant és az ondansetron a metoklopramidnál és a klórpromazinnál jobb volt az ipecac sziruphoz kapcsolódó hányás megelőzésében kutyákban.
Ebben a tanulmányban a metoklopramid, az ondansetron és a maropitant hányáscsökkentő hatásait hasonlítottuk össze PVE által kiváltott hányás esetén.
2. Anyagok és módszerek
2.1 Vizsgálati populáció
Harminckét, kliens tulajdonában lévő, 4–12 hónapos kutya került bemutatásra az Uludagi Egyetem Állatorvos-oktató Kórházának Kisállatklinikájára, a kutya PVE-jére utaló klinikai tünetekkel és a kutya parvovírus – kutya koronavírus SNAP tesztjén pozitív eredményt kapott. giardia antigén1 1 Anigen Rapid, Bionote Inc., Dél-Korea
bekerültek a vizsgálatba. A giardiázist minden kutyánál kizárták a trophozoiták hiánya a befogadáskor vizsgált, fekáliára nedvesen rögzített tárgylemezen és két egymást követő negatív cink-szulfátos flotációs teszt. Egyetlen kutyát sem oltottak be semmilyen betegség ellen.
A kutyák különböző súlyúak voltak (átlagosan 4,7 ± 0,2 kg), fajtájúak (23 vegyes fajta, három német juhászkutya, három anatóliai juhászkutya, három rottweiler), nemük (17 hím és 15 nő) és koruk (négy és tizenkét hónap között volt) átlagosan 5,1 ± 0,1 hónap). A csoportok között nem volt szignifikáns különbség az életkor, a testsúly és a nem tekintetében.
Valamennyi kutya fizikai vizsgálatot kapott, súlyos depresszióban, étvágytalanságban szenvedett; vizes, véres hasmenése volt; és gyakran hányt (≥ négyszer 12 óránként). A klinikai vizsgálatok kiterjedtek a nyálkahártya és a nyirokcsomók vizsgálatára, valamint a szív és a légzés gyakoriságának, a testhőmérséklet és a kapilláris feltöltési idő mérésére. Vérmintákat gyűjtöttünk hematológiai és biokémiai elemzésekhez. Minden klinikai vizsgálatot 24 óránként megismételtünk öt napig. A tanulmány javaslatát az Uludagi Egyetem Etikai Bizottsága felülvizsgálta és jóváhagyta (2010‐06/03).
2.2 Tanulmányi eljárás
Valamennyi kutyát öt napig kórházban hozták kórházba a fertőző betegség elkülönítő egységében, és az újrafertőzés megakadályozása érdekében a ketreceket nyolc óránként megtisztították. A hányás gyakoriságának és súlyosságának meghatározása érdekében a kutyákat videofelvevő rendszeren keresztül figyelték a vizsgálat során. A vak megközelítés biztosítása érdekében az egyik kutató kezelte az állatokat és adta a gyógyszereket (GOK), a másik (EY) csak az állatokat figyelte meg. A hányás gyakoriságát (0-tól> 3-ig) és súlyosságát (enyhe, mérsékelt, súlyos) a De La Puente-Redondo és munkatársai által korábban leírt módon értékelték. (2007). Röviden, a hányás súlyosságát a következőképpen osztályozták: enyhe: nem produktív retching állatok; mérsékelt: epével hányó állatok; és súlyos: epét tartalmazó hányásos állatok. Bármilyen veszteség (n = 4) a kezelés első három napjában előforduló eseményeket kizártuk a vizsgálatból.
A felvétel napján az összes kutyát 6 órán át rehidratáltuk Ringer laktátos oldatával 5% dextrózzal2 2 Eczacibasi ‐ Baxter Ltd, Törökország
és kálium-klorid2 2 Eczacibasi ‐ Baxter Ltd, Törökország
(20 mEq/L) hozzáadva. Az antibiotikum-terápia ampicillin3-ból állt 3 Musztafa Nevzat, Törökország
(22 mg/kg, q8h, iv, öt nap, majd 30 mg/kg, q12h, orálisan, 10 nap), gentamicin4 4 Fako, Törökország
(2 mg/kg, q12h, iv, öt nap, rehidrálás után kezdődött) és metronidazol5 5 I.E. Ulagay, Törökország
(25 mg/kg, 12 óra, iv., Öt nap). A kezelési protokollt Macintire és Smith-Carr (1997) és Prittie (2004) adaptálta. Az első 8 órában nem végeztek hányáscsökkentő gyógyszert.
A kutyákat randomizálták, hogy bármelyik metoklopramidot kapják6 6 Metpamid, Yeni, Törökország
, ondansetron7 7 Zofran, Glaxo SmithKline, Egyesült Királyság
, maropitant8 8 Cerenia, Pfizer, Franciaország
mint elsődleges hányáscsillapító. A kontroll csoport véletlenszerűen kiválasztott állatok nem kaptak hányáscsökkentő gyógyszert. A kezeléseket és a monitorozást öt napig végeztük; a kezeléseket ezután folytattuk, amíg az összes állat meg nem gyógyult. Az 1. táblázat mutatja az alkalmazott hányáscsökkentő gyógyszerek adagját, beadási módját és gyakoriságát.
| 1 | Metoklopramid | 0,5 mg/kg, intravénásan | Egyszer 8 óra alatt |
| 2 | Ondansetron | 0,5 mg/kg, intravénásan | Egyszer 8 óra alatt |
| 3 | Maropitant | 1 mg/kg, szubkután | Egyszer 24 órán belül |
| 4 | Ellenőrzés | Nincs kezelés | - |
2.3 Statisztikai elemzés
Az eredményeket átlag ± szórásként adjuk meg. Az ismétlődő mérésekhez varianciaanalízist (anova) és Kruskal – Wallis tesztet használtak9 9 SigmaStat 3.5, Systat szoftver
. Diákok t-Tesztet használtak két csoport összehasonlítására; nemparametrikus (Friedman ismételt mértékű anovát a rangsorokban) teszteket használtunk a hányás számának és súlyosságának meghatározásához. Megerősítették az adatok normális eloszlását az anova megkezdése előtt . o
3 találat
3.1 A hányás gyakorisága és súlyossága
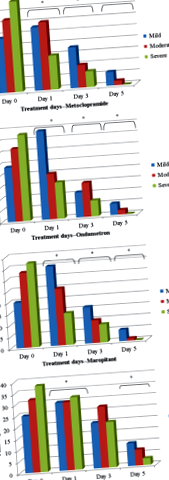
Amikor a hányás gyakoriságát összehasonlítottuk a csoportok és a kezelési napok között, a 0. napon nem tapasztaltunk különbséget. A csoportok csoporton belüli összehasonlítása a kezelési napok szerint nem mutatott különbséget a 0. és a 3. és 5. nap között metoklopramidban, ondansetronban és maropitáns csoportok (o
4. Megbeszélés
Az antiemetikumok a folyadékpótlás és az antibakteriális gyógyszerek mellett nagyon gyakoriak a PVE kezelésében. A hányáscsökkentő gyógyszerek rövid időn belül lehetővé teszik a beteg szájon át történő táplálását és minimalizálják a kiszáradást kiváltó folyadékvesztést. A metoklopramid jól reagál antiemetikus gyógyszerként, és hagyományos módon alkalmazzák, de nyolc óránként kell használni (Mantione & Otto, 2005; Willard, 2009; Prittie, 2004). A metoklopramid antiemetikus és prokinetikus tulajdonságokkal rendelkezik, és ez korlátozza annak alkalmazását invaginációs kockázatú betegeknél. Az ondansetront, amelyet az állatorvosok a rezisztens hányás és posztchemoterápia során előnyben részesítenek, naponta 2-3 alkalommal alkalmazzák. Használata korlátozott, mivel csak intravénásan alkalmazható. A maropitant, amely orális és injektálható (szubkután és nemrégiben engedélyezett intravénás alkalmazásra) piacon újabb, hatékonyan naponta egyszer használják, de PVE-ben való hatékonysága még nem ismert (Mantione & Otto, 2005; Ramsey et al., 2008; Vail és mtsai, 2007; Watson és mtsai, 1995). A maropitant alkalmazása korlátozott lehet, mivel mérsékelt csontvelőt elnyomó hatása van a 8 hetesnél fiatalabb kutyáknál (Food and Drug Administration, 2007), és alacsonyabb költséghatékony ára, mint a többi gyógyszeré. A fő előnye azonban a napi egyszeri használat elegendő hatása.
A hányás súlyossága az 1., a 3. és az 5. napon csökkent, összehasonlítva a 0. nappal minden kezelési csoportban, és az 5. napon, összehasonlítva a 0. és 1. nappal a kontrollcsoportban (o
- A nátrium-hipoklorit és savanyított nátrium-klorit hatékonysága a barnulás és a mikrobák megelőzésében
- Étrendi tanácsok terhesség alatt a terhességi cukorbetegség megelőzésére - Tieu, J - 2007 Cochrane
- Áfonyalé a baktériumok megelőzésére a vizeletben terhesség alatt - teljes szöveg megtekintése
- Az étrend okozta elhízás, a máj citokróm P450 és a lidokain metabolizmusának összehasonlító hatásai
- Cuprizone-modell, mint a szklerózis multiplex-diagnózis hatékonyságának preklinikai vizsgálatának eszköze