A szekretin és receptorának fiziológiai szerepe
Syeda Afroze 1, Fanyin Meng 1,2,3, Kendal Jensen 1, Kelly McDaniel 2, Kinan Rahal 1, Paolo Onori 4, Eugenio Gaudio 5, Gianfranco Alpini 1,2,3, Shannon S. Glaser 1,2,3
Absztrakt: A szekretint az S-sejtek választják ki a vékonybélben, és számos szervrendszer működését befolyásolja. A szekretin receptorok (SR) több sejttípus bazolaterális doménjében expresszálódnak. A szekretin számos hám kiválasztásának szabályozásán túl (például a hasnyálmirigyben és az epe epitéliumában a májban) több sejttípusban is trofikus hatást fejt ki. Ebben a cikkben átfogó áttekintést adunk a szekretin és az SR jelátvitelének számos szerepéről a hámfunkciók szabályozásában a különféle szervrendszerekben, különös tekintettel a májra. Megbeszéljük a szekretin és receptora szerepét az egészség és az epebetegségek patogenezisében. Végül javasoljuk a jövőbeni kutatási területeket a szekretin/szekretin receptor tengely további értékeléséhez a máj patofiziológiájában.
Kulcsszavak: Secretin; Szekretin receptorok
Beküldve 2012. november 08. Elfogadásra váró kiadás 2012. december 13.
Általános háttér
A gasztrointesztinális peptid hormont, a szekretint, eredetileg Bayliss és Starling azonosította 1902-ben (1). A szekretin a szekretin-glukagon család tagja, és a duodenum S sejtjei választják ki Lieberkühn kriptáiban (2). A szekretin számos szervrendszer és sejttípus működését befolyásolja (1-7). A szekretin biológiai hatásait G-fehérjéhez kapcsolt szekretin receptorokon (SR) keresztül fejti ki, amelyek számos sejt bazolaterális doménjében expresszálódnak (3,5,8-11). Amellett, hogy a gyomorsav-szekréció szabályozásával szabályozza a nyombéltartalom pH-ját (12), a szekretin szabályozza a hasnyálmirigy- és az epeutakat bélelő epitheliából a bikarbonátionok kiválasztását a duodenumba (3,6,7,13). A víz homeosztázisának szabályozása mellett (4) a szekretint neuropeptid hormonnak tekintik, mivel a központi idegrendszerben (CNS) is expresszálódik (14-16). A legújabb bizonyítékok azt mutatják, hogy a szekretinnek számos szervrendszerben (beleértve az epehámot is) pleiotróp hatása van (17), és neuroendokrin hormonnak (18) nevezik.
A neuroendokrin hormon szekretin
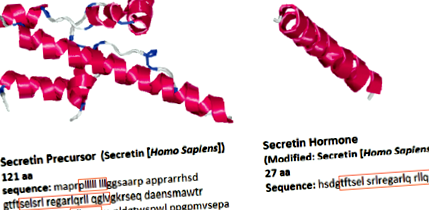
A szekretin szerkezete
A szekretin szintézisének és szekréciójának anatómiai helyei
A szekretin biológiai hatásainak rövid általános háttere
A Secretin számos szervben farmakológiai hatást fejt ki, beleértve a szívet, a vesét, a tüdőt és az agyat (40–43). A szekretinről kimutatták, hogy serkenti az epe- és hidrogén-karbonát-szekréciót a duodenumban (44), a hasnyálmirigy- (45) és az epeutakban (3,7,46), valamint a gyomor pepszin-szekrécióját (47). A szekretin gátolja a gyomorsav-szekretin és az élelmiszer által stimulált gasztrin felszabadulását (48), valamint a felső vékonybél motilitását és az alsó nyelőcső záróizomnyomást (49). A szekretin indukálja az inzulin felszabadulását a hasnyálmirigyből a glükóz bevitele után, és fontos lehet a vércukorszint szabályozásában (50).
A G-fehérjéhez kapcsolt szekretin receptor
A szekretin expressziója különböző szövetekben és sejttípusokban
Az emberi szekretin-receptort eredetileg a tüdõsejtekbõl izolálták (51), és a tercier bronchusban található hám bazolaterális doménjén találták (52). A szekretin receptor kifejeződését számos szerv, köztük az emberek agya (kisagy, hippocampus és központi amygdala), rágcsálók (33,53,54), hasnyálmirigy (14), gyomor (14,55), vese bizonyította (14,41), valamint a máj epehámja (3,8,56-58). A szekretin receptorok immunreaktivitása a vese medullájában, a proximális tubulusokban és a vesében lévő Henle hurok emelkedő vastag szegmensében van (53).
Jelző mechanizmusok
A gyomorsav szekréciójának szabályozása szekretinnel
Számos tanulmány és áttekintő cikk létezik a szekretin szerepéről az oxyntikus sejtek savszekréciójának szabályozásában (12,79-82). Például a szekretin patkányokban egy vagális afferens útvonalon keresztül gátolja a gyomorsav-szekréciót és a motilitást (79). Ezek az eredmények azt mutatják, hogy a pentagasztrinnal stimulált savszekréció szekretin általi gátlását egy kapszaicin-érzékeny vagális afferens út közvetíti (79). Patkányokon végzett egyéb vizsgálatok kimutatták, hogy a szekretin gátló hatását a pentagasztrinnal stimulált gyomorsav-szekrécióban mind a szomatosztatin, mind a prosztaglandinok szabályozzák (80,81). Ez a téma meghaladja a felülvizsgálat célját, és további vizsgálatokra hivatkozunk a további nyomozás céljából (12,79–82).
A hasnyálmirigy-hidrogén-karbonát szekréciójának szabályozása
A szekretin serkenti a bikarbonátban gazdag hasnyálmirigy-folyadék szekrécióját (45). A szekretin bejut a véráramba vagy a bél lumenébe, és serkenti a hidrogén-karbonát szekrécióját (kölcsönhatásba lépve a hasnyálmirigy ductalis sejtjeivel), amely a vékonybélbe kerülve semlegesíti a gyomorkémény pH-ját (83,84). A cAMP-jelátvitel kulcsfontosságú szerepet játszik a hasnyálmirigy-csatornák bikarbonát-ionjainak kiválasztásában. A szekretin által kiváltott hidrogén-karbonát-szekréció a cAMP-függő anioncsatorna, a CFTR aktivációjától függ, amely a különböző hámsejtek apikális membránjában lokalizálódik, beleértve a hasnyálmirigyet és az epevezetékeket is (6). Valójában a CFTR-null egerek hasnyálmirigy-csatornái alacsonyabb mennyiségben választanak ki vizet és hidrogén-karbonátot, mint a vad típusú állatok (85).
A szekretin szerepe a víz homeosztázisában
A szekretin szerepe a központi idegrendszerben
Számos tanulmány azt sugallja, hogy a szekretin az agyban expresszálódik, és szabályozza a központi idegrendszer (CNS) működését (24,35,36). Például a szekretinhiányos egerekben kimutatták a károsodott hippocampalis szinaptikus funkciót (16). A szekaptikus plaszticitás és a társas viselkedés romlását mutatták ki a szekretin receptorhiányos egerekben (14). A vizsgálatok azt mutatják, hogy a szekretin/szekretin receptor tengely fontos lehet a központi idegrendszer működésének szabályozásában (14, 16). Más vizsgálatok kimutatták, hogy a szekretin gént a fejlődés során szerotoninerg mezencephalikus neuronokban fejezik ki (93). Kimutatták, hogy a szekretin trofikus hatással van ezekre az idegsejtekre, ezek a hatások elvesznek a neurodegeneratív rendellenességekben (93). További bizonyítékok arra utalnak, hogy a szekretin neuropeptidként működhet a központi idegrendszerben (94).
A szekretin szerepe a szívben és a szív- és érrendszerben
A szimpatikus és a paraszimpatikus idegrostokról kimutatták, hogy autonóm rendszeren keresztül szabályozzák a szív- és érrendszeri funkciókat (95). Valójában számos neuropeptid választódik ki a szívben (95-97), és fontos szerepet játszhatnak a szívműködés autonóm szabályozásában, mint neurotranszmitterek vagy neuromodulátorok (95). Ebben az áttekintésben megvitatjuk a szekretin szerepét a szívműködés szabályozásában, amely nemcsak hormonként, hanem neurotranszmitterként vagy neuromodulátorként is működik (98). Általánosságban elmondható, hogy a szekretin hatásokat a cAMP szintézis aktiválása közvetíti, amely a szív patológiái alatt csökken. Például a szív-szekretin-stimulált adenilát-cikláz csökkent reakciókészségét figyelték meg a spontán hipertenzív patkány szívmodellben (99,100). Hasonlóképpen, a hipertrófiás patkányszív modellben csökkent a szekretin által stimulált adenilát-cikláz szintje, ami valószínűleg a szívizomsejtekben a szekretin-receptorok számának csökkenése miatt következett be (101). Macskákban és kutyákban kimutatták, hogy a szekretin növeli a szívteljesítményt és a pulzusszámot, míg csökkenti a szisztémás arterioláris ellenállást és a bal kamra végső diasztolés nyomását, a stroke térfogatában nem változik jelentősen (102 103).
A szekretin szerepe kolangiocitákban
A szekretin által kiváltott koleresis
Számos tanulmány kimutatta, hogy a szekretin stimulálja a víz és az elektrolitok kiválasztását a kolangiocitákban, aktiválva a cAMP szintézist, amely a PKA foszforilációját, a CFTR megnyitását és az apikálisan elhelyezkedő Cl -/HCO3 - cserélő AE2 aktiválását indukálja (3,7,56, 57,61,68,70,72,104) (2. ábra). Ezekkel az adatokkal összhangban a cAMP szerepe a szekretin által kiváltott kolerézis modulálásában, egy tanulmány kimutatta, hogy a cAMP agonisták (azaz a forskolin) krónikus beadása fokozza a szekretinnel stimulált epe- és epeváladékot (105). Más vizsgálatok kimutatták, hogy az epesav-medence fenntartása fontos az epeválasztás szempontjából, ezt a hatást közvetíti az AE2 klorid-hidrogén-karbonát-csere funkciója (106). További mechanisztikus vizsgálatok azt is kimutatták, hogy a szekretin által stimulált epeváladékot az aquaporin-1 vízcsatornák (AQP1) mikrotubulus-függő beépítése közvetíti a rágcsálók cholangiocytáinak apikális membránjába.
A legújabb vizsgálatok kimutatták, hogy a szekretinnel stimulált víz és a hidrogén-karbonát szekréció anatómiai helyei a nagy, de nem kicsi kolangiociták (amelyek kis és nagy epeutakat bélelnek) (3,57,107) (3. ábra). Valójában ezek a sejtek az egyetlen hámsejtek a májban, amelyek expresszálják az SR, CFTR és Cl -/HCO3 - cserélő AE2-t, és reagálhatnak a szekretinre fokozott cAMP-szinttel, Cl - efflux és klorid-hidrogén-karbonát-cserélővel (3,56,57). Kimutatták, hogy a nagy (de nem kicsi) epevezetékek expresszálják az SSTR2 receptorokat, és a szomatosztatinra a cAMP-szint gátlásával, az exocitózissal és a duktális epeválasztással reagálnak (56,70).
A kicsi kolangiociták (amelyek nem expresszálják a CFTR-t) (3,58) a Ca 2+ -függő utak aktiválásával vizet és elektrolitokat választanak ki (3. ábra). Például az adenozin-trifoszfát felszabadulását és a purinerg (P2) receptor által közvetített szekréciót bizonyították kicsi egér kolangiocitákban (108). A TMEM16A csatornák és a Ca 2+ -aktivált Cl - efflux azonosítása kis cholangiocytákban az extracelluláris nukleotidokra reagálva alátámasztja egy alternatív, nem cisztás fibrózis transzmembrán vezetőképesség-szabályozó, Cl - csatorna cholangiocytákban koncepcióját, amely fontos kompenzációs szekréciós mechanizmus lehet. nagyobb, cAMP-re reagáló epevezeték károsodása során (109). Ezenkívül a kicsi, mitotikusan szunnyadó kolangiociták de novo szaporodnak és szekretálódnak (a Ca 2+ -függő szignalizáció amplifikálásával), és e sejtek károsodását követően, például CCl4-gyel vagy GABA-val végzett kezelés után, megszerzik a nagy cholangiocyták markereit (63-65).
Tényezők, amelyek modulálják a szekretin által stimulált ductalis epe szekréciót
Az epesavakról is kimutatták, hogy megakadályozzák az epe károsodását (például a koffeinsav és a CCl4 által) és a szekretinnel stimulált duktális szekréció elvesztését (121). Például az epesav, a taurokolsav kolesztatikus patkányokkal történő táplálása megakadályozza a koffeinsav által kiváltott epeúti károsodást a fokozott kolangiocita vaszkuláris endoteliális növekedési faktor (VEGF) expresszió révén (121). A taurocholsav-táplálás megakadályozza a tumor nekrózis faktor-α által kiváltott epeúti károsodást és a szekretin által kiváltott hidrogén-karbonátban gazdag kolerézis elvesztését a PI3K által közvetített úton (122).
A szekretinnel stimulált duktális szekréció mechanizmusait illetően egy tanulmány kimutatta, hogy az adenilil-cikláz izoformát, az AC8-ot többnyire nagy kolangiociták expresszálják (123), amelyek az egyetlen sejttípusok, amelyek expresszálják a szekretin-receptorokat és a szekretin-kolerézis célpontját (57, 124) . Így ez a tanulmány azt sugallja, hogy az AC8 kulcsszereplő lehet a szekretin által kiváltott kolerézis szabályozásában a nagy epevezetékekben (123). Ezenkívül az aril-alkil-amin-N-acetil-transzferáz (az enzimkulcs a melatoninszintézisben) biliáris expressziójának gátlása az AANAT Vivo-Morpholinos alkalmazásával növeli a kolangiociták autokrin proliferatív válaszait és a cAMP/CFTR/Cl -/HCO3 - AE2 szignál expresszióját és csatornaválasztás (125).
Számos nemi hormonról kimutatták, hogy modulálják az epefunkciókat. Kolesztatikus patkányokban végzett kasztrálást követően a tesztoszteron szérumszintje csökkent (a tesztoszteron beadása megakadályozta), és csökkent epe-proliferációval és szekretinnel stimulált cAMP-szinttel, valamint epe- és hidrogén-karbonát-szekrécióval társult (126). Ezenkívül a follikulusstimuláló hormon fokozza az epe szaporodását és a szekretinnel stimulált cAMP-függő epeváladékot (127). A szekretinnel stimulált kolerézist szabályozó tényezők közül néhányat az 1. táblázat is összefoglal.
A szekretin hatása az epeúti hiperpláziára
Számos tanulmány azt sugallta, hogy az SR funkcionális expressziója az epe növekedésének indexe lehet, mivel fokozott biliáris hiperpláziával rendelkező modellekben fokozottabb az SR expressziója és fokozott a válasz a szekretinre (7,8,17,56,62-65,105,127) . Ezzel szemben az epeúti károsodás/apoptózis modelljeiben (például CCl4 vagy GABA kezelés után) megfigyeltük az SR expresszió és a szekretinre adott choleretic válasz csökkenését (7,8,17,56,62-65,105,127). A legújabb eredmények azt mutatták, hogy a szekretin az egér kolangiocitáinak trofikus tényezője, és hogy az SR in vivo és in vitro ablációja csökkenti az epeúti hiperpláziát BDL egerekben (4. ábra) és kolangiocita vonalakban (17). A tanulmány a szekretin lehetséges alkalmazását javasolja ductopeniás májbetegségek terápiájaként (17). További vizsgálatokra van szükség annak megállapításához, hogy a szekretin a kolangiociták által kiválasztott autokrin hormon.
A szekretin szerepe az emberi epebetegségekben
Egyre több információ van a szekretin és receptora szerepéről az epe rendellenességek diagnosztizálásában és kezelésében. Például Prieto és mtsai. emberekben a pozitronemissziós tomográfiát alkalmazták a bazális és szekretin által stimulált biliáris hidrogén-karbonát-szekréció értékelésére, mint az epehám funkcionalitásának indexe normál és kolesztatikus (pl. PBC) körülmények között (128). A szekretin epeúti megbetegedésekben betöltött jelentőségével összhangban kolesztatikus és kezeletlen PBC-betegeknél a szekretinre adott choleretic válasz hiányát figyelték meg (128). A közelmúltban szekretin által közvetített géntovábbítást fejlesztettek ki, amely kifejezetten az epe- és hasnyálmirigy-megbetegedések kezelésében potenciálisan fontos intracelluláris utakat célozza meg cisztás fibrózisban (9). A szekretinnel stimulált mágneses rezonancia-kolangiopancreatográfiát diagnosztikai eszközként alkalmazták az epe- és hasnyálmirigy-betegségek betegségében (129). A szekretinnel fokozott cholangiopancreatography (MRCP) diagnosztikai szerepét javasolták sikertelen endoszkópos retrográd cholangiopancreatography (ERCP) betegeknél (130).
A legújabb tanulmányok alátámasztják azt az elképzelést, hogy az epebikarbonát fontos védőmechanizmus lehet a kolangiopathiákban, mivel az epeúti rendellenességekben, például a PBC-ben, és az elsődleges szklerotizáló cholangitisben (131-134) hibás HCO3-ernyőt figyeltek meg. Ezen megállapítások alátámasztására egy nemrégiben végzett kutatás kimutatta, hogy a miR-506 a PBC-ből származó kolangiocytákban fokozottan szabályozott, megköti az AE2 mRNS 3'UTR régióját, megakadályozza a fehérje transzlációját, ezáltal csökkent AE2 aktivitást és károsodott ductalis szekréciót okozva (135). A tanulmány azt sugallja, hogy a miR-506 potenciális terápiás célpont lehet a PBC kezelésében (135).
Következtetések/jövőbeli perspektívák
Megbeszéltük, hogy a szekretin és receptorai számos szervszövet szekréciós aktivitását szabályozzák, beleértve a gyomrot, a belet, a hasnyálmirigyet, a szívet és a májban lévő epehámot. Az epebél epitéliuma kapcsán kimutattuk, hogy a szekretin és receptora (amelyet csak a májban található kolangiociták expresszálnak) kulcsszerepet játszik a nagy kolangiociták szekréciós és proliferatív aktivitásában, az egyetlen sejttípus, amely expresszálja az SR-t és reagál a szekretinre. A kis kolangiociták (amelyek konstitutív módon nem expresszálják az SR-t) nagy kolangiocita fenotípusokat kapnak a nagy kolangiociták károsodásával járó kóros állapotokban, és felerősítik a Ca 2+ -függő jelátvitelt, hogy kompenzálják a nagy epeúti funkciók elvesztését és fenntartsák a máj homeosztázisát. Megmutattuk azt is, hogy a szekretin fontos trofikus autokrin tényező lehet, amely fenntarthatja az epe proliferációt a ductopeniás állapotokban. Javasolta továbbá a szekretin diagnosztikai szerepét az epebetegségekben, például a PBC-ben és az epe-atresiában. További vizsgálatok szükségesek a szekretin prognosztikai szerepének meghatározásához a ductopeniás epeúti betegségek diagnosztizálásában.
Köszönetnyilvánítás
Ennek a munkának egy részét Dr. Nicholas C. Hightower százéves gasztroenterológiai elnöke támogatta a Scott & White Kórházból, VA Merit díjat és az NIH DK58411, DK062975 támogatást Dr. Alpini és Glaser, DK081442 és Veterans Administration CDA-2 díj Dr. Glaser számára.
Közzététel: A szerzők nem jelentenek összeférhetetlenséget.
- Milyen színészeket várnak a tömeges felzárkózás miatt a filmszerepekért először ünnepeljük
- Súlygyarapodás-receptor az antipszichotikus gyógyszerekhez kapcsolódva - Neuroscience News
- TTC Utazás (korai, tesztek, arány, gyógyszer) - Terhesség; 2. oldal - City-Data fórum
- A legjobb idő az északnyugati orvostudomány fogyasztására
- Fogyás terhesség előtt A prekoncepció fontossága Súly Michigan Medicine