Az androgének szerepe a metabolizmusban, az elhízásban és a cukorbetegségben férfiaknál és nőknél
Guadalupe Navarro
2 Endokrinológiai és anyagcsere osztály, Orvostudományi Tanszék, Stanford Egyetem, Stanford, CA 94305-5165, USA
Camille Allard
1 Endokrinológia és anyagcsere szekció, Tulane University Health Sciences Center, Orvostudományi Kar, New Orleans, LA 70112, USA
Weiwei Xu
1 Endokrinológia és anyagcsere szekció, Tulane University Health Sciences Center, Orvostudományi Kar, New Orleans, LA 70112, USA
Franck Mauvais-Jarvis
1 Endokrinológia és anyagcsere szekció, Tulane University Health Sciences Center, Orvostudományi Kar, New Orleans, LA 70112, USA
Absztrakt
Célkitűzések
A férfiaknál az androgénmegvonás hozzájárul a metabolikus szindróma és a 2-es típusú cukorbetegség (T2D) kialakulásához. Nőknél az androgénfelesleg hajlamosít az inzulinrezisztenciára és a T2D-re. Van egy kétirányú glükóz homeosztázis moduláció androgén által férfiaknál és nőknél, amelyeket ebben az áttekintésben elemzünk.
Mód
Áttekintjük a rágcsálók és az emberek irodalmát az androgének és az androgén receptor (AR) szerepéről a glükóz és az energia anyagcseréjének szabályozásában az egészség, az elhízás és a T2D szempontjából.
Eredmények
Az AR nemi specifikus aktiválása a hipotalamuszban, a vázizomban, a májban, a zsírszövetben és a hasnyálmirigy-szigetecske β-sejtjeiben az energia-anyagcsere és a glükóz homeosztázis fenntartását vagy megzavarását okozza.
Következtetés
Azt állítjuk, hogy az AR célpont az androgénnel kapcsolatos anyagcserezavarok megelőzésében.
Bevezetés
Ebben a jelentésben áttekintjük mind a rágcsálók, mind az emberek szakirodalmát a tesztoszteron és az androgén receptor (AR) szerepéről a glükóz/energia homeosztázis szabályozásában, valamint a metabolikus diszfunkció kialakulásában férfiaknál és nőknél, különös hangsúlyt fektetve a szövetszelektív tevékenységekre vázizomban, zsírban, szövetben, máj hasnyálmirigy β-sejtekben és a központi idegrendszerben.
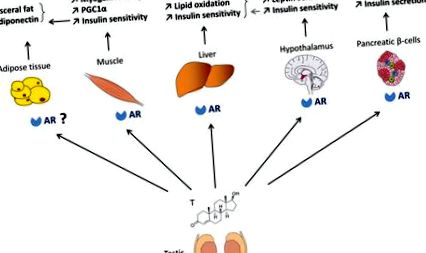
Az AR szerepe a férfi glükóz homeosztázisában (1. ábra)
A hímeknél az androgének elősegítik a glükóz és az energia homeosztázisát a vázizomzatban, a májban, a hasnyálmirigy béta-sejtjeiben és a hipotalamuszban található anyagcsere központokban kifejtett AR-ra gyakorolt hatásuk révén. A zsírszöveten található androgén hatások közvetett módon közvetíthetők az izomban fellépő AR-akciók révén.
A tesztoszteronhiány hajlamosítja a férfiak T2D-jét
Kétirányú kölcsönhatás van az androgén és a cukorbetegség között olyan férfiaknál, amelyekben az alacsony tesztoszteron hajlamosít a cukorbetegségre, a hiperglikémia pedig hipogonadizmushoz vezet (7). Jelentős bizonyíték van arra, hogy az alacsony tesztoszteron a cukorbetegséghez társul és azt jósolja férfiaknál. 28 keresztmetszeti és prospektív vizsgálat metaanalízisében Ding és mtsai azt találták, hogy a teljes tesztoszteronszint mindig alacsonyabb volt a cukorbeteg férfiaknál, mint a nem diabéteszes kontrolloknál, és hogy a magasabb tesztoszteronszint az alacsonyabb incidens diabétesz kockázatával járt ( 8.) A prospektív és keresztmetszeti vizsgálatok egy újabb metaanalízise azt is kimutatta, hogy a T2D függetlenül társult a férfiak alacsony teljes tesztoszteronszintjéhez (7). Ezenkívül a tesztoszteron-helyettesítő terápia metabolikus hatásának ugyanazon metaanalízise azt találta, hogy a tesztoszteron-terápia a férfiak éhomi plazma glükóz-, HBA1c-, zsírtömeg- és trigliceridszintjének jelentős csökkenésével járt (7). Bár az alacsony tesztoszteron és az elhízás közötti összefüggés egyértelmű, a cukorbeteg férfiaknál még mindig alacsonyabb a tesztoszteron szint, még a BMI beállítása után is (7, 9).
A prosztatarák androgén-deprivációs terápiája során a nagyon alacsony tesztoszteronszint számos nagy tanulmányban összefüggésbe hozható a cukorbetegség fokozott kockázatával (10, 11). A közelmúltban a Veterans Healthcare Administration megfigyelési tanulmánya kimutatta, hogy a prosztatarákos betegek körében a GnRH agonistákkal végzett androgén-deprivációs terápia a T2D fokozott kockázatával jár (12). Egy másik tanulmány markáns hiperglikémiát és csökkent hasnyálmirigy-β-sejtek működését mutatta ki a prosztatarákos betegek körében androgén-deprivációs terápia után (13). Nevezetesen a tesztoszteronhiány az éhomi éhgyomri glükóz és a glükóz intolerancia csökkenésével is összefüggésben van, függetlenül a férfiak elhízásától és metabolikus szindrómájától (14). Összességében ezek a tanulmányok azt sugallják, hogy az alacsony tesztoszteron hajlamosít a cukorbetegségre férfiaknál.
Az androgének megakadályozzák a zsigeri zsír felhalmozódását és javítják az inzulinérzékenységet
A vázizomzat tesztoszteron hatása elősegíti a férfiak inzulinérzékenységét
A májban található androgén hatások elősegítik a lipid homeosztázist és az inzulinérzékenységet
A központi androgén hatások szabályozzák a férfiak energiaháztartását
Az AR bőségesebben expresszálódik a hím rágcsálók agyában, mint a nőké (41). A hím egész test AR-hiányos egereinél az elhízás az energiafogyasztás növekedése nélkül, de csökkent mozgásszervi aktivitással jár. Ezek az egerek csökkent barna zsírszövet termogenezist mutatnak, ami csökkenti az energiafelhasználást (24). Az AR a hím hipotalamuszban is működik, hogy elősegítse a központi leptin működését. AR hiányos hím egereknél a leptin valóban nem segíti elő a STAT3 mag lokalizációját az arcuate nucleus (ARC) idegsejtekben, és nem nyomja el a táplálékfelvételt vagy csökkenti a testtömeget még a nyilvánvaló elhízás megjelenése előtt sem (41). Továbbá a neuronspecifikus ARKO (NARKO) egereknél elhízás, inzulinrezisztencia és glükóz intolerancia alakul ki. Ezek az egerek hipotalamusz inzulinrezisztenciát mutatnak a hipotalamusz NFκB aktiválásával, amely fokozza a gyulladást (42). Ezek a megfigyelések együttesen azt mutatják, hogy hím rágcsálókban az AR központi és perifériás hatásokon keresztül részt vesz a zsírszövet tömegének szabályozásában.
Androgén hatás hím β-sejtekben
Korai tanulmányok arról számoltak be, hogy amikor a streptozotocin a β-sejtek pusztulását indukálja inzulinhiányos cukorbetegség hím egérmodelljeiben (43, 44), a tesztoszteron AR-függő módon gyorsítja a hiperglikémiás dekompenzációt. Ugyanakkor arról is beszámoltak, hogy a tesztoszteron az AR révén megvédi a streptozotocin által a hím patkány hasnyálmirigyében kiváltott korai apoptotikus károsodást (45, 46). Egy korábbi jelentés azt is javasolta, hogy a tesztoszteron serkenti a szigetecske inzulin mRNS-ét és a kultúrában és in vivo tartalmát (47). Ezért az AR szerepe a hím β-sejtekben nem egyértelmű. Hoztunk létre egy β-sejt-specifikus AR knockout egeret, hogy megvizsgáljuk az AR közvetlen szerepét a férfi β-sejt fiziológiában (βARKO -/y) (48). A hím βARKO -/y egerek csökkent glükózstimulált inzulinszekréciót (GSIS) mutatnak, ami glükóz intoleranciához vezet, és β-sejtek elégtelensége alakul ki az étrend okozta inzulinrezisztencia kompenzálására. A csökkent GSIS szaporodik tenyésztett hím βARKO -/y szigeteken, valamint tenyésztett humán szigeteken, amelyeket flutamiddal kezeltek, egy AR antagonistát. Ez arra utal, hogy az AR a férfi β-sejtek fiziológiás szabályozója, amely megállapítás fontos következményekkel jár a hipoandrogén férfiak T2D megelőzésében.
Az AR szerepe a nő glükóz homeosztázisában (2. ábra)
A hiperandrogenémiában szenvedő nőknél a vázizomzatban, a makrofágokban, a hasnyálmirigy béta-sejtjeiben és a hipotalamuszban található metabolikus központokban a túlzott AR-aktiváció szinergizálódik az anyagcsere-diszfunkció, a gyulladás, a visceralis adipozitás és a T2D elősegítésére.
A hiperandrogenizmus hajlamosítja a nők T2D-jét
Az AR-hiány szerepét a női anyagcserében nem vizsgálták jól, bár a jelentések szerint nincs hatása a nőstény egerek testsúlyára (49). Ezzel szemben a nők androgénfeleslege és a cukorbetegség közötti összefüggés Achard és Thiers 1921-es korai leírása óta ismert a „szakállas nők cukorbetegségéről” (4).
A svéd nők prospektív, 12 éves tanulmányában Bjorntorp és munkatársai eredetileg arról számoltak be, hogy a nemi-hormon kötő globulin (SHBG) alacsony koncentrációja - amely növeli a szabad tesztoszteront - erős független kockázati tényező volt a T2D kialakulásában (50). Hasonlóképpen, Larsson és Ahren kimutatták, hogy a postmenopauzás nőknél, akiknek csökkent a glükóz toleranciája, az androgén aktivitásuk magasabb, mint a normál glükóz toleranciájú nőknél, és hogy az androgén aktivitás korrelál a glükóz intolerancia mértékével (51, 52). A szabad tesztoszteron magasabb szintjét és az alacsonyabb SHBG-szintet többször összefüggésbe hozták a nők glükóz-intoleranciájával és inzulinrezisztenciájával (53, 54, 55, 56, 57). A tesztoszteron, az SHBG és az ösztradiol szintjét érintő, a T2D kockázatával kapcsolatos prospektív és keresztmetszeti vizsgálatok metaanalízisében Ding et al. számoltak be arról, hogy a magas szabad tesztoszteronszint a nőknél a T2D magasabb kockázatával jár (8). Az ösztradiol szintje azonban emelkedett volt a cukorbetegségben szenvedő posztmenopauzás nőknél is, ami arra utal, hogy az ösztrogénfelesleg is szerepet játszhatott a T2D kockázatában. A posztmenopauzás nőknél az ösztradiol és a tesztoszteron magasabb plazmaszintje erősen és perspektíva összefüggésben állt a T2D kialakulásának fokozott kockázatával (58).
A hiperandrogenizmus elősegíti a nők inzulinrezisztenciáját
Az androgénfelesleg inzulinérzékenységben betöltött szerepének megértése érdekében több csoport vizsgálta az androgénnel kitett nők metabolikus válaszát hiperglikémiás és euglikémiás-hiperinzulinémiás bilincsek során. Globálisan ezek a tanulmányok arról számoltak be, hogy a magas tesztoszteronszint inzulinrezisztenciát eredményez azáltal, hogy csökkenti az inzulin által stimulált teljes test glükózfelvételét egészséges menopauza előtti és utáni nőknél (54, 59, 60, 61). Továbbá a csökkent inzulin-stimulált, az egész test glükózfelvétele nem a máj inzulinrezisztenciájának tulajdonítható, amely változatlan maradt, támogatva a vázizmok inzulinrezisztenciában betöltött szerepét (59). A nőstény rágcsálókon végzett vizsgálatokban a tesztoszteron feleslegének szerepe a vázizom inzulinrezisztenciájának elősegítésében rost típusú kapcsolóval is megerősítést nyert (62, 63). Ennek ellenére az androgénfelesleg mechanizmusai, amelyek elősegítik az izom inzulinrezisztenciáját, továbbra sem ismertek.
Annak ellenére, hogy felhalmozott bizonyíték van arra, hogy a tesztoszteronfelesleg megváltoztatja a nők inzulinérzékenységét, nem világos, hogy a tesztoszteronfelesleg elindítja-e vagy fenntartja-e az inzulinrezisztenciát. Általában az inzulinérzékenység javul, ha a hiperandrogenizmus megfordul anti-androgén terápiával, súlycsökkenéssel együtt (40, 64, 65). Ez utóbbi vizsgálatok arra utalnak, hogy az androgénfelesleg önmagában meghatározó lehet az inzulinrezisztenciában. Az AR antagonistákkal végzett kezelés vagy a petefészek-androgéntermelés GnRH analógokkal történő elnyomása a hiperandrogén nőknél azonban nem mindig javítja az inzulinrezisztenciát (66), ami arra utal, hogy a nőkben lévő androgének feleslege nem okozhatja ezeket az anyagcsere-rendellenességeket, hanem súlyosbító tényező.
A hiperandrogenizmus növeli a zsigeri zsírosságot a nőknél
A hiperandrogenizmus hajlamosít a β-sejtek diszfunkciójára a nőknél
Annak érdekében, hogy megvizsgáljuk a β-sejt AR szerepét a β-sejtek diszfunkciójában androgénfelesleggel rendelkező nőknél, olyan egereket állítottunk elő, amelyek feltételes AR-kiütéssel a β-sejtekben. Nőstény egerekben a krónikus androgénfelesleg β-sejtek hiperfunkcióit és a szigetek kudarcát képezi, hogy kompenzálja a magas zsírtartalmú táplálkozás által kiváltott inzulinrezisztenciát, amely T2D-hez (80) vezet, hasonlóan a PCOS-ban szenvedő nőknél megfigyelthez. Az androgénfelesleg által indukált T2D-t azonban nem figyelték meg a nőstény βARKO -/- egerekben. Így androgénfeleslegben szenvedő nőknél a T2D-re való hajlam legkevésbé közvetített a β-sejtek túlzott AR-aktivációján keresztül.
Következtetések
Nyilvánvaló, hogy hímeknél és nőknél kétirányú moduláció van a glükóz homeosztázis androgének általi módosítására. Az AR hiány drámai metabolikus diszfunkcióhoz vezet az idősödő férfiaknál, a nőknél azonban nem. Valószínűleg a tesztoszteron és a DHT alacsonyabb koncentrációját tükrözve a keringésben és a sejtekben, az AR-aktiváció gyengébb a nőknél, és ezért az AR kevésbé fontos a női emlősök energiaháztartásának fenntartásához. Mégis, amikor az androgénkoncentráció nőstényekben patológiás szintre emelkedik, az ebből eredő túlzott AR-aktiváció metabolikus diszfunkcióhoz vezet. Az ebben a felülvizsgálatban bemutatott bizonyítékok arra utalnak, hogy a hímek androgénhiánya, a nőknél pedig az androgénfelesleg hiányos vagy túlzott AR hatással járó anyagcsere-diszfunkciókat eredményez több szövetben, beleértve a központi idegrendszert, a májat, a vázizomzatot, a zsírszövetet és a β-sejteket. Férfiaknál a kezelés szelektív androgén receptor modulátorokra (SARM) támaszkodhatott. Hiperandrogén nők esetében további vizsgálatokra van szükség annak meghatározásához, hogy az androgén milyen hatással van a központi idegrendszerben, a májban, a vázizomban, a zsír- és a β-sejtekben a T2D kialakulásában.
Amit már tudunk erről a témáról?
Az androgénhiány hajlamosít a metabolikus szindrómára és a 2-es típusú cukorbetegségre a férfiaknál.
Az androgénfelesleg hajlamosít a metabolikus szindrómára és a 2-es típusú cukorbetegségre a nőknél.
- A kapcsolat a cukorbetegség és az elhízás között Az elsődleges alapellátás alapellátási gyakorlata
- Az elhízás és a diabetes mellitus hatása a hasnyálmirigyrákra Molekuláris mechanizmusok és klinikai
- Az elhízás és a cukorbetegség kapcsolata Nova Orvos Wellness Központ fogyás szakemberei
- Az elhízás és a cukorbetegség kapcsolata - komoly tudomány
- Az elhízás és a cukorbetegség kapcsolata Medinet Családgondozó Klinika Sürgősségi ellátás