Bioinformatika
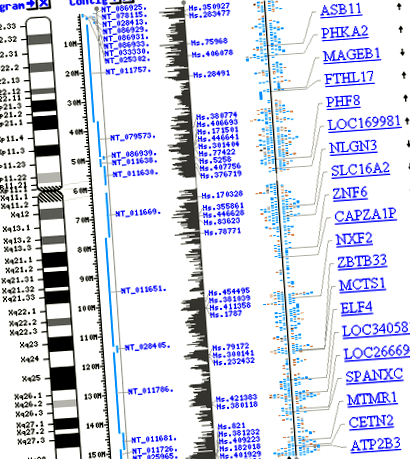
Az emberi X kromoszóma térképe (az NCBI honlapjáról). Az emberi genom összeállítása a bioinformatika egyik legnagyobb eredménye.
Bioinformatika és számítási biológia magában foglalja az alkalmazott matematika, az informatika, a statisztika és az informatika technikáinak felhasználását a biológiai problémák megoldására. A számítási biológia kutatása gyakran átfedésben van a rendszerbiológiával. A terület fő kutatási erőfeszítései közé tartozik a szekvencia összehangolása, a génkeresés, a genom összeállítása, a fehérje szerkezet összehangolása, a fehérje szerkezetének előrejelzése, a génexpresszió és a fehérje-fehérje kölcsönhatások előrejelzése, valamint az evolúció modellezése.
A feltételek bioinformatika és számítási biológia gyakran felváltva használják. azonban bioinformatika pontosabban utal algoritmusok, számítási és statisztikai technikák, valamint elméletek létrehozására és továbbfejlesztésére a biológiai adatok kezeléséből és elemzéséből fakadó vagy ihletett formai és gyakorlati problémák megoldására. Számítási biológia, másrészt egy adott biológiai probléma hipotézisvezérelt vizsgálatára utal számítógépek segítségével, kísérleti és szimulált adatokkal, a felfedezés és a biológiai ismeretek előmozdításának elsődleges céljával. Hasonló megkülönböztetést tesznek az Országos Egészségügyi Intézetek a bioinformatika és a számítástechnikai biológiai definíciókban, ahol azt is hangsúlyozzák, hogy szoros összefüggés van a fejlemények és az ismeretek között a hipotézisvezéreltebb számítástechnikai és technikavezérelt kutatások között. a bioinformatikában. A számítástechnikai biológia tartalmaz olyan kevésbé ismert, de ugyanolyan fontos alágazatokat is, mint a számítási biokémia és a számítási biofizika.
A bioinformatikai és a számítási biológiai projektek közös vonása az, hogy matematikai eszközöket használnak hasznos információk kinyerésére olyan nagy zajterhelésű adatokból, amelyeket nagy áteresztőképességű biológiai technikákkal, például genomikával hoztak létre (Az adatbányászat területe e tekintetben átfedésben van a számítási biológiával). A bioinformatika reprezentatív problémája a kiváló minőségű DNS-szekvenciák összeállítása a töredékes "shotgun" DNS-szekvenálásból, míg a számítási biológiában egy reprezentatív probléma lehet a közös génszabályozás hipotézisének statisztikai tesztelése az mRNS mikro-sugarak vagy tömegspektrometriás adatok felhasználásával.
Tartalom
- 1 Fő kutatási területek
- 1.1. Szekvenciaelemzés
- 1.1.1 Genom annotáció
- 1.2 Számítási evolúciós biológia
- 1.3 A biológiai sokféleség mérése
- 1.4 A génexpresszió elemzése
- 1.5 A szabályozás elemzése
- 1.6 A fehérje expressziójának elemzése
- 1.7 A rák mutációinak elemzése
- 1.8 A fehérje szerkezetének előrejelzése
- 1.9 Összehasonlító genomika
- 1.10 Biológiai rendszerek modellezése
- 1.11 Nagy teljesítményű képelemzés
- 1.1. Szekvenciaelemzés
- 2 Szoftvereszközök
- 3 Lásd még
- 3.1 Kapcsolódó mezők
- 4 Külső linkek
- 5 Megjegyzések és hivatkozások
- 6 Irodalomjegyzék
Főbb kutatási területek [szerkesztés | forrás szerkesztése]
Szekvenciaelemzés [szerkesztés | forrás szerkesztése]
A bioinformatika másik aspektusa a szekvenciaelemzésben a gének és szabályozó szekvenciák automatikus keresése egy genomban. A genomban található összes nukleotid nem minden gén. A magasabb rendű organizmusok genomjában a DNS nagy részei nem szolgálnak nyilvánvaló célt. Ez az úgynevezett szemét DNS azonban felismerhetetlen funkcionális elemeket tartalmazhat. A bioinformatika segít áthidalni a szakadékot a genom és a proteom projektjei között - például a DNS-szekvenciák alkalmazásában a fehérje azonosításában.
Genom annotáció [szerkesztés | forrás szerkesztése]
A genomika összefüggésében, annotáció a gének és más biológiai jellemzők DNS-szekvenciában történő megjelölésének folyamata. Az első genom annotációs szoftver rendszert 1995-ben Owen White tervezte, aki annak a csapatnak a tagja volt, amely szekvenálta és elemezte a szabadon élő organizmus, a Haemophilus influenzae baktérium első genomját. Dr. White szoftver rendszert épített fel a gének (a fehérjét kódoló DNS-szekvencia helyeinek), az átviteli RNS és egyéb jellemzők felkutatására, valamint a funkciók kezdeti hozzárendelésére ezekhez a génekhez. A legtöbb jelenlegi genom annotációs rendszer hasonlóan működik, de a genomi DNS elemzésére rendelkezésre álló programok folyamatosan változnak és javulnak.
Számítási evolúciós biológia [szerkesztés | forrás szerkesztése]
Az evolúciós biológia a fajok eredetének és leszármazásának, valamint azok időbeli változásának vizsgálata. Az informatika számos kulcsfontosságú módon segítette az evolúciós biológusokat; lehetővé tette a kutatók számára, hogy:
- nagyszámú organizmus fejlődésének nyomon követése a DNS-ben bekövetkező változások mérésével, nem pedig kizárólag fizikai taxonómiával vagy fiziológiai megfigyelésekkel,
- újabban hasonlítsa össze a teljes genomokat, amely lehetővé teszi az összetettebb evolúciós események, például a gének duplikációja, az oldalsó géntranszfer és a baktériumspecifikációs tényezők előrejelzését,
- a populációk komplex számítási modelljeinek felépítése a rendszer időbeli előrejelzéséhez
- nyomon követheti és megoszthatja az információkat egyre több fajról és élőlényről
A jövőbeni munka arra törekszik, hogy rekonstruálja az élet most bonyolultabb fáját.
A számítástechnikában a genetikai algoritmusokat használó kutatási területet néha összekeverik a számítási evolúciós biológiával. Az ezen a területen végzett munka magában foglalja a speciális számítógépes szoftverek használatát az egyenletek, algoritmusok vagy integrált áramköri tervek fejlesztése érdekében. Olyan evolúciós elvek ihlették, mint a replikáció, a rekombináció vagy mutáció révén történő diverzifikáció, a fitnesz, a szelekción vagy selejtezésen keresztüli túlélés és az iteráció, amelyeket együttesen darwini gépnek vagy darwini racsnisnek neveznek.
A biológiai sokféleség mérése [szerkesztés | forrás szerkesztése]
Az ökoszisztéma biológiai sokfélesége meghatározható egy adott környezet teljes genomiális kiegészítéseként, az összes jelen lévő fajból, legyen szó egy elhagyott bányában lévő biofilmről, egy csepp tengervízről, egy gombóc talajról vagy az egész bioszféráról. a Föld bolygó. Az adatbázisokat a fajnevek, leírások, eloszlások, genetikai információk, a populációk állapotának és méretének, élőhelyigényeinek, valamint az egyes szervezetek más fajokkal való kölcsönhatásának összegyűjtésére használják. Speciális szoftverprogramokat használnak az információk megkeresésére, vizualizálására és elemzésére, és ami a legfontosabb, másokkal való kommunikációra. A számítógépes szimulációk modellezik például a populáció dinamikáját, vagy kiszámítják a tenyészállomány (a mezőgazdaságban) vagy a veszélyeztetett populáció (a természetben) összesített genetikai egészségét. Ennek a mezőnek az egyik nagyon izgalmas lehetősége, hogy a teljes DNS-szekvenciák vagy veszélyeztetett fajok genomjai megőrizhetők, lehetővé téve a természet genetikai kísérleteinek emlékezetét in silico, és a jövőben esetleg újrafelhasználható, még akkor is, ha ez a faj végül elveszik.
A génexpresszió elemzése [szerkesztés | forrás szerkesztése]
Számos gén expressziója meghatározható az mRNS szintjének mérésével többféle technikával, beleértve a mikro-sugarakat, az expresszált cDNS szekvencia tag (EST) szekvenálást, a génexpresszió (SAGE) tag szekvenálás soros elemzését, a masszívan párhuzamos aláírás szekvenálást (MPSS), vagy a multiplexelt in-situ hibridizáció. Mindezek a technikák rendkívül zajra hajlamosak és/vagy a biológiai mérések során elfogultságnak vannak kitéve, és a számítási biológia egyik fő kutatási területe statisztikai eszközök kifejlesztését foglalja magában a zaj és a jel szétválasztására a nagy áteresztőképességű génexpressziós vizsgálatokban. Ilyen vizsgálatokat gyakran használnak a rendellenességben szerepet játszó gének meghatározásához: összehasonlíthatjuk a rákos hámsejtek mikrorajz-adatait a nem rákos sejtek adataival annak a transzkriptumnak a meghatározása érdekében, amely a rákos sejtek adott populációjában felfelé és lefelé szabályozott.
A szabályozás elemzése [szerkesztés | forrás szerkesztése]
A szabályozás az események komplex hangszerelése, amely egy sejten kívüli szignálból indul ki, és végül egy vagy több fehérjemolekula aktivitásának növekedéséhez vagy csökkenéséhez vezet. Bioinformatikai technikákat alkalmaztak a folyamat különféle lépéseinek feltárására. Például a promóter elemzése magában foglalja a szekvencia motívumok tisztázását és tanulmányozását egy gén kódoló régióját körülvevő genomi régióban. Ezek a motívumok befolyásolják az adott régió mRNS-be való átírásának mértékét. Az expressziós adatok felhasználhatók a génszabályozás következtetésére: összehasonlíthatjuk az organizmus sokféle állapotából származó mikroszkópos adatokat, hogy hipotéziseket alkothassunk az egyes állapotokban részt vevő génekről. Egysejtű organizmusban összehasonlíthatjuk a sejtciklus szakaszait a különféle stresszállapotokkal (hősokk, éhezés stb.). Ezután alkalmazhatunk klaszterező algoritmusokat arra az expressziós adatra, hogy meghatározzuk, mely gének expresszálódnak együtt. A további elemzés sokféle irányt vehet igénybe: egy 2004-es tanulmány elemezte az együtt expresszált (összegyűjtött) gének promóter-szekvenciáit, hogy megtalálják a közös szabályozási elemeket, és gépi tanulási technikákat használtak az egyes klaszterek szabályozásában részt vevő promóter elemek azonosítására [1] .
A fehérje expressziójának elemzése [szerkesztés | forrás szerkesztése]
A fehérje mikro-sugarak és a nagy áteresztőképességű (HT) tömegspektrometria (MS) pillanatfelvételt nyújthatnak a biológiai mintában jelen lévő fehérjékről. A bioinformatika nagyon sokat foglalkozik a fehérje mikroarray és a HT MS adatok értelmezésével; az előbbi megközelítés hasonló problémákkal szembesül, mint az mRNS-re célzott mikrorajzok esetében, az utóbbi azzal a problémával jár, hogy nagy mennyiségű tömegadatot illesztenek a fehérjeszekvencia-adatbázisokból előre jelzett tömegekhez, valamint a minták bonyolult statisztikai elemzését, ahol az egyes fehérjékből több, de hiányos peptid található. észlelték.
A rák mutációinak elemzése [szerkesztés | forrás szerkesztése]
Jelenleg masszív szekvenálási erőfeszítések folynak a rák különböző génjeinek pontmutációinak azonosítására. Az előállított adatok rengeteg mennyiségéhez automatizált rendszerek szükségesek a szekvenciaadatok olvasásához, és a szekvenálási eredmények összehasonlításához az emberi genom ismert szekvenciájához, beleértve az ismert csíravonal polimorfizmusokat.
Az oligonukleotid mikrorangokat, beleértve az összehasonlító genomi hibridizációt és az egy nukleotid polimorfizmus tömböket, amelyek képesek a genomban akár több százezer hely egyidejű vizsgálatára, a rák kromoszomális nyereségének és veszteségének azonosítására használják. Rejtett Markov-modellt és változás-pont elemzési módszereket fejlesztenek ki annak érdekében, hogy következtethessenek a valódi példányszám-változásokra a gyakran zajos adatokból. További informatikai megközelítéseket dolgoznak ki annak érdekében, hogy megértsék a sok daganaton ismétlődő elváltozások következményeit.
Néhány modern eszköz (pl. Quantum 3.1) biztosítja az aminosavak megváltoztatásával a fehérje szekvencia megváltoztatását meghatározott helyeken, és megjósolja a mutációk utáni bioaktivitás változását.
A fehérje szerkezetének előrejelzése [szerkesztés | forrás szerkesztése]
A fehérje szerkezetének előrejelzése a bioinformatika másik fontos alkalmazása. Egy fehérje aminosav-szekvenciája, az ún elsődleges szerkezet, könnyen meghatározható az azt kódoló gén szekvenciájából. Az esetek túlnyomó többségében ez az elsődleges szerkezet egyedülállóan meghatározza a struktúrát natív környezetében. (Természetesen vannak kivételek, például a szarvasmarha szivacsos agyvelőbántalom - más néven Mad Cow Disease - prion.) Ennek a szerkezetnek az ismerete létfontosságú a fehérje működésének megértésében. Jobb kifejezések hiányában a strukturális információkat általában a következők közé sorolják másodlagos, harmadlagos és kvaterner szerkezet. Az ilyen jóslatok életképes általános megoldása továbbra is nyitott probléma. Mostanáig a legtöbb erőfeszítés a legtöbbször működő heurisztikára irányul.
A bioinformatika egyik legfontosabb ötlete a homológia fogalma. A bioinformatika genomi ágában homológiát használnak egy gén működésének előrejelzésére: ha a gén szekvenciája A, amelynek funkciója ismert, homológ a génszekvenciával B, akinek a funkciója ismeretlen, arra lehet következtetni, hogy B megoszthatja A funkcióját. A bioinformatika szerkezeti ágában homológiát alkalmaznak annak meghatározására, hogy a fehérje mely részei fontosak a szerkezet kialakításában és a más fehérjékkel való kölcsönhatásban. A homológiai modellezésnek nevezett technikában ezt az információt felhasználják a fehérje szerkezetének előrejelzésére, ha a homológ fehérje szerkezete ismert. Jelenleg ez az egyetlen módja a fehérjeszerkezetek megbízható előrejelzésének.
Ennek egyik példája az emberi hemoglobin és a hüvelyesek hemoglobinja (leghemoglobin) hasonló fehérjehomológiája. Mindkettő ugyanazt a célt szolgálja, hogy oxigént szállítson a szervezetben. Bár ezeknek a fehérjéknek teljesen különböző aminosav-szekvenciája van, fehérjeszerkezetük gyakorlatilag azonos, ami tükrözi majdnem azonos céljaikat.
A fehérjeszerkezet előrejelzésének egyéb technikái közé tartozik a fehérjefűzés és de novo (a semmiből) fizika alapú modellezés.
Összehasonlító genomika [szerkesztés | forrás szerkesztése]
Az összehasonlító genomelemzés lényege a gének (ortológiai elemzés) vagy más genomikus jellemzők közötti megfelelés megállapítása a különböző organizmusokban. Ezek az intergenomikus térképek teszik lehetővé a két genom divergenciájáért felelős evolúciós folyamatok nyomon követését. A különböző szervezeti szinteken működő evolúciós események sokasága alakítja a genom evolúcióját. A legalacsonyabb szinten a pontmutációk hatással vannak az egyes nukleotidokra. Magasabb szinten a nagy kromoszomális szegmensek duplikáción, oldalirányú transzferen, inverzión, transzpozíción, deléción és inszerción mennek keresztül. Végül az egész genomok részt vesznek a hibridizáció, a poliploidizáció és az endoszimbiózis folyamataiban, amelyek gyakran gyors speciációhoz vezetnek. A genom evolúciójának bonyolultsága sok izgalmas kihívást jelent a matematikai modellek és algoritmusok fejlesztői számára, akik algoritmikus, statisztikai és matematikai technikák spektrumához folyamodnak, a pontos, heurisztikus, rögzített paraméteres és közelítő algoritmusoktól kezdve a parsimónia modelleken alapuló problémákig Markovig Chain Monte Carlo algoritmusok a problémák Bayes-i elemzéséhez valószínűségi modellek alapján.
Ezen tanulmányok közül sok a homológia detektálásán és a fehérjecsaládok számításán alapul.
Biológiai rendszerek modellezése [szerkesztés | forrás szerkesztése]
A rendszerbiológia magában foglalja a sejtes alrendszerek (például a metabolitok és enzimek hálózatai, amelyek magukban foglalják az anyagcserét, a jelátviteli útvonalakat és a génszabályozó hálózatokat) számítógépes szimulációit e sejtfolyamatok összetett összefüggéseinek elemzésére és vizualizálására. A mesterséges élet vagy a virtuális evolúció megkísérli megérteni az evolúciós folyamatokat az egyszerű (mesterséges) életformák számítógépes szimulációján keresztül.
Nagy teljesítményű képelemzés [szerkesztés | forrás szerkesztése]
Számítógépes technológiákat használnak nagy mennyiségű nagy információtartalmú biomedicinikus kép feldolgozásának, mennyiségi meghatározásának és elemzésének felgyorsítására vagy teljes automatizálására. A modern képelemző rendszerek a pontosság, az objektivitás vagy a sebesség javításával növelik a megfigyelő képességét arra, hogy nagy vagy összetett képkészletből méréseket hajtson végre. Egy teljesen kifejlesztett elemzési rendszer teljesen helyettesítheti a megfigyelőt. Bár ezek a rendszerek nem csak az orvosbiológiai képalkotásokra jellemzők, a biomedicinális képalkotás mind a diagnosztika, mind a kutatás szempontjából egyre fontosabbá válik. Néhány példa:
- nagy áteresztőképességű és nagy pontosságú kvantifikáció és szubcelluláris lokalizáció (nagy tartalmú szűrés, citohisztopatológia)
- morfometria
- klinikai képelemzés és vizualizáció
- az élő állatok légzési tüdejének valós idejű légáramlási mintáinak meghatározása
- az okklúzió méretének számszerűsítése valós idejű képeken az artériás sérülés kialakulásából és helyreállításából
- viselkedési megfigyelések készítése a laboratóriumi állatok kiterjesztett videofelvételeiről
- infravörös mérések a metabolikus aktivitás meghatározásához
Szoftvereszközök [szerkesztés | forrás szerkesztése]
A biológusok körében legismertebb számítási biológiai eszköz valószínűleg a BLAST, egy algoritmus nagy fehérje- vagy DNS-szekvenciák adatbázisainak keresésére. Az NCBI egy népszerű megvalósítást kínál, amely masszív szekvencia-adatbázisukban keres. A bioinformatikai metakeresők (Entrez, Bioinformatic Harvester) segítenek megtalálni a releváns információkat több adatbázisból. Vannak olyan ingyenes webalapú szoftverek is, amelyeket a strukturális bioinformatikához terveztek, például az [1] STING.
Számítógépes szkriptnyelveket, például Perl és Python, gyakran használnak a biológiai adatbázisokkal való interakcióhoz és a bioinformatikai programok kimenetének elemzéséhez. A bioinformatikai programozók közösségei ingyenes/nyílt forráskódú projekteket hoztak létre, mint például az EMBOSS, a Bioconductor, a BioPerl, a BioLinux, a BioPython, a BioRuby és a BioJava, amelyek közös programozási eszközöket és objektumokat fejlesztenek és terjesztenek (mint programmodulok), amelyek megkönnyítik a bioinformatikát.
A fent leírt sok ingyenes/nyílt forráskódú eszközből és sok másból álló integrált szoftveres munkaasztal VigyaanCD néven ismert. A Taverna egy nyílt forráskódú bioinformatikai munkaasztal, amely a kísérleti tervezés munkafolyamat-modelljét használja. A Taverna az e-science szoftver myGRID csomagjának része. A Quantum 3.1 példa a QSAR utáni bioinformatikára, amely statisztikai módszerek helyett kvantum- és molekulafizikát alkalmaz. A Genevestigator egy példa arra, hogy a nagyméretű génexpressziós mikroszkópos adatok felhasználásával megjósolják a gén működését a kontextus információi alapján.
Újabban a SOAP-alapú interfészeket sokféle bioinformatikai alkalmazáshoz fejlesztették ki, mint például robbanás, fasta, EMBOSS, clustalw, t-coffee, MUSCLE és még sok más. Ezek elérhetők az EBI-től az EBI Web Services webhelyen.
- Cacomorphobia Phobia Wiki rajongó
- Adiposogenitalis dystrophia Pszichológia Wiki rajongó
- Buggin Out Survivor Wiki rajongó
- Banán; Cheese Total Drama Wiki rajongó
- Bariatric Surgery Endoluminal Techniques - A SAGES Wiki cikk