Diétás szénhidrátok és gyermekkori funkcionális hasi fájdalom
Bruno P. Chumpitazi
gyermekgyógyászati osztály, Baylor College of Medicine, Houston, Tex., USA
b Gyermekgasztroenterológiai, hepatológiai és táplálkozási részleg, Texas Gyermekkórház, Houston, Tex., USA
Robert J. Shulman
gyermekgyógyászati osztály, Baylor College of Medicine, Houston, Tex., USA
b Gyermekgasztroenterológiai, hepatológiai és táplálkozási részleg, Texas Gyermekkórház, Houston, Tex., USA
c Gyermektáplálkozási Kutatóközpont, Houston, Tex., USA
Absztrakt
Bevezetés
A gyermekkori hasi fájdalommal kapcsolatos funkcionális gasztrointesztinális rendellenességek (AP-FGID) világszerte a gyermekek 20% -át érintik, és az Egyesült Államokban az összes gyermekorvosi rendelő látogatásának legalább 5% -át teszik ki [1, 2]. Ezeknek a rendellenességeknek nincs azonosítható szerves etiológiája a hagyományos diagnosztikai vizsgálatok alapján; mindazonáltal az AP-FGID-ben szenvedő gyermekek életminőségének csökkenése és az iskolai hiányzások növekedése társaikhoz képest [3]. Az ezekhez a rendellenességekhez kapcsolódó gyomor-bélrendszeri (GI) tünetek (például hasi fájdalom) évekig és felnőttkorban is fennmaradhatnak [4]. A gyermekkori AP-FGID-kben ezeket a tüneteket enyhítő sikeres beavatkozások felnőttkorra is hatással lehetnek [4]. Sajnos, az egyre növekvő érdeklődés és kutatások ellenére, ezeknek a betegségeknek a jelenlegi klinikai beavatkozásai gyakran hatástalanok.
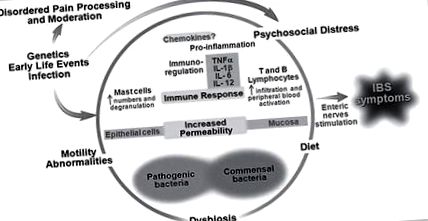
Noha korábban a visszatérő hasi fájdalom (RAP) széles kategóriája alatt definiálták, a Rome III kritériumok alapján, az AP-FGID-eket ma az alábbiakban sorolják fel: irritábilis bél szindróma (IBS), funkcionális dyspepsia, funkcionális hasi fájdalom és hasi migrén [5]. Az AP-FGID-k etiológiáját úgy gondolják, hogy multifaktoriális, és a legjobban a biopszichoszociális modell alkalmazásával közelíthető meg (1. ábra). A lehetséges tényezők a következők: pszichoszociális szorongás (pl. Szomatizáció, szorongás); a bél mikrobiomjának összetételében és működésében bekövetkező változások; alacsony fokú bélgyulladás; fokozott béláteresztő képesség; zsigeri túlérzékenység; megváltozott GI motoros funkció és étrend. Különösen az étrend okozott érdeklődést bűnösként, tekintve, hogy az AP-FGID-ben szenvedő gyermekek gyakran társítják a tüneteket bizonyos ételek bevitelével [6].
Az FGID-k biopszichoszociális modellje. Módosítva Rodriguez-Fandino és mtsai. [45] a Journal of Neurogastroenterology and Motility engedélyével.
A szénhidrátok adják a nyugati étrendben elfogyasztott kalóriák nagy részét [7]. Hosszú évtizedek óta az egyes szénhidrátok (pl. Laktóz) egyaránt szerepet játszanak a tünetek etiológiájának tettesében és potenciális terápiás szerekként (pl. Rost) AP-FGID-ben szenvedő gyermekeknél. Ez az áttekintés a szénhidrát-intolerancia javasolt patofiziológiáját és a jelenlegi bizonyítékokat vizsgálja, amelyek az egyes szénhidrátokat és szénhidrátcsoportokat vonják maguk után a gyermekkori AP-FGID-k tüneteinek előidézésében vagy javításában. Röviden megvizsgálja a rost javasolt emésztési fiziológiáját és a jelenlegi bizonyítékokat, amelyek rámutatnak a rost AP-FGID-ben szenvedő gyermekeknél történő alkalmazására.
Szénhidrát intolerancia
Javasolt közös kórélettani mechanizmusok
AP-FGID-ben szenvedő gyermekeknél több egyéni szénhidrát (köztük a laktóz és a fruktóz) is szerepet játszik a GI tüneteinek súlyosbításában [8, 9]. Ezeket az egyes szénhidrátokat csoportként fruktánokkal, galaktánokkal és poliolokkal kombinálva fermentálható oligoszacharidoknak, diszacharidoknak, monoszacharidoknak és poliolok (FODMAP) szénhidrátoknak nevezzük (1. táblázat). A FODMAP szénhidrátokat a vastagbél baktériumai gyorsan fermentálják, és ozmotikusan aktívak (2. ábra). Ezek a fiziológiai hatások vastagbél-elválasztást okozhatnak a víz beáramlásából a lumenbe, és hasi fájdalom, laposodás, puffadás, laza és/vagy gyakoribb széklet tüneteihez vezethetnek. Ezeket a szénhidrátokkal szembeni nemimmunológiai mellékhatásokat szénhidrát-intoleranciának nevezik.
A rosszul felszívódó szénhidrátok javasolt patofiziológiai mechanizmusa FGID-ben. Módosítva: Barrett et al. [46] a gyakorlati gasztroenterológia engedélyével.
Asztal 1
A szénhidrátok felsorolása és az azokat tartalmazó élelmiszerek példái a FODMAP csoporton belül
| Fruktóz | Monoszacharid | Bizonyos gyümölcsök: alma, körte; édesem; gyümölcslevek |
| Laktóz | Diszacharid | Tejtermékek: tehéntej, sajt |
| Fruktánok | Fruktóz polimerek | Búza, hagyma, rozs |
| Galaktánok | Galaktóz polimerek | Bab, hüvelyesek, spárga |
| Poliolok | Cukoralkoholok | Bizonyos gyümölcsök és zöldségek: sárgabarack, cseresznye, körte |
Bár FODMAP szénhidrátként csoportosítva, minden egyes rosszul felszívódó szénhidrátnak eltérő fiziológiai hatása lehet. A mágneses rezonancia képalkotás értékelése egészséges felnőtteknél azt mutatja, hogy a fruktóz jelentősen növeli a vékonybél víztartalmát; a fruktánok azonban sokkal kisebb mértékben növelik a vékonybél víztartalmát [10]. Összehasonlításképpen, egészséges felnőtteknél a fruktánok jelentősen eltolják a vastagbél lumenét; a fruktóz azonban jóval kisebb mértékben növeli a vastagbél disztenzióját [10]. A laktóz, galaktánok és poliolok mágneses rezonancia képalkotással mért egyedi hatása a GI fiziológiás funkciójára még tisztázatlan. Ezenkívül nem ismert, hogy ugyanazok a fiziológiai változások jelentkeznek-e a FODMAP szénhidrát bevitelét követően AP-FGID-ben szenvedő gyermekeknél (vagy felnőtteknél).
További tényezők, amelyek szerepet játszhatnak a laktóz-intoleranciában szenvedő betegek tüneteinek kialakulásában, többek között az alacsony fokú bélgyulladás és a zsigeri túlérzékenység [11]. Ezt Yang et al. [11] IBS-ben szenvedő felnőtteknél laktóz-provokációt és lélegző hidrogén-tesztet követően a laktóz-malabszorberek azonosítására (fokozott hidrogéntermelés a laktóz-provokációt követően). Az IBS-ben szenvedőket, akiknek laktóz malabszorpciója volt, a két csoport egyikébe soroltuk: laktóz malabszorpciót laktóz intoleranciával (a GI tüneteinek egyidejű növekedése a laktóz kihívással együtt) és laktóz malabszorpciót laktóz intolerancia nélkül (a GI tünetek nem nőttek). Yang és mtsai. [11] megállapította, hogy az IBS-ben szenvedő, laktóz malabsorbcióval és intoleranciával küzdő felnőtteknél (összehasonlítva a csak malabsorbcióval rendelkezőkkel) mind az ileokolonikus biopsziákban mind a hízósejtek száma megnőtt, és a visceralis túlérzékenységük is megnőtt. Jelenleg nem ismert, hogy ezek a tényezők szerepet játszanak-e a gyermekkori AP-FGID-k szénhidrát-intoleranciájában is.
Laktóz
Hippokratész először Kr. E. 400 év körül írta le a laktóz intoleranciát, de a klinikai tünetek csak az elmúlt 50 évben ismertek fel [12]. A laktóz diszacharid (két összekapcsolt cukor), amely egyedülálló abban, hogy csak emlőstejben van jelen, emberi anyatejben 5,5–8,0 g/100 ml, tehéntejben pedig 4,5–5,0 g/100 ml. Ahhoz, hogy felhasználható legyen, a laktózt a laktáz enzimnek le kell bontania (hidrolizálnia). A laktáz a vékonybél villiáinak csúcsain található, és két monoszacharidra - galaktózra és glükózra - bontja a laktózt. Ezeket a monoszacharidokat ezután a vékonybél felszívja és metabolizálja.
Az emberek születésének idején a laktáz aktivitása a csúcson van. A laktáz aktivitása azonban korai gyermekkorban kezd csökkenni az emberek körülbelül 70% -ánál; felnőttkorára a laktáz aktivitása nagyon alacsony, vagy nem mutatható ki [14, 15]. A lakosság hozzávetőlegesen 30% -ának van laktáz-perzisztenciája, ezáltal a laktáz-aktivitás az elválasztáson túl és felnőttkorig is megmarad [14, 15]. A laktáz-perzisztencia elsősorban észak-európai származású embereknél fordul elő.
A tünetek kiváltásához szükséges laktózmennyiség olyan személynél, aki laktóz-intoleráns, számos tényezőtől függ. Ide tartoznak: (1) a bevitt laktóz mennyisége; (2) a fogyasztás étkezéssel vagy más étellel jár-e; (3) a gyomor kiürülésének sebessége (az étkezés milyen gyorsan jut be a vékonybélbe); (4) a vékonybél átmeneti ideje (az az idő, amely ahhoz szükséges, hogy az étkezés belépjen a vastagbélbe, miután először belépett a vékonybélbe); (5) az étkezés tartalmaz-e olyan baktériumokat, amelyek enzimjei (béta-galaktozidáz) képesek lebontani a laktázt, és (6) vastagbél baktériumok alkalmazkodnak-e az előző étrendhez [16, 17]. Például egy vizsgálatban a ≥ 15 g egyszeri laktózterhelés tüneteket okozott a laktázhiányos felnőttek többségénél; a 12 g-ig terjedő laktózterhelés (különösen, ha a nap folyamán elterjedt) minimális vagy semmilyen tünetet nem eredményezett [18]. Hasonlóképpen, az alanyok tejbázisú joghurtok életképes mikrobiális tenyészeteivel történő táplálása, amelyek béta-galaktozidáz aktivitású baktériumokat tartalmaznak, kevesebb laktóz felszívódási jelet eredményeztek, mint kevés pasztörizált, kevés béta-galaktozidáz aktivitással rendelkező joghurtot táplálni [17]. A tünetek kiváltásához szükséges laktózmennyiség (egészséges vagy AP-FGID-vel rendelkező) laktóz malabszorpciós gyermeknél jelenleg nem ismert.
Két másik tanulmány alátámasztja a laktóz expozíció és a tünetek dózis-válasz gradiensét. Egy tanulmány 13 egészséges felnőttet váltott ki laktóz-rosszindulatban, változó mennyiségű laktózzal (0, 2, 6, 12 és 20 g) [16]. Ez a tanulmány megállapította, hogy a legfeljebb 6 g-os dózisok (amelyek 120 ml tejet képviselnek) jól tolerálhatók, de a tünetek 12 g-os expozíciónál kezdtek megjelenni [16]. Hasonló eredményeket figyeltek meg a laktózzal hidrolizált tejkészítményben növekvő mennyiségű laktózzal kezelt felnőtteknél; a tünetek súlyossága elsősorban a jelenlévő laktóz mennyiségétől függ [19].
Laktózzal kapcsolatos vizsgálatok AP-FGID-s gyermekeknél
AP-FGID-ben szenvedő gyermekeknél három randomizált, kontrollált vizsgálat zárult le, bár egyik sem értékelt kontrollált módon korlátozott laktóz-diétát (2. táblázat). Nagyobb számú megfigyelési vagy kontrollálatlan kísérlet történt (3. táblázat). Lebenthal és mtsai. [20] mind randomizált, kontrollált provokációt, mind egy kontrollálatlan kezelési komponenst használt. A vizsgálatok többségében vagy laktóz-kihívást alkalmaztak a laktóz-intoleránsok azonosítására a kihívást követő GI-tünetek kialakulása alapján, vagy egy laktóz-hidrogén lélegeztető teszt segítségével, hogy azonosítsák azokat a gyermekeket, akik rosszul szívják fel a laktózt, kimutatva a túlzott mennyiségű hidrogéntermelést. meghatározott idő a laktóz bevétele után.
2. táblázat
Prospektív randomizált kontrollált laktózvizsgálatok AP-FGID-ben szenvedő gyermekeknél
- Funkcionális hasi fájdalom Riley gyermekek egészsége
- Funkcionális hasi fájdalom gyermekeknél Boston gyermekek; s Kórház
- Az étrendi rost segíthet a gyermekkori elhízás megelőzésében Dr
- Görcsösség terhesség alatt - mit jelent a hasi fájdalom
- Krónikus hasi fájdalom és visszatérő hasi fájdalom - Emésztési rendellenességek - Merck Manuals Consumer