Elhízás, DNS károsodás és az elhízással kapcsolatos betegségek kialakulása
Marta Włodarczyk
1 Biokémiai és Farmakogenomikai Tanszék, Gyógyszerésztudományi Kar, Laboratóriumi Orvosi Osztály, Varsói Orvostudományi Egyetem, Banacha 1B, 02-097 Varsó, Lengyelország; [email protected]
2 Preklinikai Kutatóközpont, Varsói Orvostudományi Egyetem, Banacha 1B, 02-097 Varsó, Lengyelország
Grażyna Nowicka
1 Biokémiai és Farmakogenomikai Tanszék, Gyógyszerésztudományi Kar, Laboratóriumi Orvosi Osztály, Varsói Orvostudományi Egyetem, Banacha 1B, 02-097 Varsó, Lengyelország; [email protected]
2 Preklinikai Kutatóközpont, Varsói Orvostudományi Egyetem, Banacha 1B, 02-097 Varsó, Lengyelország
Absztrakt
Az elhízásról felismerték, hogy növeli az olyan betegségek kockázatát, mint a szív- és érrendszeri betegségek, a cukorbetegség és a rák. Ez azt jelzi, hogy az elhízás befolyásolhatja a genom stabilitását. Az elhízásban gyakran előforduló oxidatív stressz és gyulladás DNS károsodást indukálhat és gátolhatja a DNS helyreállítási mechanizmusait. A DNS károsodás felhalmozódása megnövekedett mutációhoz vezethet, és megváltoztathatja a génexpressziót, ami a sejtek anyagcseréjének zavarait eredményezheti. Az elhízáshoz kapcsolódó DNS-károsodás elősegítheti a rák növekedését azáltal, hogy elősegíti a rákos sejtek szaporodását és vándorlását, valamint az apoptózissal szembeni ellenállást. A DNS károsodásának és/vagy a DNS helyreállításának zavarainak becslése potenciálisan hasznos lehet az elhízással összefüggő anyagcserezavarok, valamint a rák kockázatának felmérésében és megelőzésében. Az elhízott emberek DNS-károsodása visszafordíthatónak tűnik, és mind a fogyás, mind az étkezési szokások és az étrend összetételének javítása befolyásolhatja a genom stabilitását.
1. Bemutatkozás
Az elhízás növekvő gyakorisága a felnőttek, valamint a gyermekek és serdülők körében is jelentős egészségügyi problémává vált. Az elhízás egy összetett krónikus betegség, amelyet a testzsírszövet tömegének jelentős növekedése jellemez, és összefüggésben van a lipid- és glükóz-anyagcsere zavarával, krónikus gyulladással és oxidatív stresszel, valamint számos betegség, nevezetesen a szív- és érrendszeri betegségek, a cukorbetegség fokozott kockázatával. és a rákos megbetegedések, valamint a várható élettartam csökkenésével [1,2,3]. Elhízásban szenvedőknél a DNS károsodásának felhalmozódásáról számoltak be, és azt javasolták, hogy vegyenek részt az elhízással összefüggő betegség kialakulásában [4,5,6]. A DNS-elváltozások hatással vannak a DNS-replikációra, mutációkhoz vezetnek, és ezáltal veszélyt jelenthetnek a sejtek anyagcseréjére és a sejtek túlélésére [7]. Megállapították, hogy a testtömeg-csökkenés a DNS-károsodás szintjének csökkenését eredményezi [8].
A cikk célja az elhízás mint DNS károsító tényező hangsúlyozása, valamint az elhízás, a DNS károsodás és az anyagcserezavarok kialakulása, valamint a rák közötti kapcsolat bemutatása.
2. Gyulladás és reaktív oxigénfajok (ROS) által kiváltott DNS károsodás
A gyulladás aktiválódik, hogy megvédje a testet ezektől a káros ingerektől [9]. A krónikus gyulladás összefüggésbe hozható az öregedéssel és számos olyan krónikus betegséggel, mint a szív- és érrendszeri betegségek, az autoimmun betegségek és a rák [10,11]. A gyulladásos szignál toborozza és aktiválja a neutrofileket és a makrofágokat, viszont endogén oxigén és nitrogén fajok jönnek létre. Ezenkívül reaktív oxigénfajok (ROS) is képződnek a sejtekben a mitokondriális oxidatív anyagcsere, az apoptózis vagy a nikotinamid-adenin-dinukleotid-foszfát (NADPH) -oxidázok, a szuperoxid-diszmutáz (SOD), a mieloperoxidáz (MPO) és a nitrogén-oxid-szintáz (NOS) során. [12].
A gyökökkel szembeni specifikus védekező rendszer jelenléte ellenére az állandó ROS-termelés és az alacsony antioxidáns aktivitás egyensúlyvesztéshez vezethet az ROS kialakulása és a védelmi rendszer működése között, ami oxidatív stressz kialakulásához vezetett. A megnövekedett ROS termelés és az oxidatív stressz endogén DNS károsodást, transzkripció megszakadást és sejtciklus leállást indukálhat [13,14]. A lipidperoxidációs folyamatokat ROS is indukálja, és DNS-reaktív elváltozások kialakulásához vezetnek [15].
3. DNS-károk helyreállítása
A DNS-javító rendszer létezik a DNS-károsodás leküzdésére és a DNS-szerkezet integritásának fenntartására. Általában a DNS-károsodás helyreállítási folyamata magában foglalja a DNS-károsodás felismerését specifikus szenzorokkal, a DNS-károsító jel előállítását és amplifikálását, ennek a jelnek a citoplazmába történő transzdukcióját és specifikus effektorok aktiválását [21]. A DNS-helyreállítási útvonalakban részt vevő enzimek aktivitásának egyedközi változatait írták le [22,23]. Ezért várható némi különbség a DNS-javítás hatékonyságában és az endogén DNS-károsodás megfigyelt szintjeiben [24,25].
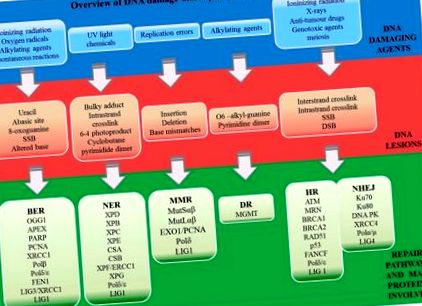
Számos ismert DNS-javítási mechanizmus közül a közvetlen helyreállítás a replikáció során, míg a közvetett helyreállítás a DNS-szintézis után történik [26]. A közvetett javítási stratégia magában foglalja az alapkivágási javítást (BER), a nukleotid-kivágás javítását (NER), a nem megfelelő javítást (MMR), a nem homológ végcsatlakozási (NHEJ) és a homológ rekombinációs (HR) útvonalakat. Három tudós elmagyarázta a DNS-helyreállítással járó utak magyarázatát azzal, hogy 2015-ben kémiai Nobel-díjat kapott nekik [27]. Tomas Lindahl leírta a BER modelljét, amely részt vesz a módosított alapjavításban [28]. Paul Modrich külön utat fedezett fel, amely detektálja és eltávolítja azokat a bázisokat, amelyek a DNS-replikáció során tévesen beépülnek. Végül Aziz Sancar a NER DNS-adduktok eltávolításának mechanizmusát javasolta [29]. A DNS-károsító szerek, az indukált DNS-elváltozások és azok helyreállítási útvonalainak áttekintését az 1. ábra mutatja be .
Áttekintés a DNS-t károsító szerekről, az indukált DNS-elváltozásokról és azok helyreállítási útvonalairól (BER - bázis excíziós javítás, NER - nukleotid kivágás javítás, MMR - nem megfelelő helyreállítás, DR - közvetlen javítás, NHEJ - nem homológ végcsatlakozás; és HR - homológ rekombináció). A parancsikonokat a rövidítés szakasz magyarázza.
4. Elhízás és DNS károsodás
Elhízott embereknél a DNS-elváltozások széles skáláját, például kettős szálszakadásokat (DSB), egyszálú töréseket (SSB) vagy oxidált bázisokat, és körülbelül kétszer nagyobb DNS-károsodást figyeltek meg a limfocitákban, mint normál testsúlyú alanyokban, és összefüggést mutattak a testtömeg-index (BMI) és a DNS-károsodás között szintén találtak [5,30,31]. A H2AX foszforilációval mért DNS károsodás szintjeiben szignifikáns különbséget figyeltek meg a túlsúlyos és elhízott gyermekeknél a sovány kontrollokhoz képest [32]. Az elhízott emberek limfocitáinak több mitomicin C által kiváltott DNS-károsodása volt a normál testsúlyú alanyok sejtjeihez képest [33]. Az elhízás és az oxidált bázisok - például a 8-oxodG és a 8-OHdG - szintje közötti összefüggésre vonatkozó adatok azonban nem konzisztensek [34,35,36,37].
Jól elfogadott, hogy az elhízás esetén a krónikus energia-túlterhelés fokozott ROS termelést és gyulladást eredményez [38]. A rendelkezésre álló adatok azt mutatják, hogy a ROS forrása az elhízás stádiumától függően változhat [39]. Az elhízás korai szakaszában a fokozott glükóz- és zsírsav-adipocita-felvétel aktiválja az NOX4-et, az adipociták fő NADPH-oxidáz izoformáját, és ROS-termelést indukál. A NOX4 csendesítéséről beszámoltak arról, hogy csökken a ROS-termelés és a monocita kemoattraktáns protein-1 gátlása [40]. A zsír túlzott felhalmozódása az adipocitákban elősegíti a proinflammatorikus adipokinek termelését. A gyulladásos citokinek az immunsejtek által a célszövet behatolását és krónikus gyulladás kialakulását idézik elő [41]. A T-limfociták és makrofágok felhalmozódása a zsírszövetben az elhízás kialakulása során elősegíti a NOX2, a gyulladásos sejtekben expresszálódó NADPH-oxidáz ROS-termelését. Ezenkívül a magas FFA (szabad zsírsav) vagy magas glükózkoncentrációnak kitett adipociták és simaizomsejtek fokozott mitokondriális hasadást és megnövekedett mitokondriális ROS termelést mutattak [42,43,44]. Az elhízásra jellemző a trigliceridek túlzott felhalmozódása az adipocitákban az FFA fokozott mitokondriális β-oxidációját és fokozott mitokondriális ROS-generációt eredményez.
Ezenkívül az elhízással járó krónikus gyulladás erősen részt vesz a DNS-elváltozás kialakulásában [38]. Az aktivált makrofágok olyan citokineket választanak ki, mint a TNFα és az IL-6, amelyek DNS-károsodást indukálhatnak a nem célzott szövetekben, amelyek távol vannak a gyulladás helyétől [45,46]. A felszabadult citokinek a test különböző régióiba utazhatnak, és aktiválhatják a rezidens makrofágokat, hogy olyan gyulladásgátló molekulákat állítsanak elő, mint COX2, NOS, szuperoxid, ROS és NO [47,48]. E molekulák felszabadulása oxidatív DNS károsodáshoz vezethet a sejtekben. Emellett az apoptotikus sejteket elnyelő makrofágok a test másik régiójába költözhetnek, majd felszabadíthatják a DNS károsodását kiváltó tényezőket [49]. A DNS károsító tényezők makrofágokon keresztül történő transzlokációja nagy mennyiségű károsító indukáló szignált juttathat el távoli helyekről, és specifikus lehet azokra a régiókra is, ahol a makrofágok valószínűleg utazni fognak (pl. Bél, lép, bőr, nyirokcsomók). Így az elhízással összefüggő oxidatív stressz és gyulladás DNS károsodást indukálhat a különböző szövetekben.
Az elhízott, a DNS károsodásának felmérését végző, publikált súlycsökkentő nyomvonalak korlátozottak. Az alacsony kalóriatartalmú étrend okozta súlycsökkenés után a DNS károsodás szintjének jelentős csökkenését találták [8,50]. A genomi stabilitás javulását, a nyál oxidatív károsodásának csökkenésével jellemezve, a bariatrikus műtétek után is megfigyelték súlyvesztéssel kóros elhízásban szenvedő betegeknél [51].
4.1. Elhízás és a DNS károsodásának helyreállítása
Beszámoltak a megnövekedett testtömeggel kapcsolatos DNS károsodás reakcióút zavarairól [52]. A BMI és a nukleotidkivágási (NER) kapacitás között inverz összefüggést találtak fiatal nőknél [53]. Az elhízás jelenlétét felismerték, hogy megváltoztatja a DSB-k genotoxikus szerek által kiváltott javulását is [34]. Az elhízáshoz kapcsolódó fokozott ROS-termelés modulálhatja a DNS károsodásának reakcióját a DNS-helyreállításban részt vevő gének expressziójára gyakorolt hatás révén (2. ábra) [54,55]. Beszámoltak az oxidatív stressz által kiváltott DNS-javító enzimek gátlásáról [56,57]. A stresszre és a toxikus szerekre adott válaszokkal összefüggő elhízott gének expressziójában szintén felismerték [58].
Elhízás és DNS károsodás. Az elhízás gyulladással és oxidatív stresszel társul, amely DNS-károsodást vált ki és gátolja a DNS-károsodás helyreállítását, ami a DNS-károsodás felhalmozódását eredményezi az adipocytákban és más szövetekben.
4.2. Elhízás és mitokondriális DNS károsodás
A DNS elváltozások mind a nukleáris, mind a mitokondriális DNS-ben (mtDNS) előfordulnak. Mivel a mitokondriumokban nincs nukleotidkivágási mechanizmus, az mtDNS hajlamosabb a reaktív fajok által okozott károkra, mint a nukleáris DNS. A gyulladáshoz és a környezeti tényezőkhöz kapcsolódó oxidatív stressz eredményeként keletkező fotodimerek és terjedelmes adduktok nem távolíthatók el hatékonyan az mtDNS-ből [66,67]. Annak ellenére, hogy az mtDNS csak a mitokondriális fehérjék 1% -át kódolja, a mitokondriális betegségek nagyszámú elváltozással társulnak az mtDNS-ben [68]. Ezenkívül az mtDNS fokozott lebomlása és a csökkent mtDNS kópiaszám összefügg a cukorbetegséggel, a rákkal vagy a neurodegeneratív betegségekkel is [69,70,71]. Az oxidatív mtDNS elváltozások felhalmozódása átrendeződéseket vagy pontmutációkat eredményezhet, amelyek anyai úton öröklődhetnek [72].
Elhízás esetén a mitokondriális diszfunkció a zsírsav (FA) oxidációjának kudarcához és a glükóz homeosztázis zavaraihoz vezet [43,73,74]. A morbid elhízott betegeknél megfigyelt megnövekedett vizelettel történő mtDNS kiválasztás a bariatrikus műtétekhez kapcsolódó súlycsökkenés után szignifikánsan csökkentnek bizonyult [75]. Az állatkísérlet kimutatta, hogy a magas zsírtartalmú étrenddel etetett egerekben az mtDNS károsodása megnövekedett, és mitokondriális diszfunkcióval járt [76]. Ezenkívül azt találták, hogy az oxidált mtDNS a gyulladásos citokinek, például az IL-6, TNF-a, a pro-IL-1β szintézisét indukálja a toll-szerű receptor 9 (TLR-9) aktiválásával [77,78]. Ezért az elhízással társult gyulladás részben oka, mind következménye lehet az mtDNS elváltozások felhalmozódásának.
4.3. A szülők elhízással kapcsolatos DNS-károsodásának hatása az utódokra
Az elhízással összefüggő DNS-károsodások legalább részben reagálhatnak az elhízott alanyok reproduktív képességének és utódaik egészségének zavaraira [79]. Felismerték, hogy az adipozitás spermiumok DNS-fragmentációját okozza, befolyásolja a DNS metilációját és rendellenességeket okoz a hím ivarsejtek kromatinjában [80,81]. Elhízott betegeknél a spermiumokban magas DNS-fragmentációs indexet (DFI) és csökkent termékenységet ismertek el [82,83]. A csírasejtek DNS-károsodása az elhízásra jellemző megnövekedett ROS-termelés következménye lehet [59,84,85]. A leánysejtekben a későbbi sejtosztódás után DNS-károsodás mutatkozott, amely hatástalan DNS-károsító reakcióra utal. Ezért gyanítható, hogy a DNS-elváltozások csírasejtekben való megjelenése átvihető a jövő generációinak genomjába [87]. Az anyai elhízás de novo mutációkat okozhat az embrióban, megváltoztathatja a gének metilációs állapotát az embrióban, és a miRNS révén befolyásolja az embrionális fehérjék expresszióját [88,89,90,91].
5. DNS károsodás és elhízással kapcsolatos anyagcserezavarok
Kétségtelen, hogy az elhízás DNS károsodást okozó oxidatív stresszel jár. Az oxidált, telített és gyűrűs töredezett bázisok BER útvonalon történő javítása kritikusan fontos a genomi stabilitás fenntartása szempontjából. Másrészt megmutatták a DNS-javító fehérjék fontos szerepét a mitokondriális energetika és az egész test energiamérlegének modulálásában [116]. Az olyan gének termékei, mint az OGG1, NTH1, NEIL1 és NEIL2, részt vesznek az oxidatív DNS-elváltozások helyrehozásának megindításában. A NEIL1 egy olyan enzim, amely a gyűrűs töredezett purinok és néhány telített pirimidin BER-jét indítja el [117, 118]. A neil1 knockout egereknél a metabolikus szindrómának megfelelő tünetek jelentkeztek: súlyos elhízás, zsírmáj, diszlipidémia és inzulinrezisztencia [119]. Az OGG1, a BER helyreállítási útjának kritikus enzime, részt vesz a leggyakoribb oxidatív DNS elváltozás kijavításában, mivel a 8-oxo-7,8-dihidroguanin (8-oxoG) és az OGG1 expresszió magas zsírtartalmú étrendre reagálva [120]. Az OGG1 hiányában szenvedő egereknél (Ogg1 -/-) a metabolikus szindróma jellemzői alakultak ki, többek között megnövekedett zsírszint, zsírmáj, emelkedett trigliceridszint és csökkent glükóz tolerancia [116].
Ezért az elhízás DNS károsodást és a DNS helyreállításának zavarait idézheti elő, amelyek a DNS károsodásának sejtbeli felhalmozódását eredményezhetik, ami gyulladást és változásokat okoz a génexpresszióban, valamint zavarokat okoz a sejtanyagcserében (3. ábra). Ezen változások következtében anyagcserezavarok alakulhatnak ki, és a DNS károsodásának csökkentése fontos lehet az elhízással összefüggő anyagcsere-betegségek megelőzésében és kezelésében [5,121].
- Az új gyógyszer megakadályozza a májkárosodást, az elhízást és a glükóz intoleranciát a magas zsírtartalmú étrendben
- Az új gyógyszer megakadályozza a májkárosodást, az elhízást és a glükóz intoleranciát a magas zsírtartalmú étrendben
- Roster APA iránymutatás-fejlesztési panel az elhízáshoz
- Az új gyógyszer megakadályozza a májkárosodást, az elhízást és a glükóz intoleranciát a magas zsírtartalmú étrendben
- A parazita férgek segíthetnek az elhízással járó betegségek kezelésében - írja a ScienceDaily