Elhízás és pszichotikus rendellenességek: közös mechanizmusok feltárása metabolomikán keresztül
Matej Orešič
1 Rendszerbiológia és bioinformatika, Finnországi VTT Műszaki Kutatóközpont, Espoo, FIN-02044 VTT, Finnország
Absztrakt
Az elsődleges elhízás és a pszichotikus rendellenességek hasonlóak az energiamérleg és a társbetegségek, beleértve a metabolikus szindrómát, kapcsolódó változásait illetően. Az ilyen hasonlóságok nem feltétlenül mutatnak ok-okozati összefüggéseket, ehelyett arra utalnak, hogy az elhízás specifikus okai és anyagcserezavarai kórokozó szerepet játszanak a társbetegségek kialakulásában, még az elhízás kialakulása előtt is. A metabolomika - a metabolitok, amelyek az anyagcsere folyamata során keletkező kismolekulák, szisztematikus vizsgálata - fontos volt az elhízáshoz társuló társbetegségek hátterében. Ez az áttekintés azt mutatja be, hogy a közelmúltbeli metabolomikus vizsgálatok miként tették lehetővé a biomarkerek felfedezését, valamint az elhízás és társbetegségei mögött álló mechanizmusok tisztázását, különös tekintettel a metabolikus szindrómára és a pszichotikus rendellenességekre. Hangsúlyozzák a betegséggel összefüggő köztes fenotípusok - a modulált, de a DNS-szekvencia által nem kódolt tulajdonságok - metabolikus markereinek azonosításának fontosságát. Az ilyen markerek diagnosztikai eszközökként alkalmazhatók személyre szabott egészségügyi környezetben, és új terápiás lehetőségeket is nyithatnak.
Bevezetés
Az elhízást a testfelesleg jellemzi, amely túlnyomórészt a zsírszövetben tárolódik. Az elhízás és az ezzel járó társbetegségek - köztük az alkoholmentes zsírmájbetegség (NAFLD), a 2-es típusú cukorbetegség és a szív- és érrendszeri betegségek - prevalenciája az elmúlt 40–50 évben folyamatosan nőtt, kiemelve az obesogén környezet (Catenacci et al., 2009). Mivel az elhízás, az inzulinrezisztencia, a cukorbetegség, a dyslipidaemia és a zsírmáj általában ugyanazon egyénnél fordul elő együtt, hasznos volt ezt a megnyilvánulási klasztert „metabolikus szindrómának” nevezni. E patológiák csoportosulása nem véletlenszerű esemény: inkább valószínűleg közös kórokozó mechanizmusokkal rendelkeznek. Amint informatikánk kifinomultabbá válik, és a betegek epidemiológiai adatai jobban integrálódnak, a metabolikus szindróma megértése fokozatosan gazdagodik. Különösen az, hogy mára egyértelmű, hogy a metabolikus rendellenességek nagy gyakorisággal fordulnak elő skizofréniában és más pszichotikus rendellenességekben szenvedő egyéneknél (Saarni et al., 2009; Suvisaari et al., 2007). Így a metabolikus szindrómában szerepet játszó kórokozó mechanizmusok szintén hozzájárulhatnak e pszichiátriai rendellenességek kialakulásához és/vagy felgyorsulásához (bár fordítva is igaz lehet).
A komplex betegségeknek vitathatatlanul erős genetikai összetevője van. Például az öröklődést a metabolikus szindróma esetén legalább 40% -ra becsülik (Lusis et al., 2008) és skizofrénia esetén legalább 65% -ra (Lichtenstein és mtsai, 2009). Ennek ellenére egyre nyilvánvalóbbá válik, hogy a betegség jellemzőivel kapcsolatos genetikai összefüggések tanulmányozására használt jelenlegi megközelítések az ismert betegségörökölhetőségnek csak kis részét magyarázzák (Maher, 2008). Rendszerbiológiai nézet szerint a komplex betegség-fogékonyság genetikai összetevőjének nagy része nem egyedi gének, hanem más génekkel és a környezettel való kölcsönhatásukban (Tang et al., 2009). Ebben az összefüggésben a modulált, de a DNS-szekvencia által nem kódolt - általában köztes fenotípusnak nevezett tulajdonságok (Meyer-Lindenberg és Weinberger, 2006) - mérése különösen érdekes.
A metabolitok specifikus csoportjainak (az anyagcsere folyamatában keletkező kis molekulák) koncentrációjának változásai érzékenyek és specifikusak olyan kórosan releváns tényezőkre, mint a genetikai variáció (Illig et al., 2010), az étrend (Holmes et al., 2008), fejlődés (Nikkilä et al., 2008), életkor (Maeba et al., 2007), immunrendszeri állapot (Oresic et al., 2008b) és a bél mikrobiota (Martin et al., 2007; Velagapudi et al., 2010). Bár évtizedekkel ezelőtt felismerték a metabolitok tanulmányozásának fontosságát az egészség és a betegség összefüggésében (Pauling és mtsai., 1971), a metabolitok átfogó tanulmányozásához korábban nem voltak analitikai eszközök. Ez az elmúlt évtizedben megváltozott, az analitikai és a bioinformatikai technológiák számos jelentős előrelépésével a biológiai rendszerek metabolitjainak érzékeny és átfogó mérését teszik lehetővé (Goodacre et al., 2004; Katajamaa és Oresic, 2007). Így a metabolomika - a metabolitok globális vizsgálata - gyorsan megjelent, mint hatékony eszköz a komplex fenotípusok jellemzésére és a specifikus fiziológiai válaszok biomarkereinek azonosítására (Oresic et al., 2006). Különösen a metabolom érzékeny mind a genetikai, mind a környezeti tényezőkre, ami a metabolomikát a személyre szabott orvoslás hatékony fenotipizáló eszközévé teszi.
Ez a cikk rövid áttekintést nyújt a metabolomika közelmúltbeli fejlődéséről a biomarkerek felfedezésénél, valamint az elhízás és társbetegségei hátterében álló mechanizmusok tisztázásában, különös hangsúlyt fektetve a metabolikus szindrómára és a pszichotikus rendellenességekre.
Az egyének és a populációk összehasonlítása
Úgy gondolják, hogy a metabolikus diszfunkció részben a lipidbevitel által okozott lipotoxicitásból származhat, amely meghaladja azt, amit az egyén zsírszövete képes tárolni (Unger, 1997; Virtue és Vidal-Puig, 2010). A zsírszövet lipidek tárolási képessége genetikai és környezeti tényezőktől függ. Epidemiológiai vizsgálatokból meggyőző bizonyítékok állnak rendelkezésre arról, hogy a testtömeg (azaz a lipidek tárolása) és az inzulinrezisztencia között szinte lineáris összefüggés van. Egy ilyen összefüggés azonban a populációra kiterjedő elemzés „átlagolási hatásának” köszönhető. A zsírszövet tágulási hipotézise azt sugallja, hogy minden egyén számára létezik egy testtömeg-küszöb, amely attól függ, hogy az illető zsírszövet képes-e lipideket tárolni (Virtue és Vidal-Puig, 2008). Ennek a testtömeg-küszöbnek a túllépése az inzulinérzékenység jelentős csökkenésével jár együtt a lipidek túlterhelése és más perifériás szervekbe történő áramlásuk miatt. E hipotézis szerint a testtömeg növekedése még mindig lineárisan összefügg az inzulinérzékenységgel. A populációra kiterjedő elemzés során azonban elvesznek az egyes emberek zsírszövet-tágulási küszöbéről szóló információk.
Hagyományosan az olyan molekuláris biomarkereket, mint amilyeneket a metabolomika eredményez, az epidemiológiai vizsgálatok során specifikus klinikai végpontokkal társítottak. Az ilyen markerek statisztikailag jól teljesítenek nagy populációs körülmények között, de mint fentebb kifejtettük, csekély értékkel bírhatnak, ha egyénekre alkalmazzák őket. Ehelyett a biomarkereknek érzékenyeknek kell lenniük a szervspecifikus genetikai sérülékenységre és az elhízással összefüggő szövődményekhez vezető specifikus patofiziológiai mechanizmusokra. Például egy olyan biomarkert, amely érzékeny a zsírszövet metabolikus állapotára, fel lehet használni azon személyek azonosítására, akiknek az adipocitái közel vannak a lipidtárolókapacitás eléréséhez - és akiket ezért a megnövekedett testtömeg miatt az inzulinrezisztencia kialakulásának veszélye fenyeget. Az ilyen biomarkerek megtalálása hatékony eszközöket kínálna a veszélyeztetett személyek sokkal korábbiak felderítésére, mint a jelenleg lehetséges, és javítaná a személyre szabott egészségügyet.
A lipidóm egészségben és betegségekben
Hiányoztak a lipidek globális és kvantitatív vizsgálatának érzékeny platformjai a sejtektől a szervezet szintjéig. Az utóbbi időben azonban a „lipidomika” mint a metabolomikához szorosan kapcsolódó tudományág jelent meg; ez a megközelítés globálisan értékeli a lipidómákat, amelyek a sejt lipidjeinek útjait és hálózatait tartalmazzák a biológiai rendszerekben (Oresic et al., 2008a). A lipidek az esszenciális metabolitok sokféle csoportja, számos kulcsfontosságú biológiai funkcióval, például a sejtmembránok szerkezeti komponenseiként, energiatároló forrásokként és köztitermékekként a jelátviteli utakban. A lipidek szoros homeosztatikus kontroll alatt állnak (Oresic et al., 2008a), és térbeli és dinamikus komplexitást mutatnak több szinten. Ezért nem meglepő, hogy a megváltozott lipid-anyagcsere globális kiterjedésű, mint patogén mechanizmus, és részt vesz a cukorbetegségben és a lipotoxicitás okozta inzulinrezisztenciában (Medina-Gomez et al., 2007; Medina-Gomez et al., 2009; Unger, 1997 ), Alzheimer-kór (Han és mtsai, 2001; Oresic és mtsai, 2011a), skizofrénia (Kaddurah-Daouk és mtsai, 2007; Oresic és mtsai, 2012; Oresic és mtsai, 2011b; Schwarz és mtsai, 2008), rák (Hilvo és mtsai, 2011) és érelmeszesedés (Lusis, 2000).
A lipidomikát az anyagcserezavarok tanulmányozásának egyik kulcsfontosságú technológiájának tekintik. Például a lipotoxicitást a reaktív (lipo) toxikus lipidek, például a ceramidok és a diacilglicerinek túltermelése jellemzi a perifériás szervekben. Ez a zsírszövetből származó zsírsavak megnövekedett áramlása miatt következik be - vagyis azért, mert az egyén túllépte a zsírszövetben történő zsírraktározás képességét (Virtue és Vidal-Puig, 2010). Az anyagcsere-szervek, például a máj vagy az izom lipidprofiljainak jellemzésénél ezért nem elegendő megmérni a lipidek mennyiségét ezekben a szervekben; figyelembe kell venni a lipidek minőségét is - vagyis meg kell vizsgálni a szövetben található lipidek részletes molekuláris összetételét. Ilyen információt lipidomikával nyerhetünk.
Az anyagcserezavarok korai markereinek kimutatása
Az elhízáshoz kapcsolódó metabolikus profilok és metabolikus társbetegségei meghatározása aktív kutatási terület. Például az inzulinérzékenység és a szív- és érrendszeri betegségek (RISC) kohorszának összefüggését vizsgáló nagyszabású metabolomikai tanulmány az α-hidroxi-butirátot az inzulinrezisztencia korai markerként azonosította (Gall et al., 2010). Számos más tanulmány az elágazó láncú aminosavak fokozott koncentrációját is összekapcsolta a keringésben az inzulinrezisztenciával és a diabetes mellitus kockázatával (Newgard et al., 2009; Pietiläinen et al., 2008; Wang et al., 2011). A lipidómikus vizsgálatok azt is kimutatták, hogy az alacsonyabb szénatomszámú és kettős kötéstartalmú trigliceridek összefüggenek az inzulinrezisztenciával (Kotronen és mtsai, 2009b), a magas májzsírral (Kotronen és mtsai, 2009a; Westerbacka és mtsai, 2010) és a cukorbetegséggel. kockázat (Rhee et al., 2011).
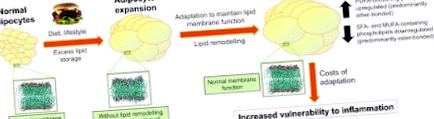
Modell a lipidmembrán összetételének fiziológiai szabályozására az elhízásban. Egészséges elhízás esetén a lipidmembránok alkalmazkodnak, amikor az adipociták méretének növekedése megtörténik. Tekintettel arra, hogy az adaptáció a gyulladásgátló mediátorok prekurzorainak relatív növekedését vonja maga után, az adaptáció növelheti a gyulladás iránti sebezhetőséget. MUFA, egyszeresen telítetlen zsírsav; PUFA, többszörösen telítetlen zsírsav; SFA, telített zsírsav. Engedéllyel reprodukálva (Pietiläinen et al., 2011).
Nevezetesen, az elhízott ikrek adipocitáinak membránjában felhalmozódott lipidek olyan gyulladásgátló lipid mediátorok prekurzorai, mint a leukotriének és a prosztaglandinok (Murphy, 2001). Így, bár metabolikusan kompenzált, elhízott egyéneknél a membrán lipidjeinek átalakítása hozzájárulhat a normális membránfunkció fenntartásához, a zsírszövetet sebezhetőbbé teheti a gyulladással szemben is. Ezek a megállapítások megmagyarázhatják, hogy az elhízott egyének miért nagyobb kockázattal járnak a gyulladásos rendellenességek, például a diabetes mellitus kialakulásában.
Ennek az ikervizsgálatnak az eredményei arra utalnak, hogy az adipociták membránjai utalnak az elhízáshoz társuló társbetegségek korai patofiziológiai folyamataira. A zsírszöveti membrán lipidjeinek vagy ezeknek a vérben való korrelációjának mérése, mint köztes fenotípus, ezért hatékony korai markerekkel szolgálhat. A tanulmány azt is sugallja, hogy új lehetőségek merülhetnek fel az elhízással összefüggő metabolikus szövődmények megelőzésében vagy kezelésében, ha a zsírszöveti lipidhálózatot modulálni lehetne a membrán funkcionális fenntartásának és/vagy a gyulladás iránti sérülékenység szabályozásának érdekében.
A máj egy másik kulcsfontosságú anyagcsere-szerv, amelyről ismert, hogy a cukorbetegség kockázatával jár. A krónikus májbetegséghez és májelégtelenséghez vezető NAFLD-t a májban lévő zsírlerakódások jellemzik, elsősorban trigliceridek formájában. A NAFLD előfordulása az Egyesült Államokban felnőtteknél megduplázódott 5,51% -ról 11,01% -ra 1988 és 2008 között, és járványos méreteket érhet el, ha az elhízás és a cukorbetegség jelenlegi aránya továbbra is növekszik (Younossi et al., 2011). Továbbá a májzsír a metabolikus szindróma fő meghatározója (Cohen és mtsai., 2011; Kotronen és Yki-Järvinen, 2008; Van Gaal és mtsai, 2006).
A májzsírt általában szövettan határozza meg, vagy mágneses rezonancia spektroszkópiával becsüljük meg. Az előbbi módszer nagyon invazív, májbiopsziát igényel, ezért csak krónikus májbetegségekben alkalmazzák, míg az utóbbi módszer túl drága egészségügyi szűrési célokra. Nem elérhető invazív teszt, amelyet széles körben alkalmazhatnának egészségügyi környezetben, ezért sürgősen meg kell határozni a vérben jelen lévő molekuláris markereket, amelyek nagy érzékenységgel tükrözik a máj zsírmennyiségét. Bátorító módon az előzetes lipidomikai és metabolomikai vizsgálatok már reményt adtak arra, hogy a NAFLD-hez kapcsolódó megbízható biomarkerek hamarosan kiderülhetnek (Barr et al., 2010; Puri et al., 2007).
Az elhízás társbetegségének értékelése a metabolikus szindrómán túl
Az elhízás és a pszichotikus rendellenességek közötti összefüggés a növekvő kutatási érdeklődés másik területe (Kaidanovich-Beilin et al., 2012). A pszichotikus rendellenességek olyan mentális rendellenességek, amelyeket a valóság tesztjének romlása vagy a valóság torzulása jellemez. A pszichotikus tünetek közé tartoznak a téveszmék, a hallucinációk, a rendezetlen beszéd és a furcsa vagy katatonikus viselkedés. A pszichotikus rendellenességek előfordulási gyakorisága fiatal felnőttkorban csúcsos (Suvisaari et al., 1999), egy olyan fejlődési periódus, amikor az agykéregben az axonos mielinizáció miatt jelentős változások következnek be a zsírsavösszetételben. Ezeknek a rendellenességeknek az életkori prevalenciája 3,5%, a leggyakoribb a skizofrénia, amelynek életkori prevalenciája ~ 1% (Perälä et al., 2007).
Következtetések
Sürgősen szükség van olyan molekuláris markerek azonosítására, amelyek lehetővé teszik az elhízás társbetegségéhez vezető patofiziológiai folyamatok korai felismerését. Noha az epidemiológiai vizsgálatok összefüggéseket fedeznek fel konkrét betegségkockázati tényezők között populációs szinten, nagyobb hangsúlyt kell fektetni a betegséggel összefüggő köztes fenotípusok és markereik azonosítására és megértésére az egyénekben. A releváns köztes fenotípusok markerei jobban alkalmazhatók lennének a személyre szabott egészségügyi ellátási környezetben, mint a betegséggel összefüggő kockázati tényezők, amelyeket a populáció egészére kiterjedő szűrés során szereznek be, mert képesek kimutatni egy adott betegséggel összefüggő patofiziológiai folyamat jelenlétét. Ezenkívül a köztes fenotípusok és markereik tisztázása új terápiás és diagnosztikai stratégiákhoz vezethet az elhízással járó társbetegségek, köztük a cukorbetegség, valamint más betegségek, köztük a rák, az Alzheimer-kór és a pszichiátriai rendellenességek számára.
Köszönetnyilvánítás
A szerző hálás Antonio Vidal-Puignak, Celso Arangónak és Jaana Suvisaarinak a hasznos beszélgetésekért.
Lábjegyzetek
Ez a cikk az elhízásról szóló különszám része: lásd a kapcsolódó cikkeket a Vol. 5. szám, Dis. Modell. Mech. a http://dmm.biologists.org/content/5/5.toc címen.
VERSENY ÉRDEKEK
A szerző kijelenti, hogy nincsenek pénzügyi vagy versengő érdekeik.
FINANSZÍROZÁS
Ezt a munkát a Finn Akadémia Molekuláris Rendszerek Immunológiai és Élettani Kutatási Kiválósági Központja (SyMMyS, 2012–2017, 250114 számú határozat) és a „Bél mikrobiotája által közvetített étrendi hatások jellemzése és modellezése a lipidanyagcserén” projekt támogatta., amelyet az Európai Bizottság támogatott a 7. keretprogram keretében (FP7-KBBE-222639 szerződés).
- PRIME PubMed A hasi zsír, az elhízás és a gyakori mentális rendellenességek kapcsolata eredményez
- Szájzavarok Gyakori szájproblémák MedlinePlus
- Elhízás és hasnyálmirigyrák Az epidemiológiai bizonyítékok és a molekuláris mechanizmusok frissítése -
- Elhízás és rák mechanizmusai Daganat mikrokörnyezet és gyulladás Journal of Clinical Oncology
- AZ ELHÍZÁS ÉS A PELVIC PADLÓ ZAVARAI AZ IRODALOM ÁTTEKINTÉSE