Hosszú távú metformin-kezelés elhízással és inzulinrezisztenciával rendelkező serdülőknél, egy nyílt kiterjesztéses vizsgálat eredménye
Tárgyak
Absztrakt
Háttér/Célkitűzések
Az off-label metformint napjainkban gyakran használják serdülők elhízásának kezelésére. Az elhízásban szenvedő serdülőknél azonban hosszú távú metformin-kezelésre vonatkozó vizsgálatok kevések. Ezért 18 hónapos, nyílt kiterjesztésű vizsgálatot végeztek 18 hónapos randomizált, placebo-kontrollos vizsgálatot (RCT) követően a metformin hatékonyságáról, biztonságosságáról és tolerálhatóságáról elhízással és inzulinrezisztenciával rendelkező serdülőknél.
Tantárgyak/módszerek
Az RCT befejezése után a metformint felajánlották minden résztvevőnek, testtömeg-index standard deviációs pontszámmal (BMI-sds)> 2,3 és az inzulinrezisztencia homeosztázis-modelljének értékelésével (HOMA-IR) ≥ 3,4. A végpontok a BMI és a HOMA-IR változásai voltak.
Eredmények
Összességében 31/42 résztvevő fejezte be a kiterjesztett vizsgálatot (74% lány, medián életkor 14,8 (11,6 - 17,9), BMI 31,2 (22,3 - 45,1), HOMA-IR 3,4 (0,2 - 8,8)). Kezdetben 22/42 (52,4%) résztvevő volt jogosult a metforminra, ebből 13 (59,0%) egyetértett a kezeléssel. A metformint folytató résztvevőknél a BMI (+2,2 (+0,2 és +9,0)) és a HOMA-IR (+13,7 (+1,6 és +48,3)) növekedését figyelték meg. Metforminnal nem kezelt résztvevőknél a BMI egy kezdeti csökkenés után stabilizálódott (+0,5 (−2,1 és +5,1)). A HOMA-IR esetében csökkenést figyeltünk meg (−1,1 (−4,6 - +1,4)).
Következtetés
Bár úgy tűnik, hogy a metforminnal nem kezelt résztvevőknél a metformin-kezelés a BMI és a HOMA-IR kezdeti csökkenését eredményezi, serdülőknél történő hosszantartó alkalmazás után nincs bizonyíték a tartós hatásra. A korlátozott megfelelés és/vagy az elégtelen dózis magyarázhatja a serdülők és a felnőttek közötti hosszú távú hatások különbségeit.
Bevezetés
Az elhízás világszerte jelentős egészségügyi probléma 1, a gyermekek és serdülők becsült prevalenciája 2025-ben legfeljebb 5,4% 2. Az elhízás olyan szövődményekkel jár, mint a metabolikus szindróma, a 2-es típusú diabetes mellitus (T2DM), a szív- és érrendszeri betegségek és a máj steatosis 2,3. Az inzulinrezisztencia (IR) fontos szerepet játszik a szövődmények kialakulásában, mivel ez a megzavart glükóz tolerancia 4,5 előfutára, amelyet a szív- és érrendszeri betegségek független kockázati tényezőjeként ismernek el 4, és az 5,6 metabolikus szindróma része. Mivel az elhízás egyre fiatalabb korban mozog, a kapcsolódó szövődmények gyermekkorban 3 fognak megnyilvánulni. A multidiszciplináris életmódbeli beavatkozás a (gyermekkori) elhízás kezelésének sarokköve 7. Ez azonban csak marginális hosszú távú hatással jár a magas lemorzsolódás és a korlátozott motiváció miatt, amelyet szinte az összes tanulmány megfigyelt 7,8 .
Az utóbbi években a tanulmányok az életmódbeli beavatkozásokon felül további terápiákra összpontosítanak, mint például a gyógyszeres terápia és a bariatrikus sebészet 7. Bár a bariatrikus műtét még nem tekinthető standard terápiának, hatásosnak tűnik a posztpubertus korú serdülőknél, akiknek terápiás rezisztens elhízásuk van, 9,10,11. A farmakoterápiát illetően az orlistat és a metformin a két legtöbbet vizsgált gyógyszer 7,12. Az orlisztát, a lipáz inhibitor, az egyetlen jóváhagyott gyógyszer a gyermekkori elhízás kezelésére. Azonban a napi klinikai gyakorlatban a hasznosság korlátozott a gyakran jelentett gyomor-bélrendszeri káros hatások miatt, és csak mérsékelt súlycsökkenés, a kardiometabolikus szövődményekre gyakorolt kedvező hatások nélkül 7,12,13,14 .
A metformin, a T2DM kezelésére 10 éves kortól engedélyezett orális antihiperglikémiás szer, többszörös vizsgálat középpontjába került, mint kiegészítő terápia a gyermekkori elhízás kezelésében 15,16,17,18,19,20,21, 22,23,24. Kisebb, de jelentős súlycsökkenéssel jár és általában jól tolerálható 15,16,17,18,19,20,21,22,23,24. Bár az irodalom nem következetes, a metformin kardiometabolikus szövődményekre gyakorolt kedvező hatásait 15,16,17,18,21. Ezért azt javasoljuk, hogy a metformin potenciálisan késleltesse és/vagy megelőzze a (gyermekkori) elhízás szövődményeit 25. A serdülőknél végzett metformin hatékonyságának vizsgálata azonban túlnyomórészt egy 6 hónapos követési időszakra korlátozódik 15,16,17,18,19,20. Csak néhány vizsgálatot végeztek hosszabb, legfeljebb 24 hónapos követési időszakkal 21,22,23,24. Következésképpen nem világos, hogy a serdülőknél a tartós metformin-kezelés hosszan tartó pozitív hatást eredményez-e a testsúlyra.
Ezért ennek a vizsgálatnak a célja egy 18 hónapos nyílt kiterjesztésű vizsgálat eredményeiről beszámolni egy randomizált, placebo-kontrollos vizsgálat (RCT) után 18 hónapos metforminnal vagy placebóval történő kezelés során, a metformin hatékonysága, biztonságossága és tolerálhatósága szempontjából. elhízásos és IR 22 serdülők kezelése. Ezenkívül értékelik az elhízással kapcsolatos metabolikus és kardiovaszkuláris szövődmények kialakulását.
Anyagok és metódusok
Mivel a vizsgálati protokollt és a 18 hónapos RCT eredményeit másutt jelentették 22, 26, itt csak a tanulmány tervezésének rövid leírását mutatjuk be.
Tanulmányterv és résztvevők
Következésképpen ebben a nyílt kiterjesztésű vizsgálatban négy vizsgálati csoport volt, attól függően, hogy ebben a vizsgálatban a metformint vagy a placebót alkalmazták-e az RCT és a metformin kezelés alatt. A nyílt kiterjesztésű vizsgálat során a metforminnal rendelkező résztvevőket MM vagy PM, a metformin nélküli résztvevőket MP vagy PP jelöléssel látták el. Az első betű az RCT alatti kezelést jelenti (M a metformin, P a placebo), a második betű a nyílt kiterjesztésű vizsgálat során végzett kezelést.
A méréseket a részt vevő kórházak gyermek ambulanciáin vagy napközi osztályain végezték. Valamennyi résztvevőnek három ütemezett kórházi látogatása és három telefonhívása volt, kivéve a metformin-használókat, akiknek a telefonálás helyett további látogatásuk volt a biztonság és az elviselhetőség ellenőrzése érdekében. A fitnesz teszteket a Szent Antonius Kórház fizikoterápiás ambulanciáján és a Jeroen Bosch Kórház Sportorvosi Központjában végezték el. Az RCT-vel ellentétben nem kínáltak külön felügyelt testedzési programot. Az RCT-hez hasonlóan a metformin-terápiában résztvevők azonnali felszabadulású 500 mg metformin-tablettát kaptak növekvő adagolási rend szerint, a negyedik héten naponta kétszer legfeljebb két tablettát kaptak. Gasztrointesztinális panaszok esetén az adagot az utolsó jól tolerálható dózisra csökkentették. A tünetek megszűnése után az adagot a maximálisan tolerált dózisra emelték 26. Az RCT-vel ellentétben nem végeztek tablettaszámlálást.
Eredmények
A végpontok a BMI (ΔBMI) és a HOMA-IR (ΔHOMA-IR) változásai voltak. Ezenkívül értékelték a metformin biztonságosságát és tolerálhatóságát. Ezenkívül értékelték a HbA1c, a testzsír százalék, az életminőség és a fizikai erőnlét változását. Végül értékelték az elhízással kapcsolatos metabolikus és kardiovaszkuláris szövődmények százalékos arányát.
A BMI-t súly (kg)/(magasság (m)) 2-ben számítottuk. A megfelelő életkorral és nem szerint korrigált BMI-t, a BMI-sds-t a TNO növekedési kalkulátor segítségével számoltuk ki a szakemberek számára 28. Az IR-t a HOMA-IR (éhomi plazma-glükóz (mmol/l) × éhomi plazma inzulin (mU/l))/22,5)) 29 alkalmazásával számítottuk, és HOMA-IR ≥ 3,4 30 .
A biztonságot az esetek számaként jelentették, amikor a máj- és/vagy vesefunkciós tesztek meghaladták a biztonsági határértékeket (ALAT> 69U/l (lányok) vagy> 78 U/l (fiúk), glomeruláris filtrációs ráta (GFR) 26 .
A metabolikus szövődmények meghatározása: a megzavart glükóz tolerancia az éhomi glükóz károsodása (IFG) ≥ 5,6–31. Magas triglicerid értéket ≥ 1,7 mmol/l, az alacsony nagy sűrűségű lipoproteint (HDL) pedig 31 értékként határoztak meg. A magas szisztolés vérnyomást szisztolés és/vagy diasztolés vérnyomásként határozták meg, amely ≥ 95. percentilis volt az életkor és a magasság között. A metabolikus szindróma a következő kritériumok közül legalább 3 jelenlétének minősül: derék kerülete ≥ 95. percentilis az életkor számára, szisztolés és/vagy diasztolés vérnyomás ≥ 95. percentilis az életkor számára, magas trigliceridszint, alacsony HDL és zavart glükóz tolerancia 6. A mikrovaszkuláris szövődményeket 30-300 mg/l vizeletalbuminként határozták meg egy kora reggeli vizeletmintában 31. A szív- és érrendszeri szövődményeket az artériás merevség alapján értékeltük. Az artériás merevséget nem invazív módon értékeltük a pulzushullám sebességének (PWV) és az augmentációs index (AIX) mérésével a SphygmoCor (Model SCOR-Px, szoftver verzió, 7.01; AtCor Medical Pvt. Ltd, Sydney, Ausztrália) alkalmazásával.
Az antropometriai és laboratóriumi paramétereket félévente értékelték. A testzsírszázalékot, az IWQOL-gyerekeket, a fizikai erőnléti tesztet és az artériás merevséget csak a kiterjesztéses vizsgálat végén értékelték, ezért összehasonlításra az RCT végén kapott adatokat használták.
Statisztikai analízis
A statisztikai elemzést az IBM SPSS Statistics 24. verziójával (IBM SPSS Statistics, Chicago, IL, USA) használtuk. Mivel a vizsgálati karonkénti résztvevők száma kicsi volt, az eredményeket leíró jelleggel ismertettük o-értékeket a táblázatok mutatják be. A kis mintaméret miatt feltételeztük, hogy a paraméterek nem normálisan oszlanak meg, ezért a folyamatos adatokat mediánként, a kategóriákat pedig gyakoriságként, százalékban adtuk meg. Kruskal – Wallis teszttel hasonlítottuk össze a folyamatos adatok vizsgálati ágainak alapszintű jellemzőit és a χ 2 teszt vagy Fisher pontos tesztje a kategorikus változókra. Az eredmény paraméterei az időpontokban t = 0 és t A nyílt kiterjesztésű vizsgálat 18-át hasonlítottuk össze a vizsgálati ágakkal Kruskal – Wallis teszt segítségével. An α-Az 5% -os szintet szignifikánsnak tekintették az összes statisztikai teszt során.
Eredmények
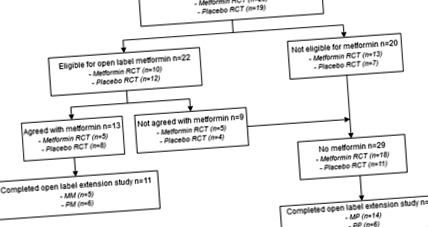
Az 1. ábra a vizsgált populáció folyamatábráját mutatja. Az RCT-t kitöltő mind a 42 résztvevő részt vett a nyílt címkés kiterjesztéses vizsgálatban. A vizsgálat kezdetén 22/42 (52%) résztvevő volt jogosult metforminra, ebből 13 (59%) egyetértett a kezeléssel. A többi résztvevő 29 (69%) nem használta a metformint 5 (17,2%) elhízás nélkül, 15 (51,7%) IR nélkül és 9 (31,0%) beleegyezés nélkül a kezeléshez). A vizsgálat során tizenegy résztvevőt veszítettek nyomon (azaz 4MP, 5PP, 2PM); ezért összesen 31 résztvevőt elemeztek.
MM metformin az RCT és az extenzív vizsgálat során, a PM placebo az RCT alatt és a metformin az extenzív vizsgálat során, az MP metformin az RCT alatt és a placebo az extenzív vizsgálat során, PP placebo az RCT és az extenzív vizsgálat során
Kiindulási jellemzők
A nyílt kiterjesztésű vizsgálatot befejező résztvevők kiindulási jellemzőit az 1. táblázat mutatja be. A demográfiai és laboratóriumi adatok széles skáláját figyelték meg az összes résztvevő és a vizsgálati ágon belüli résztvevők között. A résztvevők 84% -a elhízott és 45% -uk infravörös volt a nyílt kiterjesztésű vizsgálat kezdetén. A vizsgálati ágak a HOMA-IR esetében szignifikánsan különböztek, a BMI vagy a BMI-sd-k esetében azonban nem. A résztvevők túlnyomórészt nők voltak, pubertás (Tanner 2–4) vagy posztpubertus (Tanner 5) szakaszban. A megfigyelt Tanner stádiumok jelentősen különböztek a vizsgálati ágak között.
Hatás a BMI-re és a HOMA-IR-re
A 2. ábra a BMI és a HOMA-IR progresszióját mutatja a nyílt kiterjesztésű vizsgálat során, tanulmányi karonként rétegezve. Az MM alcsoportban a BMI általános növekedését figyelték meg a nyílt kiterjesztésű vizsgálat kezdetétől. A PM alcsoportban a BMI kezdeti csökkenését, majd növekedését figyelték meg. Az MP alcsoportban a BMI stabilizálódása észlelhető volt az első 6 hónapban, majd növekedést mutatott. A PP alcsoportban az első 6 hónapban kezdeti növekedést, majd a BMI stabilizálódását figyelték meg. A HOMA-IR esetében éles növekedést figyeltünk meg az MM alcsoportban. A többi alcsoportban hullámos mintázatot figyeltünk meg. Az abszolút értékek áttekintését, valamint a BMI, HOMA-IR és BMI-sd változásait a nyílt kiterjesztésű vizsgálat, az RCT és az RCT, valamint a nyílt kiterjesztésű vizsgálat során az 1. kiegészítő táblázat és a kiegészítő ábra mutatja be. 1.
Medián BMI (a); medián HOMA-IR (b). MM metformin az RCT és az extenzív vizsgálat során, PM placebo az RCT alatt és a metformin az extenzív vizsgálat során, PP placebo az RCT és az extenzív vizsgálat során, MP metformin az RCT alatt és a placebo a kiterjesztéses vizsgálat során
Biztonság és tolerálhatóság
Súlyos káros hatásokat nem jelentettek. A biztonsági méréseket illetően 2 résztvevőnél (1 MM és 1 MP) figyeltek meg májfunkciós rendellenességet, mint ALAT-t definiált biztonsági határt. Alacsony B12-vitamint 2 résztvevőnél tapasztaltak (1 MM és 1 MP). Veseelégtelenséget nem figyeltek meg. A metformint általában jól tolerálták. Két résztvevő hányingerről és négy hasmenésről számolt be. Két résztvevő (mindkét PM) mellékhatások (emésztőrendszeri tünetek) miatt hagyta abba a vizsgálatot.
Egyéb eredmények
A 3. ábra a HbA1c, a testzsírszázalék, a zsírtömeg és a zsírmentes tömeg medián változását mutatja. A HbA1c növekedését figyelték meg az MM alcsoportban, míg a többi alcsoportban csökkent. A testzsír százalékban stabilizációt figyeltek meg a PM és PP alcsoportban, míg az MM és MP alcsoport növekedést mutatott. A zsírtömeg nőtt az MM és PP alcsoportban, ahol az MP és PM alcsoportban a medián csökkenés széles tartományban figyelhető meg. A zsírmentes tömeg esetében minden alcsoportban növekedést figyeltünk meg. Az abszolút értékek áttekintését, valamint a HbA1c, a testzsírszázalék, a zsírtömeg és a zsírmentes tömeg változását a nyílt kiterjesztésű vizsgálat, valamint az RCT és a nyílt kiterjesztésű vizsgálat során az 1. kiegészítő táblázat mutatja be.
MM metformin az RCT és az extenzív vizsgálat során, a PM placebo az RCT alatt és a metformin az extenzív vizsgálat során, a PP placebo az RCT és az extenzív vizsgálat során, az MP metformin az RCT alatt és a placebo a kiterjesztéses vizsgálat során. A szaggatott vonal nem jelent változást
A fizikai erőnlét és az életminőség változásának megbízható elemzését nem lehetett elvégezni, mivel csak néhány résztvevő végezte el a fitnesz tesztet (n = 11) és/vagy átadta az IWQOL értékelést (n = 19) az RCT végén és a nyílt kiterjesztésű vizsgálat végén.
Az elhízással kapcsolatos szövődmények
A nyílt kiterjesztésű vizsgálat végén 8/31 (26%) résztvevőnél zavart glükóz toleranciát figyeltek meg. Az egyik résztvevő kifejlesztette a T2DM-et (amelyet további orális glükóz-tolerancia teszt igazolt), 3 IFG-t és 4 IGT-t. Magas trigliceridszintet figyeltek meg 7/31 (23%) résztvevőnél, alacsony HDL-t pedig 11/31 (36%). Továbbá 2 résztvevőnél magas szisztolés és/vagy diasztolés vérnyomás alakult ki. Mikroalbuminuriát 1/31 (3%) résztvevőnél figyeltek meg. Ezenkívül a teljes populációban az AIx-vel mért vaszkuláris merevség növekedése (−3,1 vs. 2,3; o = 0,04) figyeltek meg, a PWV esetében nem volt szignifikáns különbség (4,2 vs. 4,6; o = 0,10). Az elhízással kapcsolatos metabolikus és kardiovaszkuláris szövődmények progressziójának áttekintése az RCT és a nyílt kiterjesztésű vizsgálat során a 2. táblázatban található.
Vita
Ebben a tanulmányban a serdülők részt vettek egy 18 hónapos nyílt kiterjesztésű vizsgálatban, amely 18 hónapos kettős-vak vak RCT-t követett a metformin hosszú távú hatékonyságáról, biztonságosságáról és tolerálhatóságáról elhízott és IR 22 serdülőknél. A nyílt kiterjesztésű vizsgálat kezdetén metformint kínáltak a résztvevőknek, a BMI és a HOMA-IR függvényében; ezért 4 vizsgálati ágat hoztak létre, amelyekben a résztvevők 18 hónapot, 36 hónapot vagy egyáltalán nem használtak metformint.
A magas lemorzsolódás összhangban van más elhízási vizsgálatokkal, függetlenül a vizsgálat időtartamától 15,19,21,23,24, és megfigyelhető a gyermek (elhízás) ambulanciákon végzett rutinos klinikai ellátás során is. Mivel az elhízott populációkban végzett vizsgálatokat a befogadások száma és a magas lemorzsolódás korlátozza, javasoljuk, hogy az RCT kevésbé korlátozó befogadási/kizárási kritériumait a megfelelő befogadási számok elérése érdekében a kutatási hálózatok kialakításával együtt kell használni. Ha elhízott gyermekpopulációkat vizsgálunk, kérdéses, hogy ezeket RCT-ben kell-e elvégezni, vagy célszerűbb-e a vizsgálatokat napi klinikai ellátásban standardizált protokoll alkalmazásával elvégezni.
Következtetés
Bár úgy tűnik, hogy a metforminnal nem kezelt résztvevőknél a metformin-kezelés a BMI és a HOMA-IR kezdeti csökkenését eredményezi, serdülőknél történő hosszantartó alkalmazás után nincs bizonyíték a tartós hatásra. A korlátozott megfelelés és/vagy az elégtelen dózis magyarázhatja a serdülők és a felnőttek közötti hosszú távú hatások különbségeit.
- Hosszú távú biztonság, tolerálhatóság és súlycsökkenés a metforminnal a cukorbetegségben
- Metformin (Glucophage) gyógyszeres kezelés - 2-es típusú cukorbetegség kezelése
- A lipid és inzulin infúzió által kiváltott vázizom inzulinrezisztencia valószínűleg az anyagcsere miatt következik be
- Lorcaserin az elhízás kezelésére Nyílt szív mellékhatásainak részletesebb áttekintése
- Inzulinrezisztencia, diszlipidémia és szív- és érrendszeri betegségek cukorbetegségének ellátása