Irisin: Remény az elhízás és az anyagcsere-szindróma megértésében és kezelésében
Lidia I. Arhire
1 Belgyógyászati Klinika, „Grigore T. Popa” Orvostudományi és Gyógyszerészeti Egyetem, Jászvásár, Románia
2 Klinikai Kórház „Sf. Spiridon ”, Jászvásár, Románia
Laura Mihalache
1 Belgyógyászati Klinika, „Grigore T. Popa” Orvostudományi és Gyógyszerészeti Egyetem, Jászvásár, Románia
2 Klinikai Kórház „Sf. Spiridon ”, Jászvásár, Románia
Mihai Covasa
3 Általános Orvostudományi Tanszék, Osteopátiás Orvostudományi Főiskola, Nyugati Egészségtudományi Egyetem, Pomona, Kalifornia, Egyesült Államok
4 Egészségügyi és Humán Fejlesztési Tanszék, Suceava Egyetem, Suceava, Románia
Absztrakt
Bevezetés
A zsír termogenezise és az adipokinek
Kétféle zsírszövet létezik: fehér vagy barna. Az embereknél a zsír főleg a fehér zsírszövetből (WAT) áll, amely nagymértékben részt vesz a homeosztázisban, és amely képes auto, para- és endokrin kommunikációs módszerek kialakítására más szövetekkel és szervekkel. Az adipocitákból/preadipocitákból álló zsír endothel sejteket, multipotenciális mezenhimális sejteket, idegsejteket és immunsejteket is tartalmaz, amelyek részt vesznek a gyulladásos és metabolikus/hormonális válaszokban. Adipokineknek (adipocitokineknek) nevezett citokineket választ ki, amelyek hatással vannak a gyulladásra, az angiogenezisre és az anyagcsere folyamatokra (14). Ezen adipokinek közül néhányat elsősorban az adipocita választ ki (pl. Leptin, adiponektin, rezisztin, kemerin és visfatin), de sokakat (pl. TNFα, IL-6 vagy MCP-1) más sejttípusok is szekretálnak (15 –18). Mivel ezek a molekulák lokális és perifériás szinten képesek szignálokat létrehozni, úgy gondolják, hogy sok anyagcsere-utat, valamint az adipociták differenciálódását befolyásolják. Mediátorként is szolgálnak, összekapcsolva a gyulladást és az immunitást az elhízással és annak társbetegségeivel/szövődményeivel (19). A WAT valójában a legnagyobb endokrin szerv lehet, amely rengeteg hormont, növekedési és komplement faktorokat, valamint más molekulákat generál, beleértve ezen biológiai ágensek közül számos receptort is (20).
Egyértelmű azonban, hogy a WAT főként triglicerideket és zsírsavakat (a legnagyobb energiatartalékot) tárol, és egyetlen (egyszemű) lipidcseppekből és kevés erből álló sejtekből áll, így fehér-sárga megjelenését eredményezi. Különc magot és nagyon kevés mitokondriumot tartalmaz. Összehasonlításképpen: a barna zsírszövet az energiafelhasználásra szakosodott („kalóriát éget”) (21). Sok multilokuláris lipidcseppből és nagyon sok vasat tartalmazó mitokondriumból áll (21, 22). Ennek a szövetnek a mitokondriális membránjai tartalmazzák az úgynevezett szétkapcsoló fehérje 1 (UCP1) nevű fehérjét, amely a protonokat a mitokondriális mátrixból a mitokondriális intermembrán térbe pumpálja (23). Az aktivált UCP1 nem okoz ATP-szintézist, de hőfelszabaduláshoz vezet, szabályozva a testhőmérsékletet, különösen az újszülötteknél (23, 24). A BAT pozitívan befolyásolja az anyagcsere folyamatait, és növeli a teljes energiafelhasználást, ami a testtömeg csökkenését eredményezi (21). A BAT specifikus endokrin faktorokat (fibroblaszt-növekedési faktor-21), valamint szisztémás következményekkel járó távoli jeleket produkál (25). A BAT emelheti a vércukorszint és a lipidek felvételét is, javítva anyagcseréjüket a fogyástól függetlenül.
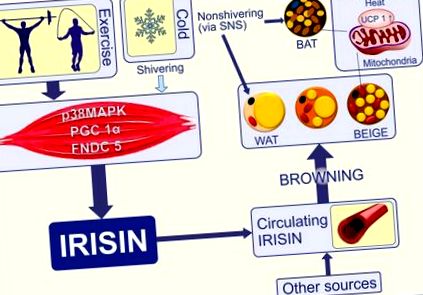
Ismeretes, hogy a BAT rágcsálókban bőségesen, nagy emlősökben kevés, az intrauterin életben emberben, valamint az interscapularis és perirenalis régióban lévő csecsemőkben van jelen, de ezek a kis mennyiségek is fokozatosan eltűnnek (26). Felnőtteknél a BAT maradék és jelentős fiziológiai aktivitás nélkül (27). Az aktív BAT nemrégiben történt felfedezése felnőtt emberekben és számos transzkripciós faktor dokumentálása, amelyek szabályozzák az új termogén adipociták képződését, vonzóvá teszi az ilyen típusú zsírszövet növelését és terápiás célként történő felhasználását (28). A szubkután zsír többféle inger, például hideg, béta-adrenerg agonisták vagy hormonszerű ingerek hatására „barnává” válhat (29) (1. ábra). Ez a zsírbarnulás magában foglalja az UCP1mRNS indukcióját és a légzést és a hőtermelést elválasztó gének expresszióját. Egerekben kimutatták, hogy a zsigeri zsír csökkenése lehetséges, például a retinaldehid-dehidrogenáz 1 (RALDH1) genetikai ablációjával (35), de ez a folyamat sokkal ritkábban fordul elő, mint a WAT barnulás. Az indukálható bézs színű adipociták felfedezése kibővítette az ezen a területen végzett kutatást, és terápiás ígérettel bír (36).
A hideg a vázizomzatban reszketést indít el és egy nem dideregő fázist, amelyben a barna és bézs zsírszövet aktiválódik, hogy az UCP-1-en keresztül hőt bocsásson ki. A borzongás és a testmozgás elősegíti a zsírszövet által közvetített termogenezist az irizin szekrécióján keresztül (30). A testmozgás növeli a transzkripciós ko-aktivátor PGC1-α-t és indukálja az FNDC5 gén expresszióját. Az FNDC5 membránfehérjét lehasítjuk, hogy az irizint felszabadítsuk a véráramba. Az irizint az adipociták is felszabadítják, így adipocitokinokká válnak (18). Más források, például az agy, a hasnyálmirigy, a gyomor, a Kupffer-sejtek, a nyelv, a végbél, a szív, a herék, a szinuszos hámsejtek és a látóideg is felszabadítja az irizint (31). Az irizin elősegíti az érett fehér zsírsejtek „barnulását” a testmozgás hatására (32, 33). A barna és a bézs zsírszövetek növelik az energiafelhasználást az oxidatív anyagcsere és az ATP termelésének elválasztása révén. Ez az UCP1 egyik kulcsfontosságú funkciója (34). PGC-1α, peroxiszóma-proliferátor-aktivált receptor gamma-koaktivátor 1 alfa; FNDC5, fibronektin III típusú doméntartalmú fehérje 5; WAT, fehér zsírszövet; BAT, barna zsírszövet; BEIGE, bézs színű adipocita, brite („barna-fehérben”) vagy indukálható BAT; UCP1, protein-1 szétkapcsolása; SNS, szimpatikus idegrendszer.
Izomtermogenezis és myokinek
Irisin eredete
Az irizin, amelyet először állatokban, később pedig emberben fedeztek fel, az utóbbi években az egyik legjobban tanulmányozott testmozgás által kiváltott peptid (32), és bevezetése óta fokozott népszerűségnek örvend a „gyújtsd meg a tüzet” szlogen (62). Az irizin az adipomyokinek osztályába tartozik, mivel mind a zsír-, mind az izomszövetben (adipokin és myokin) hat, és egy termogén fehérje, amely elősegíti az energiafogyasztást a WAT barnulással (63). Az irizin hőként oszlatja el az energiát (64), és ezért felfedezése számos kutatást eredményezett az energia-anyagcsere mechanizmusainak megértésére (65). Az izomszövetben történő izolálását, a nomenklatúrát és a kezdeti kémiai jellemzést Bostrom et al. aki kimutatta, hogy az irizin 112 aminosavval rendelkező és 12 kDa molekulatömegű fehérje (32). Az irisin név az ókori görög Iris istennőtől (32) származik, Thaumas és Electra lányától, aki a görög mitológiában az Istentől az emberig tartó jó hír istennőjének hírnöke volt (66). Ez a név nagyon helyénvalónak bizonyult, mivel az irizin, mint kémiai hírvivő fő funkciójára vonatkozik, amely a testmozgás jótékony hatásait átadja a zsírszövetnek (barnulás és termogenezis) és más, az anyagcserében részt vevő szerveknek.
Irisin és testmozgás
Irisin és glükóz homeosztázis
Az irizin megkönnyíti a vázizmok glükózfelvételét, javítja a máj glükóz- és lipidanyagcseréjét, pozitív hatással van az elhízás és a metabolikus szindróma okozta hiperlipidémiára és hiperglikémiára (80), ezért inzulinszenzibilizáló hormonként működik (2. ábra). Úgy gondolják, hogy az irizin az IR csökkentésével befolyásolja a 2-es típusú cukorbetegségben részt vevő szerveket és szöveteket, például a májat és a hasnyálmirigyet, bár a hasnyálmirigy-szigetek működését moduláló mechanizmusok még mindig nem ismertek (60). Azt javasoljuk, hogy az irizin javíthatja a máj anyagcseréjét az endoplazmatikus retikulum stressz (ER stressz) csökkentésével, és hozzájárul a β-szigetecske sejtek túléléséhez és működéséhez (2. ábra). Ezért az irizin pozitívan befolyásolhatja a máj és a hasnyálmirigy szigeteit, csökkentve ezzel a 2-es típusú diabetes mellitus kialakulásának kockázatát (80).
A keringő irizin főleg a vázizmokból származik a zsírszövet aktivitása során és abból. Az irizin lokálisan, autokrin/parakrin módon hat, és a forgalomba bocsátva hormonszerű módon hat, közvetítve a perifériás aktivitást (80). Az irizinnek többféle spektrumú funkciója van a különböző szöveteken vagy szerveken, gátolja az adipogén differenciálódást, miközben elősegíti az oszteogén differenciálódást (59). Az irizin befolyásolja a vázizomzat, a hasnyálmirigy (81), a máj (82), az agy (83) és a csont (84, 85) működését, fokozza az inzulinérzékenységet, az anyagcserét, a kogníciót és az osteogenezist. Az irizin javítja az inzulinrezisztenciát és a 2-es típusú cukorbetegséget azáltal, hogy növeli az inzulinreceptor érzékenységét a vázizomban és a szívben, javítja a máj glükóz- és lipidanyagcseréjét, elősegíti a hasnyálmirigy β-sejtjeinek működését és a fehér zsírszövet barnulását (86). WAT, fehér zsírszövet; BDNF, agyi eredetű neurotróf faktor.
A májnak a glükóz homeosztázisban való részvétele az egyensúly fenntartása a máj glükóztermelése és a glükóz tárolása között. A glükoneogenezis sebességét elsősorban a glükoneogenezis enzimek, a foszfoenol-piruvát-karboxikináz (Pepck) és a glükóz-6-foszfatáz (G6Páz) transzkripciós szintje szabja meg. Másrészt a GSK-3 gátlása elősegíti a glikogénszintáz aktivitását, ami glikogenezishez vezet (87). A máj lipid anyagcseréje szintén alapvető szerepet játszik a glükóz homeosztázisban. Amikor a szénhidrátbevitel meghaladja a raktározás és oxidáció képességét, de novo lipogenezissel zsírokká alakulnak. A májban a lipidfelesleg azonban gyulladást és IR-t okoz (88). Jelentős bizonyítékok szerint az ER stressz, különösen a máj ER, szorosan kapcsolódik az anyagcsere-betegségekhez, elősegítve a máj glükóztermelését, az elhízásnál a lipogenezist és az IR-t, valamint a cukorbetegséget (89). A máj AMPK aktivációjának antidiabetikus szerepe van a májban a glükóz és a zsír anyagcseréjének modulálásával, a lipogenezis és a glükoneogenezis csillapításával, valamint a lipid oxidáció és a glikolízis elősegítésével (90).
Irisin és elhízás
Bár az irizint elsősorban miokinnak ismerik, a zsírszövetből is felszabadul (18, 60), nevét adipokinként kapva, és közvetítve a testmozgás jótékony metabolikus hatásait (101). Rágcsálóknál az FNDC5/irizin elsősorban a SAT adipocitáiból és kisebb mennyiségben a zsigeri zsírszövet adipocitáiból (VAT) szekretálódik (18). Emberekben azonban az FNDC5 expresszió 100–200-szor alacsonyabb a WAT-ban, mint az izomban, ami azt jelzi, hogy a WAT kisebb mértékben járul hozzá a keringő irizin szintjéhez (102). A zsírszövet hozzájárulását a keringő irizin szintjéhez molekuláris állat-alapú vizsgálatok igazolták, hogy a zsírszöveti szekréció hozzájárul az FNDC5/irizin keringéséhez (18). Ezenkívül az emberi eredetű zsírszövet expresszálja és szekretálja az FNDC5/irizint (103). In vitro kísérletek azt mutatták, hogy az irizin humán preadipocitákban és adipocitákban, valamint 3T3-L1 adipocitákban termelődik (73). Ennek eredményeként az irizin prekurzor PGC1α szintje magasabb a zsírszövetben, mint az izomban, az edzés után, és ez korrelál az irizin szekréciós mintázatával. Ezenkívül, hasonlóan más adipokinekhez, az irizin szekrécióját a SAT-októl befolyásolja az irizin keringő szintje (18).
Viták az irisin szekréciójáról és működéséről
Szerző közreműködései
LA, LM és MC részt vett a kézirat elkészítésében, szerkesztésében és megírásában, jóváhagyta a kézirat végleges változatát. LA tervezte az ábrákat.
Összeférhetetlenségi nyilatkozat
A szerzők kijelentik, hogy a kutatást bármilyen kereskedelmi vagy pénzügyi kapcsolat hiányában végezték, amely potenciális összeférhetetlenségként értelmezhető.
- A magas cukor- és vajtartalmú étrend elhízást és metabolikus szindrómát vált ki a szabályozás csökkenésével
- JCI - A bél mikrobioma, elhízás és metabolikus diszfunkció
- Irányelvek - elhízás és anyagcserezavarok Elhízási műtét
- A magas olajsavas földimogyoró-olaj és az extra szűz olívaolaj-kiegészítés csillapítja a metabolikus szindrómát
- Jesse Santiano; t Beteg legyen! Pikkelysömör és metabolikus szindróma