Krím-kongói vérzéses lázban szenvedő betegek esetkezelése és támogató kezelése
Fertőző betegségek és klinikai mikrobiológia tanszék, Ondokuz Mayis Egyetem Orvosi Iskola, Samsun, Törökország.
Fertőző betegségek és klinikai mikrobiológiai osztály, Ankara Numune Oktatási és Kutató Kórház, Ankara, Törökország.
Fertőző betegségek és klinikai mikrobiológiai osztály, Ankara Numune Oktatási és Kutatási Kórház, Ankara, Törökország.
Fertőző betegségek és klinikai mikrobiológia tanszék, Cumhuriyet University Medical School, Sivas, Törökország.
Fertőző betegségek és klinikai mikrobiológiai osztály, Atatürk Oktatási és Kutató Kórház, Ankara, Törökország.
Fertőző betegségek és klinikai mikrobiológia tanszék, Karadeniz Műszaki Egyetem Orvostudományi Kar, Trabzon, Törökország.
Fertőző betegségek és klinikai mikrobiológia tanszék, Ankara Egyetem Orvostudományi Kar, Ankara, Törökország.
Fertőző betegségek és klinikai mikrobiológiai osztály, Diskapi Yildirim Beyazit Oktatási és Kutatási Kórház, Ankara, Törökország.
Absztrakt
A krími-kongói vérzéses láz (CCHF) egy kullancs által terjedő fertőzés, amely 2000 óta növekszik Törökországban és az európai országokban. A betegség a Közel-Keleten és néhány afrikai országban különösen endemikus. Az európai országokban utazási fertőzésnek is tekintik. A megerősített diagnózissal rendelkező betegeket általában kórházba helyezik monitorozás céljából, míg a jó általános állapotú betegeket ambulánsan is ellenőrizhetik. A CCHF-t kezelő kórházaknak könnyen hozzáférniük kell a vérbankhoz, a tercier kórházakban pedig jól felszerelt intenzív osztálynak kell lenniük. A CCHF-expozíció korlátozása érdekében szigorú vér- és testnedv-szabályozási óvintézkedéseket kell kezdeni a felvételkor. Az egyes betegek követési periódusát az egyedi klinikai állapot és a laboratóriumi értékek alapján határozzák meg. Mivel a CCHF esetében nincs specifikus vírusellenes kezelés, elengedhetetlen a támogató kezelés. Ez az áttekintés kiemeli az esetfigyelés és a szupportív kezelés néhány fő jellemzőjét a CCHF-ben.
Bevezetés
1. táblázat: Támogató ellátás krími-kongói vérzéses lázban a
PT, protrombin idő; INR, nemzetközi normalizált arány; aPTT, aktivált parciális tromboplasztin idő; P ao 2, parciális artériás oxigénnyomás; F io 2, az inspirált oxigén frakciója; P aco 2, parciális artériás szén-dioxid-nyomás.
Normál megközelítés és esetkezelés
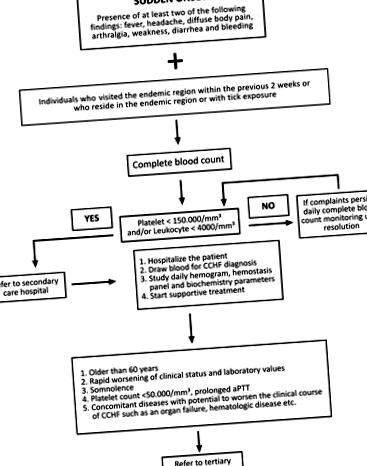
A CCHF 2003-as meghatározása után az Egészségügyi Minisztérium török CCHF tudományos bizottsága kidolgozott egy algoritmust az esetkezelésre (1. ábra; Törökország Egészségügyi Minisztériuma 2011). Az algoritmus szerint az egyes betegek követési periódusát az egyedi klinikai állapot és a laboratóriumi értékek alapján határozzák meg. A megerősített diagnózissal rendelkező betegeket monitorozás céljából általában kórházba hospitalizálják, míg a jó általános állapotú betegeket, akik képesek rendszeresen jelentést tenni a megfigyelő látogatások alkalmával, ambulánsan ellenőrizhetik. A járóbeteg-ellenőrzésnek magában kell foglalnia az alanin-aminotranszferáz (ALT), az aszpartát-aminotranszferáz (AST), a kreatin-kináz (CK), a laktát-dehidrogenáz (LDH), a nemzetközi normalizált arány (INR), a protrombin idő (PT), az aktivált parciális tromboplasztin-időt (aPTT). ) és a teljes vérkép (CBC). Egy-két hétre lehet szükség ahhoz, hogy az ALT és az AST visszatérjen a normális tartományba, és ezek a paraméterek nem igényelnek napi ellenőrzést; 3-5 naponta végzett mérések elegendőek. Ha a hemosztatikus paraméterek (PT, aPTT és INR) rendellenességei továbbra is fennállnak, még akkor is, ha az általános állapot jó, a beteget kórházba kell helyezni monitorozás céljából, amíg az értékek vissza nem térnek a normális szintre.
ÁBRA. 1. A CCHF esetkezelésére használt algoritmus (CCHF, krími-kongói vérzéses láz; aPTT, aktivált parciális tromboplasztin idő).
A török CCHF Tudományos Bizottság esetkezelési algoritmusa szerint (1. ábra) a betegek kezelhetők Törökországban mind a közép-, mind a tercier kórházakban. A CCHF-betegeket kezelő kórházaknak könnyen hozzáférniük kell egy vérbankhoz a vérkészítmények megszerzéséhez (házon belül vagy a közelben), a tercier kórházaknak pedig jól felszerelt ICU-val kell rendelkezniük. Megfelelő számú orvosnak és egyéb személyzetnek kell jelen lennie a CCHF-betegek gondozásában, különösen nyáron, és mindannyian jól tájékoztatni kell a CCHF-ről. A CCHF-expozíció korlátozása érdekében szigorú vér- és testfolyadék-ellenőrzési óvintézkedéseket kell megkezdeni a felvételkor, és a kórházi kezelés alatt is folytatni kell, amikor a beteget áthelyezik az osztályok között. Minden beteget el kell különíteni egy szobában, amelynek szomszédos előszobája az egyetlen bejárata. Mindenesetre a CCHF-betegeket el kell különíteni más betegektől.
A beteg klinikai állapota és laboratóriumi paraméterei kritikusak a monitorozás szempontjából, ideértve a vérlemezkéket, a PT, aPTT és az INR értékeket, amelyek meghatározzák a kezelés következő lépéseit. Vérzéses betegeknél naponta fel kell mérni a hemogramot és a hemosztatikus paramétereket. Szükség lehet a hemogram naponta kétszer vagy háromszor történő értékelésére, ha a vérlemezkeszám 40 000/mm 3 alá csökken. A vér karbamid-nitrogént, kreatinint, ALT-t, AST-t és bilirubint (ha sárgaság van) naponta vagy minden másnap felül kell vizsgálni, a szervelégtelenség jelenlététől függően. Hasonlóképpen, amikor a páciens klinikai állapota potenciális disszeminált intravaszkuláris koagulációt (DIC) jelez, az artériás vérgázok, a fibrinogén, a D-dimer és a fibrin bomlástermékei értékelhetők. Ha ezt monitorozás jelzi, vizeletvizsgálat és okkult széklet vérelemzés is elvégezhető.
Azokat a betegeket, akiknek általános állapota és laboratóriumi értékei normalizálódni kezdenek, és akiknek már nincs szükségük kórházi kezelésre, át lehet állítani a járóbeteg-monitorozásra. Azok a betegek, akiknél nem találtak vérzést normál koagulációs értékekkel és növekvő vérlemezkeszámmal, kiürülhetnek, feltéve, hogy a vérlemezkeszint körülbelül 100 000/mm 3. A lehető legnagyobb mértékben kerülni kell az intramuszkuláris injekciókat és az invazív beavatkozásokat.
Támogató kezelések
Intravénás folyadék
Az iv. Folyadékok nem szükségesek, ha a beteg általános állapota jó és elegendő szájon át bevitt. Ha nem, akkor adható, figyelembe véve bármely krónikus állapotot (pl. Szívelégtelenség vagy magas vérnyomás), de kerülni kell a szükségtelen folyadéktámasztást. Izotóniás folyadékok (például Ringer-laktát és izotóniás nátrium) adhatók be. Hipotonikus folyadékokat (pl. 5% -os szőlőcukor) nem szabad használni, mivel ezek nem maradnának az erekben (Schierhout és Roberts 1998). A korlátozott szájon át bevitt betegek parenterális táplálkozással támogathatók.
Trombocita szuszpenzió (PS)
Az egyetlen véletlenszerű donor PS-ket az egész vérből centrifugálással nyerik, míg az aferézis PS-ket úgy kapják meg, hogy a donor anyagától csak a vérlemezkéket választják el speciális készletek segítségével, aferézis eszközök segítségével. A donoranyagból nyert vérlemezkék száma megegyezik a véletlen donor PS 5–6 egységében lévő vérlemezkeszámmal (minden egyes PS egység 0,75 × 10 11/L vérlemezkét tartalmaz, míg a tromboferézissel nyert vérlemezke koncentrátum kb. 3 × 10 11/L vérlemezkék; McCullough 2010).
Klinikailag jelentős vérzés (pl. Hematemesis, melena és orrvérzés), a vérlemezkeszám 50 000/mm 3 alatt van (vérző betegeknél a vérlemezkeszámot nem szabad 50 000/mm 3 alá csökkenteni), a vérlemezkeszám 20 000 alatt/mm 3 plusz magas láz jelenléte és szisztémás hemosztatikus hiány jelei, a vérlemezkeszám 10 000/mm 3 alatt azoknál a betegeknél, akiknél nincs láz vagy koagulációs paraméterek rendellenességei, és a vérlemezkeszám 50 000/mm 3 alatt azoknál a betegeknél, akiken át kell esni invazív beavatkozáshoz mind PS transzfúzió szükséges (British Committee for Standards in Hematology Blood Transfusion Task Force 2003; Bosly et al. 2007).
A PS transzfúzió első 15 percében a sebesség nem haladhatja meg az 5 ml/perc értéket. A véletlenszerű donorszuszpenzióval vagy tromboferézissel nyert 6–8 egységnyi vérlemezke-koncentráció esetén a transzfúzió ajánlott időtartama 30 perc. Gyermekgyógyászati betegek sebessége 20–30 ml/kg/h. A beteget szorosan ellenőrizni kell, mivel a transzfúzió során allergiás reakciók és/vagy anafilaxia alakulhat ki. A transzfúzió utáni purpura ritka, de végzetes komplikáció. Ez a vérlemezke-specifikus alloantitestekkel kialakuló reakció jellemzően a transzfúzió megkezdése utáni első 5–9 napon történik (Bosly és mtsai 2007).
Az adott indikációtól függően 1 egység aferézislemez vagy 6 egység véletlenszerű vérlemezke adható be. Az aferezis vérlemezkék egy egysége 6 egység véletlenszerű vérlemezkének felel meg. A véletlenszerű vérlemezkék adagját a testtömegnek megfelelően állítják be, és a jó kezdő adag 1 egység véletlenszerű vérlemezke/15 kg testtömeg (British Committee for Standards in Hematology Blood Transfusion Task Force 2003; Bosly et al. 2007).
Ha a PS-t a meglévő vérzés megállítására adták, a javulás a klinikai válasz alapján figyelhető meg. Az általános gyakorlatban a beteg vérértékét az alkalmazás után körülbelül 24 órával vizsgálják. A vérzéses betegeknél azonban gyakoribb ellenőrzési paraméterek szükségesek. Különösen azokban az esetekben, amikor a vérlemezkeszám a transzfúzió ellenére sem nő, a vérlemezkék beadása után 60 perccel újraértékelhető (Spiess 2010; McCullough 2010; Refaai et al. 2011). A PS minden egysége várhatóan legalább 2000/mm 3 -al megnöveli a vérlemezke-szintet (ideális koncentráció esetén 5000–10 000/mm 3; 8 egységes vérlemezke-koncentráció esetén a várható hozam 50 000–80 000/mm 3). Gyermekeknél 1 egység thrombocyta koncentrátumnak 3500/mm 3 hozamot kell eredményeznie (Bosly és mtsai 2007; Refaai és mtsai 2011).
A thrombocyta refrakteritása az a tény, hogy nem sikerült elérni a thrombocyta-szám megfelelő növekedését 1 és 24 órán belül 3-4 egység transzfúzióját követően. A szepszis, a DIC, a hatalmas vérzés, a fertőzés, a láz és a hiperplenizmus az emberi leukocita antigén (HLA) vagy a thrombocyta antigének ellen kialakuló alloimmunizáció egyik legfontosabb oka. Az anti-HLA antitesteket értékelni kell olyan esetekben, amikor a thrombocyta refrakteressége nem magyarázható klinikai eredményekkel (British Committee for Standards in Hematology Blood Transfusion Task Force 2003). Visszatérő transzfúziók esetén a vérlemezke-koncentrátumokat beadás előtt át kell vezetni egy leukocita-szűrőn az alloimmunizáció megelőzése érdekében. Az alloimmunizáció megelőzését tekintve a véletlenszerű vagy apheresis PS felsőbbrendűségét nem bizonyították. Leukocita szűrés ajánlott az alloimmunizáció kockázatának minimalizálása érdekében. A leukocita szűrés a vérlemezkék 25–35% -os veszteségét eredményezi (Spiess 2010; McCullough 2010).
Frissen fagyasztott plazma (FFP)
A plazma egy sejtmentes folyadék, amely vízből, elektrolitokból és fehérjékből, beleértve a globulint és az albumint, áll a véradóktól kapott vér elválasztásával. 1 egység teljes vér képződött elemeinek plazmaferezisével vagy centrifugálásával nyerik (O'Shaughnessy és mtsai 2004; Simon és mtsai 2009). Elkészítése és tárolása után a vérzsákban található véralvadási faktorok és antikoagulánsok képezik a fehérjeszegmens legnagyobb részét. A plazma nem tartalmaz vérlemezkéket, eritrocitákat vagy leukocitákat (Simon és mtsai 2009). A labilis koagulációs faktorokat tartalmazza. A folyadék káliumszintje a normál szérum szintnél van, és nincsenek aggregátumok (O'Shaughnessy és mtsai 2004). Az alvadási faktorok mellett a plazma körülbelül 500 mg fibrinogént is tartalmaz (Simon és mtsai 2009).
A véradás után a plazmát szobahőmérsékleten 6–8 órán belül elválasztják, és FFP-ként definiálják, ha –18 ° C vagy annál alacsonyabb hőmérsékleten fagyasztva tárolják. Az FFP 12 hónapig -18 ° C alatt tárolható (O'Shaughnessy és mtsai 2004; Simon és mtsai 2009).
Az FFP minden egységének térfogata 200–250 ml, és aferézissel 800 ml-ig (jumbo egységig) készíthetjük. A felnőtt betegnek beadandó napi FFP-dózis körülbelül 10–15 ml/kg vagy 2–4 egység/nap, bár a dózis növelhető masszív vérzésű betegeknél, az egyéni klinikai állapottól függően. A napi adagot két részre osztva adják be. A beteg válaszát a beadott FFP transzfúzióra a véralvadási aktivitást igazoló klinikai állapot és standard laboratóriumi vizsgálatok alapján kell értékelni (O'Shaughnessy et al. 2004).
Az FFP nem alkalmazható kontrollálatlan tüdőödéma vagy pangásos szívelégtelenség jelenlétében plazma expanderként vagy fehérje pótlásként, vagy koagulopátiákban, amelyeket K-vitamin kezeléssel lehet korrigálni. Az FFP infúzió során láz és hidegrázás figyelhető meg. Ritka allergia (1–3%) és transzfúzióval összefüggő akut tüdőkárosodás alakulhat ki (O'Shaughnessy és mtsai 2004).
Vörösvértest szuszpenzió (ES)
Minden ES egység (150–200 ml) 100 ml normál sóoldatot, adenint, glükózt, mannitot (SAG-M) vagy ezzel egyenértékű további oldatokat tartalmaz, minimális plazmát, 45 g/egység hemoglobint és 50–70% hematokritot. A teljes vér centrifugálása után az eritrocitákat és a plazmát elválasztjuk. Ezután további oldatokat (pl. SAG-M) adagolunk és gondosan keverünk. A szuszpenziót 2–6 ° C-on tároljuk. A hűtőszekrényből való kivétele után 30 percen belül fel kell használni, és a transzfúziót 4 órán belül be kell fejezni (Egészségügyi Világszervezet 2001).
A hideg lánc körülményeket meg kell őrizni az ES beadásáig, és a módszer lassú transzfúziós legyen. Ha a vénás katéteren belüli áramlással kapcsolatos problémák merülnek fel a transzfúzió során, akkor az optimális megközelítés a komponens hígítását jelenti a transzfúzióhoz. A vérkomponens hígításához csak normál sóoldatot és elkerülhetetlen körülmények között 5% -os albumin oldatot szabad használni. A transzfúziónak az adagolás kezdeti 5–10 percében lassúnak (2–5 ml/perc) kell lennie, hogy lehetővé tegye az esetleges transzfúziós reakciók megfigyelését. Ezután a transzfúzió sebességét a beteg által tolerálható sebesség alapján kell beállítani, a vitális jelek óránkénti figyelemmel kísérésével a transzfúzió befejezéséig. A teljes vér és az ES transzfúziójának időtartama általában 1-3 óra, bár ez az egyes betegek klinikai állapotától függően változhat. Sürgősségi esetekben 1 egység vért csak néhány perc alatt át lehet transzfundálni, feltéve, hogy a beteget gondosan figyelemmel kísérik. A hűtőszekrényből kivett 1 vagy 2 egység normál periódus alatt történő vérátömlesztése nem jár hátránnyal. A vért azonban nem szabad melegíteni, ha a transzfúzió sebessége meghaladja az 50 ml/kg/h értéket (Uluhan és mtsai 1998; McCullough 2005).
- Az FDA jóváhagyja a Novo Nordisk Saxendáját a krónikus testsúly-kezelés diaTribe kezeléseként
- Esettanulmány az intraoperatív trachealis repedés sikeres kezeléséről thoracoscopos során
- 1. eset Láz és lymphadenopathia
- Diétacsapdák - Súlykezelés
- A női hajhullás okai és kezelése Egészség és jólét The Guardian