Mi új a pattanások patofiziológiájában, áttekintés
Nantes Egyetem Bőrgyógyászati Tanszék, Nantes, Franciaország
Nantes Egyetem Bőrgyógyászati Tanszék, Nantes, Franciaország
Összeférhetetlenség:
A szerzőnek nincs összeférhetetlensége.
Finanszírozók:
Ez a jelentés részletezi a 2016. november 8–9-én Mexikóban, Mexikóvárosban megrendezett Dermatology World Rendez-vous adatait. Ezt a találkozót a francia Fondation Bioderma finanszírozta a Fondation de France égisze alatt.
Absztrakt
Bevezetés
A pattanás a pilosebaceus egység krónikus gyulladásos betegsége. 1 Általában pubertáskor fordul elő, de felnőtteknél is megfigyelhető. 2 Patofiziológiája három szereplőt érint: hiperseborrhoea, abnormális follikuláris keratinizáció és Propionibacterium acnes burjánzás a pilosebaceous egységben. Interakciójuk eredményeként a bőr mikrokörnyezete megváltozik, és a gazdaszervezet gyulladásos reakcióihoz vezet, amelyek elősegítik a pattanások elváltozásának előrehaladását. 2, 3 A legújabb kutatások új megvilágításba helyezték a faggyúmirigy bevonását, valamint a bőr mikrobiomjának gyulladásgátló aktivitását a pattanások patofiziológiájában.
A cikk célja a faggyúmirigy, a veleszületett immunitás és a bőr mikrobiomjának pattanásokban való részvételének frissítése volt. A második cél a kezelési lehetőségek új perspektívájának megnyitása volt.
Mód
A szerző irodalmi áttekintést készített a pattanások patofiziológiájáról szóló legfrissebb adatokról.
A faggyúmirigy
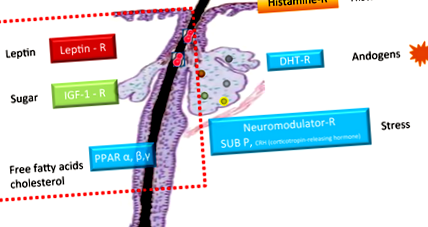
A faggyútermelést a faggyúmirigy által expresszált különböző receptorok indukálják. A hisztaminok által aktivált, jól leírt hisztaminreceptor, az androgének által aktivált hormonális DHT-receptor és a neuromodulátor-receptor, elsősorban a P anyag és a kortikotrofin-felszabadító hormon (CRH) receptorok mellett, amelyeket főként a stressz aktivál, nemrégiben végzett molekuláris kutatások három másik receptort azonosított, amelyeket a szebocita expresszál, és amelyek szabályozzák a faggyútermelést (1. ábra). 4-6
Ezen újonnan azonosított receptorok mindegyikét étrendi anyag aktiválja. A peroxiszóma proliferátor által aktivált receptorokat (PPARα, β és γ) a szabad zsírsavak és a koleszterin, az inzulinszerű növekedési faktor (IGF) -1 receptort a cukor, a leptin receptort pedig a zsír stimulálja. A 7-9. A leptin az adipociták által kiválasztott hormon, amely szabályozza a testtömeget, és a lipid anyagcserét a különböző sejttípusok gyulladásával is összekapcsolja. A sebocitában a lipidcseppek képződéséért felelős a sejtben, és a közelmúltban kimutatták, hogy pro-gyulladásos enzimeket és citokin (interleukin (IL) -6 és IL-8) szekréciót is indukál. 9 Ez az eredmény arra utal, hogy a leptin újszerû szerepet játszik a gyulladás kiváltásában és a sebociták lipidprofiljának megváltoztatásában, és kapcsolat lehet az étrend és a gyulladásos pattanások kialakulása között.
A pattanások és az étrend közötti kapcsolatot támasztja alá a pattanások prediktív tényezőinek közelmúltbeli esettanulmánya. 10 A családtörténet és a pattanások közismert kapcsolatán kívül a kutatók azt találták, hogy a magas testtömeg-index (BMI) szintén prediktív tényező volt a középsúlyos vagy súlyos pattanások kialakulásának fokozott kockázatához serdülőknél és fiatal felnőtteknél. Ezenkívül egy serdülőkön végzett, pattanásokkal és BMI-vel végzett populációalapú tanulmány arról számolt be, hogy a túlsúly és az elhízás potenciálisan társulhat a pattanásokkal a 18 és 19 év közötti lányokban, 11 annak ellenére, hogy még nincsenek bizonyítékok.
Perifériás hiperandrogenia
Bár a spironolaktont sem az EMEA, sem az FDA nem jelzi pattanásokra, ennek az állapotnak a használatára van ok: a spironolakton zavarja a hormon által szabályozott faggyú- és verejtékmirigy-szekréciót, valamint az androgén által stimulált hajnövekedést. 15 Ennek alapján egy kísérleti vizsgálatot végeztek 16 betegnél, akik 75–150 mg/nap orális spironolaktont és egy harmadik generációs tablettát és helyi BPO 0,25% -ot vagy helyi retinoidot kaptak naponta, nagyon pozitív eredményekkel a 6. és 12. hónapban, megerősítve az orális spironolakton klinikai előnyeit pattanásos felnőtt nőknél. 16 Ettől az időponttól kezdve a spironolakton alkalmazását a betegek ezen alcsoportjában tovább tesztelték. 17, 18 A közelmúltban a spironolakton helyi bejuttatása jobbnak bizonyult szilárd lipid nanorészecskékkel, amelyek a hatóanyagot a dermisbe juttatják. 19 Ennek klinikai igazolásához azonban további vizsgálatokra van szükség.
Az endokannabinoid rendszer
Az endokannabinoidok az endogén lipid mediátorok egy csoportját képviselik, amelyek központi és perifériás úton egyaránt részt vesznek különféle biológiai folyamatokban. 20
A legújabb tanulmányok érdekes módon azt sugallják, hogy funkcionális endokannabinoid rendszer (ECS) létezik a bőrben, és különféle biológiai folyamatokban vesz részt (pl. Proliferáció, növekedés, differenciálódás, apoptózis és citokin, mediátor vagy hormontermelés a bőr és a függelékek különféle sejtjeiben), például a szőrtüsző és a faggyúmirigy). Úgy tűnik, hogy a bőr ECS fő fiziológiai funkciója a bőrsejtek megfelelő és kiegyensúlyozott proliferációjának, differenciálódásának és túlélésének, valamint immunképességének és/vagy toleranciájának konstitutív ellenőrzése. Ennek a kényes egyensúlynak a megbomlása megkönnyítheti a bőr több kóros állapotának és betegségének kialakulását. 21, 22
A közelmúltban az ECS némi érdeklődést váltott ki a pattanások kezelése iránt a faggyúelválasztás szabályozásával. 23 An in vitro egy 2014-ben elvégzett tanulmány megállapította, hogy a kannabidiol liposztatikus, antiproliferatív és gyulladáscsökkentő hatású, ami ezt a nem pszichotróf kannabinoid szert ígéretes terápiává teheti acne vulgaris. 24.
A bőr mikrobioma
A bőr mikrobioma a rezidens mikrobiális lakosok (vírusok, baktériumok, gombák és paraziták) kollektív genomja, más néven mikrobiota, amely jelen van a bőrön és mellékletein. Ez egy egyedi mikrobiális ujjlenyomat. 25, 26 Ellenőrzi a mikrobiota és az átmeneti mikrobiális kolonizáció egyensúlyát, és segíti a gazda veleszületett immunitását. Folyamatosan változik, potenciálisan külső (mechanikai tényezők, komedogén kozmetikumok, agresszív mosószerek, gyógyszerek, étrend) és belső tényezők (hormonális vagy genetikai tényezők) befolyásolhatják. 10, 27-29
Annak ellenére, hogy közönséges, egyes lakosok a bőr gyulladásos betegségei, például P. acnes (pattanás), Malassezia furfur (seborrhoeás dermatitis) és demodex (rosacea). Egyéb átmeneti mikrobák, mint pl Staphylococcus aureus és Streptococcus pyogenes, ismert kórokozók. 30-33
Kiegyensúlyozott bőr mikrobiomban, Staphylococcus epidermidis korlátozza a túlkolonizációt és a bőr gyulladásos válaszát P. acnes a borostyánkősav, egy zsírsav fermentációs termék felszabadulásával azonosított törzsek, és elnyomják P. acnes‐a keratinociták IL-6 és TNF-α termelését indukálta. 34-38 fordítva, P. acnes korlátozza a S. aureus és S. pyogenes a pilosebaceus tüsző savas pH-értékének fenntartásában a faggyú-trigliceridek hidrolizálásával és a propionsav kiválasztásával. 33., 39
Ezért a természetes mikrobiom összetétel bármilyen módosítása zavart bőrgáthoz vezethet, ezt a hatást diszbiózisnak is nevezik, és amely kiváltja a veleszületett immunitás aktiválódását, amely gyulladáshoz vezet. 40 A pattanásokban a dysbiosis párhuzamos lehet a faggyú minőségi és mennyiségi változásával, az úgynevezett dysseborrhoea-val és a P. acnes, mind a hat különböző filotípus különbözik a pattanásos és pattanás nélküli betegek között. 41, 42 Ennek eredményeként a gyulladás súlyosbodik. Mint ilyen, bebizonyosodott, hogy a TLR ‐ 2 expresszió a betegség súlyosságával növekszik, és hogy citokinek termelődnek a P. acnes és a TLR ‐ 2, defenzinek és MMP PAR ‐ 2R aktiválással. 43, 44 Ez a TLR-2, IL-8 és MMP-9 stimulációja révén súlyosbodó jel, amely a pilosebaceus mirigyből a dermisbe és az epidermisbe diffundálódik, ötször volt gyulladásgátlóbb, mint S. aureus vagy Streptococcus pyogenes. 43, 45-49
A mikrobiom természetes egyensúlyának kiegyensúlyozása, amely lehetővé teszi a természetes bőrgát helyreállítását, ezért a pattanások kezelésének egyik fő célja ma.
A veleszületett immunitás és P. acnes
A bőrön belül mind a veleszületett, mind az adaptív mechanizmusok hozzájárulnak a gazda immunfunkciójához. 50-52 a keratinociták fontos szerepet játszanak a bőr immunválaszában. Számos mintázatfelismerő receptort (PRR) fejeznek ki, beleértve a Toll-szerű receptorokat (TLR) és a proteáz-aktivált receptorokat (PAR), amelyek különböző konzervált molekuláris entitások felismerésével ismerik fel a mikrobákat. Miközben számos antimikrobiális peptid (AMP, például dermcidin), citokin (INF ‐ γ, IL ‐ 8, IL ‐ 12, TNF, IL ‐ 1, MMP) és kemokin expresszálódik egyensúlyi állapotban, a PRR aktiválása gyorsan növelheti ezen molekulák expressziója, amely közvetlen antimikrobiális hatásokat eredményez, valamint további immunsejtek toborzását és oktatását eredményezi. 53-55
Az által kiváltott gyulladás folyamatában P. acnes, Megfigyelték az IL ‐ 1β szekrécióját monociták és sebociták által az NLRP3 gyulladásos kulcsgén aktiválásával. Ezt a mechanizmust proteázok és reaktív oxigénfajok (ROS) szabályozzák. 56-58 Sőt, P. acnes elősegíti a vegyes Th17/Th1 válaszokat azáltal, hogy in vitro specifikus CD4 (+) T-sejtekből IL-17A és IFN-y szekréciót indukál. Ezért az IL ‐ 17A-pozitív T-sejtek jelenléte és a Th17-rokon citokinek aktiválása pattanáselváltozásokban azt jelzi, hogy a Th17 útvonal kulcsfontosságú szerepet játszhat a betegség folyamatában, esetleg új terápiás célokat kínálva. 59
Újabban, P. acnes megállapították, hogy nagyon érzékeny a nitrogén-oxid különböző koncentrációira a nanorészecskékben (NO-np). Az NO ‐ np jelentősen elnyomta az IL ‐ 1β-t, a tumor nekrózis-faktort (α (TNF ‐ α), az IL ‐ 8 és IL ‐ 6 humán monocitákból, valamint az IL ‐ 8 és IL ‐ 6 humán keratinocitákból és perifériás vér mononukleáris sejtekből. Ezek az adatok arra utalnak, hogy az NO ‐ np hatékonyan képes megakadályozni P. acnes-Indukált gyulladás a szervezet tisztításával és a veleszületett immunválasz mikrobiális stimulációjának gátlásával. 60
Számos faggyúmentes zsírsav (FFA), mint például a linolsav és a szapieninsav, antibakteriális hatást fejtenek ki az antimikrobiális peptid (AMP) termelésének stimulálása révén a Gram-pozitív baktériumok széles skálájával szemben, mint pl. P. acnes. 61 Különböző tanulmányok kimutatták, hogy az AMP-k a bőr veleszületett immunitásának fő hozzájárulói. Ezek közül az emberi β-defenzin (hBD) -2 a gyulladás során a keratinocitákban szabályozódik, majd felhalmozódik a bőrben. 64, 65 Közvetlen antimikrobiális hatásuk miatt ezen peptidek szekréciója védelmet nyújt a mikrobákkal szemben, mint pl. P. acnes. 61 Ezt Choi megerősítette et al. 66 a gyulladásos pattanáselváltozások regionális különbségét értékelő tanulmányon keresztül, a hBD ‐ 2 expresszió szerint.
Ezen elemek alapján az AMP-k integrálása a gyulladást célzó jelenlegi kezelések, például a helyi retinoidok fegyverzetébe a pattanások kezelésének jövőjének tekinthető.
Propionibacterium acnes és a biofilm
Propionibacterium acnes képes extracelluláris poliszacharidokból készült biofilmet létrehozni. Ez a biológiai ragasztó növeli a tapadást P. acnes a follikuláris falakhoz, elősegítve az integrinek modulációját. Ezenkívül szabályozza a baktériumok növekedését és anyagcseréjét, indukálja a P. acnes kolóniák és rezisztenciát biztosít az antimikrobiális szerekkel és a gazda gyulladásos sejtekkel szemben, ami a bakteriális rezisztencia második mechanizmusát eredményezi. 67 Az P. acnes biofilm gyakrabban figyelhető meg pattanásos betegeknél. 68 Ezekben a betegeknél a propionsav szekréciója P. acnes szabálytalan sejtmorfológiájú keratinociták képződéséhez vezetett, megerősítve ezt P. acnes modulálja a keratinociták differenciálódását, ami arra utal, hogy szerepet játszik a gyulladásos pattanáselváltozások kialakulásában és a mikrokomedonok képződésében. 69, 70
Következésképpen a helyi antibakteriális vegyületek, például a benzoil-peroxid vagy a botanikus szerek alkalmazása, amelyek nem váltanak ki antibakteriális rezisztenciát, kiváltságos alternatíva lehet a bőr korlátozásában. P. acnes biofilm. 71.
Következtetések
Összefoglalva, a pattanások megjelenése különböző tényezőket foglal magában, amelyek gyulladást és különböző típusú pattanások kialakulását eredményezik. Ezek a tényezők magukban foglalják a faggyú pubertáskori mennyiségi és minőségi megváltozását, az úgynevezett dysseborrhoea-t, amelyet belső tényezők, például hormonális vagy genetikai tényezők váltanak ki, és külső tényezőket, például komedogén kozmetikumokat, agresszív detergenseket vagy gyógyszereket, amelyek stimulálhatják a pattanás. A stressz és az étrend hatása a dysseborrhoea-ban még tisztázatlan. A diszbiózis, a zavart bőrgáthoz vezető folyamat és a bőr mikrobiomjának egyensúlyhiánya, ami a P. acnes törzsek, más fontos folyamatok, amelyek kiváltják a pattanásokat. P. acnes aktiválja a veleszületett immunitást a PAR-ek, a TNF-α és a TLR-ek expresszióján keresztül, valamint az INF-γ, IL-8, IL-12, TNF, IL-1 és MMP termelésével keratinociták által, ami a pilosebaceus egység hiperkeratinizációját eredményezi.
(i) A bőr természetes mikrobiomjának kiegyensúlyozása a természetes bőrgát helyreállításával a citokin receptorok megcélzásában, (ii) a bőr szaporodásának korlátozása P. acnes a bőrön olyan helyi antibakteriális szerek alkalmazásával, amelyek nem okoznak rezisztenciát, és (iii) a faggyú kiáramlásának és összetételének szabályozása lesz a fő pattanáskezelési kihívás a jövőben.
Köszönetnyilvánítás
A szerző elismeri Karl Patrick Göritz, az SMWS ‐ Scientific and Medical Writing Services, Franciaország írásbeli támogatását.
- Pajzsmirigy működése és elhízás - FullText - European Thyroid Journal 2012, Vol
- A pattanások pszichológiájának túllépésének titka ma
- A zsír titkos élete, Sylvia Tara, PhD Book Overview; A Queen Anne Diet
- Krónikus székrekedés kezelése - Jewish Journal
- A zsír eltűnésének tendenciái az Egyesült Államokban, 1909–65. The Journal of Nutrition Oxford Academic