Stressz az elhízásban és a kapcsolódó anyagcsere- és kardiovaszkuláris rendellenességekben
Paul Holvoet
Atherosclerosis and Metabolism Unit, Kardiovaszkuláris Tudományok Tanszék, KU Leuven, Herestraat 49, P.O. Box 705, 3000 Leuven, Belgium
Absztrakt
1. Bemutatkozás
Az Egészségügyi Világszervezet előrejelzései szerint 2015-ig körülbelül 2,3 milliárd felnőtt lesz túlsúlyos és több mint 700 millió elhízott. Az Egyesült Államok (USA) jelenleg a fogyókúrás gyógyszerek legnagyobb egységes piaca, a lakosság mintegy 68 százaléka túlsúlyos vagy elhízott, ezt követi az Egyesült Királyság és más európai országok. Csak az Egyesült Államokban több mint 9 millió gyermek és tizenéves elhízott. Sőt, Kína, Oroszország, India és Brazília hamarosan elkezdheti meghaladni elhízott népességével a nyugati országokat.
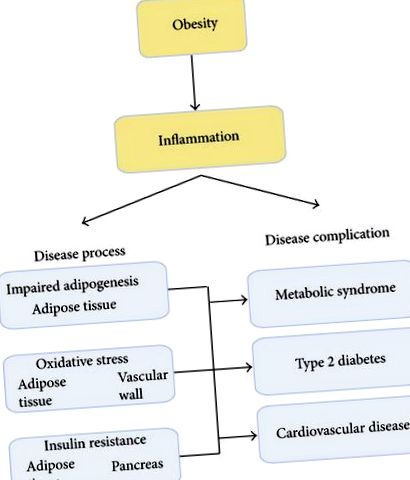
Első célunk annak bemutatása, hogy az elhízás krónikus gyulladásos betegségállapot, amely más betegségfolyamatokkal társul, mint például a zsírszövet (AT) átalakulása, oxidatív stressz és inzulinrezisztencia (IR). Ezek a betegségfolyamatok hozzájárulnak a 2-es típusú cukorbetegség (T2DM) és a metabolikus szindróma (MetS) kialakulásához [1]. A MetS gyakori és összetett rendellenesség, amely egyesíti az elhízást, a diszlipidémiát, a magas vérnyomást és az IR-t [2–5]. Ez a T2DM és a szív- és érrendszeri betegségek (CVD) elsődleges kockázati tényezője [3, 6–13] (1. ábra).
A gyulladás központi szerepének sematikus ábrázolása elhízás okozta rendellenességekben. Az elhízás során a túlzott kalóriabevitelhez kapcsolódó gyulladásos állapot a zsírszövet átalakulását, oxidatív stresszt és inzulinrezisztenciát vált ki, ami a metabolikus szindróma, a 2-es típusú dibéták és a szív- és érrendszeri betegségek fokozott kockázatával jár együtt.
Második célunk a viselkedés, valamint a személyes és környezeti stressz tényezők hatásainak elemzése az elhízás és a társuló rendellenességek kialakulására. Hangsúlyozzuk a stressz tényezők hatásait a betegség folyamatainak epigenetikus szabályozó mechanizmusainak elvesztésére, elsősorban a gyulladásra összpontosítva.
Végül megvitatjuk az elhízás jelenlegi gyulladáscsökkentő és antioxidáns kezelésének korlátait és a kapcsolódó anyagcsere- és kardiovaszkuláris rendellenességeket, bemutatva a betegség folyamatainak nem megfelelő irányítását.
2. Az elhízás krónikus gyulladásos betegség
Az alacsony fokú gyulladás az elhízott állapot jellemzője (2. ábra). Sok gyulladásos marker keringési koncentrációja elhízott személyeknél magasabb, mint sovány embereknél, és vélhetően szerepet játszanak az IR és más anyagcserezavarok előidézésében. A gyulladásos markerek az elhízott emberek AT-ban is magasabbak; beszivárgó makrofágok és maguk az adipociták választják el őket. A gyulladásos markerek vérkoncentrációja csökken a fogyás után [14]. A magas glükózszintű és a magas zsírtartalmú ételek étkezés utáni gyulladást okozhatnak. Ez utóbbit rontják a fejlett glikációs végtermékek (AGE), és részben ellensúlyozza bizonyos antioxidánsok vagy antioxidánsokat tartalmazó élelmiszerek étkezésbe történő felvétele [15].
Alacsony fokú krónikus gyulladás és oxidatív stressz a zsírszövetben az elhízás során. Az elhízás során a zsírszövet túlzott felhalmozódását az immunsejtek toborzása jellemzi. Az aktivált T-sejtek és kemokinek monocita vándorlást indukálnak a zsírszövetekben, ahol proinflammatorikus M1 makrofágokká differenciálódnak. Az aktivált T-sejtek, a makrofágok és a diszfunkcionális adipociták közötti kölcsönhatás diszregulált adipokint és exoszómaszerű vezikulák termelését eredményezi, ami inzulinrezisztenciát (IR) okoz. Az elhízás során a zsírszövet hipoxiája ROS és ox-LDL termeléssel, valamint habsejtképződéssel jár. Ezenkívül a hipoxia és a megnövekedett oxidatív stressz az adipociták apoptózisát indukálja, hozzájárulva az inzulinrezisztenciához.
Mechanikusan a citokin-interleukin- (IL-) 1β az elhízás során kialakuló proinflammatorikus válasz kiemelkedő ösztönzőjeként jelent meg [16]. Valójában az Il-1 receptor-I (Il-1RI) hiánya megvédi az egereket a magas zsírtartalmú étrend okozta AT gyulladástól, egybeesve a javuló glükóz homeosztázissal [17]. A gyulladás másik kiváltója az NLR pirintartalmú-3 (Nlrp3, más néven Nalp3 vagy kriopirin) gyulladásos; indukciója IR-hez kapcsolódik. Az Nlrp3 ablációja egerekben csökkentette az Il-18 és az interferon-y (Ifn-y) szintjét, és javította az inzulin jelátvitelt [18]. Az angiopoietin-szerű protein-2 (Angptl2) fokozott szekréciója AT által is aktivál egy gyulladásos kaszkádot és kiváltja a monociták/makrofágok kemotaxisát. Az Angptl2 deléció enyhítette az AT gyulladását és a szisztémás IR-t étrend okozta elhízott egerekben [19].
Ezenkívül a gyulladást az adipokinek szintjének változása okozza. Az adipocitákból származó egérrezisztin túlzott mértékű expressziója felgyorsult fehér AT (WAT) gyulladáshoz vezet, amely fokozott lipolízissel és szérummentes zsírsavakkal (FA) és IR-vel társul [20]. Ezzel szemben az adipocita eredetű adiponektin véd a gyulladás ellen azáltal, hogy elősegíti a makrofágok polarizációját egy gyulladásgátló fenotípus felé [21]. Az adiponektin növekedése csökkent zsírtartalom és gyulladásos citokinek tumor-nekrózis-faktor (Tnf-) α és Il-6 elhízott patkányokban [22].
Összességében elmondható, hogy az AT gyulladásának hozzájárulása az elhízás kialakulásához nagyon hasonlít az artériás szövetek ateroszklerózisának kialakulásához való hozzájárulásához [37–39]. Ebben kulcsfontosságú az M2 makrofágokról az M1 makrofágokra történő fenotípusos váltás hozzájárulása a gyulladáshoz és az IR-hez. Valóban, az I LIKE HOMe vizsgálat hasonló monocita heterogenitást mutatott az elhízásban és a szubklinikai érelmeszesedésben. A testtömeg-index (BMI) szignifikánsan korrelált a carotis intima-media vastagságával (IMT). A magas CD16 (+) monocita szám szignifikánsan összefüggött mind a magasabb BMI-vel, mind a carotis IMT növekedésével. A CD16 (+) monocitaszám korrekciója gyengítette a korrelációt a BMI és a carotis IMT között, ami arra utal, hogy az elhízásban a CD16 (+) monocita szám növekedése részben magyarázhatja az elhízás és az IMT közötti kapcsolatot [40].
3. Az elhízás a metabolikus szindrómához kapcsolódik
Az elhízás gyakran más kardiovaszkuláris kockázati tényezőkkel, például diszlipidémiával, hipertóniával és hiperglikémiával csoportosul a MetS-ben. A Nemzeti Koleszterin Oktatási Program Szakértői Testületének harmadik jelentése a magas vérkoleszterin felnőttek kimutatásáról, értékeléséről és kezeléséről (ATPIII) kiemeli a MetS-ben szenvedő betegek kezelésének fontosságát a CVD megelőzése érdekében [2]. A MetS összetevőket az alábbiak szerint határozta meg: (1) a derék kerülete ≥102 cm a férfiaknál és ≥88 cm a nőknél; (2) éhomi trigliceridek ≥150 mg/dl (1,70 mmol/l); (3) HDL-koleszterin 12 év). Az emelkedett ox-LDL, de nem emelkedett LDL-koleszterinszint a jövőbeni MetS magasabb kockázatával járt. A megemelkedett ox-LDL különösen a hasi elhízás, a hiperglikémia és a hipertrigliceridémia előfordulásához kapcsolódott [49].
Az ox-LDL növekedése a MetS-szel és az ateroszklerózissal összefüggésben az antioxidáns kapacitás csökkenésének oka lehet az antioxidáns enzim szuperoxid-diszmutáz (SOD) [59] alacsony szérumaktivitása vagy alacsony HDL-asszociált paraoxonáz (PON) antioxidáns aktivitás [58]. . Az ox-LDL növekedése a megnövekedett oxidáló képességnek is köszönhető, például a NADPH-oxidáz (NOX) fokozott expressziójával. Valójában a reaktív oxigénfajok (ROS) termelése szelektíven megnőtt az elhízott egerek AT-jában, amelyet a Nox magasabb expressziója és az antioxidáns SOD csökkent expressziója okozott. A tenyésztett adipocitákban az emelkedett FA növelte az oxidatív stresszt a Nox-aktiváció révén, az oxidatív stressz pedig csökkentette az adiponektin termelését, valamint az Il-6 és a Mcp-1 szintjét. Végül elhízott egerekben a Nox gátlóval végzett kezelés csökkentette az AT ROS-értékét, csökkentette a gyulladásos adipokinek szintjét, valamint csökkentette a cukorbetegséget, a hiperlipidémiát és a máj steatosisát [60].
5. Metabolikus szindróma társul a szív- és érrendszeri betegségekkel
Grundy és munkatársai egy sor kardiovaszkuláris rizikófaktort mértek 59 820 férfiban és 22 192 nőben. A rizikófaktor-profilokat a cardiorespiratoris fitnesz (CRF) öt kvintjébe soroltuk. A CRF csökkenésével nőtt az elhízás, a trigliceridek, a triglicerid/HDL lipoprotein arány, a vérnyomás, a MetS és a cukorbetegség, valamint a dohányzás [64]. A magas vérnyomásról, a hiperglikémiáról és a hiperlipidémiáról szóló tajvani felmérés során a CVS MetS által tulajdonított kockázata férfiaknál 39%, nőknél 44% volt. Az összes MetS-komponens közül a nőknél a központi elhízás volt a legmagasabb (57%), míg a magas vérnyomás férfiaknál a legmagasabb (57%) [65]. A kínai Jiangsuban a MetS több mint kétszer magasabb CVD-kockázattal társult az életkor, a nem, a nem, a BMI, az alkoholfogyasztás, a CVD családi kórtörténete és a dohányzás kiigazítása után [66].
Juonala és mtsai. négy prospektív vizsgálat adatainak meta-elemzését végezte annak megállapítása érdekében, hogy ez a kockázat csökkent-e azoknál a személyeknél, akik túlsúlyosak vagy elhízottak gyermekként, de felnőttként nem. A követés átlagos hossza huszonhárom év volt. Azoknál az alanyoknál, akiknél gyermekkoruktól felnőttkorig folyamatosan magas adipozitási státusz volt, a T2DM ötször nagyobb, a nyaki artéria megnövekedett IMT-jével kétszer magasabb a magas vérnyomás és az alacsonyabb HDL-koleszterin kockázat. Érdekes módon ezeknek az eredményeknek a kockázata a túlsúlyos vagy elhízott gyermekek körében, akik felnőttkorukban elhízottak, hasonlóak voltak azokhoz, akik soha nem voltak elhízottak [67].
6. Viselkedés és elhízás
Egyre több bizonyíték áll rendelkezésre arról, hogy a testmozgás, a dohányzás és a zsírban gazdag étrend hiánya hozzájárul az elhízás és a kapcsolódó rendellenességek kialakulásához (3. ábra).
- A kerekféreg elfojtja az elhízást és a kapcsolódó anyagcserezavarokat - ScienceDaily
- A perivascularis zsírszövet, mint az elhízás kardiovaszkuláris kockázatának releváns zsírraktára
- A resveratrol és emberi metabolitjai - hatások a metabolikus egészségre és az elhízásra
- Az egyik megközelítés megakadályozhatja a tinédzserek elhízását, étkezési rendellenességeit, új irányelvek szerint - írja a ScienceDaily
- Elhízás, fogyás és feltételes kardiovaszkuláris kockázati tényezők - Tzotzas - 2011 - Elhízási vélemények