TÁPLÁLKOZÁSI ÁLLAPOT ÉS DELIRIUM A HOSSZÚ TÁVÚ ÁPOLÓ IDŐSEKBEN
Kennith R. Culp
1 docens, Iowa Egyetemi Ápolási Főiskola, Iowa City.
Pamela Z. Cacchione
2 egyetemi docens, Saint Louis University School of Nursing, St. Louis, Missouri.
1. Bemutatkozás
Népességként a tartós gondozásban (LTC) lakóknak számos korlátja van, amelyek hozzájárulhatnak a fogyáshoz és a táplálkozási problémákhoz, beleértve a csökkent funkcionális állapotot és a dysphagia-t; mások már a rossz táplálkozási állapotot összefüggésbe hozták egyes pszichiátriai rendellenességekkel, beleértve a depressziót és a demenciát (Buchanan, Wang, Tai-Seale és Ju, 2003; Chouinard, Lavigne és Villeneuve, 1998). Az idősebb felnőtteknél a csökkent táplálékfogyasztás klinikailag összefüggésbe hozható a rossz étvágyzal, a krónikus betegséggel, a demenciával (Chouinard et al., 1998; Gil Gregorio, 2003), a neuroszenzoros veszteséggel és a rossz száj/fogak egészségével (Baumgartner, 2000; Guigoz, Lauque, & Vellas, 2002; Nordenram és Ljunggren, 2002). Az alultápláltság jatrogén okai a tartós gondozási intézményekben túl kevés ápoló-asszisztenst tartalmaznak étkezés közben (Kayser Jones & Schell, 1997), rossz minőségű ételeket (Crogan, Evans, Severtsen és Shultz, 2004) és polifarmáciát (Evans, Crogan, & Shultz, 2004; Fabiny és Kiel, 1997; Perry és Turner, 2001). Mindezek a tényezők hozzájárulnak ahhoz, hogy az alultápláltság jelentős klinikai probléma legyen a hosszú távú ellátásban, az időskorúak becslései az időskorúak 30 és 85% -a között mozognak (Crogan & Pasvogel, 2003). A tanulmány elsődleges célja a delírium és az alultápláltság közötti összefüggés értékelése volt az idősek otthonában.
1.1 Elméleti keret
A delíriumot a tünetek akut megjelenése jellemzi, amelyek magukban foglalják a tájékozódási zavarokat, a tudatszintet, a memóriát, a figyelmet, a gondolkodást, a viselkedést és az alvás-ébrenlét ciklust, a probléma hátterében konkrét fiziológiai tényezők állnak (Inouye, Rushing, Foreman, Palmer, És Pompei, 1998). Általában ezek a tünetcsoportok ingadozó folyamatot követnek, és a kezdő klinikus könnyen összetévesztheti demenciával. A delírium problémáját az LTC-ben súlyosbítja a delírium ismert rizikófaktorainak nagyobb előfordulása, nevezetesen a demencia, a betegség súlyossága, a társbetegség és a polifarmácia (Cacchione, Culp, Dyck és Laing, 2003; McCusker, Cole, Dendukuri, Han és Belzile, 2003). A legújabb munkák szerint az alultápláltság, különösen az alacsony testtömeg-index (BMI) és a fehérje-alultápláltság negatívan befolyásolja az életminőséget és más eredményeket. (Crogan és Pasvogel, 2003).
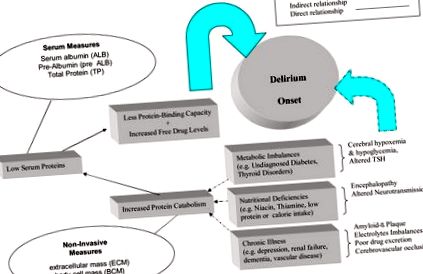
Az 1. ábra fogalmilag bemutatja a rossz táplálkozás és a delírium megjelenésének szerepét. Először is biológiailag elfogadható, hogy számos betegségállapot alacsony szérumfehérjéhez vezet, vagy megváltozott oxigén-, glükóz- és alacsony agyi perfúziós nyomáson keresztül zavarja a kognitív működést (Foreman, Wakefield, Culp és Milisen, K. (2001) Ezek az állapotok magukban foglalják az anyagcsere-rendellenességeket, az alacsony kalóriatartalmú fogyasztást, a táplálkozást, az agyi érrendszeri betegségeket és a krónikus betegségeket, például a magas vérnyomást és a vesebetegségeket. A hosszú távú gondozásban más problémák is előfordulnak, például depresszió, demencia, stroke és rossz nyelés, amelyek szintén befolyásolják a táplálékfelvétel (Crogan és Corbett, 2002). A fehérje katabolizmus számos táplálkozási értékelési paramétert megváltoztat, beleértve az antropometriai méréseket és a szérum kémiai tulajdonságait is, de számos idősotthonban nincsenek helyszíni laboratóriumok a szérum albumin mérésére; egyszerűen csak súlyra támaszkodnak. testösszetétel kiszámítása (Fabiny & Kiel, 1997; Friedmann, Elasy és Jensen, 2001; Guigoz et al., 2002).
Az alultápláltság kettős negatív hatása a delírium kialakulására a Frail idősek otthonában
A fehérje katabolizmus és az ebből eredő alacsonyabb plazmafehérje-probléma egyik fő problémája a normál fehérjéhez kötött gyógyszerek szérumszintjének emelkedése (van Vliet, Schuurmans, Grypdonck és Duijnstee, 2006). A gyógyszeres túladagolás és a polifarmácia gyakori probléma az idősek otthonában; néhány gyakori gyógyszer antikolinerg tulajdonságokkal rendelkezik, amelyekről ismert, hogy hozzájárulnak a delíriumhoz (Holden & Kelly, 2002; McCusker, Cole, Dendukuri, Han és Belzile, 2003).
Mikroelemek hiánya az ásványi anyagokban és nyomelemekben, antioxidánsokban és egyéb vitaminhiányokban, például a B12 státuszban (Ledikwe, Smiciklas-Wright, Mitchell, Miller és Jensen, 2004; Ortega et al., 1997; Wendland, Greenwood, Weinberg és Young, 2003) szintén ismerten befolyásolják a delírium megjelenését. Azonban túlnyomórészt az alacsony szérumfehérje és a polifarmácia (azaz a túlzott gyógyszeres kezelés) a delírium tényezőinek legveszélyesebb kapcsolata. Az alultápláltság egyértelműen befolyásolja az ápolási otthon ellátásának minőségét (Crogan és Pasvogel, 2003). Mivel sok tartós ápoló intézményben nincsenek orvosi laboratóriumok a szérumfehérje közvetlen mérésére, praktikusnak tűnt néhány nem invazív táplálkozási intézkedést felvenni a protokolljainkba a táplálkozási állapot felmérése érdekében, mivel ezek könnyebben megvalósíthatók a hosszú távú gondozásban.
1.2 Táplálkozási értékelés
Az Egyesült Államokban a táplálkozással és a fogyással foglalkozó hosszú távú gondozási vizsgálatok közül a legtöbb a minimális adatsort használja (MDS), és nem a súly vagy kognitív állapot közvetlen klinikai megfigyelését használja (Corbett, Crogan, & Short, 2002; Crogan & Corbett (2002; Keller és Hirdes, 2000). Az MDS egy szövetségi felhatalmazással ellátott átfogó értékelőlap, amelyet minden egyes, az Egyesült Államokban lakó idősotthonra kitöltenek. Az LTC ápolószemélyzete több feladattal és korlátozott létszámmal áll fenn, és nem szánnak időt az értékelés befejezésére (Davidson & Getz, 2004). Jelenleg az Egyesült Államok szövetségi szabályozói alig igényelnek többet a fogyás dokumentációjánál (Corbett et al., 2002). A fiatalabb és középkorú felnőttek testösszetételének vizsgálata az Egyesült Államokban általában antropometriai adatokon alapul, a testtömeg, a testalkat, a bőrréteg vastagság és a kerületek mérésével (Maitland, Myers, Hipp, Hayes és Greenspan, 1993; Shaikh & Mahalanabis, 2004; Tai, Ho, Fok és Tan, 1999). Ezek az intézkedések a zsírosság (azaz a testtömeg-index; BMI) vagy a teljes testzsír becslésének összefüggéseit adják meg (Chumlea et al., 2002), de az idősebb felnőtteket ritkán veszik bele ezekbe a mintákba. Ezen módszerek némelyikét a fejlettebb technikákkal összehasonlítva megkérdőjelezték pontosságuk szempontjából (Piers, Soares, Frandsen és O'Dea, 2000).
A bioelektromos impedancia elemzés (BIA) felhasználható a testösszetétel becslésére, bár ezt a beállítást technikaként elhanyagolták (Culp, Mentes és Wakefield, 2003). Egyszerűen leírva a BIA olyan technika, amelynek során a víz és a folyadékok által szállított nagyon kicsi elektromos jelet továbbítják a testen; az impedancia a zsírszövetben a legnagyobb, amely csak 10–20% vizet tartalmaz (Di Iorio, Scalfi, Terracciano és Bellizzi, 2004). A zsírmentes testtömeg, amely 70–75% vizet tartalmaz, sokkal könnyebben engedi át a jelet.
1.3 Hipotézisek
Az idősek otthonában élő felnőtteknél a tápláltsági állapot csökkenése és a delírium közötti összefüggés jelentősége gyengén megfogalmazott, annak ellenére, hogy a tartós gondozásban részesülő idősek körében széles körű érdeklődés mutatkozik az étrendi bevitel kezelése iránt. Néhányan a rossz táplálkozást összekötik a mortalitással (Hirdes, Frijters és Teare, 2003; Volpato és mtsai, 2004), vagy az idősek otthonában lévő betegek etetésére és a végstádium demenciájára összpontosítanak (Gessert & Calkins, 2001; Mitchell, Kiely és Gillick, 2003; Murray, 2000; Okada és mtsai, 2001; Sheiman és Pomerantz, 1998; Silver, Wellman, Arnold, Livingstone és Byers, 2004). A következő hipotéziseket javasoljuk:
Azoknál a résztvevőknél, akiknél pozitív a delírium, a testzsír kevesebb lesz (% BF,% FFM,% ECM és% BCM), mint a delírium nélkül.
Azoknak a résztvevőknek, akiknek pozitív a delíriumja, a szérumalbumin és az összes fehérje szintje alacsonyabb lesz, mint a delírium nélkül.
Demenciában szenvedő résztvevők (a Mini-Mental Status pontszám átlagos kiindulópontja a fent leírtak szerint.
Két vagy több pont csökkenése a Mini-Mental állapotban az alapvonaltól kezdve.
A NEECHAM pontszáma 24 vagy kevesebb.
A Confusion Assessment Method (CAM) képernyő pozitív
2.3.2 Egyéb intézkedések
A geriátriai depresszió skálájának rövid formája (GDS), egy 15 tételes igen-nem formátumú kérdőívet használtak az affektus értékelésére; ≥ 5-ös cut-off pontszám adta a legjobb érzékenységet és specificitást; 0,93 és 0,48 (Burke, Roccaforte és Wengel, 1991; Lesher és Berry hill, 1994; Sheikh és mtsai, 1991). A GDS kritikus pontjai 0–4 pontszámot értek el, mint depressziót, az 5–9 pont enyhe depressziót, a 10–15 pontszám pedig közepes vagy súlyos depressziót jelentett (Lesher & Berry hill, 1994).
A táplálkozási változásokat BIA, magasság és súly (WT) alkalmazásával mértük a testtömeg-index (BMI) kiszámításához. A WT-t és a BIA-t a kiindulási és a 7., 14. és 28. napon követtük a testsúly (WT) szempontjából. A BIA eljárás becslései magukban foglalták a testsejtek tömegét (BCM), az extracelluláris tömeget (ECM), a testzsír százalékát (BF) és a zsírmentes tömeget (FFM). Az FFM az összesített BCM és ECM. A BCM a test összes sejtelemének teljes tömege, ezért a test metabolikusan aktív összetevőjét képviseli, ideértve az oxigénfogyasztást, a szén-dioxid-termelést, a glükóz-oxidációt és a fehérjeszintézist (Volpato és mtsai, 2004). Az ECM a test támasztó tömege és metabolikusan inaktív. Az ECM extracelluláris folyadékokból és szilárd anyagokból áll, mint például csont és porc; elsődleges funkciója a támasz és a szállítás. A BIA méréseket legalább 2 órával étkezés után, és legalább 6 órával a vizelethajtó gyógyszeres kezelés után végezték el.
2.3.3 A szérum fehérjeszintje
2.4 Adatok elemzése
Az egyirányú varianciaanalízist (ANOVA) alkalmazták a NEECHAM és MMSE pontszámok közötti különbségek kimutatására a résztvevők táplálkozási indexek szerinti csoportosításával. Ismételjük meg az ANOVA mértéket, mivel a függő változókat a kiindulási napon, a 7. és a 14. napon mértük. A delírium kimutatásához becsült esélyhányadost alkalmaztunk 95 százalékos konfidencia intervallummal. A BMI vágási pontjait 28-ban határozták meg, és általában a sovány, normális és elhízott eredményeket osztályozzák (Wilson, D'Agostino, Sullivan, Parise és Kannel, 2002). A% BF,% FFM,% ECM és% BCM nyers mértékét úgy kaptuk meg, hogy az egyén testtömegét ezekre a paraméterekre osztottuk, így összehasonlítás céljából egy százalékot kaptunk.
3. Megállapítások
Az% FFM nem és BMI csoport szerint az 1. táblázatban látható. Arra lehet számítani, hogy alacsony BMI-vel rendelkező résztvevők (pl. 28), és ez a helyzet volt ebben a mintában. Ismételt mérést végeztünk ANOVA-val a BIA négy megfigyelési időpontjának mindegyikéhez (kiindulási érték, 7. nap, 14. nap és 28. nap) a BCM, az ECM és az FFM esetében. Nem voltak szignifikáns különbségek a BCM, az ECM, a BF és az FFM időpontjai között, amikor a nemet bevitték a modellbe.
Asztal 1
Testtömeg-százalék zsírmentes tömeg (FFM), amelyet a BIA számított, összehasonlítva a hagyományos BMI-besorolással
| Nők | |||
| 28. | 89 | 59.58 | 9.65 |
| Teljes | 239 | 68.21 | 11.55 |
| Férfiak | |||
| 28. | 40 | 59.31 | 11.00 |
| Teljes | 73. | 65.04 | 12.5 |
Megjegyzés: BIA = Bioelektromos impedancia elemzés; FFM = zsírmentes tömeg; BMI = testtömeg-index, súly kg-ban osztva a méter magasságával, négyzetben kifejezve
3.1 Delírium és táplálkozási állapot
Összesen 312 résztvevőből 69-en vettek részt, akik 28 napos megfigyelés alatt pozitívan vizsgálták a delíriumot (21,8%). A delíriumban szenvedők átlagos életkora 88,5 év volt (SD = 6,13), szemben a delírium nélküli betegek 85,5 évével (SD = 7,25), ami szignifikáns volt (t = −3,03, p 28 (M = 26,58, SD = 2,34, n) = 129). A delírium esélyarányait a 2. táblázat mutatja be, szignifikánsan megnövekedett delírium szűrési valószínűséggel% FFM,% ECM és% BCM esetében, ha nemek szerint van rétegezve. Ezek az esélyek> 1,0-nél nagyobbak azt jelzik, hogy idős korban az idősek otthonában résztvevő résztvevők „soványabbá” váltak, a delírium kockázata megnőtt, a delirium patogenezis szempontjából azonban figyelemre méltó a megnövekedett kockázat megállapítása% BCM-rel (lásd a vitát).
2. táblázat
A delírium és a testösszetétel esélyének aránya nemenként
| Nők | ||||
| Esélyhányados | 0,99 | 1,024 * | 1,033 * | 1,050 * |
| 95% CI | .97–1.02 | 1.015–1.020 | 1.025–1.041 | 1.038–1.062 |
| Férfiak | ||||
| Esélyhányados | 0,97 | 1,016 * | 1,029 * | 1,042 * |
| 95% CI | .93–1.01 | 1.009–1.020 | 1.015–1.043 | 1.021–1.063 |
3. táblázat
Mini-mentális állapot testtömeg-százalékos testösszetétel szerint
| % FM | |||
| MMSE 23 | 161 | 34.09 | 11.42 |
| % FFM | |||
| MMSE 23 | 161 | 65,92 | 11.43 |
Megjegyzés: FM = Fat Mass;
FFM = zsírmentes tömeg;
MMSE = Mini-Mental Status Exam
3.3 Szérum fehérje és delírium
A szérum albumin szintjét és a delírium eredményeit a 4. táblázat mutatja az alapvonalra vonatkozóan; a követés 7. és 14. napja, ahol az ismételt mérés ANOVA eredményei szignifikánsak voltak. A delírium pozitív résztvevők albuminszintje alacsonyabb volt, mint a nem delírium csoportjában (F = 3,55, p = 0,06). A szérum pre-albumin és az összes fehérje ismételt mérése nem volt statisztikailag szignifikáns, ezért csak a kiindulási értéket használtuk. A pozitív screen delirium résztvevőinek szintén alacsonyabb volt az előzetes albumin szintje (M = 22,91 mg/dl, SD = 7,38), mint a delírium nélkül (M = 23,81 mg/dL, SD = 7,40), de az pre-albumin nem növeli a kockázatot, ha folytonos változóként elemezzük (OR = 1,017, 95% CI 0,98–1,06). A kiindulási összes fehérje szint a delírium esetekben is valamivel alacsonyabb volt (M = 6,86 g/dL, SD =, 57) a nem esetekhez képest (M = 6,88 g/dL, SD =, 60), de ez sem volt statisztikailag szignifikáns.
4. táblázat
Ismételje meg az ANOVA mérését a szérumalbumin esetében delírium állapot szerint
| Alapvonal | Delírium | 3.70 | 0,33 | 3.55 | 0,06 |
| Nincs delírium | 3.79 | 0,37 | |||
| 7. nap | Delírium | 3.74 | 0,40 | ||
| Nincs delírium | 3.80 | 0,37 | |||
| 14. nap | Delírium | 3.66 | 0,36 | ||
| Nincs delírium | 3.78 | 0,39 |
3.4 Depresszió
A GDS-rel mért depressziós pontszámok azt mutatták, hogy 53,8% (n = 168) negatív, 36,9% (n = 115) enyhe depressziót mutat, és 9,3% (n = 29) közepesen súlyos vagy súlyosan depressziós. Nem voltak különbségek a GDS-pontszámokban a delíriummal (M = 5,06, SD = 3,45) és a delíriummal nem rendelkezők (M = 4,52, SD = 3,02) között. Nem voltak különbségek a% FFM,% BCM,% ECM vagy% BF között a GDS osztályozás szerint. Jelentősen alacsonyabb szérum összes fehérje szintet találtunk a közepesen súlyos és súlyos depresszióban szenvedőknél, összehasonlítva azokkal, akik a negatív szűrést végezték, és az enyhe depresszióban szenvedőkkel (F = 3,75, p = 0,024), amint azt az 5. táblázat mutatja. Nem volt különbség a NEECHAM pontszámai között a depresszió kimenetelének osztályozása szerint a három csoportban (azaz negatív, enyhe, valamint közepes vagy súlyos depresszió).
5. táblázat
A szérumalbumin, az előalbumin és a szérum fehérjeszintje depressziós besorolás szerint
- Táplálkozási állapot felnőtteknél alternatív vagy hagyományos étrend mellett - PubMed
- Urolithiasisos alanyok táplálkozási állapota és táplálkozási szokásai
- Táplálkozási gond peptikus fekély esetén
- A vényköteles vizelethajtó hidroklorotiazid többszörös előfordulása az összetett táplálkozásban
- A rendelési pont táplálkozási receptjei és az élelmiszer-sorrend pszichológiája ma